Salen双核Cu2+配合物的合成及催化染料降解
2016-12-20江银枝程本能孙红英时永强
江银枝, 程本能, 孙红英, 时永强
(浙江理工大学 化学系, 浙江 杭州 310018)
表1 配合物的表征
表2 Cu2ClL·6H2O催化甲基橙的降解效果
表3 Cu2ClL·6H2O催化酸性蓝9的降解实验
Salen双核Cu2+配合物的合成及催化染料降解
江银枝, 程本能, 孙红英, 时永强
(浙江理工大学 化学系, 浙江 杭州 310018)
以水杨醛、N,N’-二胺丙基乙二胺和CuCl2为原料得到了双核配合物Cu2ClL·6H2O,并进行了表征.利用UV-Vis研究了Cu2ClL·6H2O催化甲基橙和酸性蓝9的降解性能,利用GraphPad Prism 5软件绘制了染料降解的V-S曲线,利用HPLC研究了染料的降解产物.结果发现:(1)Cu2ClL·6H2O能有效催化甲基橙和酸性蓝9的氧化降解,10 h后酸性蓝9和甲基橙的降解率分别达到90%与60%;(2)染料的降解动力学符合酶促动力学过程,V-S曲线符合米氏动力学方程,Cu2ClL·6H2O催化甲基橙和酸性蓝9降解米氏常数Km分别为3.29×10-2和1.93×10-1mmol·L-1;(3)降解产物有马来酸,并给出了催化剂的催化机理和染料的降解机理.说明Cu2ClL·6H2O可以作为仿酶催化剂,与底物甲基橙和酸性蓝9有较好的结合效果.这为设计作用底物广、效果好的仿酶催化剂提供了理论基础,为染料降解新方法和新技术的开发提供了实践依据.
合成;配合物;染料降解;仿生催化;废水
工业废水、矿山排水和生活污水的不合理排放是造成水污染最主要的原因.染料废水是主要的有害工业废水之一.偶氮类、三苯甲烷类和蒽醌类3大染料多有苯环结构,结构稳定、生物可降解性差.传统的规模化生物处理工艺投菌法和活性淤泥法难以达到水处理要求,且存在大量淤泥的后处理问题[1-4];而传统的物理法和化学氧化法处理成本高,难以规模化[5-6].近年出现的生物法与氧化法联用技术[7]均无法从根本上解决问题.所以寻找新的染料降解技术将成为相关学科的热点.
相对于物理法和化学氧化法,生物法中的投菌法和活性淤泥法具有环保、可规模化等优势,一直是染料降解研究的热点[8].生物法降解染料的途径是通过有效酶系促进染料的氧化还原降解[9].这类酶主要为过氧化氢酶、漆酶等氧化酶,尤其漆酶,是一类单核到多核的含铜氧化酶,能有效降解偶氮类、三苯甲烷类染料.但酶法存在产酶率低、难以回收、价格昂贵和环境适应性差等缺点,限制了其规模化和工业化发展.于是有文献报道了用酶的固化[10]和模拟[11]来解决酶缺陷的问题,其中,尤令学者感兴趣的是酶的模拟.
江银枝等[12]设计合成了二乙烯三胺缩水杨醛席夫碱单核Cu2+配合物,并研究了其对甲基橙和酸性蓝9的降解性能,发现这个单核Cu2+配合物能有效催化酸性蓝9的氧化降解,且具有仿酶特性,Km=2.006×10-2mmol·L-1.在此基础上,笔者希望通过增加2个配位螯合中心Salen Schiff base间的距离(两者之间有乙二胺的N原子作为桥连中心),设计合成双核或多核Cu2+配合物,以增加活性位点,拓展作用底物.合成所得的二胺丙基乙二胺缩水杨醛H3L见图1.研究了此合成物与CuCl2的配位反应,得到了一个新的双核铜配合物;考察了此双核铜配合物对甲基橙和酸性蓝9的催化降解过程,并测定了米氏常数和降解产物,给出了可能的降解机理和催化循环机理.

图1 H3L及其配合物的合成Fig.1 Synthesis of H3L and its complex
1 材料和方法
1.1 试剂与仪器
试剂均为市售商品,未经处理直接使用.有水杨醛、二胺丙基乙二胺、乙醇、三乙胺、氯仿、乙醇、甲醇、石油醚、氯化铵、二水合氯化铜、浓氨水、醋酸、醋酸钠、碳酸钙、六水合氯化镁、EDTA(乙二胺四乙酸二钠)、PAN(1-(吡啶基偶氮)-2-萘酚)指示剂、EBT指示剂、浓硝酸、蒸馏水、甲基橙、酸性蓝9、30% H2O2、0.1 mol·L-1HCl溶液、纯净水、色谱纯甲醇.
1H NMR和13C NMR谱用Bruker 400 UltraShiedTM(400 MHz)核磁共振谱仪(瑞士,布鲁克公司)测得,CDCl3为溶剂,TMS为内标;红外波谱用Avatar 370 FI-IR(Nicolet)红外光谱仪(美国,尼高力仪器公司)测得,KBr固体压片;C、H、N元素分析在Carlo-Erba 1106元素分析仪(意大利,卡拉巴尔)上进行;Cu2+质量分数用EDTA络合滴定法测定,PAN为指示剂;降解过程用CARY 50 Cone紫外-可见分光光度计(美国,瓦里昂公司)进行跟踪;降解动力学曲线的绘制、模拟及米氏常数测定由GraphPad Prism 5软件完成;降解产物利用SPD-15C&LC-15C高效液相色谱仪(日本,岛津)测定.
1.2 配合物合成方法
参照文献[13-14]的方法,在冰浴搅拌条件下,0.5 h内将水杨醛的无水甲醇溶液(2.44 g,20 mmol,20 mL)滴入N,N’-双(3-氨丙基)乙二胺(5.4 g,90 mmol,10 mL).滴加完毕后,继续搅拌2 h析出黄色沉淀,抽滤,滤渣用甲醇洗涤3次,50 ℃真空干燥得到N,N-双-水杨醛-缩2-(2(1,3-双(3-胺丙基)-咪唑基))苯酚(H3L).黄色固体,产率约62%;熔点:70.1~73.3 ℃;IR(KBr压片,cm-1)3 431,1 631,1 595,1 547,1 487,1 459,1 278,1 266;1HNMR(400 MHz,CDCl3)δ13.47(s,2 H),10.91(s,1 H),8.12(s,2 H),7.30-7.26(m,2 H),7.16(d,J=7.4 Hz,2 H),7.10(t,J=7.4 Hz,2 H),6.90(d,J=8.0 Hz,3 H),6.84(t,J=7.4 Hz,2 H),6.78(d,J=8.0 Hz,1 H),6.66(t,J=7.4 Hz,1 H),3.64(m,3 H),3.49-3.34(m,4 H),2.63(m,2 H),2.53(m,2 H),2.36-2.25(m,2 H),1.87-1.76(m,4 H);13CNMR(100 MHz,CDCl3)δ165.4,161.2,157.9,132.0,131.4,130.9,130.0,121.2,118.7,118.6,118.3,116.9,116.6,89.7,77.3,77.0,76.7,56.6,49.8,49.6,28.9;13CDEPT135NMR(100 MHz,CDCl3)δ165.4,132.04,131.4,131.0,130.0,118.6,118.3,116.9,116.6,89.7,56.7,49.8,49.7,28.9.
向反应瓶中依次加入乙醇(20 mL)、H3L(5 mmol),搅拌溶解,升温回流,向反应体系中加入CuCl2乙醇溶液(10 mmol,20 mL),加毕保温反应,TLC跟踪其反应进程,结束反应.趁热过滤,滤饼多次用水+乙醇(1+1)洗涤至无Cu2+,PAN指示剂检验.得Cu2ClL·6H2O,深绿色固体;产率90%;熔点大于300 ℃;IR(KBr压片,cm-1):3 430(m,OH),1 629(m,CN),1 600,1 538,1 482,467,1 244 (m,ArO),1 266(m,ArO),600,525,465,425,405;Cu元素分析,测定值16.97%,理论值16.84%.
1.3 降解性能实验方法
选择甲基橙或酸性蓝9的起始浓度25 mg·L-1进行试验.以30%H2O2为氧源,对配合物进行甲基橙或酸性蓝9的催化降解实验,n配合物∶n染料∶n双氧水=1∶10∶1 000,用分光光度计跟踪脱色进程.
降解反应结束后,对降解液进行HPLC分析,采用外标法确定其降解产物.HPLC条件:柱子Wondasil C18,4.6 mm×150 mm,流动相V甲醇∶V水=4∶6,流速1.00 mL· min-1,进样量25 μL,检测器SPD-15C型UV检测器(日本,岛津)),波长285 nm.
2 结果与分析
2.1 配合物的表征
采用元素分析仪对所合成的配合物进行C、H、N元素分析.样品经600 ℃马弗炉灼烧,0.5 mol·L-1HNO3浸取,以PAN为指示剂,用EDTA络合滴定测定Cu2+质量分数.用KBr压片法,在400~4 000 cm-1测定相关配体及配合物的红外光谱.实验结果见表1.
表1 配合物的表征

Table 1 Characterization of the complex
从表1中的元素分析结果发现,测定值与理论值吻合,说明推测的配合物的分子组成是正确的,配体L与中心离子配位比为1∶2.表1中红外数据显示配合物Cu2ClL·6H2O的νC=N吸收峰出现在1 631 cm-1,相对于配体H3L的νC=N吸收峰1 629 cm-1发生了一定的偏移,说明C=N中的N原子参与了配位;在525 cm-1处出现的Cu-N吸收峰,进一步说明C=N中的N原子参与了配位;配合物Cu2ClL·6H2O的νPh—O吸收峰出现在1 266,1 244 cm-1,相对于配体H3L的νph—O吸收峰1 278,1 266 cm-1发生了一定的移动,说明Ph—O中的O原子参与了配位;在425 cm-1处出现的Cu—O吸收峰,进一步说明2类Ph—O中的O原子参与了配位;配合物Cu2ClL·6H2O在600,465,405 cm-1处的吸收峰分别是H2O参与配位时H2O的面外、面内和M—O的振动吸收,说明配位H2O存在.
分析表征数据发现,合成的配合物是一个双核Cu配合物,配体L3-提供了4个配位N原子,3个配位O原子,其中与咪唑环相连的Phen—O-的O原子为桥配原子;1个Cl-作为桥配原子连结2个Cu2+中心;每个Cu2+中心均连有一分子配位H2O;配合物分子中有丰富的氢键,类似天然金属酶活性中心的氢键区域.说明Salen型配体通过加大2个螯合配位点之间的距离,在链间引入桥配单元(二胺基或氧原子),可以实现从单核配合物到双核配合物的合成[12].依据文献[13-15],推测配合物结构如图2所示.

图2 配合物结构Fig.2 The structure of the complex
2.2 Cu2ClL·6H2O催化染料的降解
2.2.1 甲基橙的降解
废水的甲基橙起始浓度设置为25 mg·L-1,pH=7.2,T=37 ℃,以H2O2为氧源,n配合物∶n染料∶n双氧水=1∶10∶1 000,在λ=468 nm时进行甲基橙的催化降解实验跟踪,降解效果见表2.
表2 Cu2ClL·6H2O催化甲基橙的降解效果

Table 2 Degradation effect of methyl orange using Cu2ClL·6H2O as catalyst
表2说明配合物对甲基橙具有催化降解作用,10 h脱色率达到60%.为了进一步研究其催化降解特性,采用分光光度计分析Cu2ClL·6H2O催化甲基橙的降解动力学过程,绘制了P-t曲线(见图3).

图3 不同浓度甲基橙的P-t曲线Fig.3 P-t curves of methyl orange degradation with different concentrations
从图3可以发现,Cu2ClL·6H2O对甲基橙的脱色经历了明显的延滞期和线性脱色期,这种特性与典型酶促反应相符[16],说明合成的Cu2ClL·6H2O对甲基橙的降解具有仿酶催化活性;其底物浓度的改变会导致延滞期和线性区间速度的变化.利用图3的数据,采用GraphPad Prism 5软件绘制了V-S曲线(见图4).
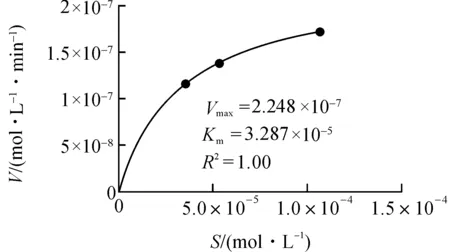
图4 甲基橙降解V-S曲线Fig.4 V-S curve of methyl orange degradation
图4显示,Cu2ClL·6H2O催化甲基橙降解的V-S曲线与米氏方程曲线相吻合[16],拟合常数为1.00,呈现典型的酶催化动力学特性.进一步说明Cu2ClL·6H2O对甲基橙的催化降解具有酶催化特性,可用作仿酶催化剂,且米氏常数Km为3.287×10-5mol·L-1.
采用外标保留时间定性,利用HPLC检测降解液发现,Cu2ClL·6H2O作为氧化酶的模型物催化甲基橙的氧化降解,主要降解产物有顺式丁烯二酸.利用导管将降解气导入澄清的Ca(OH)2溶液中,产生混浊现象,说明降解产物中有CO2.
2.2.2 酸性蓝9的降解
设置废水的酸性蓝9的起始浓度为25 mg·L-1,pH=7.2,T=37 ℃,以H2O2为氧源,n配合物∶n染料∶n双氧水=1∶10∶1 000,在λ=630 nm时对配合物催化酸性兰9的降解实验进行跟踪,降解效果见表3.
表3 Cu2ClL·6H2O催化酸性蓝9的降解实验

Table 3 Degradation effect of acid blue 9 using Cu2ClL·6H2O as catalyst
表3数据显示,酸性蓝9在脱色10 h后,脱色率达到了90%以上.采用分光光度计进一步研究Cu2ClL·6H2O催化酸性蓝9的降解动力学过程,绘制了P-t曲线(见图5).

图5 不同浓度酸性蓝9的降解P-t曲线Fig.5 P-t curve of acid blue 9 degradation with different concentration
从图5可以发现,Cu2ClL·6H2O对酸性蓝9的脱色经历了明显的延滞期和线性脱色期,最后进入饱和期,这种特性与典型酶促反应相符[16],说明合成的Cu2ClL·6H2O对酸性蓝9的催化降解具有仿酶催化活性;底物浓度的改变可导致延滞期和线性区间速度的变化.利用图5数据,通过GraphPad Prism 5软件绘制了V-S曲线(见图6).

图6 酸性蓝9的V-S曲线图Fig.6 V-S curve of acid blue 9 degradation
图6数据显示,Cu2ClL·6H2O催化甲基橙降解的V-S曲线与米氏方程曲线吻合[16],拟合常数为0.998 1,米氏常数Km为1.928×10-4mol·L-1.说明Cu2ClL·6H2O催化酸性蓝9的降解过程与底物形成了复合过渡态.
采用外标保留时间定性,利用HPLC对降解液进行检测发现,Cu2ClL·6H2O作为氧化酶的模型物,催化酸性蓝9氧化降解的主要产物为顺式丁烯二酸;利用导管将降解气导入澄清的Ca(OH)2溶液,发生了混浊现象,说明降解产物中有CO2.
2.2.3 配合物催化循环机制和染料的降解机制
分析配合物催化甲基橙和酸性蓝9的降解效果和降解动力学的数据发现,双核配合物Cu2ClL·6H2O既可以催化降解偶氮染料甲基橙,也可以催化降解三苯甲烷染料酸性蓝9,是对单核配合物的拓展[2];而且,配合物催化甲基橙和酸性蓝9的降解过程均符合酶促动力学过程,在催化过程中催化剂与底物形成复合物的一种过渡态.推测可能的催化循环机制如图7.
如图7所示,催化剂Cu2ClL·6H2O(1)首先与底物之一的H2O2通过配位键和氢键结合得到中间体(2).中间体(2)中咪唑环上苯基的酚氧负离子从H2O2得到一个H+变成酚,H2O2变成H-O-O-.接着桥连Cl-发生翻转,H-O-O-作为桥连配体与2个Cu2+配位,同时与周围的H2O生成氢键网络,此时通过氢键与底物二染料结合,这就是中间结构(3).受氢键和双Cu2+中心的共同影响,H-O-O-发生裂解,生成单线[O]和OH-.OH-与1个Cu2+配位,同时与咪唑换上的取代苯基的酚羟基形成氢键,见中间结构(4).单线[O]通过氢键转移至底物染料,实现染料的氧化降解.结构(4)中酚羟基的H与OH-结合生成水离去,催化剂完成一次循环回到结构(1).
研究降解产物发现,无论是甲基橙还是酸性蓝9降解,不仅染料分子生色团发生断裂,而且苯环也发生开环断裂.说明Cu2ClL·6H2O可以作为氧化酶的仿生催化剂催化染料甲基橙和酸性蓝9的降解,且可以实现真正意义的矿化.推测染料可能的降解机制见图8.

图7 Cu2ClL·6H2O的催化机理Fig.7 Catalytic mechanism of Cu2ClL·6H2O

图8 甲基橙和酸性蓝9的降解机理Fig.8 Degradation mechanism of methyl orange and acid blue 9
3 结 论
3.1 通过增加螯合位点(双Salen席夫碱中心),并延长2个螯合位点之间的距离,从二缩二乙基三胺[12]到三缩二胺丙基乙二胺,成功设计合成了双核配合物Cu2ClL·6H2O.
3.2 考察了Cu2ClL·6H2O催化甲基橙和酸性蓝9降解的性能和产物,发现V-S曲线符合米氏方程,催化过程具有酶促效应;降解产物有顺丁烯二酸;给出了催化剂的催化循环机理和染料的降解机制.
3.3 增加Sanlen螯合中心之间的距离,插入桥连基团,可以实现多核配合物的合成;相对于单核配合物,多核配合物增加了活性位点,拓展了底物,而降解效果不变.这一发现为设计合成新型、底物范围广的高效仿酶催化剂,研发新的高效环保的染料降解技术提供了基础资料.
本工作得到了浙江省自然科学基金(LY13B010004,LY14B010005)、国家自然科学基金(21472174)和化学工程与技术浙江省重中之重(一级)学科的资助,特此致谢!
[1] PHALE P S, BASU A, MAJHI P D, et al. Metabolic diversity in bacterial degradation of aromatic compounds [J]. Omics, 2007,3(11):252-279.
[2] BRILLAS E A. Review on the degradation of organic pollutants in waters by UV photoelectro-fenton and solar photoelectro-fenton [J]. Journal of the Brazilian Chemical Society, 2014,25:393-417.
[3] 周春晓,范雪荣,王强.氧化还原酶在印染中的应用(一)[J].印染,2014(6):47-50. ZHOU Chunxiao, FAN Xuerong,WANG Qiang. Application of oxidoreductases in textile wet processing(I)[J]. Dyeing & Finishing, 2014(6):47-50.
[4] AFSANEH S, FATEMEH S, HAMIDREZA S, et al. Facile approach to the synthesis of carbon nanodots and their peroxidase mimetic function in azo dyes degradation [J]. RSC Adv,2012(2):7367-7370.
[5] MARYIN L R, ANDRÉS R G, HUGO R Z, et al. Azo-dye orange II degradation by the heterogeneous Fenton-like process using a zeolite Y-Fe catalyst-Kinetics with a model based on the Fermi’s equation [J]. Applied Catalysis B: Environmental, 2014,146:192-200.
[6] BOKARE A D, CHOI W Y. Review of iron-free Fenton-like systems for activating H2O2in advanced oxidation processes [J]. Journal of Hazardous Materials, 2014,275:121-135.
[7] YU X M, ZHOU M H, HU Y S. Recent updates on electrochemical degradation of bio-refractory organic pollutants using BDD anode: A mini review [J]. Environmental Science and Pollution Research, 2014,21:8417-8431.
[8] FOCKEDEY E, LIEEDE A V. Coupling of anodic and cathode reactions for phenol electro-oxidation using three-dimensional electodes[J]. Water Research,2002,36:416-417.
[9] LAURA C C, JOSE L S, BLANCA E B. Biodegradation of organic pollutants in saline waste water by halophilic microorganisms: A review [J]. Environmental Science and Pollution Research. 2014,21:9578-9588.
[10] VERNEKAR M, LELE S S. Laccase: Properties and applications [J]. Bioresources,2009(4):1694-1717.
[11] 高键,关可兴,焦晶,等.细菌漆酶的结构催化性能及其应用[J].分子催化,2014,28:188-196. GAO Jian, GUAN Kexing, JIAO Jing, et al. Structure, catalytic properties and application of laccase[J]. Journal of Molecular Catalysis, 2014,28:188-196.
[12] 江银枝,时永强,史银瓶,等.双水杨醛缩二乙烯三胺Cu(II)配合物的合成及催化染料降解性能[J].中国科学:化学,2014,44(10):1528-1535. JIANG Yinzhi, SHI Yongqiang, SHI Yinping, et al. Synthesis and dye degradation performance of the complex of Cu(II) with bis-salicylidene diethylenetriamine Schiff base[J]. Scientia Sinica:Chimica, 2014,44(10):1528-1535.
[13] LOULOUDI M,MITOPOULOU K, EVAGGELOU E. Homogeneous and heterogenized copper(II) complexes as catechol oxidation catalysts [J]. J Mole Cata A,2003,198:231-240.
[14] SUPRITI P, PRASANT K N, CORINE M, et al. Aqua bridge cleavage and metal ion extrusion by thiocyanate anions in a dicopper complex[J]. Inorganica Chimica Acta, 2011,370:108-116.
[15] BRENDA W T, CARLA J M, PHILLIP E F, et al. Green structure-distribution relationships for metal-labeled myocardial imaging agents:Comparison of a series of cationic gallium(II1) complexes with hexadentate bis(salicyla1dimine) ligands[J]. J Med Chem, 1994,37:4400-4406.
[16] PRASANT K N, DEBASHREE M, DEBASHIS R. Coordination induced 2-(2-hydroxyphenyl) imidazolidine ring hydrolysis of dinucleating amine-imine-phenol ligands:X-ray structures of hardness-matched mononuclear cobalt(III) complexes as end products having isomeric N4O2coordination spheres[J].Polyhedron, 2006,25:702-710.
JIANG Yinzhi, CHENG Benneng, SUN Hongying, SHI Yongqiang
(DepartmentofChemistry,ZhejiangSci-TechUniversity,Hangzhou310018,China)
The binuclear Cu2+complex with salen schiff base: Synthesis and catalytic properties in dye degradation. Journal of Zhejiang University(Science Edition), 2016,43(6):733-739
The complex, Cu2ClL· 6H2O was prepared from salicylaldehyde N,N’-bis-aminopropyl-1, 2-ethanediamine and CuCl2. Its structure and composition were examined by IR spectra and elemental analysis, respectively. Then, its catalytic properties were investigated via degradation of methyl orange and acid blue 9 that were detected by UV-Vis spectra, and theirV-Scurves were drawn by GraphPad Prism 5 software. The degraded products of these two dyes with the presence of complex as mimetic enzyme were determined by HPLC method. The results show that the degradation rates of acid blue 9 and methyl orange are 90% and 60% after 10 h, respectively, which indicates that the catalytic activity in the degradation of acid blue 9 is better than in methyl orange degradation. It is found that the experimentalV-Scurve fits Michaelis-Menten equation well, andKmvalues are 1.93×10-1and 3.29×10-2mmol· L-1for the degradation of acid blue 9 and methyl orange, respectively, implying that the complex could be used as bio-mimetic catalyst in dye degradation. Maleic acid as the degraded product was checked. Moreover, the catalytic mechanism of the complex for degradation of acid blue 9 was deduced. All these provide theoretical and experimental supports for a new dye removal technology and novel bio-mimetic catalyst design in dye degradation.
synthesis; complex; dye degradation; bio-mimetic catalysis; waste water

2015-10-20.
浙江省自然科学基金资助项目(LY13B010004,LY14B010005);国家自然科学基金资助项目(21472174).
江银枝(1973-),ORCID:http://orcid.org/0000-0003-2393-9654,女,博士,副教授,主要从事配位化学和分析化学研究, E-mail:jiangyinzhi@zstu.edu.cn.
10.3785/j.issn.1008-9497.2016.06.019
O 614.12
A
1008-9497(2016)06-733-07
