两种定值方法测定阿司匹林丁香酚酯对照品的含量
2016-12-19杨青青刘希望杨亚军李剑勇
杨青青,刘希望,杨亚军,李剑勇,查 飞
(1.西北师范大学化学化工学院,甘肃 兰州 730070; 2.中国农业科学院兰州畜牧与兽药研究所,农业部兽用药物创制重点实验室,甘肃省新兽药工程重点实验室,甘肃 兰州 730050)
两种定值方法测定阿司匹林丁香酚酯对照品的含量
杨青青,刘希望,杨亚军,李剑勇,查 飞
(1.西北师范大学化学化工学院,甘肃 兰州 730070; 2.中国农业科学院兰州畜牧与兽药研究所,农业部兽用药物创制重点实验室,甘肃省新兽药工程重点实验室,甘肃 兰州 730050)
目的:采用质量平衡法与核磁共振法,测定阿司匹林丁香酚酯(aspirin eugenol ester,AEE)对照品含量。方法:采用高相液相色谱测定纯度,采用干燥失质量法测定水分和挥发性物质,炽灼残渣测定无机盐杂质,根据质量平衡法计算AEE对照品含量。建立核磁共振定量测定AEE含量的方法,仪器温度25 ℃,扫描次数(NS)16次,弛豫延迟时间(Dl)15 s。结果:质量平衡法测定的AEE对照品含量为99.82%;核磁共振定值结果为99.55%,AEE和内标物(1,4-二硝基苯)峰面积的比值与质量比在3~21 mg范围内呈良好线性关系(R2=0.999),日内精密度的RSD值为0.04%(n=5),重复性的RSD值为0.19%(n=5),稳定性测定的RSD值为0.57%。结论:2种方法相互验证,测定结果基本一致。
质量平衡法; 核磁共振法; 对照品; 阿司匹林丁香酚酯; 方法验证
阿司匹林丁香酚酯(aspirin eugenol ester,AEE),是由阿司匹林与丁香酚酯化反应制得的具有解热、镇痛、降血脂、抗血栓作用的新型化合物[1-2]。根据临床试验和相关文献记载,阿司匹林治疗范围极广,包括上呼吸道感染、发热、头痛、关节痛、风湿痛等,还能预防术后血栓形成、心肌梗死和中风。一般阿司匹林剂量较少时,不会引起不良反应,但长期大量用药会出现恶心、呕吐、胃肠道出血等不良反应[3-5]。丁香酚具有解热、抑菌、抗氧化、抗肿瘤作用,但也存在腐蚀性、刺激性和毒性等副作用[6-7]。AEE在不改变阿司匹林和丁香酚单独发挥临床作用的结构部位的基础上,较前2种药物具备以下优势:低毒性、降低了丁香酚的刺激性和易氧化性,同时也降低了阿司匹林对胃肠道直接的酸刺激[8]。该药是自主研发的新型化学合成药物,目前处于临床研究阶段,故开展AEE标准物质含量测定方法的研究可以为原料药及相关制剂质量标准的制定奠定基础。核磁共振(nuclear magnetic resonance,NMR)波谱分析被广泛用于化学、食品、农业及医药等现代科学研究领域,主要用于有机化合物结构的确定和化学动力学的研究,在其他领域的应用也在扩大。除了定性测定外,NMR的定量测定方法也被各国药典收录。定量测定时需选择合适的定量峰,确定积分面积即可计算物质含量。本研究通过质量平衡法与NMR定量方法测定了AEE对照品的含量,报告如下。
1 材料
1.1 仪器
Waters 2695型高效液相色谱(配2998二极管阵列检测器,Waters Corporation);Varian 400型NMR仪(美国瓦里安公司);BS124S型电子天平(北京赛多利斯仪器系统有限公司);DZF-6030A型真空干燥箱(上海一恒科学仪器有限公司);马弗炉(北京盈安美诚科学仪器有限公司)
1.2 药品与试剂
氘代氯仿(纯度99.8%,含0.03%四甲基硅烷,Sigma)、甲醇及乙腈(色谱纯,Fisher);1,4-二硝基苯(纯度99.4%,Sigma)、AEE对照品(由中国农业科学院兰州畜牧与兽药研究所制)。AEE的结构式见图1。
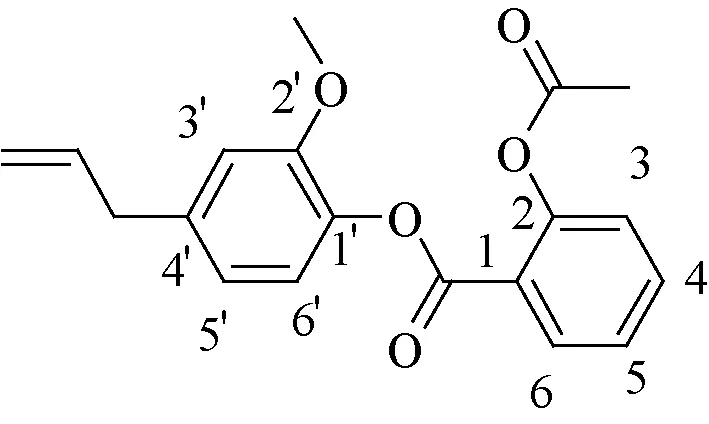
图1 AEE的结构式Fig 1 Structure of AEE
2 方法
2.1 质量平衡法测定AEE对照品的含量
质量平衡法计算公式:含量(%)=色谱纯度×(1-干燥失重-炽灼残渣)×100%[9]。
2.1.1 纯度测定:(1)液相色谱。①条件1。色谱柱Hypersil ODS C18(100 mm×4.6 nm,3 μm);流动相甲醇-水(V∶V=80∶20);流速1 ml/min;检测波长279 nm;进样量10 μl。②条件2:色谱柱Hypersil BDS C18(150 mm×4.6 nm,5 μm);流动相乙腈-水(V∶V=85∶15);流速1 ml/min;检测波长279 nm;进样量10 μl。(2)配制AEE供试品溶液:准确称量AEE对照品3份,每份10.0 mg,加甲醇配制为1 mg/ml的溶液,精密量取1 ml置于10 ml容量瓶,稀释至刻度得A溶液。准确称量AEE对照品3份,每份10 mg,加乙腈配制为1 mg/ml的溶液,精密量取1 ml置于10 ml容量瓶,稀释至刻度得B溶液。(3)测定方法:采用色谱条件①、②分别测定对照品的纯度。
2.1.2 挥发性物质:水分与残留溶剂都是挥发性物质,参照《中华人民共和国药典:四部》(2015年版)[10]0831干燥失质量测定方法,将研磨的粉末AEE于(25±2)℃、800 Pa的真空干燥箱,无水氯化钙为干燥剂,计算干燥失质量。
2.1.3 炽灼残渣:参照《中华人民共和国药典:四部》(2015年版)[10]0841炽灼残渣检查法,将试样灼烧至完全碳化,再加H2SO40.5~1.0 ml并炽灼(700~800 ℃)至恒质量后,称量计算遗留的金属氧化物或其硫酸盐。
2.2 NMR法测定AEE对照品含量
按NMR条件平行测定供试品溶液5份,采集图谱,处理图谱,对定量峰积分,按照核磁定量方法计算AEE含量[11-13]。计算公式为:ms=ms×(As/Ar)×(Es/Er)[14],其中,E=样品分子量/产生该共振峰的基团中的质子数;Er为内标物在该化学位移处的质子当量。经公式化简推倒得:Ws(%)=[(As/ns)×Ms×mr] / [(Ar/nr)×Mr×ms]×Wr,其中,As为被测样品定量峰的积分面积,ns为被测样品定量峰包含的质子数,Ms为被测样品的相对分子质量,Ar为内标物质定量峰的积分面积,nr为内标物质定量峰包含的质子数,Mr为内标物质的相对分子质量,mr为称取的内标质量,Wr为内标的质量百分含量,ms为样品质量。
2.2.1 仪器参数:温度25 ℃,扫描次数(NS)16次,弛豫延迟时间(D1)15 s,其他条件为仪器内设条件。
2.2.2 供试品溶液配制:分别精密称量AEE与1,4-二硝基苯15.0、9.0 mg,加入氘代氯仿0.6 ml溶解,振荡摇匀,转移至核磁管待测。
2.2.3 含量测定:将配置好的供试品溶液分别进行测定,采集图谱,经傅里叶变换、相位校正和基线校正,归属确认为AEE的结构[13],对内标和对照品的定量峰积分,取多次积分的平均值减少积分误差,根据NMR定量方法计算AEE对照品含量。
2.2.4 线性范围:分别准确称量AEE 3.0、6.0、9.0、12.0、15.0、18.0、21.0 mg,置于7支核磁管,并加入标准物对硝基苯9.0 mg,加入0.6 ml的氘代氯仿溶解,测定1H-NMR谱,并对样品与内标物的定量峰积峰。以AEE与对硝基苯的质量比为横坐标,以AEE和对硝基苯的积峰面积比为纵坐标,作线性回归。
2.2.5 精密度试验:将同一样品溶液连续测定5次,以AEE的不同定量峰(δ=3.901、2.294)与内标物的定量峰(δ=8.412)积分面积的比值计算RSD值。
2.2.6 重复性试验:平行制备测试溶液5份,测定1H-NMR,按方法中的公式计算AEE的含量,并计算RSD值。
2.2.7 稳定性试验:设内标物定量峰峰面积为100,在1、2、3、4、5 d分别测定样1H-NMR谱,计算样品峰的峰面积的RSD值。
3 结果
通过液相色谱测定AEE对照品的纯度,测定结果除了主峰以外,无其他杂质峰,按峰面积归一化法处理,纯度为100%,见图2。据干燥失质量法测定水分与挥发性物质的质量百分比为0.13%(n=8)。炽灼残渣法测定金属氧化物或其硫酸盐含量为0.0475%(n=8)。分别代入公式计算AEE对照品含量=100%×(1-0.13-0.0475)×100%=99.82%。NMR法以AEE的定量峰(δ=2.294)与内标物的定量峰(δ=8.412)的积分面积代入实验数据,并求5次计算的平均值,计算结果为99.55%。线性回归方程Y=0.003 47+0.426 58X,回归系数R2=0.999,表明其在3~21 mg范围内线性关系良好。精密度试验结果显示,以AEE的不同定量峰(δ=3.901、2.294)与内标物的定量峰(δ=8.412)积分面积的比值计算RSD值均为0.04%,表示该方法精密度良好。平行测定5份样品分别计算AEE的含量,其RSD值为0.19%,表示该方法重复性良好。稳定性试验结果显示,在1、2、3、4、5 d测定样品,样品峰的峰面积RSD值为0.57%,说明AEE在5 d内稳定性良好。

1.内标物苯环氢;2.AEE甲氧基氢(—OCH3);3.AEE乙酰氧基氢(—OAc)1.Inner standard hydrogen of benzene;2.Methyoxy hydrogen of AEE(-OCH3);3.Acetoxyl hydrogen of AEE(-OAc)图2 AEE与内标物的氢谱图Fig 2 1H-NMR spectra of AEE and internal standards
4 讨论
质量平衡法是常用的进行含量测定的方法之一,具有简单方便、结果可靠的优点。NMR法主要在于内标物的选择、溶剂与定量峰的选择、仪器参数的选择。(1)NMR定量分析常用的内标物有:1,4-二硝基苯、对苯二甲酸二甲酯、马来酸、富马酸等。综合考虑,1,4-二硝基苯作为内标物,苯环上的4个氢为单峰,其化学位移δ=8.41,能与样品峰很好地分离,且不与样品发生反应,故选择1,4-二硝基苯为内标物。(2)常用的氘代试剂有重水、二甲基亚砜、氘代氯仿、氘代甲醇等。实验过程选择氘代氯仿作为溶剂,该试剂对样品和内标物都有很好的溶解性,且氘代氯仿的溶剂峰化学位移δ=7.26,不干扰内标和样品的定量峰,不影响实验结果。(3)AEE的氢谱归属δ为7.15~8.24(4H,m,C6H4)、6.79~7.05(3H,m,C6H3)、5.92~6.02(1H,m,—CH=)、5.09~5.15(2H,m,=CH2)、3.80(3H,s,OCH3)、3.39(2H,d,—CH2—)、2.29(3H,s,OAc)。定量峰优先选择含有多个氢的单峰,故选择δ=3.80(OCH3)与δ=2.29(OAc)作为定量峰,两者测定结果基本相同,故选择δ=2.29的峰作为定量峰。(4)设定准确的弛豫时间Dl,确保所有的信号被检测到,保证积分的正确性,对实验测定结果的准确性有重大意义。据文献报道,Dl应>5倍的纵向弛豫时间(T1)。使用不同Dl值试验其对积分面积大小的影响,结果选择D1=15 s。(5)对NMR法定量测定AEE含量的方法进行了方法学研究,考察了方法的线性范围、精密度、重复性及稳定性。结果显示,该方法简便易行、精密度高|重复性好。
综上所述,本研究通过质量平衡法和NMR法等2种不同定值方法对AEE对照品的含量进行了测定。实验结果证明,质量平衡法和NMR法测定结果基本一致,两者互相佐证能更好地确定AEE对照品含量的准确性。本研究中AEE含量的确定为今后制定其原料药及制剂的质量标准提供了基础,也为其他新物质对照品的定值提供了相关依据。
[1]叶得河,于远光,李剑勇,等.阿司匹林丁香酚酯的高效解热作用及作用机制[J].中国药理学与毒理学杂志,2011,25(2):151-155.
[2]李剑勇,王棋文,于远光,等.阿司匹林丁香酚酯的抗炎作用及其可能的作用机制[J].中国药理学与毒理学杂志,2011,25(1):57-61.
[3]李玲,吴蓝鸥,刘伟平,等.阿司匹林铜镇痛活性及毒副作用研究[J].昆明医学院学报,1996,17(4):1-3.
[4]高建军.肠溶阿司匹林致急性黄疸型肝损害1例报告[J].职业与健康,2004,20(4):109.
[5]张秋霞,王玉玲.小剂量肠溶阿司匹林致肾损害16例分析[J].药物不良反应杂志,2004,6(2):82-84.
[6]吕世明,陈杖榴,陈建新,等.丁香酚体外抑菌作用研究[J].食品科学,2008,29(9):122-124.
[7]孔晓军,刘希望,李剑勇,等.丁香酚的药理学作用研究进展[J].湖北农业科学,2013,52(3):508-511.
[8]王棋文,李剑勇,牛建荣,等.炎毒热清及其微乳制剂小鼠急性毒性试验和体外抑菌作用[J].安徽农业科学,2008,36(36):15912-15914.
[9]冯艳春,刘书好,胡昌勤.比阿培南标准物质的研制[J].中国抗生素杂志,2010,35(9):679-683.
[10] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:103,105.
[11] 周晓力,陈华,南楠.1H NMR定量测D3吗啡对照品的含量[J].药物分析杂志,2015,35(5):906-909.
[12] 张琪,朱红波,吴先富,等.邻苯二甲酸酯类标准物质核磁共振定量方法的建立[J].药物分析杂志,2015,35(7):1287-1291.
[13] 刘静,胡晓茹,王明娟,等.金丝桃苷对照品的定值研究[J].药物分析杂志,2015,35(3):524-527.
[14] Li JY,Yu YG,Wang QW,et al.Synthesis of aspirin eugenol ester and its biological activity[J].Med Chem Res,2011,21(7):995-999.
Content Determination of Aspirin Eugenol Ester Reference Substance by Two Measuring MethodsΔ
YANG Qingqing1, LIU Xiwang2, YANG Yajun2, LI Jianyong2, ZHA Fei1
(1. College of Chemistry and Chemical Engineering, Northwest Normal University,Gansu Lanzhou 730070, China; 2.Key Laboratory of New Animal Drug Project, Gansu Province; Key Laboratory of Veterinary Pharmaceutical Development, Ministry of Agriculture; Lanzhou Institute of Husbandry and Pharmaceutical Sciences of CAAS,Gansu Lanzhou 730050, China)
OBJECTIVE:To determine the content of aspirin eugenol ester(AEE) reference substance by by the mass balance method and the nuclear magnetic resonance(NMR) method. METHODS: Chromatogram purity was determined by HPLC, the moisture and volatile substance were determined by weightlessness method and inorganic impurities was determined by the residue on ignition method. The content of AEE reference substance was calculated by the mass balance method. NMR quantification method for AEE was established with determine temperature of 25 ℃, scan times of 16 and the relaxation delay time of 15 s respectively. RESULTS: The results of content determination were 99.82% by the mass balance method and 99.55% by the NMR method.Fitting line between peak area ratio and weight ratio of sample AEE to inner standard(1,4-dinitrobenzene) ranged from 3 mg to 21 mg with correlative coefficient of 0.999. Method validation of the NMR about the precisionRSDwas 0.04%(n=5)and the repeatabilityRSDwas 0.19%(n=5)and the stability ofRSDwas 0.57%. CONCLUSIONS: Two methods can verify each other and the determination results are basically identical.
Mass balance method; NMR method; Reference substance; Aspirin eugenol ester; Aspirin
中国农业科学院科技创新工程(No.CAAS-ASTIP-2014-LIHPS-02)
R927.2
A
1672-2124(2016)11-1466-03
2016-08-22)
*硕士研究生。研究方向:现代分离分析技术。E-mail:1327571141@qq.com
#通信作者1:研究员,博士。研究方向:兽药的研究与开发。E-mail:lijy1971@163.com
#通信作者2:教授,博士。研究方向:环境与能源化工、现代分离分析技术。E-mail:zhafei@nwnu.edu.cn
DOI 10.14009/j.issn.1672-2124.2016.11.007
