一种含末端炔基的手性亚磷酰胺酯配体的合成
2016-12-14欧阳华杨逸钒董新荣
欧阳华,杨逸钒,董新荣,张 凤
(湖南农业大学理学院,湖南 长沙 410128)
一种含末端炔基的手性亚磷酰胺酯配体的合成
欧阳华,杨逸钒,董新荣,张 凤
(湖南农业大学理学院,湖南 长沙 410128)
手性亚磷酸酰胺酯配体在不对称催化反应中有着广泛的应用。末端带官能团的手性亚磷酰胺酯配体的合成却很少有报道。以炔丙基溴、对羟基苯甲醛、S-BINOL为原料通过烷基化,亲核加成-消除,还原以及膦酰化反应以较高收率制得含炔键的手性亚磷酰胺酯配体。目标产物经过了1H NMR、13C NMR、31P NMR、LC-MS表征。为探讨该类配体以及“点击化学方法”负载手性催化剂在不对称催化反应中的应用研究奠定了基础。
不对称催化;合成;手性亚磷酸酰胺酯配体;末端炔基
虽然早在1968年,Knowles[1]和Horner[2]就将单膦配体应用于不对称催化氢化反应中,但是很快被以BINAP等为代表的双膦配体的巨大成功所湮没。直到20世纪90年代,人们对单膦配体[3]才有了重新认识,并在不对称催化反应中有了广泛的应用。与双膦配体相比,单膦配体具有易于合成、结构灵活多样、改造简便,催化性能优异等优点[4]。亚磷酰胺酯配体是众多优秀手性单膦配体研究最多的,已在不对称氢化[5]、硅氢化[6]、烯丙基取代[7]和共轭加成[8]等不对称催化反应中表现出高活性及选择性,成为不对称催化领域中一个新的研究热点。虽然目前有成千上万的手性亚磷酸酰胺酯配体被合成出来,但是末端带官能团的手性亚磷酸酰胺酯配体的合成却很少有报道。本论文从价廉易得的炔丙基溴、对羟基苯甲醛及(S)-BINOL等出发,得到末端炔基修饰的手性亚磷酸酰胺酯配体,目标配体见图1。

图1 目标化合物的结构
1 实 验
1.1 主要试剂和仪器
炔丙基溴、对羟基苯甲醛、丙酮、苄胺、碘化钾、碳酸钾、
二氯甲烷、硫酸镁、四氢铝锂、四氢呋喃、三氯化磷、甲苯、N-甲基吡咯烷酮等均为化学纯,均购自于国药集团化学试剂有限公司。二氯甲烷、三乙胺、四氢呋喃、甲苯使用前需作无水处理,其它试剂直接使用。
Bruker Advance 400 MHz核磁共振波谱仪,德国Bruker以期有限公司;FA 2400 精密天平,上海民桥精密科学仪器有限公司;DF-101S恒温加热磁力搅拌器, 河南省巩义予华仪器有限公司。
1.2 合成路线
首先以4-羟基苯甲醛为原料, 通过与以炔丙基溴的醚化得到炔丙氧基苯甲醛,随后与苄胺反应生成席夫碱,经过四氢铝锂还原得到炔丙基功能化的仲胺。仲胺与联二萘骨架的氯膦经过膦酰化反应制得含炔键的单膦配体。目标产物的合成路线如图2所示。
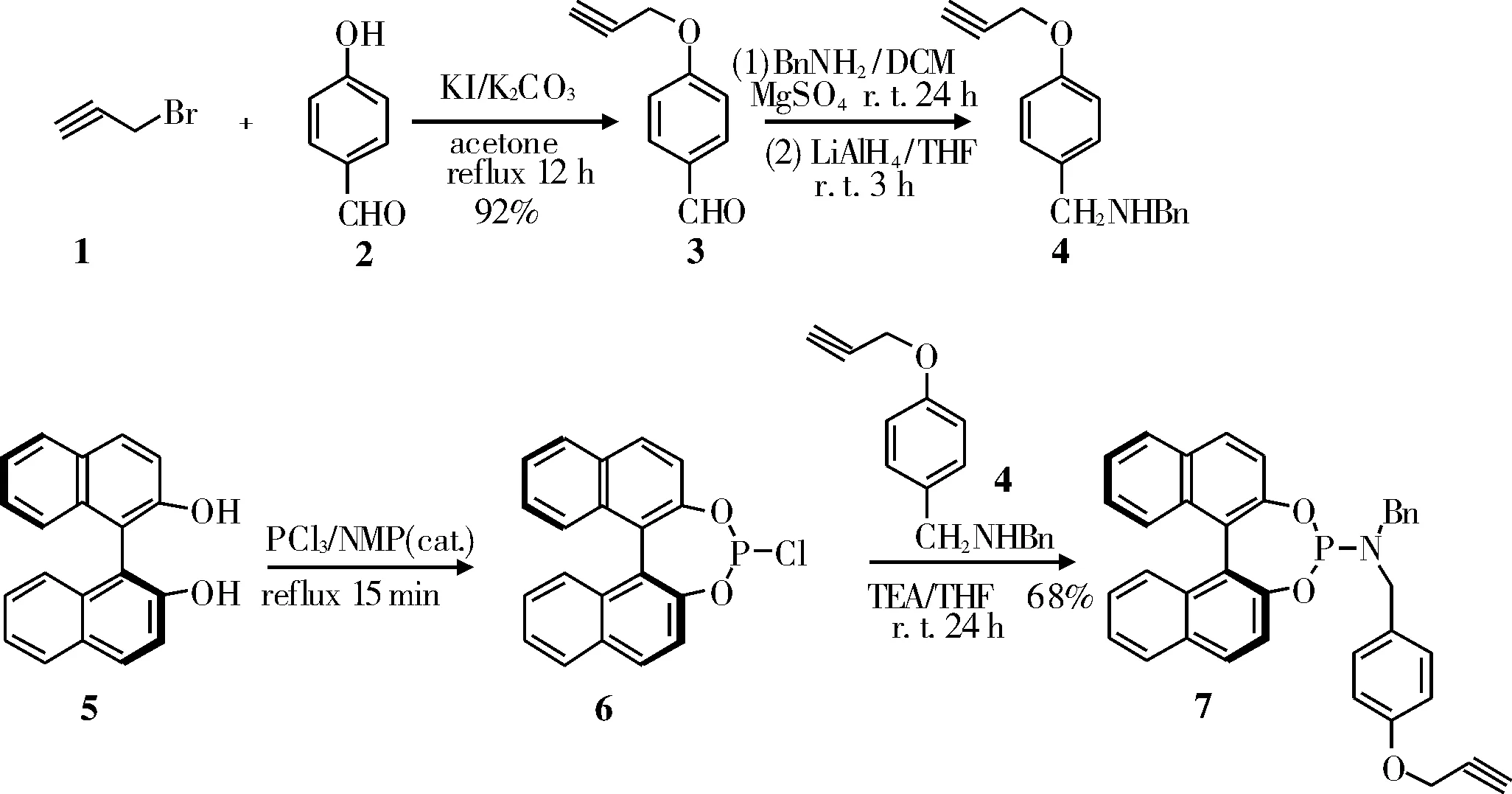
图2 目标产物的合成路线
1.3 合成方法
1.3.1 4-羟基苯甲醛的烷基化反应[9]
干燥的100 mL 圆底烧瓶中依次加入4-羟基苯甲醛1(2.08 g,16.4 mmol,1 eq)、碳酸钾(6.80 g,49.2 mmol,3 eq)、碘化钾(8.17 g,49.2 mmol,3 eq)及丙酮50 mL,回流1 h后,冷至室温,加入炔丙基溴 2(1.75 mL,19.7 mmol,1.2 eq),继续回流6 h,TLC 跟踪反应,冷却至室温,过滤,减压脱除溶剂,分液,水相用3×100 mL二氯甲烷萃取,合并有机相,硫酸钠干燥后,再次减压脱除溶剂,真空干燥得淡黄色产品3 2.41 g, 产率为92%, 熔点为77~79 ℃。1H NMR (400 MHz, CDCl3): δ (ppm)=2.56~2.57 (t,J=2.4 Hz, 1H), 4.77~4.78 (d,J=2.4 Hz, 2H), 7.06~7.10 (m, 2H), 7.83~7.87 (m, 2H), 9.89 (s, 1H);13C NMR (100 MHz, CDCl3): δ (ppm)=56.0, 76.4, 76.7, 77.0, 115.2, 130.6, 131.9, 162.4, 190.8。
1.3.2 炔丙基功能化的仲胺4的合成[10]
干燥的100 mL 圆底烧瓶中依次加入3 (1.60 g,10 mmol,1 eq)、苄胺(1.07 g,10 mmol,1 eq)、硫酸镁(3.60 g,30 mmol,3 eq)及重蒸二氯甲烷50 mL,室温反应24 h,TLC 跟踪反应。过滤, 分液,水相用3×100 mL二氯甲烷萃取,合并有机相,硫酸钠干燥后,减压脱除溶剂,所得产物(未经纯化)用50 mL重蒸后的四氢呋喃溶解,冰浴下分批加入四氢铝锂(0.57 g,15 mmol),室温下反应3 h,TLC 跟踪反应。加入饱和氯化铵焠灭多余的四氢铝锂,过滤,减压脱除溶剂, 分液,水相用3×100 mL二氯甲烷萃取,合并有机相,硫酸钠干燥后,再次减压脱除溶剂,真空干燥得1.95 g淡黄色液体4,产率为78%。1H NMR (300 MHz, CDCl3): δ (ppm)=1.75 (s, 2H), 2.52 (s, 1H), 3.76 (s, 2H), 3.81 (s, 2H), 4.69 (s, 2H), 6.94~6.96 (d,J=6.3 Hz, 2H),7.27~7.29 (d,J=6.0 Hz, 3H), 7.34~7.35 (d,J=3.0 Hz, 3H);13C NMR (100 MHz,CDCl3): δ (ppm)=52.4, 53.1, 55.9, 75.4, 76.7, 77.0, 78.7, 114.9, 127.0, 128.2, 128.2, 128.4, 129.4, 129.6, 133.3, 140.2, 156.6。1.3.3 末端含炔键的手性亚磷酸酰胺酯7的合成[11]
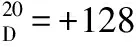
2 讨 论
合成过程中第一步为4-羟基苯甲醛与炔丙基溴的烷基化反应,该反应中投料比很重要。我们采取炔丙基溴与4-羟基苯甲醛的投料比为1.2时,收率高,且纯化容易,仅需真空干燥便可得纯产品,无需柱层析分离。
第二步生成席夫碱的反应中,可以采用甲苯作为溶剂,反应体系生成的水分通过分水器除去。我们通过调研文献,采用二氯甲烷作溶剂,体系生成的水用无水硫酸钠吸收的方法,操作更为简单,且副产物少。席夫碱用四氢铝锂还原得到炔丙基功能化的仲胺。该反应过程中要注意:(1)席夫碱要先用四氢呋喃溶解,然后在冰浴下分批加入四氢铝锂,否则容易出安全事故;(2)应根据TLC分析跟踪反应进程,反应时间过长可导致副产物增多,分离提纯困难;(3)后处理过程中,用饱和氯化铵焠灭多余的四氢铝锂的方法(比酸或碱处理)现象更为明显,操作更为简单。
仲胺与联二萘骨架的氯膦经过膦酰化反应制得含炔键的单膦配体是合成末端炔基修饰的手性亚磷酸酰胺酯配体最关键步骤。这步成功与否取决于:(1)反应试剂(三氯化磷、N-甲基吡咯烷酮、甲苯、三乙胺、四氢呋喃等)必须经过无水处理;(2)反应在惰性气体保护下进行;(3)多余的三氯化磷必须除去;(4)柱层析溶剂(二氯甲烷、石油醚)需无水无氧处理,采用100~200目硅胶于无水无氧下进行柱色谱分离。
3 结 论
由于手性亚磷酸酰胺酯在不对称催化反应中取得了较好的催化性能,本文从价廉易得的4-羟基苯甲醛、炔丙基溴和S-BINOL出发,经历三步反应,以较高收率合成了末端炔基修饰的手性亚磷酸酰胺酯配体。目标产物经过了1H NMR、13C NMR、31P NMR、LC-MS等表征,为探讨该类配体以及“点击化学方法”负载[12]手性催化剂在不对称催化反应中的应用研究奠定了基础。
[1] Knowles W S, Sabacky M J. Catalytic asymmetric hydrogenation employing a soluble, optically active, rhodium complex [J]. Chem. Commun. (London), 1968: 1445-1446.
[2] Horner L, Siegel H, Büthe H. Asymmetric catalytic hydrogenation with an optically active phosphinerhodium complex in homogeneous solution [J]. Angew. Chem. Int. Ed., 1968, 7: 942.
[3] Uozumi Y, Hayashi T. Catalytic asymmetric synthesis of optically active 2-alkanols via hydrosilylation of 1-alkenes with a chiral monophosphine-palladium catalyst [J]. J. Am. Chem. Soc., 1991, 113 (26): 9887-9888.
[4] Ansell J, Wills M. Enantioselective catalysis using phosphorus-donor ligandscontaining two or three P-N or P-O bonds [J]. Chem. Soc. Rev., 2002, 31: 259-268.
[5] Minnaard A J, Feringa B L, Lefort L, et al. Asymmetric hydrogenation using monodentate phosphoramidite ligands [J]. Acc. Chem. Res., 2007, 40(12): 1267-1277.
[6] Feng Zhang, Qing-Hua Fan. Synthesis and application of bulky phosphoramidites: highly effective Monophosphorus ligands for asymmetric hydrosilylation of styrenes [J]. Org. Biomol. Chem., 2009, 7: 4470-4474.
[7] López F, Ohmura T, Hartwig J F. Regio- and enantioselective iridium-catalyzed intermolecular allylic etherification of achiral allylic carbonates with phenoxides [J]. J. Am. Chem. Soc., 2003, 125(12): 3426-3427.
[8] Boiteau J G, Imbos R, Minnaard A J, et al.Rhodium-catalyzed asymmetric conjugate additions of boronic acids using monodentate phosphoramidite ligands [J]. Org. Lett., 2003, 5 (5): 681-684.
[9] Ge Z, Hu J, Huang F, et al. Responsive supramolecular gels constructed by crown ether based molecular recognitio [J]. Angew.Chem. Int. Ed. 2009, 48: 1798-1802.
[10]Giguère J B, Thibeault D, Cronier F, et al. Synthesis of [2]- and [3]rotaxanes through Sonogashira coupling [J]. Tetrahedron Letters, 2009, 50(39):5497-5500.
[11]Korostylev A, Gridnev I, Brown J M. Mechanistic and synthetic aspects of hydroboration with a simple atropisomeric ligand prepared from 1-(1′-(isoquinolyl)-2-naphthol, [J]. J. Organomet. Chem., 2003, 680: 329-334.
[12]Wu L, Zhang X, Tao Z M. A mild and recyclable nano-sized catalyst for the stille reaction in water [J]. Catal. Sci. Technol., 2012, 2: 707-710.
Synthesis of An Alkynyl-terminated Chiral Phosphoramidite
OUYANGHua,YANGYi-fan,DONGXin-rong,ZHANGFeng
(Collage of Science, Hunan Agricultural University, Hunan Changsha 410128, China)
Chiral phosphoramidites are widely used in asymmetric catalysis. However, there are few reports on functional groups, such as terminated chiral phosphoramidites. Alkynyl-terminated chiral phosphoramidite was obtained from propargyl bromide, 4-hydroxybenzaldehyde and S-BINOL via alkylation,nucleophilic addition-elimination,reduction and phosphorylation reactions with high yields. The target product was characterized by1H NMR,13C NMR,31P NMR and LC-MS. This work laid the foundation for the application of the ligand and supported chiral catalysts via“click chemistry”method.
asymmetric catalysis; synthesis; chiral phosphoramidite; alkynyl-terminated
湖南农业大学大学生创新实验计划项目(No:2016ZK30);湖南农业大学青年基金项目(No:15QN10);湖南省自科基金青年基金(No:14JJ3091);国家自科基金青年基金(No:21302051)。
欧阳华(1992-),女,硕士研究生,主要方向为不对称催化。
张凤(1982-),女,博士,硕士生导师,主要研究方向为有机合成方法学和不对称催化。
O621.3
A
1001-9677(2016)022-0027-03
