GC-MS结合保留指数分析聚苯乙烯发泡餐盒中化学成分
2016-12-07宋雪超林勤保吴宇梅王志伟
宋雪超,林勤保,*,方 红,吴宇梅,王志伟
(1.暨南大学包装工程研究所,广东普通高校产品包装与物流重点实验室,广东 珠海 519070;2.深圳出入境检验检疫局,广东 深圳 518000)
GC-MS结合保留指数分析聚苯乙烯发泡餐盒中化学成分
宋雪超1,林勤保1,*,方 红2,吴宇梅1,王志伟1
(1.暨南大学包装工程研究所,广东普通高校产品包装与物流重点实验室,广东 珠海 519070;2.深圳出入境检验检疫局,广东 深圳 518000)
采用正己烷超声提取发泡餐盒中的化学物质,经气相色谱-质谱法分析,在NIST质谱检索库检索的基础上,结合保留指数对化学物进行定性分析,再用峰面积归一法确定各个物质的含量。3 种发泡餐盒分别分离出35、39、38 种化学成分,分别确定了其中25、27、23 种物质,大都为含有苯环的有毒有害物质,相对标准偏差在2.26%~6.06%之间。本方法提高了定性分析的准确性和效率,可为发泡餐盒成分分析提供参考。
气相色谱-质谱联用;保留指数;聚苯乙烯发泡餐盒;定性
由聚苯乙烯为主要原料制成的发泡餐盒具有密度小、体积大、易存放等特点,加工工艺简便,价格低廉,因此广泛应用于快餐行业。但发泡餐盒在高温条件下会释放出苯乙烯单体、芳香族化合物和加工过程中加入的增塑剂、抗氧化剂等,对消费者健康构成直接威胁[1-8]。因此对于发泡餐盒中化学物质全面的定性就显得尤为重要。
发泡餐盒化学成分非常复杂。目前,国内对于发泡餐盒的研究较少,国际上对于发泡餐盒的安全性研
究集中在20世纪90年代,已取得较大的进展。例如,Abrantes[9]采用气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)对用于牛奶包装的聚苯乙烯塑料中的低聚物进行定性,共鉴定出包括苯乙烯在内的20 种化合物。Verzera等[10]利用顶空固相微萃取联合快速GC法检测聚苯乙烯包装材料中有害物质向酸奶中的迁移量。Khaksar等[11]研究了通用聚苯乙烯和耐冲性聚苯乙烯中苯乙烯单体向茶、牛奶、可可牛奶等热饮料的迁移行为,研究发现热饮料的温度和脂肪含量都会影响苯乙烯的迁移。国内对于发泡餐盒的研究主要集中在苯乙烯等小分子物质的上[12-18],郑建珍等[12]用GC-MS联用技术研究了泡沫塑料中易挥发组分在不同环境温度条件下的释放行为。实验结果表明:泡沫塑料在一定温度条件下可以释放出近20 种化合物,其中绝大多数是含有苯环的有毒有害物质。林华影等[13]用GC-MS测定了聚苯乙烯在不同的温度加工条件下,释放于空气中的有害物质的种类和数量,但只重点鉴定了7 种常见物质,对于其中结构较为复杂的成分未做分析。周相娟等[14]则建立了顶空-GC-MS联用法来测定食品包装中残留乙苯、苯乙烯单体的含量。因此对发泡餐盒进行全面定性,确定其中结构较复杂的物质就很有必要。
保留指数是目前广泛使用并且被国际公认的定性指标,可以有效地区分结构上存在细微差别的同分异构体。目前,国内研究主要把保留指数定性应用到植物成分的鉴别上。例如,任恒鑫等[19]采用GC-MS对藿香挥发油进行分析,结合自动质谱退卷积定性系统和保留指数对其定性,鉴定出46 种化学成分,取得良好的鉴定结果。杨帅等[20-21]采用水蒸气蒸馏法提取白花蛇舌草和半枝莲挥发性成分,GC-MS结合保留指数分析,分别鉴定出29、41 种物质。但我国把保留指数应用在塑料成分定性上的研究少有报道。
本实验采用正己烷超声提取发泡餐盒的化学物质,为提高结果准确性,采用双柱定性的方法。以HP-5MS色谱柱为主,HP-1MS色谱柱为辅,分别对提取出的物质进行分析,在NIST质谱库检索的基础上,结合保留指数对其主要化学成分进行定性。采用峰面积归一法对HP-5MS色谱柱的总离子流图分析,得到化学成分的相对含量。该实验为全面了解发泡餐盒中化学成分并为下一步的迁移实验提供重要的参考依据。
1 材料与方法
1.1 材料与试剂
发泡餐盒 暨南大学珠海校区附近的餐饮店;正构烷烃混合对照品C7~C40(品牌:RS-Suplco) 西格玛奥德里奇(上海)贸易有限公司;二氯甲烷、乙酸乙酯天津科密欧化学试剂有限公司;甲醇、正己烷 美国Tedia试剂公司;溶剂均为色谱纯。
1.2 仪器与设备
7890A-5975C型GC-MS联用仪 美国Agilent科技有限公司;GZX-9420MBE型电热恒温鼓风干燥箱 上海博讯实业有限公司医疗设备厂;EPED-10TS超纯水器 南京易普易达科技发展有限公司;AL204电子分析天平 梅特勒-托利多仪器(上海)有限公司。
1.3 方法
1.3.1 发泡餐盒化学成分的提取
将发泡餐盒分别标注1、2、3号,每样品做3 组平行实验。用剪刀剪成(1×1)cm2左右,准确称量0.25 g试样加入到具塞三角瓶中,加入15 mL正己烷,超声提取30 min,用滤纸过滤后,再用5 mL正己烷重复上述步骤2 次,合并提取液,将其放至棕色试剂瓶中。取1.5 mL萃取液经0.45 μm有机滤膜过滤后,4 ℃贮存,待测。
1.3.2 GC条件
色谱柱:HP-5MS石英毛细管柱(30 m×0.25 mm,0.25 μm),不分流进样;色谱柱:HP-1MS石英毛细管柱(30 m×0.25 mm,0.25 μm),分流比20∶1。升温程序:40 ℃保持1 min,以5 ℃/min升至280 ℃,保持15 min;载气(He)流速1.0 mL/min;进样量1 μL。
1.3.3 MS条件
电子电离源;电子能量70 eV;离子源温度230 ℃;进样口温度280 ℃;溶剂延迟4 min;质量扫描范围m/z 50~550。
1.3.4 保留指数的计算[22]
取正构烷烃混标标准品稀释至1 mg/L,按照1.3.2节和1.3.3节实验条件分析,记录各正构烷烃保留时间,采用线性升温公式计算各组分的保留指数。

式中:RI为保留指数;tx为被测组分的保留时间/min,tn、tn+1分别为碳原子数为n和n+1的正构烷烃的保留时间/min,且tn<tx<tn+1。
2 结果与分析
2.1 萃取溶剂的选择
本实验选取甲醇、二氯甲烷、乙酸乙酯、正己烷4 种溶剂萃取剪碎的发泡餐盒,比较其萃取效果。实验发现,发泡餐盒遇二氯甲烷、乙酸乙酯发生溶胀,加入甲醇使聚合物沉淀。静置,取上清液进样分析。实验比较了甲醇、二氯甲烷-甲醇、乙酸乙酯-甲醇和正己烷的萃取效果,结果发现正己烷提取效果都要好于其他三者,故
本实验选择正己烷作为发泡餐盒的萃取剂。其中乙酸乙酯-甲醇萃取和正己烷萃取的色谱图见图1。

图1 不同萃取溶剂的总离子流图Fig. 1 Total ion chromatograms with different extraction solvents on HP-5MS column
2.2 分析方法的精密度
依照上述实验方法,做6 次平行实验,选取其中含量较高的7 种物质,计算峰面积的相对标准偏差,分别为乙苯(2.26%)、苯乙烯(4.64%)、1,3-二苯丙烷(3.33%)、顺式-1,2-二苯基环丁烷(6.06%)、2,4-二苯基-1-丁烯(2.43%)、反式-1,2-二苯基环丁烷(2.75%)、2,4,6-三苯基-1-己烯(2.33%),7 种物质峰面积的相对标准偏差在2.26%~6.06%之间,均小于10%,符合实验要求。
2.3 发泡餐盒化学成分分析结果
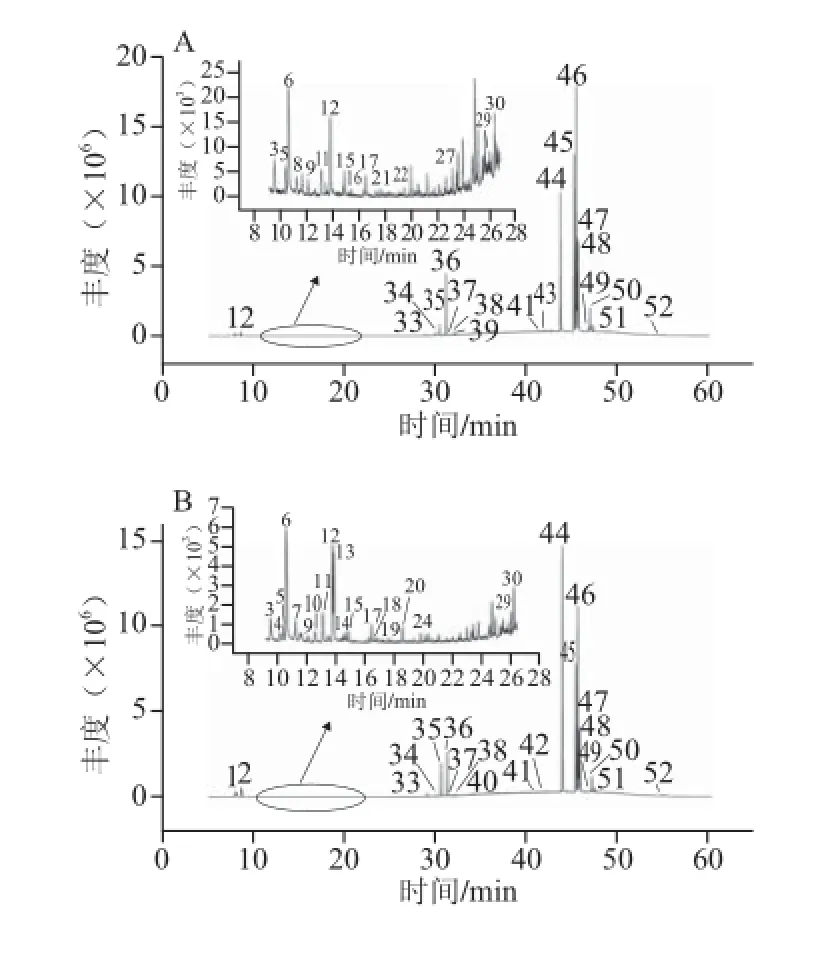

图2 发泡餐盒化学成分总离子流图Fig. 2 Total ion chromatograms of chemical compounds from polystyrene food container separated on HP-5MS column
取1.3.1节样品的萃取液,按照1.3.2节和1.3.3节实验条件对发泡餐盒成分进行GC-MS分析,其中,1、2、3号发泡餐盒的总离子流图见图2。
计算总离子图中各色谱峰的RI值,对色谱峰进行NIST谱库检索,选取匹配度较高的10 个化合物,通过网上(http://webbook.nist.gov/chemistry/)搜索文献(HP-5MS以及与其固定相相同的色谱柱,HP-1MS以及与其固定相相同的色谱柱)查得其保留指数,以质谱图和保留指数匹配度最高的化学结构为最佳鉴定结果。采用峰面积归一法估算各组分相对含量,3 次平行实验得到相对含量的平均值,结果见表1。

表1 发泡餐盒化学成分分析结果Table 1 Analytical results for the determination of chemical compounds in polystyrene food containers

续表1
由表1可知,3 种发泡餐盒分别分离出35、39、38 种化学物质,确定出其中的25、27、23 种,3 种餐盒中检测出的物质种类大体相同,都含有乙苯、苯乙烯等含苯环的烷烃、烯烃、醇、醛、酮、酯类物质,但每种物质的百分含量差别很大,以2,4,6-三苯基-1-己烯为例,3 种餐盒中的2,4,6-三苯基-1-己烯占检出物总峰面积的相对百分含量分别为15.304%、30.156%、23.857%。考虑到该物质的相对标准偏差为2.33%,样品前处理和测定方法对鉴定结果的影响很小,故生产厂家的不同是物质百分含量不同的主要原因。
3 讨 论
本实验和其他研究对比,检测出的物质也有很高的相似之处。Hathcock等[23]对工业级别的发泡聚苯乙烯定性检测,除检测出乙苯、二甲苯、苯乙酮等小分子物质外,还确定了1,3-二苯丙烷、1,4-二苯基-1,3-丁二烯等芳香族化合物,进一步验证了本实验结果的可靠性。Kusch等[24]利用固相微萃取前处理方式检测发泡聚苯乙烯中的挥发有机物质,检测得到二甲苯,二甲苯的保留时间在乙苯和苯乙烯之间,本实验中未曾出现,其原因还需进一步求证。另外,本实验中45、46、47、48号物质参考Kawawura等[25]对食品接触聚苯乙烯材料做的研究,研究指出该4 种物质为结构相似的同分异构体。
本实验中,采用HP-5MS和HP-1MS两种色谱柱定性,不仅可以提高定性的准确度,还可以实现不同色谱柱之间的互补,实现更多物质的鉴定。其原因有以下3 点:第1,对于两柱都能检测到的物质来说,实验结果可以相互证明。例如:1号峰在两种色谱柱中都有检测到,通过查阅文献,都确定其结果为乙苯,这样可以提高实验结果的准确性;第2,由于两色谱柱极性不同,对同一样品的分离效果也不同。例如:HP-5MS色谱柱对45~48四种物质有效的分离开,但HP-1MS却只分离出3 个峰,故实验结果会采用前者;第3,由于保留指数库的不完善,并不是所有的物质都可以查到HP-5MS或HP-1MS色谱柱下的保留指数。例如:36号峰检索结果中有反式-1,2-二苯基环丁烷,通过检索,该物质只有在SE-30(此色谱柱固定相与HP-1MS相同)下有参考保留指数,为1 720,故只能由HP-1MS得到鉴定结果。
4 结 论
本实验采用GC-MS结合保留指数分析发泡餐盒化学成分,结果3 种发泡餐盒分别分离出35、39、38 种化学物质,确定出其中25、27、23 种物质,物质种类相差不大,含量有很大区别。研究结果为揭示发泡餐盒化学成分构成提供理论依据,为下一步发泡餐盒中有害物质的迁移实验提供参考。
[1] GARRIGOS M C, MARIN M L, CANTO A, et al. Determination of residual styrene monomer in polystyrene granules by gas chromatography-mass spectrometry[J]. Journal of Chromatography A, 2004, 1061(2): 211-216. DOI:10.1016/j.chroma.2004.10.102.
[2] REINAS I, OLIVEIRA J, PEREIRA J, et al. Migration of two antioxidants from packaging into a solid food and into Tenax[J]. Food Control, 2012, 28(2): 333-337. DOI:10.1016/j.foodcont.2012.05.023.
[3] GUART A, BONO-BLAY F, BORRELL A, et al. Migration of phthalates, alkylphenols, bisphenol A and di(2-ethylhexyl)adipate from food packaging[J]. Food Control, 2012, 27(1): 132-138. DOI:10.1016/ j.foodcont.2012.03.005.
[4] IOANNIS S A, LOULOUDA B. Migration of substances from food packaging materials to foods[J]. Critical Reviews in Food Science and Nutrition, 2004, 44(2): 63-76. DOI:10.1080/10408690490424621.
[5] 秦蓓. 塑料食品包装材料安全性研究现状[J]. 包装工程, 2011, 32(19): 33-37; 42.
[6] CHOI J O, CHOI J O, ASAKAWA F, et al. Migration of styrene monomer, dimers and trimers from polystyrene to food simulants[J]. Food Additives and Contaminants, 2005, 22( 7): 693-699. DOI:10.1080/02652030500160050.
[7] KAWAMURA Y, KAWAMURA M, TAKEDA Y, et al. Determination of styrene dimers and trimers in food co ntact polystyrene[J]. Journal of the Food Hygienic Society of Japa n, 1998, 39(3): 199-205.
[8] GENNARI O, ALBRIZIO S, MONTEIRO M. A GC-FID method to determine styrene in polystyrene glasses[J]. Food Analytical Methods, 2012, 5(6): 1411-1418. DOI:10.1007/s12161-012-9395-5.
[9] ABRANTES S. GC-MS identification of styrene and oligomers in polystyrene plastic for milk packaging[J]. Journal of High Resolution Chromatography, 1993, 16(2): 113-115. DOI:10.1002/ jhrc.1240160209.
[10] VERZERA A, CONDURSO C, ROMEO V, et al. Solid-phase microextraction coupled to fast gas c hromatography for the determination of migrants from polystyrene-packaging materials into yoghurt[J]. Food Analytical Methods, 2010, 3(2): 80-84. DOI:10.1007/ s12161-009-9088-x.
[11] KHAKSAR M R, GHAZI-KHANSARI M. Determination of migration monomer styrene from GPPS (general purpose polystyrene) and HIPS (high impact polystyrene) cups to hot drinks[J]. Toxicology Mechanisms and Methods, 2009, 19(3): 257-261. DOI:10.1080/15376510802510299.
[12] 郑建珍, 吴小琼, 刘文涵. 气相色谱-质谱联用法研究泡沫塑料中易挥发组分在环境温度下的释放行为[J]. 理化检验(化学分册), 2008, 44(8): 768-769. DOI:10.3321/j.issn:1001-4020.2008.08.023.
[13] 林华影, 张伟, 张琼, 等. 气相色谱-质谱法分析聚苯乙烯加热分解产物[J]. 中国卫生检验杂 志, 2009, 19(9): 1964-1966.
[14] 周相娟, 赵玉祺, 李伟, 等. 顶空气相色谱法同时测定食品包装中残留乙苯和苯乙烯单体[J]. 食品研究与开发, 2010, 31(10): 144-147. DOI:10.3969/j.issn.1005-6521.2010.10.044.
[15] 俞晔, 陈朝方, 刘海珍, 等. 顶空-气相色谱/质谱法测定与食品接触的聚苯乙烯塑料成型品中苯乙烯迁移量[J]. 食品安全质量检测学报, 2012, 3(2): 112-115.
[16] 朱生慧. 气相色谱法测定聚苯乙烯中残留单体苯乙烯[J]. 现代科学仪器, 2008(2): 83-85.
[17] 张文生, 宋晓涛, 武珊珊. 气相色谱法测定提取物中苯、甲苯、间二甲苯、对二甲苯、邻二甲苯和苯乙烯的残留量[J]. 药物分析杂志, 2006, 26(3): 393-395. DOI:10.16155/ j.0254-1793.2006.03.007.
[18] 王红松, 商贵芹, 刘君峰, 等. 顶空气相色谱法测定聚苯乙烯制品中的挥发性组分[J]. 检验检疫学刊, 2010, 20(3): 12-14. DOI:10.3969/ j.issn.1674-5354.2010.03.004.
[19] 任恒鑫, 张舒婷, 吴宏斌, 等. GC-MS-AMDIS结合保留指数分析藿香挥发油[J]. 食品科学, 2013, 34(24): 230-232. DOI:10.7506/ spkx1002-6630-201324048.
[20] 杨帅, 杨文文, 胡金芳, 等. GC-MS结合保留指数分析白花蛇舌草挥发性成分[J]. 中国实验方剂学杂志, 2012, 18(9): 93-95. DOI:10.3969/j.issn.1005-9903.2012.09.028.
[21] 杨帅, 杨文文, 吕青涛, 等. GC-MS结合保留指数分析半枝莲挥发性成分[J]. 现代仪器, 2012, 18(3): 47-50. DOI:10.3969/ j.issn.1672-7916.2012.03.013.
[22] 林杰, 陈莹, 施元旭, 等. 保留指数在茶叶挥发物鉴定中的应用及保留指数库的建立[J]. 茶业科学, 2014, 34(3): 261-270. DOI:10.3969/ j.issn.1000-369X.2014.03.010.
[23] HATHCOCK S L, BERTSCH W. Analysis of volatiles associated with industrial scale processing of expanded polystyrene[J]. Journal of Separation Science, 1993, 16(11): 651-659. DOI:10.1002/ jhrc.1240161106.
[24] KUSCH P, KNU PP G. Headspace-SPME-GC-MS identification of volatile organic compounds released from expanded polystyrene[J]. Journal of Polymers and the Environment, 2004, 12(2): 83-87. DOI:10.1023/B:JOOE.0000010053.20382.d7.
[25] KAWAWURA Y, SUGIMOTO N, TAKEDA Y, et al. Identifi cation of unknown substances in food contact polystyrene[J]. Journal of the Food Hygienic Society of Japan, 1998, 39(2): 110-119.
Application of GC-MS Coupled with Retention Indices to Identify the Chemical Compounds of Polystyrene Food Container
SONG Xuechao1, LIN Qinbao1,*, FANG Hong2, WU Yumei1, WANG Zhiwei1
(1. Key Laboratory of Product Packaging and Logistics, Packaging Engineering Institute, Jinan University, Zhuhai 519070, China; 2. Shenzhen Entry-Exit Inspection and Quarantine Bureau, Shenzhen 518000, China)
The chemical compounds of polystyrene food container were ultrasonically extracted with n-hexane and analyzed by gas chromatography-mass spectrometry (GC-MS) using mass spectral search in NIST library. Qualitative analysis was performed based on their retention indices (RI), and the identifi ed compounds were quantifi ed by peak area normalization method. A total of 35, 39, and 38 components were isolated, 25, 27, and 23 main components of which were identifi ed in three different polystyrene food containers, respectively, most of which were hazardous substances containing benzene ring. The relative standard derivations (RSDs) of this method were in the range of 2.26%□6.06%. This is a simple, rapid and accurate method for the analysis of volatile compounds in polystyrene food container, which can provide an effi cient approach for chemical component analysis of plastic food container.
GC-MS; retention indices; polystyrene food container; identifi cation
10.7506/spkx1002-6630-201610034
TS201.6;TS206.4
A
1002-6630(2016)10-0198-05
宋雪超, 林勤保, 方红, 等. GC-MS结合保留指数分析聚苯乙烯发泡餐盒中化学成分[J]. 食品科学, 2016, 37(10): 198-202. DOI:10.7506/spkx1002-6630-201610034. http://www.spkx.net.cn
SONG Xuechao, LIN Qinbao, FANG Hong, et al. Application of GC-MS coupled with retention indices to identify the chemical compounds of polystyrene food container[J]. Food Science, 2016, 37(10): 198-202. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201610034. http://www.spkx.net.cn
2015-07-28
国家自然科学基金面上项目(21277061;21277085);国家质量监督检验检疫总局科技计划项目(2015IK259);暨南大学优秀本科推免生科研创新培育计划项目
宋雪超(1993—),男,硕士研究生,研究方向为食品与药品包装。E-mail:2573423173@qq.com
*通信作者:林勤保(1968—),男,教授,博士,研究方向为食品与药品包装。E-mail:7899966@qq.com
