胰高血糖素样肽-1对糖尿病大鼠胰岛素敏感性及心肌微血管的保护作用
2016-12-06谢新荣赵巧玲钟慕贤黄普好
赵 妮 谢新荣 赵巧玲 钟慕贤 黄普好
(广西医科大学附属民族医院,广西 南宁 530021)
胰高血糖素样肽-1对糖尿病大鼠胰岛素敏感性及心肌微血管的保护作用
赵 妮 谢新荣 赵巧玲 钟慕贤 黄普好
(广西医科大学附属民族医院,广西 南宁 530021)
目的 探讨胰高血糖素样肽-1对糖尿病大鼠胰岛素敏感性及心肌微血管的保护作用。方法 24只成年雄性SD大鼠随机分为正常对照(NC)组(n=8)、2型糖尿病(T2DM)组(n=8)、T2DM加胰高血糖素样肽-1(GLP-1)干预组(n=8),对比GLP-1对各组大鼠葡萄糖输注率、胰岛素浓度的影响以及三组大鼠心肌微血管完整性和通透性。结果 各组大鼠的葡萄糖输注率均于60.0 min时趋向于基本稳定状态,此前T2DM+GLP-1组和T2DM组的输注率增长趋势低于NC组;在120.0 min后T2DM组葡萄糖输注率与NC组相比下降幅度约为53.0%(P<0.05);与NC组相比,T2DM+GLP-1组葡萄糖输注率有所降低,但差异无统计学意义(P>0.05);与T2DM组相比,T2DM+GLP-1组葡萄糖输注率上升约为50.8%(P<0.05),T2DM+GLP-1组葡萄糖输注率有所增高,但未上升至正常水平;实验开始时各组大鼠胰岛素水平均呈现持续上升趋势,三组大鼠间胰岛素浓度增加趋势及同一时间点胰岛素浓度均无统计学差异(P>0.05);NC组心肌微血管铸型较为平滑,且未出现明显的凹凸不平,表明无破坏发生,T2DM组心肌微血管铸型出现显著凹凸不平现象,且内皮连接完整性较差,T2DM+GLP-1组心肌微血管内皮细胞连接完整度明显优于T2DM组;NC组心肌微血管内皮细胞连接完整,未出现镧颗粒进入基底膜现象,T2DM组镧颗粒可轻易透过内皮细胞进入基底膜及其周边组织,T2DM+GLP-1组仅有少量镧颗粒进入基底膜。结论 GLP-1可改善糖尿病患者胰岛素敏感性,并对心肌微血管产生保护作用。
胰高血糖素样肽-1;糖尿病;胰岛素敏感性;心肌微血管
有学者认为分泌缺陷及胰岛素抵抗的病理机制是诱发2型糖尿病(T2DM)的重要原因〔1,2〕。因此,治疗及预防T2DM的关键在于改善胰岛素抵抗症状。人体内脂肪、肝脏等是存储与利用葡萄糖的重要脏器,这些部位胰岛素敏感性降低,会减少对葡萄糖摄取作用,发生胰岛素抵抗。心肌缺血再灌注损伤、糖尿病性心肌病的发生与心肌微血管损伤密切相关〔3〕。胰高血糖素样肽(GLP)-1不仅可改善糖尿病患者胰岛素敏感性,还可对心肌微血管发挥一定保护作用〔4〕。
1 材料与方法
1.1 实验仪器及试剂 三通管、缝合线、气管插管、止血钳、手术剪、Milli-Q超纯水系统、手术加热灯、低温离心机、MDF-382E超低温冰箱、多功能凝胶成像化学发光仪、电热恒温水浴箱、酶联免疫检测仪、血糖仪;二甲砷酸钠、硝酸镧、柠檬酸、柠檬酸三钠、胰岛素检测试剂盒、戊巴比妥钠、血糖试纸、50.0%葡萄糖注射液、抗AKt及其磷酸化抗体。
1.2 实验对象 选取24只成年雄性SD大鼠,体重180.0~200.0 g,平均(190.0±10.0)g。将24只SD大鼠随机分为正常对照组(NC组)、T2DM组、T2DM加GLP-1干预组(T2DM+GLP-1组)每组8只。将所有大鼠放入饲养室进行适应性喂养7 d,室温调至(20.0±2.0)℃,湿度控制为50.0%~60.0%。7 d后NC组继续采用普通饲料喂养,T2DM+GLP-1组及T2DM组采用高脂饲料饲养,三组大鼠均饲养1个月。
1.3 手术 大鼠腹腔注射1.2 mg/kg 5.0%戊巴比妥钠,随后将大鼠放回饲养室,待其静卧不动、掐尾无反应且四肢松弛牵拉无张力时,表明麻醉药物已生效。使其仰卧于操作台,并完全固定;在大鼠颈部正中线处行长度为1.0 cm的横向切口,分离皮下组织后充分显露气管;通过血管钳将气管一端分离出来,并将环状软骨剪开1/3左右,插入气管插管并缝合固定。通过血管钳将气管旁肌群的软组织及筋膜机进行钝性分离,直至颈动脉;将颈内动脉分离1.5 cm左右,并利用缝合线对头侧进行结扎处理;利用显微弯头镊夹起颈内动脉,型深度为1/3左右的斜形切口,将显微弯头镊插入切口并逐渐撑开;沿开口插入连接有针管的PE-50置入管,取出显微弯头镊并缝合固定;将动脉置管连接于装有戊巴比妥钠的微量注射泵。通过血管钳对颈旁肌群、颈动脉外侧皮下组织进行钝性分离处理,用镊子分离颈外静脉,对近心端通过缝合线进行结扎;用显微外科剪在血管壁行深度为1/3左右的斜形切口,向近心端插入显微外科镊,沿镊子走向将连接于注射器的PE-50置入管向内插入3.0 cm左右,随后结扎固定。另一侧置管方法与本侧相同。
1.4 动物实验方案 各组大鼠均实施高胰岛素-正葡萄糖钳夹试验。(1)T2DM组与NC组:向静脉插管中泵入胰岛素,输注速度调至3.0 mU·kg-1·min-1;2.0 min后输注葡萄糖,输注速度为3.0 μl/min,共输注120.0 min,每间隔10.0 min检测一次动脉血糖,并根据血糖水平对葡萄糖输注速度进行调整,将血糖水平维持在10.0%左右。分别于0.0、30.0、60.0、90.0、120.0 min时抽取动脉血,进行离心处理后取上清液,放入-20.0℃环境中储存备用,用以检测胰岛素水平。(2)T2DM+GLP-1组:于高胰岛素-正葡萄糖钳夹试验开始前30.0 min时开始输注GLP-1,输注速度稳定在30.0 pmol·kg-1·min-1左右,直至实验结束终止输注。其余实验过程与T2DM组及NC组相同。
1.5 血清胰岛素水平检测 采用双抗体夹心法。
1.6 心肌微血管完整性检测 选取各组大鼠,腹腔注射0.3%戊巴比妥钠进行麻醉处理,皮下注射700.0 U/kg肝素;30.0 min后剖开腹腔,主动脉内插管,并通过K-H溶液进行冲洗,注入树脂;对树脂填充组织进行热水浸泡处理,使其逐渐固化;利用蒸馏水与强碱对其进行交互漂洗,彻底清除组织,获取血管铸型;以冻干法使其干燥,随后通过扫描电镜对其进行观察。
1.7 心肌微血管通透性检测 利用Langendorff装置,通过K-H溶液对心脏进行恒压灌流,待其趋于稳定后,以硝酸镧灌流液进行20.0 min灌流处理;完成灌流后取大鼠左室前壁心肌组织,常规脱水、固定、包埋及切片处理后,于透射电镜下对样本进行观察。
1.8 统计学方法 应用SPSS19.0软件行t、χ2检验。
2 结 果
2.1 GLP-1对各组大鼠葡萄糖输注率的影响 各组大鼠的葡萄糖输注率均于60.0 min时趋向于基本稳定状态,此前T2DM+GLP-1组和T2DM组的输注率增长趋势低于NC组,表明这两组大鼠的葡萄糖摄取利用率低于正常大鼠(图1A)。在120.0 min后(钳夹试验结束),T2DM组葡萄糖输注率与NC组相比下降幅度约为53.0%左右〔(3.02±1.38)mg·kg-1·min-1、(6.51±1.72)mg·kg-1·min-1,P<0.05〕;与NC组相比,T2DM+GLP-1组葡萄糖输注率有所降低,但差异无统计学意义(P>0.05);与T2DM组相比,T2DM+GLP-1组葡萄糖输注率上升约为50.8%〔(6.08±1.74)mg·kg-1·min-1,P<0.05〕,T2DM+GLP-1组葡萄糖输注率有所增高,但未上升至正常水平。见图1。
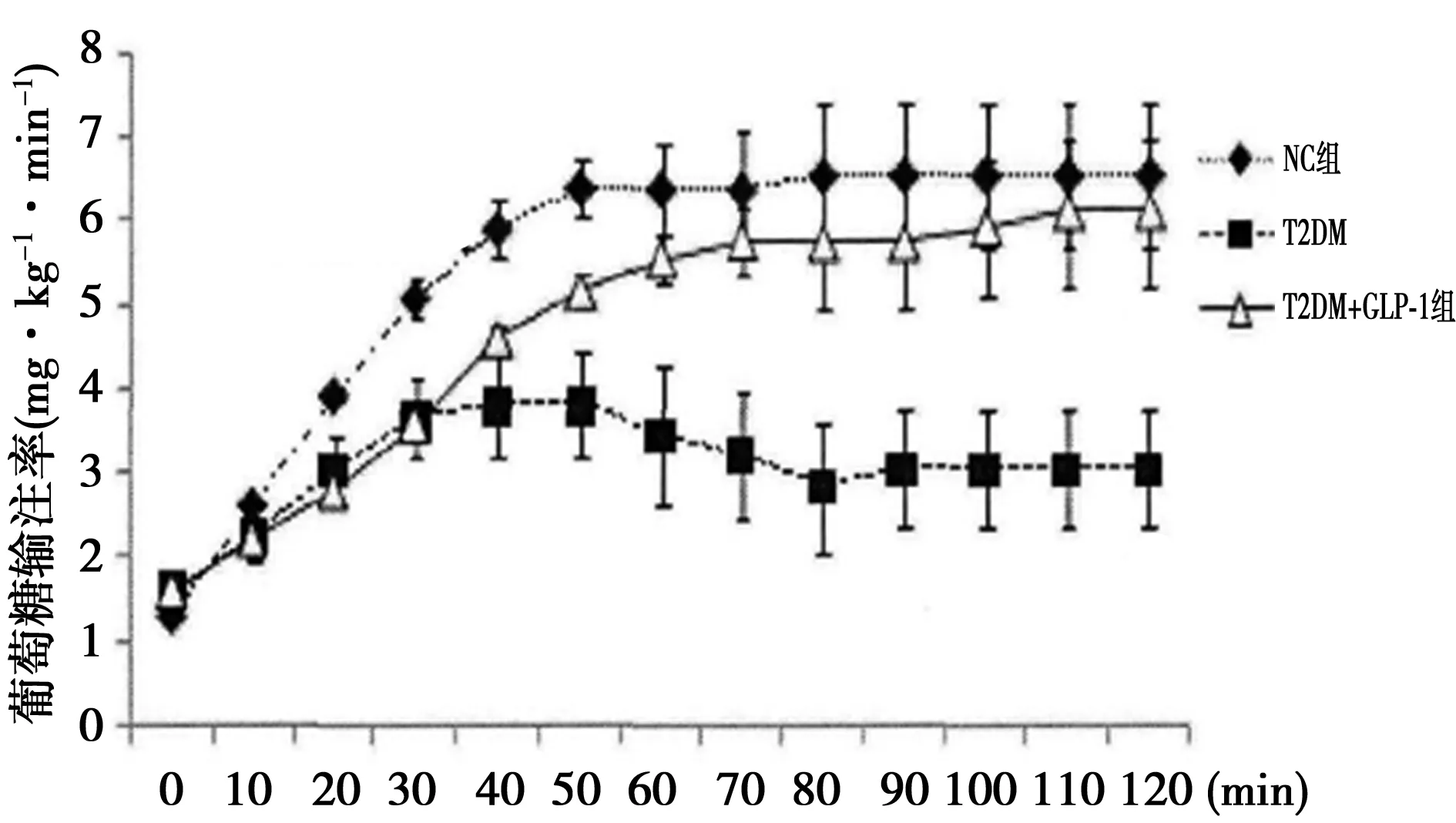
图1 GLP-1对各组大鼠葡萄糖输注率的影响
2.2 GLP-1对各组大鼠胰岛素浓度的影响 实验0.0 min及30.0 min时T2DM+GLP-1组胰岛素浓度无统计学差异(P>0.05);实验开始时各组大鼠胰岛素水平均呈现持续上升趋势,三组大鼠间胰岛素浓度增加趋势及同一时间点胰岛素浓度差异均无统计学意义(P>0.05)。见图2。

图2 三组大鼠胰岛素浓度变化
2.3 微血管铸型检测三组大鼠心肌微血管完整性 NC组心肌微血管铸型较为平滑,且未出现明显的凹凸不平,表明无破坏发生。T2DM组心肌微血管铸型出现显著凹凸不平现象,且内皮连接完整性较差。T2DM+GLP-1组心肌微血管内皮细胞连接完整度明显优于T2DM组。见图3。

图3 血管铸型三组大鼠心肌微电管完整性(×400)
2.4 电镜下观察三组大鼠心肌微血管完整性 NC组心肌微血管内皮细胞连接完整,未出现镧颗粒进入基底膜现象;T2DM组镧颗粒可轻易透过内皮细胞进入基底膜及其周边组织,表明其心肌微血管屏障功能严重下降;T2DM+GLP-1组仅有少量镧颗粒进入基底膜。见图4。
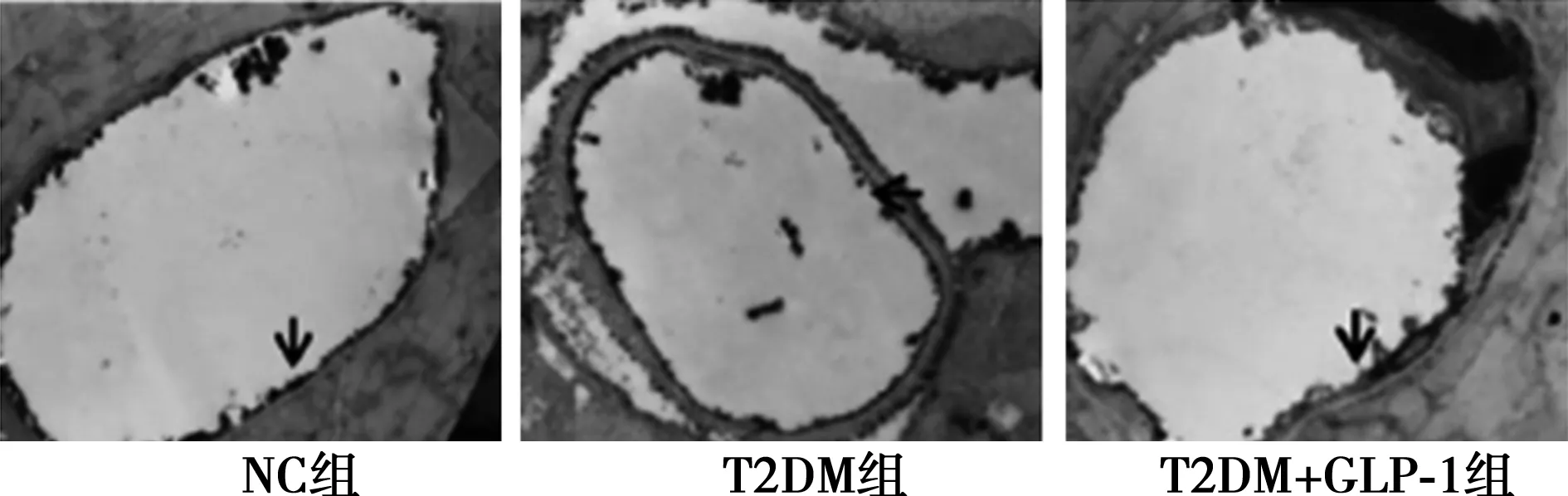
图4 电镜下观察心肌微血管(×400)
3 讨 论
糖尿病主要发病机制为胰岛素抵抗,胰岛素抵抗指外周组织对胰岛素敏感性降低,对葡萄糖的摄取利用率下降,因此改善胰岛素抵抗对提高糖尿病治疗效果具有重要意义〔5〕。与传统降糖药物相比,GLP-1生物学作用显著,且低血糖发生率低。此外,GLP-1半衰期仅为1.5 min左右,但其受体在外周神经系统、胃肠道、血管、肾、心、脑等均有分布,因此GLP-1作用范围极为广泛〔6〕。
有研究指出〔7〕,GLP-1主要通过抑制胰高血糖素分泌量及刺激胰岛素分泌发挥降糖功效。GLP-1与β细胞膜上的受体相结合,进而发挥促胰岛素分泌活性效果,且密切依赖于葡萄糖浓度。GLP-1与其受体结合后,可对G蛋白产生刺激作用,活化腺苷酸环化酶后生成cAMP,而cAMP与蛋白激酶A(PKA)对鸟嘌呤核苷酸交换因子Ⅱ的活化进行调节而引发一系列活动,如含胰岛素颗粒的胞吐作用、细胞内钙离子浓度增高、离子通道活性改变等〔8,9〕。另有研究表明〔10〕,GLP-1可对cAMP幅度及β细胞中的钙进行直接刺激调节作用,这些作用均是经葡萄糖浓度增强。GLP-1受体在葡萄糖的脂肪、肝脏和肌肉等重要摄取部位中也有一定表达,葡萄糖存储及利用的最大器官为骨骼肌,骨骼肌中分布大量微血管,确保肌纤维可获取充足能力。有研究发现〔11〕,对正常SD大鼠注射胰岛素后,骨骼肌葡萄糖摄取率得到抑制。钳夹试验时,通过对葡萄糖输注率不断调节以及不断泵入高浓度胰岛素可将血糖水平维持与基本水平,而GLP-1对β细胞产生的促胰岛素释放功效主要依赖葡萄糖浓度的升高,因此未升高的血糖水平不会导致GLP-1对β细胞分泌胰岛素产生刺激作用。此外,T2DM组心肌微血管完整性及通透性较差,而经GLP-1处理的T2DM+GLP-1组心肌细胞结构完整性与通透性得到了显著改善,接近于NC组。临床学者认为〔12〕,GLP-1对心血管具有保护作用,可改善内皮功能、缓解缺血再灌注损伤。综上,胰高血糖素样肽-1可改善糖尿病患者胰岛素敏感性,并对心肌微血管产生保护作用。
1 郭 雯,李 杰,欣 冰,等.血脂水平对胰岛功能的影响在2型糖尿病和正常人群中存在差异〔J〕.中华内分泌代谢杂志,2015;31(7):599-600.
2 王苑菲,陈立勇,赵家军.葡萄糖依赖性促胰岛素释放肽与糖尿病及肥胖〔J〕.中华内分泌代谢杂志,2015;31(8):735-8.
3 刘 畅,赵江涛,刘士超,等.胰高血糖素样肽-1对原发性高血压大鼠心肌微血管损伤的保护作用〔J〕.中华实验外科杂志,2015;32(12):3086-8.
4 Park S,Hong SM,Ahn IS.Exendin-4 and exercise improve hepatic glucose homeostasis by promoting insulin signaling in diabetic rats〔J〕.Metabolism,2010;59(1):123-33.
5 Asmar M,Holst JJ.Glucagon-like peptide 1 and glucose-dependent insulinotropic polypeptide:new advances〔J〕.Curr Opin Endocrinol Diabetes Obes,2010;17(1):57-62.
6 Simonis-Bik AM,Nijpels G,van Haeften TW.Gene variants in the novel type 2 diabetes loci CDC123/CAMK1D,THADA,ADAMTS9,BCL11A,and MTNR1B affect different aspects of pancreatic beta-cell function〔J〕.Diabetes,2010;59(1):293-301.
7 邵珠林,黄梁浒,陈 晨,等.胰高血糖素样肽1受体激动剂和脐带间充质干细胞联合治疗对2型糖尿病大鼠糖代谢和胰岛分泌功能的作用〔J〕.中华糖尿病杂志,2015;7(12):735-40.
8 Tomas E,Stanojevic V,Habener JF.GLP-1 (9-36) amide metabolite suppression of glucose production in isolated mouse hepatocytes〔J〕.Horm Metab Res,2010;42(9):657-62.
9 Gardiner SM,March JE,Kemp PA,etal.Possible involvement of GLP-1(9-36) in the regional haemodynamic effects of GLP-1(7-36) in conscious rats〔J〕.Br J Pharmacol,2010;161(1):92-102.
10 Aoki K,Miyazaki T,Nagakura J,etal.Effects of pre-meal versus post-meal administration of miglitol on plasma glucagon-like peptide-1 and glucose dependent insulinotropic polypeptide levels in healthy men〔J〕.Endocr J,2010;57(8):673-7.
11 Laudes M,Oberhauser F,Schulte DM,etal.Dipeptidyl-peptidase 4 and attractin expression is increased in circulating blood monocytes of obese human subjects〔J〕.Exp Clin Endocrinol Diabetes,2010;118(8):473-7.
12 金军华,宫 环,张恩毅,等.胰高血糖素样肽1通过调控葡萄糖调节蛋白78表达改善高糖及波动性高糖诱导的内皮细胞内质网应激及凋亡〔J〕.中华糖尿病杂志,2015;7(11):684-8.
〔2015-12-11修回〕
(编辑 袁左鸣)
赵 妮(1979-),女,硕士,主治医师,主要从事内分泌代谢性疾病研究。
R587
A
1005-9202(2016)21-5267-03;
10.3969/j.issn.1005-9202.2016.21.023
