小清咽颗粒的高效液相色谱指纹图谱研究Δ
2016-12-05朴春梅韩云霞李丽凤
杨 亮,朴春梅,韩云霞,代 欣,李丽凤
(1.贵阳中医学院第二附属医院药学部,贵州 贵阳 550001; 2.贵阳中医学院药学系,贵州 贵阳 550025)
小清咽颗粒的高效液相色谱指纹图谱研究Δ
杨 亮1*,朴春梅1,韩云霞1,代 欣1,李丽凤2
(1.贵阳中医学院第二附属医院药学部,贵州 贵阳 550001; 2.贵阳中医学院药学系,贵州 贵阳 550025)
目的:采用高效液相色谱法(High performance liquid chromatography,HPLC)对小清咽颗粒进行指纹图谱研究。方法:色谱柱为迪马Diamonsil Plus C18(250 mm×4.6 mm,5 μm),流动相为乙腈-0.1%磷酸溶液,检测波长为266 nm,柱温为30 ℃,流速为1.0 ml/min。结果:10批小清咽颗粒的HPLC指纹图谱有10个共有峰,相似度>0.950,整体相似性好。结论:本研究建立的小清咽颗粒指纹图谱的特征性和专属性强,且方法简便、稳定、重复性好,可为小清咽颗粒质量控制提供依据。
小清咽颗粒; 高效液相色谱; 指纹图谱; 相似度
小清咽颗粒是由桑叶[1-2]、射干[3]、玄参[4]等6味中药饮片提取、精制而成的医院制剂[5],具有滋阴润肺、消肿利咽之效,用于急喉痹及上呼吸道感染引起的咽喉疼痛,临床疗效确切[6]。参考相关文献[7-10],本研究采用高效液相色谱法(High performance liquid chromatography,HPLC),建立了小清咽颗粒的指纹图谱,以期为该制剂的质量控制提供科学依据。
1 材料
1.1 仪器
Aglent 1260 型HPLC仪、二极管阵列检测器(美国安捷伦科技公司);分析天平-AG135(瑞士梅特勒托利多公司);SG820OHPT型超声震荡仪(上海冠特超声仪器有限公司)。
1.2 药品与试剂
小清咽颗粒(批准文号:黔药制字Z20130007,批号:41101、41201、41202、41203、50101、50102、50301、50302、50401、50402),由贵阳中医学院第二附属医院药学部制剂室提供;射干苷对照品(中国食品药品检定研究院,批号:111632-200501)。乙腈(美国天地有限公司,色谱纯);甲醇(天津市富宇精细化工有限公司,分析纯);磷酸[重庆川东化工(集团)有限公司,分析纯];娃哈哈纯净水(杭州娃哈哈集团有限公司)。
2 方法与结果
2.1 色谱条件
色谱柱为迪马Diamonsil Plus C18(250 mm×4.6 mm,5 μm),流动相为乙腈(A)-0.1%磷酸溶液(B),梯度洗脱[11-12](洗脱程序见表1);流速1 ml/min,检测波长266 nm,柱温30 ℃,进样量10 μl。
2.2 溶液的制备
2.2.1 对照品溶液:精密称取射干苷对照品适量,加甲醇制成1 ml含40 μg射干苷的溶液,即得。
2.2.2 供试品溶液:取小清咽颗粒,研细,混匀,精密称取粉末2.0 g,置于具塞锥形瓶中,加入70%乙醇25 ml,摇匀,静置30 min,称定质量。超声处理30 min,放冷,称质量用70%乙醇补足减失的质量,摇匀,0.45 μm微孔滤膜滤过,即得。

表1 梯度洗脱程序
2.3 方法学考察
2.3.1 精密度试验及参照峰的选择:取同一批制剂(批号:41202),按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件,连续进样6次进行测定,见图1。可知4号色谱峰响应值较大,且已知为射干苷对照品的色谱峰,故设为参照(峰面积设为1)。结果表明,各共有峰相对峰面积的RSD均≤2.73%,共有峰相对保留时间的RSD均≤0.29%,表明本方法的精密度符合要求。
2.3.2 重复性试验:取同一批制剂(批号:41202),分别按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件,连续进样6次进行测定。结果表明,所有共有峰相对峰面积的RSD均≤2.83%,共有峰相对保留时间的RSD均≤0.37%,表明本方法的重复性符合要求。
2.3.3 稳定性试验:取同一批制剂(批号:41202),分别按“2.2.2”项下方法制备供试品溶液,分别在0、2、8、12、16、24、36、48 h,按“2.1”项下色谱条件进样分析。结果表明,所有共有峰相对峰面积的RSD均≤2.48%,共有峰相对保留时间的RSD均≤0.37%,表明供试品溶液在48 h内稳定。
2.4 指纹图谱的建立
将10批小清咽颗粒HPLC色谱图导入“中药色谱指纹图谱相似度评价系统(2012.130723版)”,以对照谱图上标示的色谱峰作为匹配点,经多点校正,采用中位数方法,时间窗宽度为0.5,进行自动匹配色谱峰,生成小清咽颗粒色谱指纹图谱共有模式,标定了10个共有峰,见图1。10批小清咽颗粒指纹图谱的相似度为0.951~0.997,平均值为0.969,RSD为1.69%,见图2、表2。表明各批次小清咽颗粒之间无明显差异性,本方法可用于鉴别小清咽颗粒的整体质量。
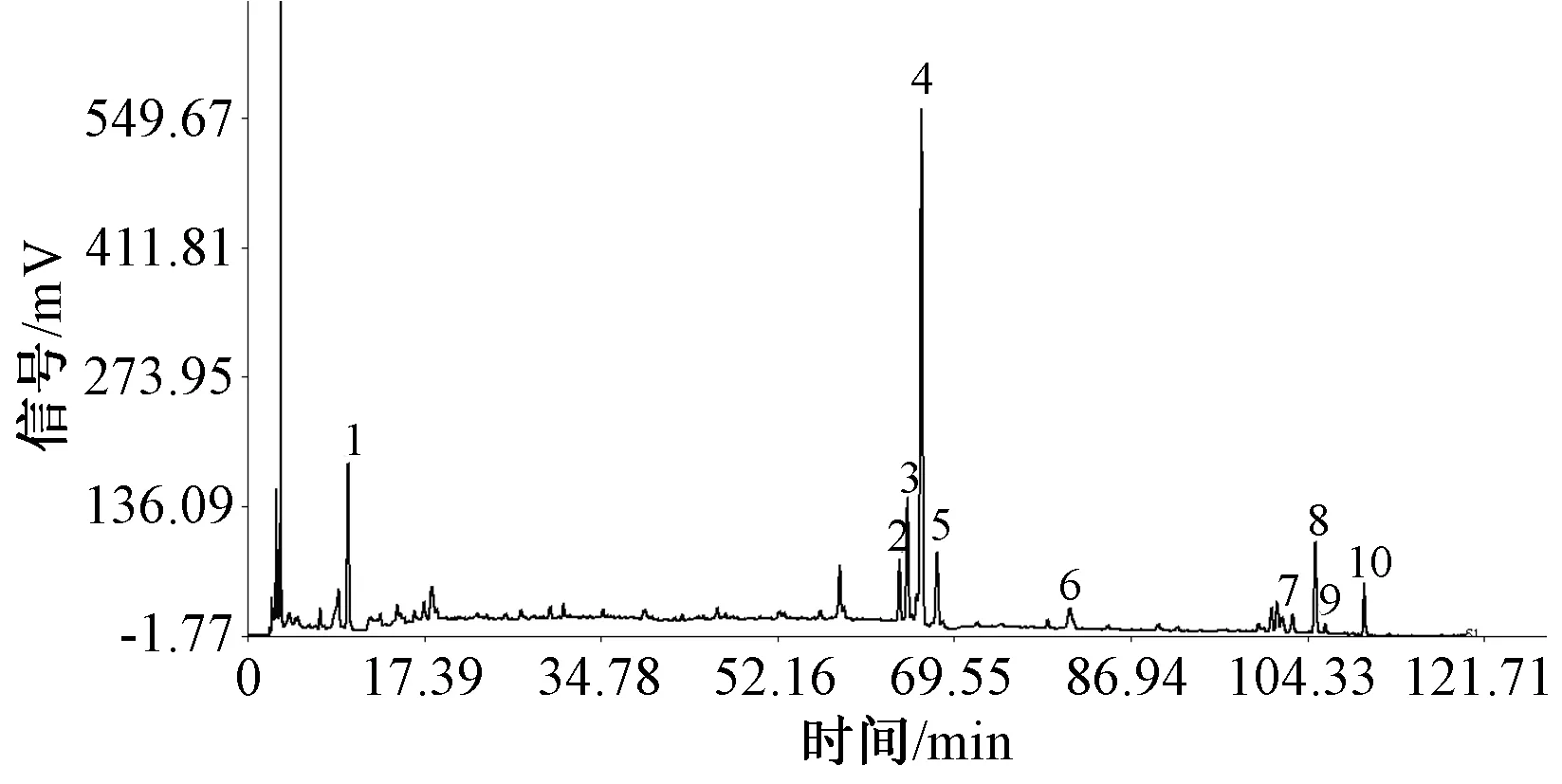
图1 小清咽颗粒对照指纹图谱Fig 1 Fingerprint and its common fingerprint peaks of Xiaoqingyan granules

图2 10批小清咽颗粒HPLC指纹图谱叠加图Fig 2 HPLC fingerprint chromatogram of 10 batches of Xiaoqingyan granules

批次S1S2S3S4S5S6S7S8S9S10RS11——————————S209871—————————S3096709751————————S40960096309681———————S509510958096309861——————S6097909870985096009561—————S70953095809730983098109641————S809510955097109790976096009811———S9097809870984096409600997096809651——S100979098709820969096609940974097109971—R09790987099009770974099409810977099609971
3 讨论
3.1 检测波长的确定
本研究分别考察了检测波长为358、266、245、237、210 nm时的指纹图谱。结果表明,在266、245、237 nm检测波长下所得色谱峰紫外吸收较大,其中又以266 nm波长所得色谱基线较平稳,吸收最大,故检测波长确定为266 nm。
3.2 流动相的选择
在梯度洗脱程序初步确定的条件下,参考相关文献[13-15]选用不同比例的乙腈-水、乙腈-0.1%磷酸溶液、甲醇-水等作为不同流动相组合进行对比试验。结果表明,采用乙腈-0.1%磷酸溶液进行系统洗脱,色谱峰信息较多,且峰型和分离度较好,故流动相确定为乙腈-0.1%磷酸溶液。
3.3 色谱柱的选择
采用反相色谱十八烷基硅烷键合相色谱柱。不同生产厂家不同牌号的色谱柱存在填料及性能上的差异,实验中分别比较了4种牌号色谱柱的分离情况,该4种色谱柱分别为:(1)Thermo Hypersil Gold(250 mm×4.6 mm,5 μm);(2)Phenomenex Synergi Hydro-RP 80A(250 mm×4.6 mm,5 μm);(3)Agilent ZOBX C18(250 mm×4.6 mm,5 μm);(4)迪马Diamonsil Plus C18(250 mm×4.6 mm,5 μm)。结果表明,色谱柱(1)和(3)的分离效果较好,但极性大的成分无法分离。色谱柱(4)可以达到良好的分离效果,故最终采用迪马Diamonsil Plus C18(250 mm×4.6 mm,5 μm)色谱柱。
3.4 柱温的选择
在不同的温度下按同样的洗脱程序进行试验,选择分离效果适宜的柱温条件,确保图谱有良好的分离度和稳定性。结果表明,在柱温25和30 ℃条件下,色谱峰的保留时间最大相差3 min,且柱温25 ℃下部分色谱峰分离度较差。因此,为了减少柱温对色谱峰分离的影响,确定柱温为30 ℃。
[1]熊斌,苏杰雄,刘贤钊,等.桑叶HPLC指纹图谱的优化及建立[J].广东药学院学报,2015,31(2):203-206.
[2]姚江雄,李春,廖端芳,等.桑叶药材HPLC指纹图谱研究[J].中国实验方剂学杂志,2013,19(10):119-121.
[3]唐跃年,金樑,张青,等.射干合剂的HPLC-UV指纹图谱分析[J].中国临床药学杂志,2012,21(5):283-286.
[4]刘洪宇,蔡铁全.玄参HPLC指纹图谱的比较研究[J].药物分析杂志,2012,32(7):1277-1282.
[5]杨亮,朴春梅.医院制剂小清咽颗粒的成型工艺研究[J].贵州科学,2013,31(6):39-41.
[6]杨亮,蒋玲,朴春梅,等.中西医结合治疗急性咽炎的临床观察[J].医药前沿.2013(27):216-217.
[7]孙国祥,闫波,侯志飞,等.中药色谱指纹图谱评价方法研究进展[J].中南药学,2015,13(7):673-681.
[8]李强,杜思邈,张忠亮,等.中药指纹图谱技术进展及未来发展方向展望[J].中草药,2013,44(22):3095-3104.
[9]陈文霞,武静莲,马东,等.小柴胡颗粒制剂-药材谱峰匹配指纹图谱研究[J].中草药,2013,44(22):3154-3161.
[10] 金莎丽,焦豪妍,聂阳,等.乐脉颗粒的HPLC指纹图谱及其成分鉴定[J].中国实验方剂学杂志,2015,21(23):68-71.
[11] 廖春玲,麦曦,冯丽华,等.抗宫炎系列药品的HPLC指纹图谱研究[J].中药材,2015,38(3):601-605.
[12] 张宇霞,昝占全,王统霞,等.丹珍头痛胶囊的HPLC指纹图谱研究[J].中国药房,2015,26(27):3864-3866.
[13] 肖作奇,潘涛,欧阳波,等.盆炎灵颗粒HPLC指纹图谱研究[J].中国新药杂志,2015,24(16):1897-1901.
[14] 贺康洪,张广春,李阳,等.复方黑参颗粒HPLC指纹图谱研究[J].解放军药学学报,2013,29(3):216-220.
[15] 张霓,赵秀莉.清咽利膈丸HPLC指纹图谱建立及4种主要成分的测定[J].中成药,2014,36(2):306-309.
Study on Fingerprint of Xiaoqingyan Granules by HPLCΔ
YANG Liang1, PU Chunmei1, HAN Yunxia1, DAI Xin1, LI Lifeng2
(1.Dept.of Pharmacy, the Second Hospital Affiliated to Traditional Chinese Medicine College of Guiyang, Guizhou Guiyang 550001, China; 2.Dept.of Pharmacy, Traditional Chinese Medicine College of Guiyang, Guizhou Guiyang 550025, China)
OBJECTIVE:To establish the fingerprint of Xiaoqingyan granules by HPLC. METHODS: Dikma Diamonsil Plus C18column (250 mm × 4.6 mm, 5 μm) was adopted; acetonitrile-0.1% phosphoric acid aqueous solution was used as the mobile phase for the gradient elution; the wavelength was set at 266 nm; the column temperature was at 30℃ with the flow rate of 1.0 ml/min. RESULTS: 10 common peaks were confirmed and similarity of 10 batches of Xiaoqingyan granules was more than 0.950; the overall similarity was good. CONCLUSIONS: The established method has characteristic and strong specificity, which is sensitive, accurate and simple, and can provide basis for the quality control of Xiaoqingyan granules.
Xiaoqingyan granules; HPLC; Fingerprint; Similarity
贵州省中医药、民族医药科学技术研究课题计划(No.QZYY2013-70号);贵州省科学技术厅贵阳中医学院科学技术联合资金(No.黔科合LH字[2014]7323号)
R927.11
A
1672-2124(2016)10-1318-03
2016-07-09)
*主管中药师,硕士。研究方向:中药临床药学、中药质量控制。E-mail:brightnet@qq.com
DOI 10.14009/j.issn.1672-2124.2016.10.007
