310种常用药品的说明书中儿童用药项标注情况调查与分析
2016-12-05李苏平
李苏平
(厦门市儿童医院药学部,福建 厦门 361006)
310种常用药品的说明书中儿童用药项标注情况调查与分析
李苏平*
(厦门市儿童医院药学部,福建 厦门 361006)
目的:了解厦门市儿童医院(以下简称“我院”)常用药品的说明书中有关儿童用药的标注情况,为规范药品说明书中儿童用药内容提供参考。方法:收集我院2016年2—4月常用的310种药品(其中注射剂91种,皮肤给药制剂37种,眼用制剂34种,吸入和喷雾剂11种,口服制剂137种)的说明书,对药品说明书中儿童用药的安全性、儿童用法与用量、新生儿用法与用量、儿童药动学参数标注情况等进行统计分析。结果:国产药品说明书中儿童用药安全性、儿童用法与用量、儿童药动学参数标注率均明显低于涉外药品,差异均有统计学意义(P<0.05);化学药说明书中儿童用药安全性标注率明显高于中成药,差异有统计学意义(P<0.05);剂型方面,吸入和喷雾剂说明书中儿童用药安全性、儿童用法与用量标注率最高;所有调查药品的说明书中,新生儿用法与用量、儿童药动学参数标注率普遍较低。结论:我院儿童专用药物的品种数较少,常用药品说明书中儿童用药相关内容标注率较低,导致临床超说明书用药现象较普遍。应加强儿童用药的临床试验,完善药品说明书中儿童用药标示项。
儿童用药; 药品说明书; 用药标项; 调查
统计结果显示,0~14岁儿童占我国总人口数的16.6%,但在我国3 500多种药物制剂品种中,专供儿童使用的却仅60多种,不足2%[1]。在不同发育阶段,人体结构、器官构造与代谢能力随年龄变化而变化,且为非线性变化,因此,不同年龄段儿童对药物的吸收、分布、代谢、排泄差别很大,对药品的反应也不尽相同。儿童并不是成人的缩小版,儿童服药剂量的计算,不能简单按照成人剂量减半。而药品说明书省略儿童的用法与用量、安全性、药动学等内容,导致临床普遍依据经验用药,或者按照年龄、体质量计算儿童用药剂量,缺乏科学性与可靠性。据报道,我国每年有近20万人因药源性疾病死亡,其中儿童病例数逐年递增[2]。北京、上海、重庆等地聋哑学校中,70%儿童的聋哑由药物使用不当造成[3]。另据调查,临床上有近50%的药品无儿童用药说明,有厂家因为担心标注儿童用药安全性等相关事项影响药品销售而忽略标注[4]。因此,对药品说明书儿童用药项标注的调查显得尤为重要,儿童医院药品中儿童用药项标注情况值得关注,儿童用药安全性迫切需要引起社会各界的重视。为了解当前药品说明书中儿童用药相关信息的标注情况,现对厦门市儿童医院(以下简称“我院”)目前使用药品的说明书进行调查分析,对药品说明书中儿童用药安全性、儿童用法与用量、新生儿用法与用量、儿童药动学参数标注情况进行统计分析,总结存在的问题,提出改进建议,为进一步规范药品说明书提供参考。
1 资料与方法
1.1 资料来源
[5-7]方法,收集我院2016年2—4月常用310种药品的说明书,其中,注射剂91种,皮肤给药剂型37种,眼用制剂34种,吸入和喷雾剂11种,口服制剂137种。
1.2 方法
参考《药品说明书和标签管理规定》[8]《化学药品和生物制品说明书规范细则》[9]《中药、天然药物处方药说明书格式内容书写要求及撰写指导原则》[10]等,对药品说明书中儿童用药安全性、儿童用法与用量、新生儿用法与用量、儿童药动学参数等进行统计分析。标注情况分为“标注”和“未标注”,另外,“遵医嘱”“尚未确定”“慎用”等也归为“未标注”,分别比较国产药与涉外药、中成药与化学药、不同剂型、不同药理作用药品的说明书中上述4个项目标注率。
1.3 统计学方法
采用SPSS 18.0软件对数据进行统计学处理,计数资料以率(%)表示,国产药与涉外药、中成药与化学药的标注率比较采用χ2检验,以P<0.05为差异有统计学意义。对不同剂型、不同药理作用药品的说明书标注率进行描述性分析。
2 结果
2.1 国产、涉外药品的说明书中儿童用药项标注情况
国产、涉外药品的说明书中儿童用药项标注情况见表1。涉外药品说明书儿童用药安全性标注率明显高于国产药品,差异有统计学意义(χ2=33.603,P<0.05);涉外药品说明书儿童用法与用量标注率明显高于国产药品,差异有统计学意义(χ2=4.097,P<0.05);涉外药品与国产药品说明书新生儿用法与用量标注率的差异无统计学意义(χ2=3.350,P>0.05);涉外药品说明书儿童药动学参数标注率明显高于国产药品,差异有统计学意义(χ2=13.722,P<0.05),见图1。
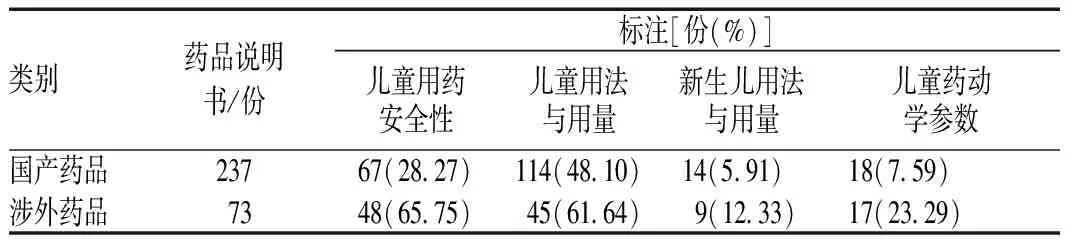
表1 国产、涉外药品的说明书中儿童用药项标注情况
注:涉外药品包含进口药、外资企业和中外合资企业生产的药品
Note:drugs produced by foreign countries contain drugs which is imported and drugs which is produced by overseas-funded enterprise and sino-foreign joint venture enterprise

注:与国产药品组比较,*P<0.05Note:vs. drug instruction,*P<0.05图1 国产与涉外药品的说明书中儿童用药项标注率比较Fig 1 Comparison of pediatric drug marking in drug instruction between drugs produced by China and drugs produced by foreign countries
2.2 中成药、化学药的说明书中儿童用药项标注情况
中成药、化学药的说明书中儿童用药项标注情况见表2。化学药说明书儿童用药安全性标注率明显高于中成药,差异有统计学意义(χ2=16.737,P<0.05);化学药与中成药说明书儿童用法与用量标注率的差异无统计学意义(χ2=0.917,P>0.05);化学药与中成药说明书新生儿用法与用量标注率的差异无统计学意义(χ2=0.528,P>0.05);化学药与中成药说明书儿童药动学参数标注率的差异无统计学意义(χ2=3.612,P>0.05),见图2。

表2 中成药、化学药的说明书中儿童用药项情况
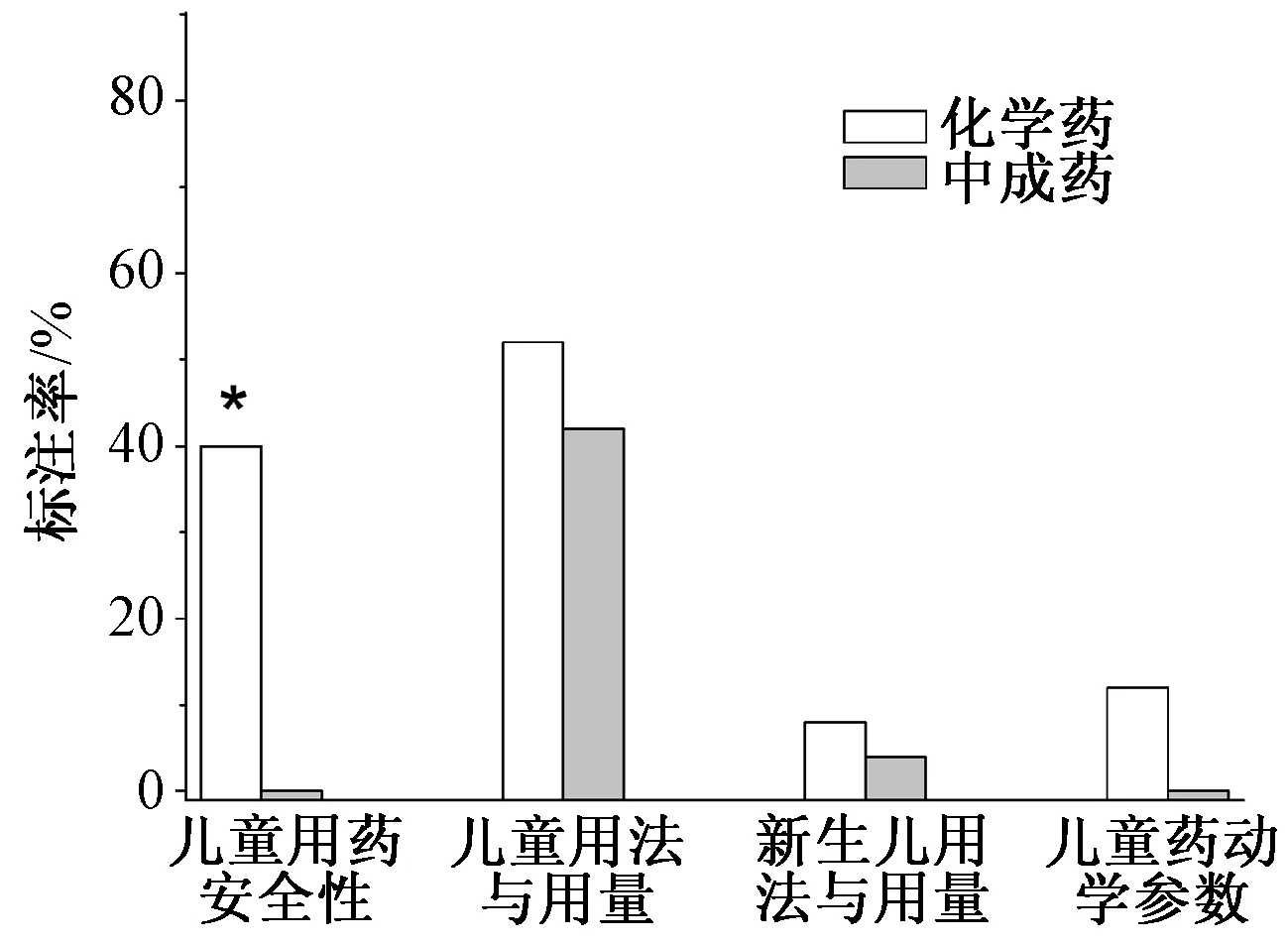
注:与中成药组比较,*P<0.05Note:vs. Chinese patent drugs, *P<0.05图2 中成药与化学药的说明书中儿童用药项标注率比较Fig 2 Comparison of pediatric drug marking in drug instruction between Chinese patent drug and chemical drug
2.3 不同剂型药品的说明书中儿童用药项标注情况
不同剂型药品的说明书中儿童用药项标注情况见表3。儿童用药安全性标注率方面,吸入和喷雾剂最高,其次为注射剂,皮肤给药剂型最低;儿童用法与用量标注率方面,吸入和喷雾剂最高,其次为口服制剂和注射剂,眼用制剂最低;新生儿用法与用量标注率普遍很低,最高的为注射剂(仅18.68%);儿童药动学参数标注率普遍不高,见图3。
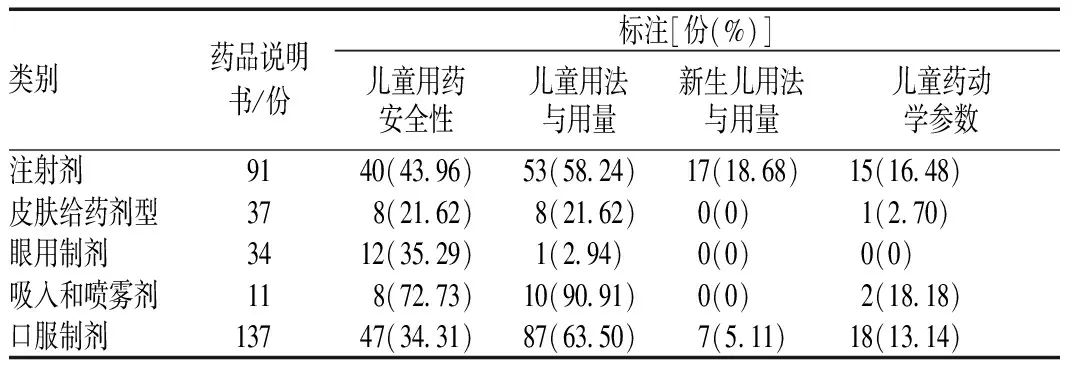
表3 不同剂型药品的说明书中儿童用药项标注情况
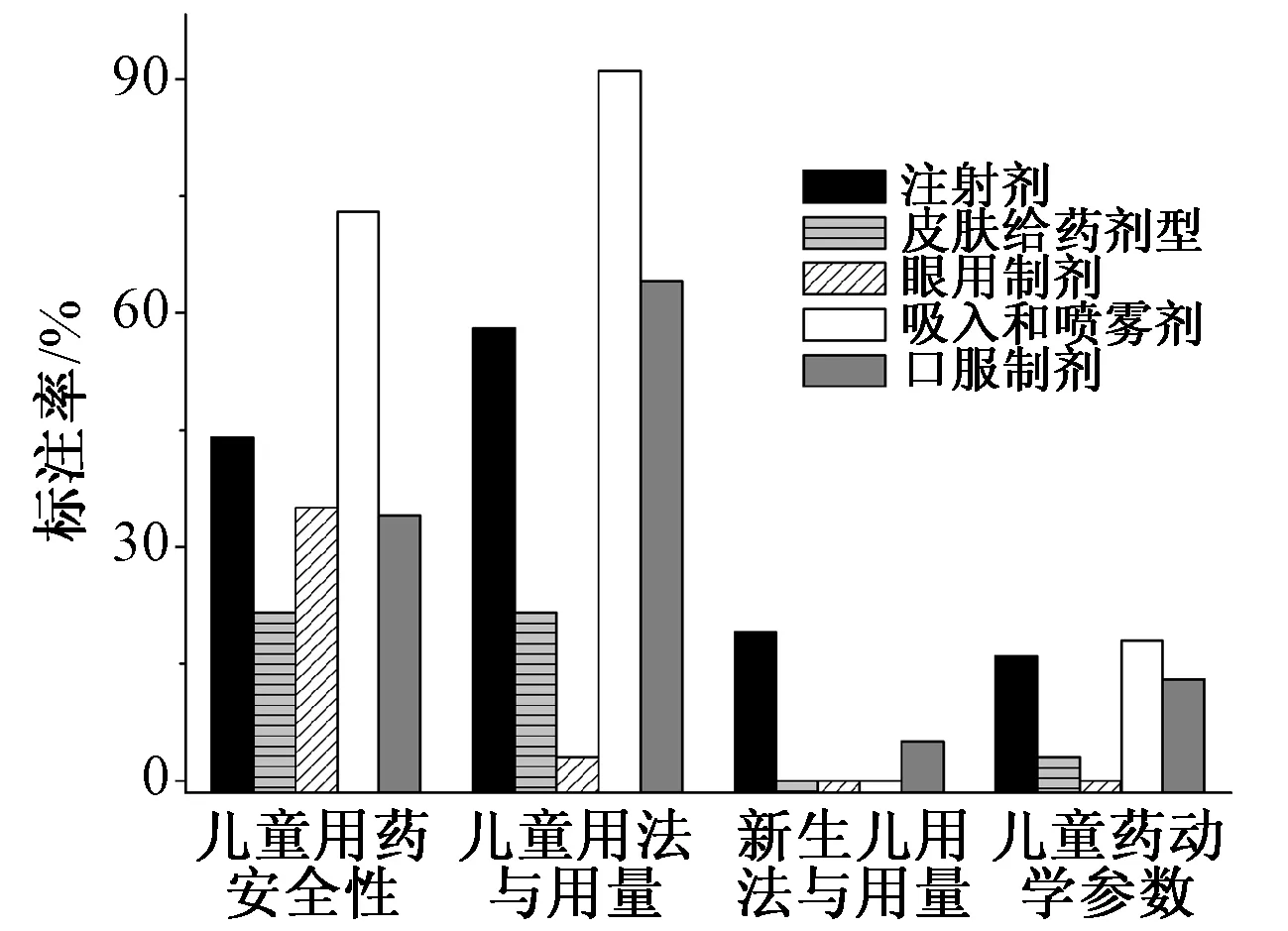
图3 不同剂型药品的说明书中儿童用药项标注率比较Fig 3 Comparison of pediatric drug marking in drug instruction among different dosage forms
2.4 品种数排序前10位药物的说明书中儿童用药项标注情况
将310种药品按照不同药理作用分类,品种数排序前10位药物的说明书中儿童用药项标注情况见表4。

表4 品种数排序前10位药物的说明书中儿童用药项标注情况
3 讨论
3.1 国产药品儿童用药项缺省问题严重
调查结果显示,国产药品儿童用药安全性、儿童用法与用量、儿童药动学参数标注率均明显低于涉外药品。部分国产药品说明书虽然标注有以上内容,但使用“未明确”“儿童慎用”等模糊语句。部分国产药品说明书虽然标注有儿童用法与用量,但在儿童用药安全性部分却标注“遵医嘱”“慎用”等模糊语句,使医务人员无法准确判断相关信息,存在用药安全隐患。国产药品儿童用药项缺省也可能直接导致儿童发生药品不良反应[11]。国产药品说明书标示内容表述较为简略,如表述为“儿童减半”。涉外药品多数分年龄段或者分体质量给药,不仅有各项内容的标注,标注内容的详细程度也令人钦佩,值得我国药品生产厂家学习。
3.2 新生儿用法与用量标注率低
随着社会对于儿童用药的重视,出现越来越多针对儿童用药相关的研究,但新生儿用药一直是令人困扰的问题,主要原因是对其伦理学与安全性的担忧,缺乏研究而冒然对新生儿使用可能过低或过高剂量的药物会使患者承担更大的风险,如新生儿过量使用氯霉素导致致命的心血管性虚脱[12]。如此造成医师为新生儿开具处方时对于药物使用剂量较为困惑。
3.3 中成药儿童用药安全性缺省严重
调查结果显示,中成药说明书均未标明儿童用药安全性,儿童用法与用量、新生儿用法与用量标注率也较低,与文献报道结论相近[11]。主要原因是我国儿童药动学、毒理学研究薄弱,我国《药事管理与法规》对中成药中儿童用药项未做要求;另外,无专项法律保障儿童参加药物药动学、药效学、毒理学等相关试验,临床试验难度大,儿童受试者招募困难,使成分复杂的儿童中成药的研究困难重重。而美国、日本等国家通过加快儿童药品法律法规的确立,确定了一些药物应用于儿童的疗效与安全性,促使儿童可以享受与成人一样的经新药临床试验后获得循证医学数据进行安全、有效治疗疾病的权益[13]。美国、日本等国家增加立法,保障儿童用药安全的行为值得我国学习,国家食品药品监督管理总局及其相关政府部门应加快相关政策制定的研究,为儿童临床试验减少障碍。
3.4 外用药和眼用制剂儿童用药项缺省问题
皮肤疾病和眼部疾病是儿科疾病中的大类,张晶晶[14]调查发现,眼科外用药品儿童用药项缺省严重,儿童用药标注多为模糊用语或“未明确”,无1例标注儿童药动学参数,与本调查结果相近。新生儿和儿童在无药动学参数和充分的临床试验保障下使用药品,有可能对健康产生危害。我院儿科门诊患者中,皮肤科和眼科患者占有很大比例,但我院所用外用药和眼科制剂说明书儿童用药标注情况不容乐观,儿童用药安全性无法得到保障,应引起足够重视。
3.5 对于儿童特殊情况使用药品的标注缺失
儿童特殊情况使用药品一般标注于药品说明书的“注意事项”中,调查发现,多数药品说明书对于儿童特殊情况使用药品标注缺失严重[7]。由于新生儿或年龄较小的儿童服用片剂较为困难,一般采用片剂泡水后服用,但药品说明书对于片剂是否能泡水,是否可用果汁、牛奶及热水浸泡等注意事项均无标注,给家长带来困扰。对于一些不能咀嚼的患者,如何服用咀嚼片,药品说明书也未标注。某些不能切割的缓、控释制剂(如氯化钾缓释片),由于没有相应的儿童专用剂型,只能切割后用于患儿,而药品说明书中也未明确指出可否切割,造成部分患儿用药效果不佳。红霉素的药品说明书规定,患儿静脉滴注红霉素时滴注速度要缓慢,而偏酸性的溶液输注时产生的疼痛往往导致患儿不配合,因此患儿输注时间往往很长,有时甚至超过8 h,长时间的酸性环境是否导致红霉素降效的问题给医护人员带来了疑惑。对使用药品时可能出现问题的解决方法,应在药品说明书“注意事项”中阐明。
综上所述,儿童用药已成为世界关注的话题。我院药品说明书中儿童用药项标注存在的问题,在一定程度上反应了厦门市、福建省甚至我国儿童用药标项的状况。虽然近年来儿童用药方面已经有了很大进步,但是我国儿童用药存在着适宜剂型规格缺乏、不合理用药现象普遍、不良反应发生率高等问题[15]。造成如此现状的原因是多方面的,药品说明书信息不完整直接影响患儿合理使用药品。国产药品说明书儿童用药项标注问题较多,政府应建立健全的儿童试验所应遵循的法规,完善儿童用药药动学、药效学、毒理学等相关数据;药品监管部门应加大监督执法力度,对药品说明书不规范的厂家给予相应处罚;药品审批部门应严格审批药品说明书中重要的儿童用药信息标注情况及,保证儿童用药安全;药厂应加大产品研发投入,进行儿童用药临床试验,提高上市药品的规范度,确保儿童用药规范化、安全化。
参考文献
[1]儿童用药令人揪心[J].中国质量万里行,2012(6):19-20.
[2]冯红云,刘翠丽,侯永芳.浅析我国儿童药品不良反应事件现状[J].中国药物警戒,2011,8(8):483-485.
[3]杨怡,张健,陆晓彤,等.儿童用药安全性和有效性影响因素分析[J].中国药房,2007,18(2):155-156.
[4]倪韶青,寿洪初,王珏,等.关于儿童用药的问题和建议[J].中国医院药学杂志,2007,27(6):815-817.
[5]张丹,李根,陈夏静,等.我院儿童适用药品的说明书标注信息的调查与分析[J].中国药房,2015,26(22):3153-3156.
[6]朱勤,孙云龙,徐进,等.628份药品说明书中有关儿童用药的调查分析[J].中国药事,2014,28(4):427-431.
[7]陶兴茹,裴保方,陈海燕,等.郑州市儿童医院药品说明书中有关儿童用药信息的调查分析[J].中国医院用药评价与分析,2015,15(3):330-333.
[8]国家食品药品监督管理局.药品说明书和标签管理规定[S].局令第24号.2006-03-15.
[9]国家食品药品监督管理局.关于印发化学药品和生物制品说明书规范细则的通知[S].国食药监注〔2006〕202号.2006-05-10.
[10] 国家食品药品监督管理局.关于印发中药、天然药物处方药说明书格式内容书写要求及撰写指导原则的通知[S].国食药监注〔2006〕283号.2006-06-22.
[11] 郑新,严健聪,刘福,等.266例儿童药品不良反应报告分析[J].中国医院用药评价与分析,2016,16(1):84-87.
[12] Ward RM,Kern SE.Clinical trials in neonates: a therapeutic imperative[J].Clin Pharmacol Ther,2009,86(6):585-587.
[13] 王晓玲.儿童药物临床试验的国内外现状研究[J].中国药物评价,2013,30(3):167-170.
[14] 张晶晶.眼科外用药说明书中儿童用药内容的分析[J].中国药物警戒,2012,9(12):757-759.
[15] 王春婷,李玉基,夏东胜,等.儿童用药现状及对策[J].中国药物警戒,2013,10(8):492-496.
Analysis and Investigation on Pediatric Drug Marking in Drug Instruction of 310 Common Drugs
LI Suping
(Dept.of Pharmacy, Xiamen Children’s Hospital, Fujian Xiamen 361006, China)
OBJECTIVE:To investigate the pediatric drug marking in drug instruction in Xiamen Children’s Hospital(hereinafter referred to as “our hospital”), so as to provide reference for the standardizing pediatric drug use in drug instruction. METHODS: Instructions of 310 drugs(91 kinds of injections, 37 kinds of skin preparation, 34 kinds of ophthalmic preparation, 11 kinds of inhalation and aerosol and 137 kinds of oral preparation) were collected in our hospital from Feb. to Apr. 2016 to conduct the statistical analysis, in terms of the safety of pediatric drugs and dosage and administration for children, dosage and administration for newborns and pharmacokinetics for children. RESULTS: The annotation ratio of the safety of pediatric drugs, dosage and administration for children and pharmacokinetics for children from domestic produced drugs were lower than those of foreign produced drugs, respectively with significant difference(P<0.05). The annotation ratio of the safety of pediatric drugs from western drugs were higher than that of Chinese patent drugs, with significant difference(P<0.05). As for the dosage form, the annotation ratio of the safety of pediatric drugs and dosage and administration for children for inhalation and aerosol was the highest; and the annotation ratio of dosage and administration for newborns, and pharmacokinetics for children were commonly low. CONCLUSIONS: There are few categories of pediatric drugs in our hospital, the annotation ratio of pediatric drug marking in drug instruction is relatively low, which commonly lead to the off-label use of drugs. Clinical experiment should be advocated to improve the basic data for completing the pediatric drug marking in drug instruction.
Pediatric drug use; Drug instruction; Drug marking; Investigation
R97
A
1672-2124(2016)10-1416-04
2016-07-15)
*主管药师。研究方向:医院药学与临床药学。E-mail:sp2100707505@163.com
DOI 10.14009/j.issn.1672-2124.2016.10.042
