提高肠得安胶囊质量标准的研究
2016-11-22张敏新侯冠雄黄爱文宋洪涛
张敏新,侯冠雄,黄爱文,宋洪涛*
(1.南京军区福州总医院药学科,福州 350025;2.福建中医药大学,福州 350122)
提高肠得安胶囊质量标准的研究
张敏新1,侯冠雄2,黄爱文1,宋洪涛1*
(1.南京军区福州总医院药学科,福州 350025;2.福建中医药大学,福州 350122)
目的 优化肠得安胶囊的质量标准。方法 对原标准中薄层色谱鉴别黄柏、大黄和厚朴3味药的鉴别项进行了优化,并增加了甘草、乌药和芍药的薄层鉴别;建立了HPLC法测定处方中黄柏的盐酸小檗碱含量,色谱柱:Agilent Zorbax XDB C18(150 mm×4.6 mm,5 μm);检测波长:345 nm。结果 各薄层色谱鉴别斑点清晰、分离好,阴性样品皆无干扰;含量测定盐酸小檗碱质量浓度在0.84~8.40 μg·mL-1范围内呈良好的线性关系 (r=0.999 9);平均加样回收率为97.3%,RSD值为0.86% (n=9)。结论 所用定性、定量方法准确可靠,且能有效控制肠得安胶囊的质量。
盐酸小檗碱;肠得安胶囊;质量标准;薄层色谱法;高效液相色谱法
A.stract:Objective To optimize the quality standard of Changdean Capsules prescription. Methods The original standard TLC methods of cork,rhubarb,and magnolia were improved.The new TLC methods for licorice,herbs obtusiloba and peony were added.An HPLC method for the determination of citrus hesperidin was estabished. The analytical column was Agilent Zorbax XDB C18(150 mm×4.6 mm,5 μm),and the UV detection wavelength was set at 345 nm. Results TLC spots were clear and well-separated without any interference. The linear range of berberine hydrochloride was 0.84-8.40 μg·mL-1.(r=0.999 9) with an average recovery of 97.3%,RSD was 0.86% (n=9). Conclusion The method is simple,specific,accurate and can effectively control the quality of Changdean Capsules.
慢性泄泻是一种常见病、多发病,从中医理论来说,系本虚标实证。本虚证常见脾肾两虚证,标实证常见湿热证,两者互为因果。本越虚则邪越实,邪越实则本越虚,以致病程缠绵,久治不愈,反复发作,给患者带来极大痛苦和不安。神州总医院高河元主任医师发现骨碎补为民间治疗泄泻的药物,经多年实践发现,单味骨碎补对标证为湿热的泄泻疗效不太理想,应健脾祛湿、理气止痛等全面兼顾,根据中医理论及临床实践,经过反复筛选,增加了黄柏、白芍等共18味药,其中9味药粉碎成细粉,另9味药水提并浓缩成浸膏与药粉共同制粒,干燥,装胶囊,即得。这样组合的肠得安胶囊,可以完全适应慢性泄泻证属脾肾两虚兼湿热的患者。为有效控制其质量,本文制定了该复方制剂中茯苓和白芍的显微鉴别,黄柏、大黄、厚朴、甘草、乌药和白芍6味药的TLC鉴别方法及有效成分盐酸小檗碱的高效液相色谱含量测定方法。
1 仪器与试药
1.1 仪器 1200型高效液相色谱仪(安捷伦化学工作站,四元梯度泵,自动进样器,DAD检测器,美国安捷伦公司);AT261万分之一电子分析天平(梅特勒-托利多仪器(上海)有限公司);TMS-F显微镜(MD30数码成像系统)。
1.2 试药 肠得安胶囊(自制);黄柏、大黄、厚朴、甘草、乌药及白芍对照药材(均购自中国食品药品检定研究院,批号121510-201301,120984-201202,121285-201303,121303-200502,121096-200509,120905-201109);盐酸小檗碱、大黄酚、厚朴酚、和厚朴酚、甘草苷、乌药醚内酯及芍药苷对照品(均购自中国食品药品检定研究院,批号:120811-201109,110796-201017,110729-200412,110730-200412,111610-201005,110626-201317,110736-201438);甲醇、乙腈为色谱纯;其他试剂均为分析纯;硅胶G、硅胶H、硅胶GF254薄层板(青岛海洋化工厂分厂)。
2 方法与结果
2.1 显微鉴别 取本品适量,在显微镜下观察:可见不规则分枝状团块,无色,遇水合氯醛液溶化;菌丝无色或淡棕色,直径4~6 μm(茯苓);草酸钙簇晶少见,直径18~32 μm(白芍)。
2.2 黄柏的鉴别
2.2.1 供试品溶液的制备 取肠得安胶囊内容物2.0 g,加甲醇15 mL,超声处理15 min,滤过,滤液蒸干,残渣加甲醇1 mL溶解,即得[1]。
2.2.2 对照品溶液的制备 取盐酸小檗碱对照品适量,加甲醇制成1 mL含1 mg的溶液,即得。
2.2.3 对照药材溶液的制备 取黄柏对照药材粉末0.2 g,加甲醇30 mL,超声处理30 min,滤过,滤液浓缩至约2 mL,即得。
2.2.4 阴性对照溶液的制备 按照处方比例和工艺制备缺少黄柏的阴性对照样品2.0 g,按照2.2.1项下方法制备阴性对照溶液。吸取上述4种溶液各5 μL,分别点于同一硅胶G薄层板上,以乙酸异戊酯-无水乙醇-甲酸(7∶1∶2)为展开剂[2],展开,取出,晾干,在紫外光灯(365 nm)下检视。供试品色谱中,在与对照品及对照药材色谱对应的位置上,显相同颜色的荧光斑点;阴性对照色谱无干扰。见图1。
2.3 大黄的鉴别
2.3.1 供试品溶液的制备 取肠得安胶囊内容物2.0 g,加甲醇15 mL,超声处理15 min,滤过,滤液加盐酸2 mL、水15 mL,置于水浴上加热30 min,立即冷却,用乙醚提取2次,每次20 mL,合并乙醚液,挥干,残渣加二氯甲烷1 mL使溶解,即得。
2.3.2 对照品溶液的制备 取大黄酚对照品适量,加甲醇制成1 mL含1 mg的溶液,即得。
2.3.3 对照药材溶液的制备 取大黄对照药材粉末0.1 g,加甲醇20 mL,超声处理15 min,滤过,滤液加盐酸2 mL、水15 mL,置于水浴上加热30 min,立即冷却,用乙醚提取2次,每次20 mL,合并乙醚液,蒸干,残渣加二氯甲烷1 mL使溶解,即得。
2.3.4 阴性对照溶液的制备 按照处方比例和工艺制备缺少大黄的阴性对照样品,再按照2.3.1项下方法制备阴性对照溶液,吸取上述4种溶液各5 μL,分别点于同一硅胶H薄层板上,以石油醚(30~60 ℃)-甲酸乙酯-甲酸(15∶5∶1)的上层溶液为展开剂,展开,取出,晾干,在紫外光灯365 nm下检视。供试品色谱中,在与对照品色谱对应的位置上,显相同颜色的荧光斑点;阴性对照色谱无干扰。见图2。

图1 黄柏的TLC图
1.盐酸小檗碱对照品;2.黄柏对照药材;3~5.供试品;6.缺黄柏阴性对照
Fig.1 TLC chromatogram ofPhellodendriChinensisCortex 1.berberine hydrochloride;2.PhellodendriChinensisCortex;3-5.sample;6.negative

图2 大黄的TLC图
1.大黄酚对照品;2.大黄对照药材;3~5.供试品;6.缺大黄阴性对照
Fig.2 TLC chromatogram ofRhubarb1.chrysophanol;2.Rhubarb;3-5.sample;6.negative
2.4 厚朴的鉴别
2.4.1 供试品溶液的制备 取肠得安胶囊内容物2.0 g,加甲醇15 mL,超声处理15 min,滤过,滤液挥干,残渣加水15 mL超声使溶解,以水饱和的正丁醇提取2次(20和20 mL),合并正丁醇液,挥干,残渣加甲醇1 mL使溶解,即得。
2.4.2 对照品溶液的制备 取厚朴酚、和厚朴酚对照品适量,加甲醇制成1 mL各含1 mg的溶液,即得。
2.4.3 对照药材溶液的制备 取厚朴对照药材粉末0.5 g,加甲醇10 mL,超声处理15 min,滤过,滤液浓缩至约2 mL,即得。
2.4.4 阴性对照溶液的制备 按照处方比例和工艺制备缺少厚朴的阴性对照样品,再按照2.4.1项下方法制备阴性对照溶液,吸取上述4种溶液各5 μL,分别点于同一硅胶GF254薄层板上,以甲苯-甲醇(17∶1)为展开剂[3-4],展开,取出,晾干,在紫外光灯254 nm下检视。供试品色谱中,在与对照品色谱对应的位置上,显相同颜色的荧光斑点;阴性对照色谱无干扰。见图3。

图3 厚朴的TLC图
1.厚朴酚对照品;2.和厚朴酚对照品;3.厚朴对照药材; 4~6.供试品;7.缺厚朴阴性对照
Fig.6 TLC chromatogram ofMagnoliaeofficinalisCortex
1.magnolol;2.honokiol;3.MagnoliaeofficinalisCortex;4-6.sample;7.negative sample
2.5 甘草的鉴别
2.5.1 供试品溶液的制备 取肠得安胶囊内容物10.0 g,加甲醇50 mL,超声处理15 min,滤过,滤液挥干,残渣加水15 mL超声使溶解,以水饱和的正丁醇提取2次(均为20 mL),合并正丁醇液,用正丁醇饱和的水洗涤3次(均为20 mL),弃去水液,取正丁醇液蒸干,残渣加甲醇1 mL使溶解,即得。
2.5.2 对照品溶液的制备 取甘草苷对照品适量,加甲醇制成1 mL含1 mg的溶液,即得。
2.5.3 对照药材溶液的制备 取甘草对照药材粉末1 g,加甲醇30 mL,超声处理30 min,滤过,滤液蒸干,残渣加水40 mL使溶解,用水饱和的正丁醇提取3次(均为20 mL),合并正丁醇液,用水洗涤3次,弃去水液,正丁醇液蒸干,残渣加甲醇5 mL 使溶解,即得。
2.5.4 阴性对照溶液的制备 按照处方比例和工艺制备缺甘草的阴性对照样品,按照2.5.1项下方法制备阴性对照溶液,吸取上述4种溶液各5 μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-甲酸-冰醋酸-水(15∶1∶1∶2)为展开剂[5],展开,取出,晾干,喷以100 mL·L-1的硫酸乙醇溶液,在105 ℃加热至斑点显色清晰,在紫外光灯365 nm下检视。供试品色谱中,在与对照品色谱对应的位置上,显相同颜色的荧光斑点;阴性对照色谱无干扰。见图4。
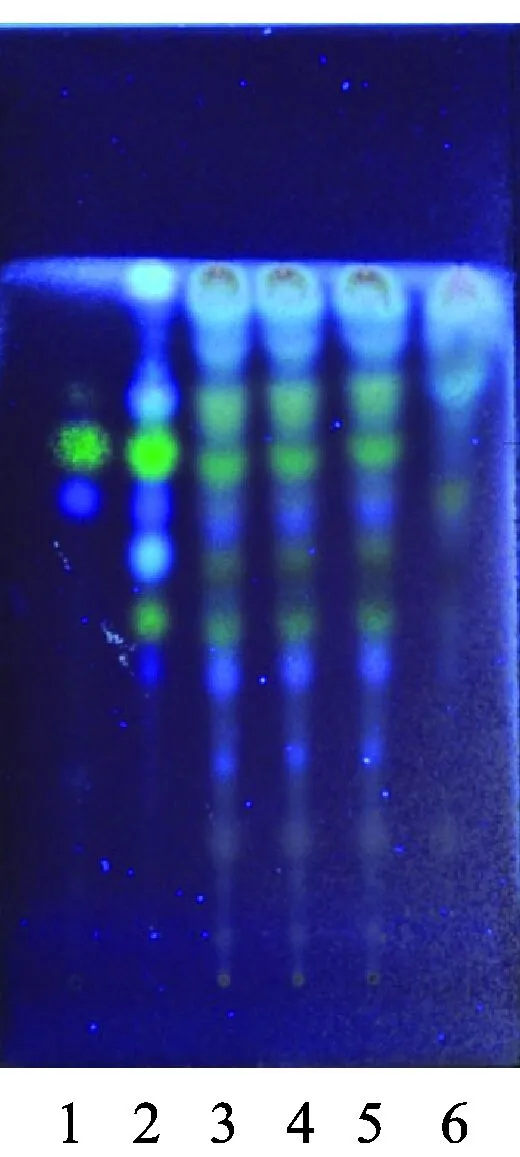
图4 甘草的TLC图
1.甘草苷对照品;2.甘草对照药材;3~5.供试品;6.缺甘草阴性对照
Fig.6 TLC chromatogram ofGlycyrrhizaeRadix et Rhizoma
1.liquiritin;2.GlycyrrhizaeRadix et Rhizoma;3-5.sample;6.negative sample
2.6 乌药的鉴别
2.6.1 供试品溶液的制备 取肠得安胶囊内容物10.0 g,加石油醚(60~90 ℃) 30 mL,超声处理(水温不高于30 ℃)15 min,滤过,滤液挥干,残渣加乙酸乙酯1 mL使溶解,即得。
2.6.2 对照品溶液的制备 取乌药醚内酯对照品适量,加乙酸乙酯制成1 mL含1 mg的溶液,即得。
2.6.3 对照药材溶液的制备 取乌药对照药材粉末1 g,加石油醚(60~90 ℃)30 mL,放置30 min,超声处理(水温不高于30 ℃)10 min,滤过,滤液挥干,残渣加乙酸乙酯1 mL使溶解,即得。
2.6.4 阴性对照溶液的制备 按照处方比例和工艺制备缺乌药的阴性样品,再按照2.6.1项下方法制备阴性对照溶液,吸取上述4种溶液各5 μL,分别点于同一硅胶H薄层板上,以环已烷-乙酸乙酯(9∶1)为展开剂[6-7],展开,取出,晾干,喷以10 g·L-1的香草醛硫酸溶液。供试品色谱中,在与对照品色谱对应的位置上,显相同颜色的斑点;阴性对照色谱无干扰。见图5。
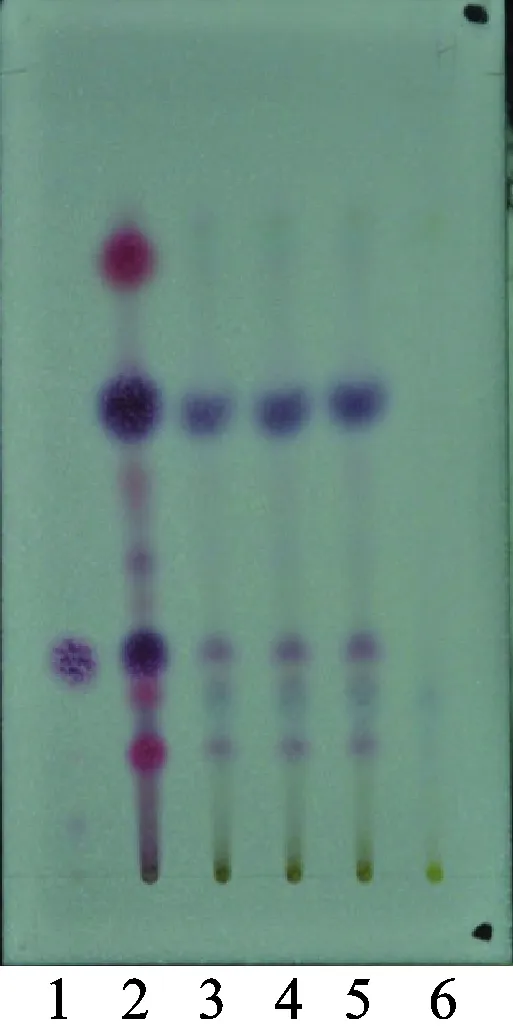
图5 乌药的TLC图
1.乌药醚内酯对照品;2.乌药对照药材;3~5.供试品;6.缺乌药阴性对照
Fig.5 TLC chromatogram ofLinderaeRadix
1.linderane;2.LinderaeRadix;3-5.sample;6.negative sample
2.7 白芍的鉴别
2.7.1 供试品溶液的制备 取肠得安胶囊内容物5.0 g,加乙醇30 mL,超声处理15 min,滤过,滤液挥干,残渣加水10 mL使溶解,以水饱和的正丁醇提取2次,每次20 mL,合并正丁醇液,加浓氨2 mL、正丁醇饱和的水10 mL洗涤1次,再以正丁醇饱和的水洗涤2次,每次10 mL,正丁醇液蒸干,残渣加乙醇1 mL使溶解,即得。
2.7.2 对照品溶液的制备 取芍药苷对照品适量,加乙醇制成1 mL含1 mg的溶液,即得。
2.7.3 对照药材溶液的制备 取白芍对照药材粉末0.5 g,加乙醇10 mL,超声处理15 min,滤过,滤液蒸干,残渣加乙醇1 mL使溶解,即得。
2.7.4 阴性对照溶液的制备 按照处方比例和工艺制备缺白芍的阴性样品,再按照2.7.1项下方法制备阴性对照溶液,吸取上述4种溶液各5 μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-甲醇-甲酸(10∶2∶0.1)为展开剂,展开,取出,晾干,喷以50 g·L-1的香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照品色谱对应的位置上,显相同的蓝紫色斑点;阴性对照色谱无干扰。见图6。

图6 白芍的TLC图
1.芍药苷对照品;2.白芍对照药材;3~5.供试品;6.缺白芍阴性对照
Fig.6 TLC chromatogram ofPaeoniaeRadix Alba
1.paeoniflorin;2.PaeoniaeRadix Alba;3-5.sample;6.negative sample
2.8 盐酸小檗碱的含量测定
2.8.1 色谱条件 色谱柱:Agilent Zorbax XDB C18(150 mm×4.6 mm,5 μm);流动相:乙腈-2 mL·L-1的磷酸溶液(含3 mL·L-1的三乙胺)(20∶80);流速:1 mL·min-1;柱温:30 ℃;检测波长:345 nm;进样量:10 μL。
2.8.2 对照品储备溶液的配制 取盐酸小檗碱对照品适量,精密称定,加盐酸-700 mL·L-1的甲醇(1∶100)(稀释液) 制成1 mL含盐酸小檗碱20 μg的对照品储备溶液。
2.8.3 对照品溶液的配制 精密吸取对照品储备溶液5 mL,置于50 mL量瓶中,以稀释液稀释至刻度,即得。
2.8.4 供试品溶液的制备 取装量差异项下肠得安胶囊内容物2.0 g,精密称定,置于100 mL量瓶中,加稀释液70 mL,超声处理30 min,取出,放冷,以稀释液稀释至刻度,摇匀,滤过,即得。
2.8.5 阴性对照溶液的制备 精密称取缺黄柏阴性对照制剂2.0 g,按照2.8.4项下方法处理,即得。
2.8.6 黄柏药材溶液的制备 取黄柏药材0.1 g,精密称定,置于100 mL量瓶中,加稀释液70 mL,超声处理30 min,取出,放冷,用稀释液稀释至刻度,摇匀,滤过,精密吸取续滤液5 mL,置于50 mL量瓶中,以稀释液稀释至刻度,摇匀,即得。
2.8.7 检测波长的确定 精密吸取盐酸小檗碱对照品溶液(C=1.68 μg·mL-1)10 μL,进样,记录扫描光谱图(190~400 nm),盐酸小檗碱在230,265和345 nm处皆有最大吸收,且吸收强度基本相同,但在230和265 nm处供试品色谱图上有杂质峰干扰,而345 nm处杂质的干扰相对较小,故最终选择345 nm为盐酸小檗碱的检测波长。
2.8.8 专属性实验 精密吸取供试品溶液及阴性对照溶液各10 μL,进样,测定。结果在阴性对照溶液色谱图上盐酸小檗碱出峰相应位置未见色谱峰,表明本方法专属性良好。色谱图见图7。
2.8.9 线性关系 精密吸取盐酸小檗碱对照品储备溶液适量,置于量瓶中,用稀释液稀释至刻度,摇匀,得系列质量浓度0.84~8.40 μg·mL-1对照品溶液,滤过,分别精密吸取各质量浓度对照品溶液续滤液10 μL,注入色谱仪,测峰面积。以峰面积(A) 对质量浓度(C)进行线性回归,得标准曲线A=36.938C+0.775,相关系数r=0.999 9。结果表明,盐酸小檗碱在测定质量浓度范围内峰面积(A)与质量浓度(C)线性关系良好。

图7 345 nm处盐酸小檗碱的HPLC图
A.盐酸小檗碱对照品溶液;B.供试品溶液;C.黄柏药材;D.缺黄柏阴性对照溶液;1.盐酸小檗碱
Fig.7 HPLC chromatograms of berberine hydrochloride detected at 345 nm
A.berberine hydrochloride; B.test sample;C.Phellodendrichinensis;D.negative control;1.berberine hydrochloride
2.8.10 精密度实验 精密吸取同一对照品溶液(C=1.68 μg·mL-1)10 μL,注入高效液相色谱仪,连续进样6次,记录峰面积,测得RSD值为0.32%,表明仪器精密度良好。
2.8.11 稳定性实验 取同一份对照品(质量浓度为1.68 μg·mL-1)溶液,分别在0,2,4,6,8和10 h时,精密吸取10 μL,注入高效液相色谱仪,记录盐酸小檗碱峰面积,测得其RSD值为0.13%,表明盐酸小檗碱在10 h内稳定性良好。
2.8.12 重复性实验 分别取同一批胶囊 (批号20141202)6份,每份2.0 g,精密称定,按照2.8.4项下方法制备供试品溶液,精密吸取续滤液10 μL,注入高效液相色谱仪,测定,计算盐酸小檗碱含量,结果RSD值为1.33%,表明该方法重复性良好。
2.8.13 加样回收率实验 分别取同一批胶囊(批号20141202,含量99.43 μg·g-1)2.0 g,精密称定,共9份,分别置于100 mL量瓶中,精密吸取2.8.2项下盐酸小檗碱对照品储备液8.0,10.0和12.0 mL,各3份,制备加样量分别为80%,100%和120%的供试品溶液,按照供试品溶液的制备同法进行操作,进样测定样品含量,计算加样回收率,结果盐酸小檗碱的平均回收率为97.3%,RSD值为0.86%,见表1。
表1 加样回收率实验结果
Tab.1 Results of recovery tests

取样量/g样品中的量/μg加入量/μg测得量/μg回收率/%平均回收率/%RSD/%2.0048199.34159.6348.297.0197.310.862.0017199.03159.6347.696.922.0105199.90159.6347.896.742.0022199.08199.5386.096.842.0342202.26199.5387.496.432.0102199.87199.5385.896.602.0038202.64239.4432.298.532.0219201.04239.4433.198.332.0016199.02239.4431.198.33
2.8.14 样品含量测定 分别取3批肠得安胶囊(批号:20141202,20141204,20141206)各2.0 g,精密称定,每批3份,按照2.8.4项下方法操作,进样测定,并计算盐酸小檗碱含量,结果3批样品中盐酸小檗碱的含量分别为99.43,100.38和97.52 μg·g-1。
3 讨论
显微鉴别是中药品种鉴定常用的手段之一,因成方制剂中含有多种辅料或浸膏,故其显微鉴定比单味中药材的显微鉴定更加复杂,且多味药材之间产生相互干扰使其特征在显微镜下难以观察。因此,本实验选取特征显著且重复性好的茯苓的菌丝及白芍的草酸钙簇晶作为本制剂的显微特征。
《中国药典》2010年版一部中厚朴药材的鉴别是以硅胶G板为薄层板,展开后喷以10 g·L-1的香草醛硫酸溶液显色,发现其干扰较大,斑点未能完全分开,故最后将展开板换成硅胶GF254板,展开后在紫外光灯254 nm下直接观察,结果斑点清晰,干扰小,方法简便易行。
《中国药典》2010年版二部的盐酸小檗碱原料药其含量测定法为滴定法,其方法显然不适用于中药复方制剂的含量测定,而盐酸小檗碱片和胶囊的含量测定方法为高效液相色谱法,色谱柱为十八烷基硅烷键合硅胶,流动相为磷酸盐缓冲液(0.05 mol·L-1磷酸二氢钾溶液- 0.05 mol·L-1庚烷磺酸钠溶液(1∶1),含2 mL·L-1三乙胺,并用磷酸调节pH值至3.0)-乙腈(60∶40)[8],检测波长为263 nm;而《中国药典》2010年版一部中测定盐酸小檗碱含量的流动相组成主要有乙腈-0.05 mol·L-1磷酸二氢钾溶液、乙腈-水(每100 mL中加磷酸二氢钾0.34 g与十二烷基磺酸钠0.17 g)[9]、乙腈-0.05 mol·L-1磷酸二氢钾溶液(用磷酸调pH值为3.0)[10],研究发现加入离子对试剂庚烷磺酸钠或十二烷基磺酸钠对于增强保留、改善峰形和提高分离度具有较好的效果,但其在配制过程中溶液容易起泡,不易配制,且离子对试剂和色谱柱的损伤较大;经反复实验发现以依利特Hypersil ODS C18柱,流动相为乙腈-2 mL·L-1磷酸溶液(含3 mL·L-1三乙胺) (20∶80),可实现盐酸小檗碱峰与其他峰的分离度达到要求,但其峰形不理想,对称因子只有0.6,拖尾严重,理论塔板数为4 120。参阅相关文献[11]发现,可能是色谱柱填料对峰形的影响较大,故将色谱柱换成Agilent Zorbax XDB C18(150 mm×4.6 mm,5 μm) 相同液相条件,盐酸小檗碱的峰形良好,对称因子为0.98,理论塔板数为13 682,故最终选择以上方法为盐酸小檗碱的含量测定方法。
[1] 石小鹏,缪珊,李捷,等. 参蛇软膏的质量标准研究 [J]. 西北药学杂志,2014,29(2):114-117.
[2] 国家药典委员会. 中国药典2010年版[S]. 一部. 北京:中国医药科技出版社,2010:908-909.
[3] 国家药典委员会. 中国药典2010年版[S]. 一部. 北京:中国医药科技出版社,2010:235.
[4] 国家药典委员会. 中国药典2010年版[S]. 一部. 北京:中国医药科技出版社,2010:420.
[5] 邢小军,王嫦丽,窦建卫,等. 提高参苏丸质量标准的研究 [J]. 西北药学杂志,2014,29(3):233-235.
[6] 国家药典委员会. 中国药典2010年版[S]. 一部. 北京:中国医药科技出版社,2010:71-72.
[7] 国家药典委员会. 国家药品标准新药转正标准:第43册[S]. 北京:化学工业出版社,2004:37.
[8] 国家药典委员会. 中国药典2010年版[S]. 一部. 北京:中国医药科技出版社,2010:639-641.
[9] 国家药典委员会. 中国药典2010年版[S]. 一部. 北京:中国医药科技出版社,2010:557-558.
[10]汪明志,王建春,张咏梅. RP-HPLC法测定肠尔舒胶囊中盐酸小檗碱的含量[J]. 西北药学杂志,2012,27(4):312-313.
[11]国家药典委员会. 中国药典高效液相色谱图集:第一卷[S]. 北京:人民卫生出版社,2005:64.
Improvement research of the quality standard of Changdean Capsules
ZHANG Minxin1,HOU Guanxiong2,HUANG Aiwen1,SONG Hongtao1*
(1.Department of Pharmacy, Fuzhou General Hospital of Nanjing Command,PLA,Fuzhou 350025, China;2.School of Pharmacy, Fujian University of Traditional Chinese Medicine,Fuzhou 350122,China)
berberine hydrochloride;Changdean Capsules;quality standards;TLC;HPLC
基于HPLC和TLC技术提高22种军队医疗机构非标准制剂质量标准的研究项目(编号:14ZJZ17)作者简介:张敏新,男,药师
*通信作者:宋洪涛,男,博士,主任药师
10.3969/j.issn.1004-2407.2016.06.004
R282
A
1004-2407(2016)06-0562-06
2016-01-10)
