Cu/Mn/Ce三元氧化物催化剂对甲苯催化燃烧性能的研究
2016-11-15朱红娜吕德义郇昌永
朱红娜,吕德义,郇昌永
(1.浙江工业大学化学工程学院,浙江杭州310014;2.宁波化学工业区博士后科研工作站,浙江宁波315204)
Cu/Mn/Ce三元氧化物催化剂对甲苯催化燃烧性能的研究
朱红娜1,吕德义1,郇昌永2*
(1.浙江工业大学化学工程学院,浙江杭州310014;2.宁波化学工业区博士后科研工作站,浙江宁波315204)
采用浸渍法制备了不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂。通过XRD、和H2-TPR对催化剂的晶相结构和晶格氧的移动性进行了表征和分析,采用常压气-固反应装置考察了不同的铜锰铈摩尔比对催化氧化甲苯性能的影响,并讨论了催化剂晶相组成、氧移动性与催化活性的关系。结果显示,铜锰氧化物复合形成的新相Cu1.4Mn1.6O4是具有更高催化活性的中心,CeO2的加入提高了Cu1.4Mn1.6O4分散度,从而增强了催化剂的氧移动性,提高了催化剂的活性和氧化能力。当Cu/Mn/Ce摩尔比为1:1:4时,催化氧化甲苯的活性最佳,T95%为282.6℃,CO2选择性为100%。
铜锰铈三元复合氧化物;摩尔比;甲苯
0 前言
鉴于贵金属过高的成本,将过渡金属复合氧化物用于催化降解挥发性有机污染物(VOCs)被广泛关注[1]。其中,铜锰二元复合氧化物常被用作VOCs催化燃烧的催化剂[2-4],但其起燃温度与完全燃烧温度仍较高[4-5]。人们发现稀土氧化物CeO2具有较好的储氧功能,可促进晶格氧的移动性,降低催化剂的完全燃烧温度[6-9]。因此,常通过氧化铈与过渡金属氧化物形成Cu-Ce[7-8]、Mn-Ce[7,9]、Ce-Zr[10]等体系的二元催化剂来提高催化剂的催化性能。Cai LN[11]研究了Fe、Zn和Ce元素的加入对铜锰催化剂活性的影响,结果显示CuMnOx-Ce催化剂催化氧化CO的性能最佳。但不同加入量对铜锰催化剂的物相与性能的影响报道仍较少。本文将通过制备不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂,探讨不同铜锰铈摩尔比与催化剂的物相、比表面积与氧移动性的关系,进一步研究其对催化剂性能的影响。
1 实验方法
1.1催化剂的制备方法
将15mL Cu(NO3)2溶液(c1mol/L)和15 mL Mn(NO3)2溶液(c2,mol/L)及10 mL Ce(NO3)3溶液(c3,mol/L)混合均匀后配成浸渍液,各硝酸盐的浓度c见表1。将浸渍液加热到50℃时,加入2.5000 g的TiO2(锐钛矿:晶红石摩尔比为4∶1,平均粒度:20 nm)粉末,控制催化剂的负载量为40%(以CuO,MnO2,CeO2的质量计算)。于50℃下磁力搅拌5 h,然后置于80℃水浴中旋转蒸发除去水分,再在120℃下烘干12 h,得到Cu-Mn-Ce/TiO2-x-y-z催化剂(其中x、y和z分别代表Cu、Mn和Ce的摩尔比)。
将上述烘干的催化剂置于管式炉中,500℃焙烧4 h(焙烧气氛为空气,流速为10mL/min,升温速率为2℃/min)。然后,催化剂经压片、粉碎、筛分,取其中40~60目颗粒用于催化燃烧甲苯的实验。

表1 浸渍液Cu(NO3)2、Mn(NO3)2和Ce(NO3)3的浓度Table 1.Concentration of impregnation solution of Cu(NO3)3、Mn(NO3)3and Ce(NO3)3
1.2催化剂表征
采用荷兰PNAlytical公司的X'Pert PRO型的X射线衍射仪(XRD)对样品的物相进行表征分析,得到催化剂的晶型和晶粒大小。分析条件为Cu Kα射线(波长为0.1541 nm),工作电压40 kV,电流40 mA,扫描范围2θ为10°~80°,扫描步进0.0167°/s,通过Scherrer公式计算D(hkl)。
氢气程序升温还原(H2-TPR)表征以体积分数为5%H2-95%Ar为还原气体,尾气用GC1690气相色谱仪在线分析。当系统基线稳定后以10℃/min的速度从30℃升温至810℃,得到样品的H2-TPR图谱用于分析催化剂中氧的移动性。
1.3催化评价条件
铜锰铈三元复合氧化物催化剂催化燃烧性能的评价在常压气-固反应装置上进行。催化剂填充在内径为10 mm,长为500 mm的不锈钢反应管的恒温区,反应温度范围为150℃~400℃。催化剂(40~60目)用量为0.5 g(体积为0.6mL)。甲苯蒸汽是在10℃恒温水浴中采用空气鼓泡法得到,鼓泡气流速是5 mL/min,并用另一路空气进行稀释,稀释气流速是175 mL/min,最终得到进气浓度为1000 ppm的甲苯蒸汽加空气的混合气体。混合反应气空速为18000 h-1。反应尾气通过GC9650色谱仪进行在线分析。本实验采用甲苯的转化率(X)和CO2的选择性(S)来表征催化剂的催化性能。
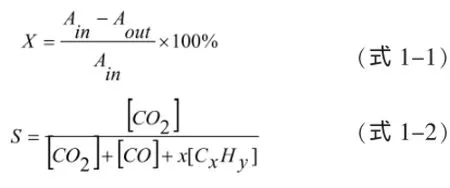
(式中Ain为进入催化剂之前甲苯的峰面积;Aout为经过催化剂后出口的甲苯的峰面积;[CO2]为反应得到CO2的组分浓度;[CO]为反应不完全燃烧产生CO的组分浓度;[CxHy]为不完全燃烧产生的CxHy的组分浓度;x为CxHy的碳原子数)
2 结果讨论
2.1Cu/Mn/Ce摩尔比对晶相结构的影响
研究表明,在浸渍法制备负载型催化剂过程中,浸渍液浓度、浸渍时间、铜锰铈摩尔比、铜锰铈负载量、焙烧温度都会影响催化剂的晶相结构。其中铜锰铈的摩尔比对晶相结构和晶粒大小的影响较大。图1和表2是不同铜锰铈摩尔比的三元复合氧化物催化剂的XRD分析结果。
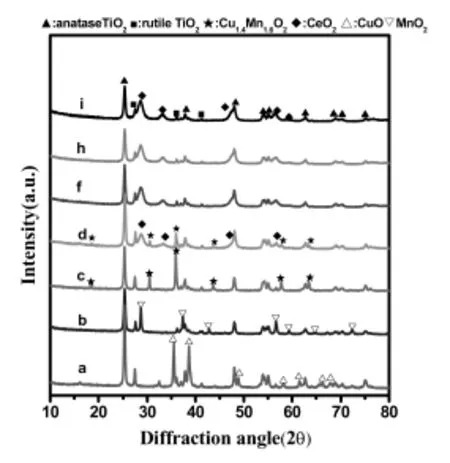
图1 不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂的XRD图Fig.1.XRD patterns of Cu-Mn-Ce ternary catalysts with different Cu/Mn/Cemolar ratios prepared by impregnationmethod
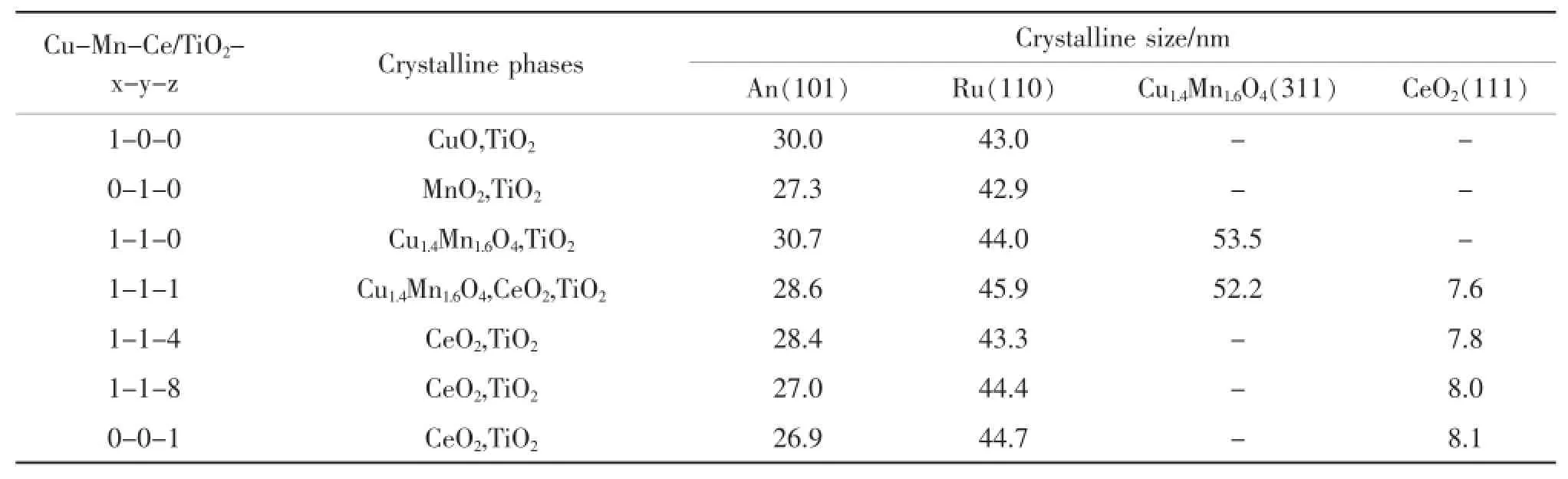
表2 不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂的活性组成和晶粒大小Table 2.Crystalline phases and crystalline size of Cu-Mn-Ce ternary catalystswith different Cu/Mn/Ce molar ratios prepared by impregnationmethod
图1为不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂的XRD衍射图。在图1中,a,b和c分别是CuO,MnO2以及CuO和MnO2以1∶1的摩尔比负载在载体TiO2上的XRD图。在a和b中,除了锐钛矿型的二氧化钛(TiO2-An)(PDF21-1272)和金红石型的二氧化钛(TiO2-Ru)(PDF21-1276)相态外,分别只有CuO(PDF48-1548)相态和MnO2(PDF24-0735)相态。当Cu/Mn的摩尔比为1:1时,在XRD图c中CuO和MnO2的特征峰消失,代之以由氧化铜和氧化锰形成的新相Cu1.4Mn1.6O4(PDF 35-1030)的衍射峰。当铈加入后,图d中同样没有观察到CuO和MnO2的特征峰,Cu1.4Mn1.6O4的衍射峰变弱,同时出现了新的CeO2(PDF43-1002)相态。随着CeO2相对含量增加(Cu/Mn/Ce的摩尔比为1∶1∶4,1∶1∶8和0∶0∶1),其XRD图(图1中f,h,i)基本没有变化,只观察到CeO2的相态,不仅没有观察到氧化铜和氧化锰的特征峰,就是Cu1.4Mn1.6O4的衍射峰也消失了。可能原因是形成了粒度很小、分散度更高的、XRD无法检测到的Cu1.4Mn1.6O4晶相[12]。也有可能是氧化铜和氧化锰以无定形的氧化态负载在载体TiO2表面,以致XRD无法检测到。可以推知较高含量的CeO2可以高度分散Cu1.4Mn1.6O4,更高含量的CeO2甚至阻碍了Cu1.4Mn1.6O4的形成。
2.2Cu/Mn/Ce摩尔比对H2-TPR峰温的影响
金属氧化物的H2-TPR峰温是催化剂的重要性质之一,代表了催化剂的氧化能力。一般而言,单一的金属氧化物都有特定的H2-TPR峰温,但当两种或三种金属氧化物形成三元催化剂时,会引起其中氧化物H2-TPR峰温的变化。主要是由于催化剂各氧化物之间的相互作用影响了氧的移动性,从而影响了氧化物的被还原性[13]。为了研究不同铜锰铈摩尔比的铜锰铈三元复合氧化物催化剂的氧化能力,本实验对其进行了H2-TPR表征。
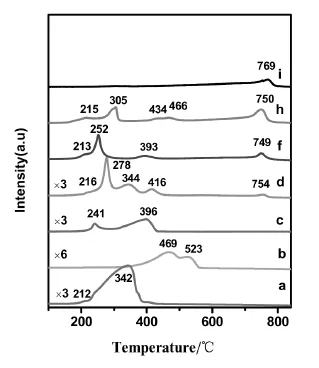
图2 不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂的H2-TPR图Fig.2.H2-TPR profiles of Cu-Mn-Ce ternary catalystswith diffferent Cu/Mn/Cemolar ratios prepared by impregnationmethod
图2为不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂的H2-TPR图。从图中可看出,不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂的H2-TPR峰型各不相同。当Cu/Mn/Ce摩尔比为1∶0∶0时,H2-TPR图a中存在着温度为212℃和343℃的两个还原峰,它们分别对应的是无定形的CuO的还原峰和晶化程度较好的大颗粒CuO的还原峰[14],说明CuO在低温段对氢有较强的氧化作用。当Cu/Mn/Ce摩尔比为0∶1∶0时,图b中存在着温度为469℃和523℃的两个还原峰,根据XRD可知,这两个峰是MnO2的还原峰[7],MnO2在中温段对氢有较强的氧化作用。当Cu/Mn/Ce摩尔比为0∶0∶1时,图i中存在着温度为769℃的还原峰,这个峰是CeO2的还原峰[7,15],说明CeO2在高温段对氢有较强的氧化作用。当催化剂Cu/Mn/Ce摩尔比为1∶1∶0时,H2-TPR图c中存在着温度为241℃和396℃的两个还原峰,低温峰为复合氧化物中铜的还原峰,高温峰为复合氧化物中锰的还原峰[16],与图a,b的单一氧化物的还原峰比,相应的峰温都有所降低,说明形成复合氧化物有利于氧的移动。随着CeO2的加入,三元复合氧化物催化剂的H2-TPR图发生了变化。当铜锰铈摩尔比为1∶1∶1时,对应的d图中出现了5个峰,216℃对应于无定形的CuO还原峰,754℃对应于CeO2的还原峰,344℃为一定粒度的CuO还原峰,278℃为复合氧化物中铜的还原峰,416℃为复合氧化物中锰的还原峰,278℃和416℃这两个峰由图c的2个峰转化而来,且都向高温方向平移。可能原因是氧化铈的作用。氧化铈的加入对铜锰复合氧化物的氢还原峰起到两个作用:一方面,复合氧化物中的铜、锰与CeO2之间存在着更强的相互作用,导致还原峰向高温方向移动;另一方面,氧化铈的加入可以高度分散Cu1.4Mn1.6O4,导致还原峰向低温方向移动。结合XRD可知,CeO2的加入后Cu1.4Mn1.6O4晶粒略微变小(表2和图1),复合氧化物中的铜、锰与CeO2之间存在着更强的相互作用,导致其还原峰向高温方向移动。随着CeO2进一步添加至铜锰铈摩尔比为1∶1∶4时,图f中出现4个还原峰,213℃对应于无定形的CuO还原峰,749℃对应于CeO2的还原峰,252℃与393℃为复合氧化物中铜、锰还原峰,此时形成的复合氧化物Cu1.4Mn1.6O4晶粒更小以至于XRD中未能出现衍射峰,此时氧化铈的加入使Cu1.4Mn1.6O4高度分散,还原峰温降低。但CeO2的过多加入阻碍了Cu1.4Mn1.6O4复合氧化物的形成。由此不难理解铜锰铈摩尔比为1∶1∶8时,图h中的5个还原峰向高温方向移动,结合H2-TPR图的a,b和i可知,215℃和305℃为CuO还原峰,434℃和466℃为MnO2的还原峰,750℃为CeO2的还原峰,还原峰分别接近单一的氧化铜,氧化锰和氧化铈的还原峰。
2.3铜锰铈三元复合催化剂的摩尔比对甲苯催化性能的影响
工业生产中所产生的挥发性气体大多是有机污染物。在这些挥发性有机污染物(VOCs)中,尤以结构稳定的含苯环的系列物(如苯,甲苯等)居多,对人体危害大。为此,实验中以甲苯催化燃烧作为探针反应,以考察不同Cu/Mn/Ce摩尔比的铜锰铈三元复合催化剂的催
化燃烧性能。实验结果如图3、4所示。
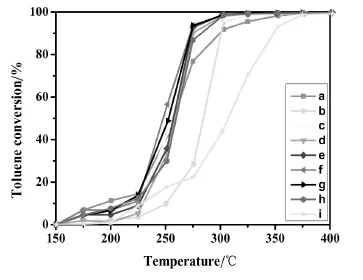
图3 不同Cu/Mn/Ce摩尔比的铜锰铈三元复合催化剂催化氧化甲苯的转化率与床层温度的关系Fig.3.Toluene conversion as a function of the reaction temperature for Cu-Mn-Ce ternary catalystswith diffferent Cu/Mn/Cemolar ratios prepared by impregnationmethod
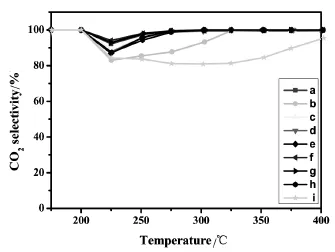
图4 不同Cu/Mn/Ce摩尔比的铜锰铈三元复合催化剂催化氧化甲苯产生CO2的选择性与床层温度的关系Fig.4.CO2selectivity as a function of the reaction temperature for Cu-Mn-Ce ternary catalysts with diffferent Cu/Mn/Cemolar ratios prepared by impregnationmethod
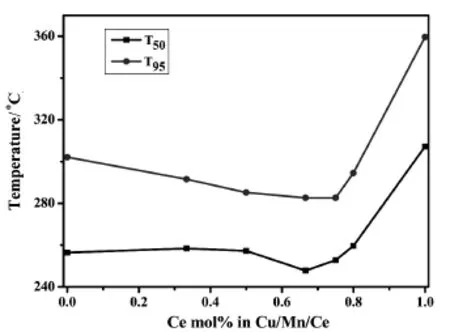
图5 不同Cemol%的铜锰铈三元复合氧化物催化剂的T50和T95Fig.5.T50,T95for Cu-Mn-Ce ternary catalystswith diffferent Cemol%prepared by impregnation method
由图3可知,随着反应温度的升高,不同Cu/ Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂对甲苯的催化转化率影响趋势大致相同,分为三个阶段:在低温阶段(150℃~225℃)时,甲苯的转化率随温度呈缓慢增加的趋势;当床层温度达到225℃之后,反应剧烈,甲苯的转化率曲线呈直线上升;直到反应温度达到275℃后,转化率趋于缓慢增加。具体分析,在不同反应温度区间,不同的催化剂所表现的反应活性不同。在低温阶段,不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂对甲苯的转化率相近。当床层温度高于225℃时,可将不同Cu/Mn/Ce摩尔比的铜锰铈催化剂分为三类情况来考察。第一类催化剂是负载有单金属氧化物催化剂,即Cu/Mn/Ce摩尔比分别为1∶0∶0,0∶1∶0和0∶0∶1的CuO/TiO2、MnO2/TiO2和CeO2/TiO2催化剂。图3和图4的结果表明,无论是甲苯的转化率,还是CO2的选择性,其催化性能的顺序是CuO/TiO2优于MnO2/TiO2,MnO2/TiO2优于CeO2/TiO2,与它们的H2-TPR峰温从低到高的顺序是一致的,这说明具有较低H2-TPR峰温的氧化物催化剂有更好的催化氧化性能。第二类是二元复合氧化物催化剂Cu-Mn-Ce/TiO2-1-1-0(即Cu-Mn/TiO2催化剂)。从图上可以看出,其甲苯的转化率和CO2的选择性明显好于上述任一单金属氧化物催化剂。由图1可知,这时形成了复合氧化物新相Cu1.4Mn1.6O4,且有更低的氧化铜和氧化锰的H2-TPR峰温(见图2中c)。由此可以推知,复合氧化物Cu1.4Mn1.6O4是具有更高催化活性的新相。在新相Cu1.4Mn1.6O4中,Cu2+和Mn4+通过相互间的协同作用[17],各自都具有较单独存在时更低的H2-TPR峰温,从而有更高的催化活性。第三类是引进CeO2后的Cu/Mn/Ce三元复合氧化物催化剂(Cu-Mn-Ce/TiO2-1-1-1,Cu-Mn-Ce/ TiO2-1-1-2,Cu-Mn-Ce/TiO2-1-1-4,Cu-Mn-Ce/ TiO2-1-1-6和Cu-Mn-Ce/TiO2-1-1-8)。从图5可以看出随着CeO2的增加,催化剂的T95先减小后增加,催化剂Cu-Mn-Ce/TiO2-1-1-4(图f)的T95最低(282.6℃),其甲苯的转化率和CO2的选择性最佳。结合图1与图2可知,当掺铈量较少时,铜锰元素主要以较大颗粒的Cu1.4Mn1.6O4尖晶石形式分散在载体和CeO2上,复合氧化物中的铜、锰与CeO2之间存在着更强的相互作用,催化剂的还原峰温较高,其T95仍较高;随着铈的进一步增加,复合物Cu1.4Mn1.6O4的晶粒度变小至XRD都无法观察到衍射峰,此时高度分散的复合氧化物形成了更多的活性中心,更好地促进氧的流动,从而有更好的催化氧化甲苯的性能;但当铈的含量增至1∶1∶8时,过多的Ce元素阻碍了Cu1.4Mn1.6O4的形成,此时没有了Cu1.4Mn1.6O4活性中心的催化剂是铜、锰、铈三种氧化物的简单混合,氧的流动性减弱,氧化铜和氧化锰的H2-TPR峰温升高,催化性能降低。
3 结论
本实验采用浸渍法制备不同Cu/Mn/Ce摩尔比的铜锰铈三元复合氧化物催化剂,对催化剂进行了XRD和H2-TPR表征分析,并对催化剂进行催化燃烧甲苯的性能评价。XRD和H2-TPR表征了不同Cu/Mn/Ce摩尔比对催化剂晶相和还原温度的影响。结果表明:铜锰复合氧化物Cu1.4Mn1.6O4形成催化活性中心,一定量CeO2的加入可以高度分散活性中心Cu1.4Mn1.6O4,催化剂的还原峰温降低;但更多量的CeO2会阻碍Cu1.4Mn1.6O4的形成,催化剂的还原峰向高温移动。因此,当Cu/Mn/Ce摩尔比为1∶1∶4时,铜锰氧化物形成的活性中心Cu1.4Mn1.6O4高度分散在供氧中心CeO2与载体上,此时的还原峰温度最低,氧移动性最强,催化剂的转化率(T95为282.6℃)与CO2选择性(100%)最高,催化氧化甲苯的性能最佳。
[1]Wang C H.Al2O3-supported transition-metal oxide catalysts for catalytic incineration incineration of toluene[J]. Cheosphere,2004,55:11-17.
[2]LiW B,Zhuang M.MCM-41 supported Cu-Mn catalysts for catalytic oxidation of toluene at low temperatures[J].J. Phys.Chem.B,2006,110:21568-21571.
[3]Chen H H,Zhang H P.Fabrication of porous copper/manganese binary oxides modified ZSM-5 membrane catalyst and potential application in the removal of VOCs[J]. Chemical Engineering Journal,2014,258:133-142.
[4]Van H V,Jamal B,Aïssa Ould-Dris,etal.Catalytic oxidation of volatile organic compounds on manganese and cop per oxides supported on titania[J].American Institute of Chemical Engineers Journal,2008,54(6):1585-1591
[5]Maria R M,Fabiola N A.Catalytic combustion of n-hexane over alumina supported Mn-Cu-Ce catalysts[J].CatalLett,2013,143:1003-1011.
[6]Larsson P O,Andersson A A.Oxides of copper,ceria promoted copper,manganese and coppermanganese on Al2O3for the combustion of CO,ethyl acetate and ethanol[J].Appl.Catal.B:environ,2000,24:175-192.
[7]Saleh M S,Dimitris IK,Xenophon EV,et al.Catalytic oxidation of toluene over binary mixtures of copper,man ganese and cerium oxides supported onγ-A l2O3[J].Applied Catalysis B:Environmental,2011,103:275-286.
[8]Unmesh M,Hilde P,Vitaliy B,et al.Nature of the active sites for the total oxidation of toluene by CuO-CeO2/Al2O3[J].Journal of Catalysis,2012,295:91-103.
[9]Dimitrios D,Theophilos I.VOC oxidation over MnOx-CeO2catalysts prepared by a combustion method[J].Applied Catalysis B:Environmental,2008,84:303-312.
[10]Beatriz de Rivas,Jose I.Gutiérrez-Ortiz,Rubén López-Fonseca,et al.Analysis of the simultaneous catalytic combustion of chlorinated aliphatic pollutants and toluene over ceria-zirconiamixed oxides[J].Applied Catalysis A:General,2006,314:54-63.
[11]Cai L N,Hu ZH,Peter B,et al.The effect of doping transition metal oxides on coppe manganese oxides forthe catalytic oxidation of CO[J].Chinese Journal of Catalysis,2014,35:159-167.
[12]Lu H F,Zhou Y,Han W F,ed al.Promoting effect of ZrO2carrier on activity and thermal stability of CeO2-based oxides catalysts for toluene combustion[J].Applied Catalysis A:General,2013,464:101-108.
[13]He C,Yu Y,Shen Q,et al.Catalytic behavior and synergistic effect of nanostructured mesoporous CuO-MnOx-CeO2catalysts for chlorobenzene destruction[J].Applied surface science,2014,297:59-69.
[14]MoralesM R,Barbero B P,Lopez T.Evaluation and characterization of Mn-Cu mixed oxide catalysts supported on TiO2and ZrO2for ethanol total oxidation[J].Fuel,2009,88: 2122-1229.
[15]Markaryan G L,Ikryannikova L N,Muravieva G P,et al. Red-ox properties and phase composition of CeO2-ZrO2and Y2O3-CeO2-ZrO2solid solutions[J].Colloids and SurfacesA:Physicochemical and Engineering Aspects,1999,151:435-447.
[16]MoralesM R,Barbero B P,Cadus L E.Total oxidation of ethanol and propane over Mn-Cumixed oxide catalysts[J]. App lied Catalysis B:Environmental,2006,67:229-236.
[17]Porta P,Moretti G,Musicanti M,et al.Characterization of copper-manganese mixed oxides[J].Catalysis Today,1991,9:211-218.
Study of the Cu/M n/Ce Ternary Catalysts on Performance for Catalytic Oxidation of Toluene
ZHU Hong-na1,LV De-yi1,HUAN Chang-yong2*
(1.College of Chemical Engineering,Zhejiang University of Technology,Hangzhou,Zhejiang 310014,China;2.National Post-Doctoral Scientific Research Center of Ningbo Petrochemical Economic& Technological Development Zone,Ningbo,Zhejiang 315204,China)
The different Cu/Mn/Cemolar ratio of Cu-Mn-Ce ternary catalystswere prepared by impregnation method and characterized by XRD and H2-TPR.Their performances for catalytic oxidation of toluene were evaluated in a fixed-bed tubular reactor,and the correlation of catalytic activity with active phases and oxygen mobility was discussed.The results showed that copper manganese oxide formed a new phase Cu1.4Mn1.6O4as the catalytic center,then the addition of CeO2highly dispersing Cu1.4Mn1.6O4increased the oxygenmobility of catalysts.So the Cu/Mn/Cemolar ratio 1∶1∶4 of Cu-Mn-Ce ternary catalyst showed the the best catalytic activity,with a lowest reaction temperature(T95was 282.6℃)and 100%selectivity of CO2.
copper-manganese-cerium ternary oxide catalyst;molar ratio;toluene
1006-4184(2016)10-0029-07
2016-04-08
朱红娜(1991-),女,硕士研究生。E-mail:337089446@qq.com。
郇昌永,E-mail:huanmy2006@163.com。
