磷石膏脱硫钙渣浸取液中杂质对碳酸钙晶型的影响
2016-11-12陈秋鸽王戬张志业王辛龙杨林钟本和杨秀山
陈秋鸽,王戬,张志业,王辛龙,杨林,钟本和,杨秀山
(四川大学化学工程学院,四川 成都 610065)
磷石膏脱硫钙渣浸取液中杂质对碳酸钙晶型的影响
陈秋鸽,王戬,张志业,王辛龙,杨林,钟本和,杨秀山
(四川大学化学工程学院,四川 成都 610065)
磷石膏脱硫钙渣是磷石膏化学分解后产生的以氧化钙为主要成分的尾渣。以氯化铵溶液浸取磷石膏脱硫钙渣并碳化浸取液以制备轻质碳酸钙是一种有效利用磷石膏脱硫钙渣中钙资源的方法。本文分析了该方法在不同氯化铵浓度下浸取液的组成、钙浸出率及pH,同时为了研究浸取液中NH4+、铁、铝、镁等对产品碳酸钙晶型的影响,配制了含有杂质离子的NH4Cl-NH3·H2O溶液,比较了其碳化产品与相同条件下脱硫钙渣碳化产品的晶型差异。结果表明,随氯化铵浓度升高,浸取液pH降低,铝含量降低,铁、镁含量升高。在氯化铵浓度范围内,NH4+对球霰石形成有促进作用,而铁、镁杂质对方解石形成有促进作用,由于铝离子存在形态不同,铝在1mol/L时对形成球霰石有促进作用,在大于1mol/L时对形成方解石有促进作用。当氯化铵浓度小于4mol/L时,各种杂质相互作用形成球霰石晶型,氯化铵浓度等于4mol/L时,各种杂质相互作用形成球霰石和方解石混合晶型。
磷石膏脱硫钙渣;氯化铵;杂质影响;碳酸钙晶型
磷石膏是湿法磷酸生产的副产物。据统计,生产1t磷酸(100%P2O5)会产生5~6t的磷石膏(干基)。据统计,目前我国堆存的磷石膏量已经超过了5亿吨,并且磷石膏的产量还将随着我国磷矿的贫化以及高浓度磷复肥产量的升高而大幅度增加[1]。目前,磷石膏利用以水泥缓凝剂、纸面石膏板等低值建材产品为主[2-3],但其综合利用率却不足30%[4],大量未能利用的磷石膏只能耗费巨资建设堆场堆存。但是磷石膏中含有P2O5、F及游离酸、有机物等有害物质[5],大量堆存对生态环境造成了严重影响和威胁[6]。
化学分解制备硫酸是利用磷石膏的重要途径之一,国内外对相关研究已有较多报道[7-12]。其中四川大学杨秀山等[10]提出了硫磺高温还原分解磷石膏制硫酸的工艺,有效实现了磷石膏中硫资源的利用,但该工艺会产生主要成分为氧化钙的磷石膏脱硫钙渣,能否高值化利用是该工艺转化应用的关键。本文作者课题组前期的研究可知,磷石膏脱硫钙渣中CaO含量为73.34%,SiO2含量为10.63%,此外,其中还含有Al2O3、Fe2O3、MgO等物质,它们的含量分别是3.09%、1.78%、0.85%[13]。对钙资源的利用,时婷等[13]提出了以氯化铵浸取磷石膏脱硫钙渣制备轻质碳酸钙的工艺,通过一步浸取、碳化,得到纯度较高的碳酸钙,实现了磷石膏脱硫钙渣的高值化利用。
碳酸钙属于多型晶体,通常有3种晶型,即方解石型、文石型、球霰石型,自然界中碳酸钙通常以方解石型存在。在某些晶型控制剂存在时,碳酸钙往往会以除方解石型以外的其他晶型存在,或者会以几种晶型混合的形式出现[14]。碳酸钙的晶型是其最重要的技术指标之一,碳酸钙晶型的不同,会直接影响到碳酸钙的应用[15]。在轻质碳酸钙的生产中,通常需要根据碳酸钙产品的用途制备不同晶型的碳酸钙,例如针状的文石型碳酸钙主要应用于橡胶行业,球形的球霰石碳酸钙主要用于造纸、油墨及塑料行业。
但是,由于浸取液中含有少量的铁、铝、镁等杂质,对轻质碳酸钙的晶型会产生重要影响[16-17]。本文首次对氯化铵浸取磷石膏脱硫钙渣的浸取液中铁、铝、镁等杂质的含量进行了分析,探讨了铁、铝、镁、NH4+等杂质对碳酸钙晶型的影响。
1 实验部分
1.1实验试剂和仪器
NH4Cl、CaCl2、FeCl3、MgCl2、AlCl3、NH3·H2O,成都市科龙化工试剂厂;去离子水,自制;磷石膏,四川宏达股份有限公司渣场;磷石膏脱硫钙渣,自制;CO2,成都市东风工业气体经营部。
恒速搅拌器,无锡申科仪器有限公司;恒温水浴槽,郑州汇成科工贸有限公司;二氧化碳流量控制器,常州双环热工仪表有限公司;PHS-25C型数字酸度计,上海鹏顺科学仪器有限公司;TP-A1000型电子天平,福州华志科学仪器有限公司;DHG-9140A型电热恒温鼓风干箱,上海圣欣科学仪器有限公司;SHB-Ⅲ型循环水式多用真空泵,北京科伟永兴仪器有限公司;7000 DV型电感耦合等离子体发射光谱仪;X'pert Pro MPD型X射线衍射仪,荷兰帕纳科公司;JSM-7500F型扫描电子显微镜,日本电子。
1.2试验方法
1.2.1磷石膏脱硫钙渣浸取液的制备
称量磷石膏脱硫钙渣10g于三口烧瓶中,加入200mL一定浓度的氯化铵溶液,将装置放入60℃恒温水浴中,550r/min搅拌下浸取30min。抽滤,滤液即为浸取液。对所得浸取液进行分析(测量pH,测量钙、铁、铝、镁等含量),pH用数字酸度计测量,钙含量用EDTA滴定法测定,分析步骤参见国标GB/T 19281—2003,钙浸出率计算见式(1),铁、铝、镁等含量用电感耦合等离子体发射光谱仪测定。

1.2.2含杂质的NH4Cl-NH3·H2O溶液制备
在氯化铵浸取脱硫钙渣的浸取液中,形成了NH4Cl-NH3·H2O的缓冲溶液。NH4+的存在形成了盐溶效应,增大了钙的溶解度,使钙离子的浓度比单纯的氧化钙溶解得到的溶液中钙离子浓度大。为了探讨溶液中NH4+和铁、铝、镁等杂质对碳酸钙晶型的影响,按照表1所用氯化铵的浓度及浸取后浸取液的pH,配制相应的NH4Cl-NH3·H2O缓冲母液。根据该浓度下所测出的各离子的含量分别配置仅有某种杂质元素的氯化物溶解后制得相应溶液。
1.2.3浸取液的碳化
将浸取液移入三口烧瓶中,放入20℃恒温水浴中,使浸取液温度为20℃。200r/min搅拌下通入CO2,CO2流量为60mL/min,待溶液pH为7时停止通CO2,过滤,用去离子水洗涤2~3次,80℃下干燥12h。产品做XRD、SEM表征:XRD扫描角度10°~85°,确定碳酸钙的晶型;SEM确定碳酸钙的形貌。
2 结果与讨论
2.1脱硫钙渣浸取分析
2.1.1浸取液分析
为了确定不同浓度时浸取液的组成,分别配制4种浓度的氯化铵溶液,1mol/L、2mol/L、3mol/L、4mol/L,制备磷石膏脱硫钙渣浸取液,对浸取液进行分析,得到分析结果如表1。
由表1可以看出,随氯化铵浓度的增加,浸出液的pH依次降低,因为氯化铵是强酸弱碱盐,其pH会随氯化铵浓度的升高而降低。氯化铵浓度由1mol/L升高至2mol/L时,钙浸出率有明显的升高,由65.84%升高至73.49%之后,随着氯化铵浓度的增加,钙浸出率变化不大。氯化铵浓度为4mol/L时钙的浸出率已基本达到平衡,并且考虑到实际原料成本,氯化铵的浓度值不宜超过4mol/L。铁、铝、镁等3种杂质元素的含量随氯化铵浓度的增加呈现不同的趋势:铝含量在氯化铵浓度为1mol/L时含量最高,之后逐渐降低,因为铝是两性的,氯化铵浓度为1mol/L时,浸取溶液pH为10.28,碱性较强,促进了铝的溶解。之后,随氯化铵浓度的增加,浸取液的pH逐渐降低,所以铝的溶解能力有所下降。而铁和镁不是两性的,在溶液中的含量则是碱性越弱含量越高,所以随氯化铵浓度的增加,它们的含量都是升高的。浸取液中杂质元素含量的不同,可能会对产品碳酸钙的晶型产生一定的影响。
2.1.2产品分析
将2.1.1节中4种浓度的浸取液按相同的碳化条件碳化,碳化温度为20℃,搅拌速度为200r/min,CO2流量为60mL/min,得到产品分别做XRD、SEM表征,得图1、图2。
由图1 XRD图与PDF标准卡(PDF Number:33-0268,05-0586)对照,可以看出当氯化铵浓度为1~3mol/L时,产品主要为球霰石相。但当氯化铵浓度为4mol/L时,产品除了主要的球霰石相以外,还可以明显看到方解石的峰,对其XRD数据进行定量分析计算得出该氯化铵浓度下所得产品中球霰石质量分数为94.2%,方解石质量分数为5.8%。氯化铵浓度为4mol/L时,溶液中铝含量低,而铁、镁两种杂质元素含量较高,有文献报道Mg2+作为晶型控制剂可以促使碳酸钙晶型为文石或球霰石[17],NH4+的存在会诱导生成球霰石[18],而浸取液中的铁、铝杂质也会对碳酸钙晶型产生影响,这些阳离子吸附在生成的碳酸钙表面,取代Ca2+在晶格中的位置,从而使碳酸钙形成不同晶型。所以这些杂质的相互作用产生了球霰石及方解石的混合晶型。

图1 不同浓度氯化铵溶液浸取脱硫钙渣碳化产品XRD

表1 不同氯化铵浓度的浸取液成分分析

图2 不同浓度氯化铵溶液浸取脱硫钙渣碳化产品SEM图
由图2中各氯化铵浓度所得产品的SEM图像也可看出,当氯化铵浓度为1~3mol/L时,碳酸钙产品的形貌主要以球形的球霰石为主,但当氯化铵浓度为4mol/L时,除了大量的球霰石之外,还能看到少量的立方形的颗粒,其晶型即为方解石型,与XRD结果相一致。
2.2不同氯化铵浓度时杂质对碳酸钙晶型影响分析
图3是不同氯化铵浓度仅有一种杂质时得到的碳酸钙与仅有NH4+的产品的XRD图。
为了探讨溶液中杂质对碳酸钙的影响,以空白实验1(仅含有NH4+)与仅有每种金属杂质所得产品相互之间作对比。对不同氯化铵浓度时各产品XRD进行定量分析得表2。

表2 不同氯化铵浓度时产品晶型比例
当氯化铵浓度为1mol/L时,仅有一种杂质时产品晶型都为球霰石和方解石的混合[图3(a)]。由第1、第2组相应产品晶型含量对比可得,仅有铁的产品与仅有NH4+的产品晶型含量一致,是由于该浓度下铁含量非常少,对产品晶型影响表现不明显;对比第1、第3组相应产品发现,仅有铝时球霰石增多,但在该氯化铵浓度下溶液的pH很高,铝可能在溶液中以铝酸根或偏铝酸根形式存在,实际的铝离子含量十分少,在氯化铵浓度为1mol/L时铝对形成球霰石有促进作用;同理,对比第1、第4组可得在该氯化铵浓度下,镁的存在有利于方解石的形成,这与文献报道的镁离子对晶型影响的结果不同,这是由于本文与文献报道的碳化溶液体系存在明显差异。该氯化铵浓度下,仅有镁存在时,由于溶液中NH4+含量相对较 少,同时又没有铝的影响,减弱了生成球霰石的趋势。而脱硫钙渣制得的产品为较纯净的球霰石。所以,在氯化铵浓度为1mol/L时,溶液中NH4+对产品晶型的作用明显强于其他3种杂质,最终形成球霰石型碳酸钙。
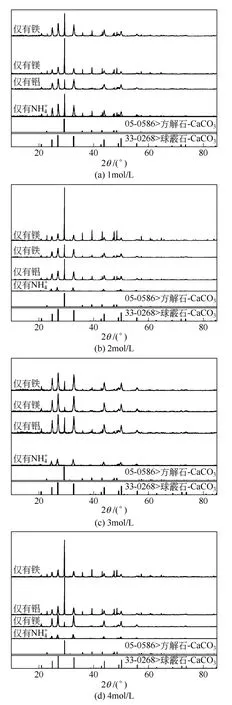
图3 不同氯化铵浓度时仅有一种杂质的碳化产品XRD图
当氯化铵浓度为2mol/L时,仅有一种杂质时产品晶型也是球霰石和方解石的混合[图3(b)]。由表2对比第1、第2组对应数据,可以看出铁的存在对方解石的形成有促进作用;对比第1、第3组对应数据,发现仅有铝时方解石的量有所增加,则此时铝对方解石形成有促进作用,这与氯化铵浓度为1mol/L时不同,这可能是由于不同氯化铵浓度时铝的形态不同导致的:氯化铵浓度为1mol/L时,溶液pH较高,大部分铝以铝酸根离子存在,对形成球霰石有促进作用,而随着氯化铵浓度增加后,溶液pH降低,铝主要以铝离子形式存在,对形成方解石却有促进作用;由第1、第4组相应数据对比可知,镁对方解石形成有促进作用。但此时溶液中NH4+含量较高,对球霰石又有促进作用。所以,该氯化铵浓度下溶液中4种离子的相互作用形成了球霰石型碳酸钙,其中NH4+对球霰石的促进作用明显比其他3种金属杂质对方解石的促进作用强。
当氯化铵浓度为3mol/L时,仅有NH4+时产品为比较纯净的球霰石,而仅有一种金属杂质时产品晶型都为球霰石和方解石的混合[图3(c)]。对比表2中第1、第2两组相应实验数据可得,在此氯化铵浓度下,铁对形成方解石有促进作用;对于铝,相比于空白试验1,仅有铝时方解石含量有所增加,是由于随氯化铵浓度增加,溶液pH降低,溶液中更多的铝以铝离子的形式存在,对方解石形成产生促进作用;由3mol/L时第1、第4组对比可知,仅有镁时,有少量方解石形成,则在此氯化铵浓度下,镁对方解石有微弱的促进作用。因此,在此氯化铵浓度下,溶液中NH4+的作用强于铁铝镁3种杂质的作用,使脱硫钙渣制得的产品晶型为球霰石。
当氯化铵浓度为4mol/L时,铝含量较少,仅有NH4+时产品比较纯净的球霰石,而仅有一种金属杂质时产品晶型都为球霰石和方解石的混合[图3(c)]。由第1、第2组在4mol/L时对比可知,铁对形成方解石的形成有促进作用。此时溶液中的铁含量达到最大,方解石含量也较多;仅有铝的产品与无杂质的产品含量相比(第1、第3组),方解石较多,溶液pH更低,溶液中对方解石形成有促进作用的铝离子也更多;由第1、第4组相应产品对比知此氯化铵浓度时镁对方解石依然表现出微弱的促进作用。所以氯化铵浓度为4mol/L时,溶液中NH4+和3种杂质对产品的晶型影响表现为较强的促进球霰石的NH4+以及少量促进方解石形成的杂质。
综上所述,在磷石膏脱硫钙渣的氯化铵浸取液中,溶液组成及pH随氯化铵浓度的增加而变化。随着氯化铵浓度的增加,溶液中铁对碳酸钙晶型的影响由1mol/L时不明显到促进方解石形成;由于铝是两性金属,在pH较高的1mol/L时由于形成铝酸根或偏铝酸根而没有表现出对方解石的促进作用,随着氯化铵浓度的增加及浸取液pH的降低,铝对方解石的促进作用随即表现出来;溶液中镁对方解石的形成也表现为促进作用。
3 结 论
(1)氯化铵浸取磷石膏脱硫钙渣的浸取液中,随氯化铵浓度升高,溶液pH逐渐降低,铝含量降低,铁、镁含量升高。
(2)不同氯化铵浓度下对碳酸钙晶型起主要作用的杂质各不相同:氯化铵浓度小于4mol/L时,溶液中杂质的相互作用使产品碳酸钙的晶型为球霰石;氯化铵浓度等于4mol/L时,溶液中杂质的相互作用使产品为球霰石和方解石的混合。
(3)在磷石膏脱硫钙渣的不同氯化铵浓度的浸取液中,NH4+对球霰石形成有促进作用;而铁、镁杂质对方解石形成有促进作用,由于铝随氯化铵浓度变化存在形态不同,其在1mol/L对形成球霰石形成有促进作用,在大于1mol/L时对方解石形成有促进作用。
[1] 杨秀山,刘荆风,余家鑫,等.磷石膏制硫酸的研究进展[J].现代化工,2010,30(9):8-12.
[2] 方祖国,宁平,杨月红,等.复合还原剂还原分解磷石膏的影响因素[J].化工进展,2009,28(3):522-527.
[3] 田立楠.磷石膏综合利用[J].化工进展,2002,21(1):56-59.
[4] 叶学东.磷石膏综合利用现状及加快发展的建议[J].磷肥与复肥,2014,29(6):1-3.
[5] 钟本和,王辛龙,张志业,等.我国磷石膏利用途径的探讨[J].磷肥与复肥,2010,25(3):61-63.
[6] 王辛龙,张志业,杨秀山,等.我国磷石膏利用新途径的分析[J].现代化工,2011, 31(5):1-5.
[7] 刘少文,张茜,吴元欣,等.热分析在磷石膏制酸反应研究中的应用[J].化工进展,2008,27(5):761-764.
[8] MA L P,NING P,ZHENG S C,et al.Reaction mechanism and kinetic analysis of the decomposition of phosphogypsum via a solid-state reaction[J].Industrial and Engineering Chemistry Research,2010,49(8):3597-3602.
[9] ZHENG S C,NING P,MA L P,et al.Reductive decomposition of phosphogypsumwith high-sulfur-concentration coal to SO2in an inert atmosphere[J].Chemical Engineering Research and Design,2011,89(12):2736-2741.
[10] YANG X S,ZHANG Z Y,WANG X L,et al.Thermodynamic study of phosphogypsum decomposition by sulfur[J].The Journal of Chemical Thermodynamics,2013,57(2013):39-45.
[11] 庞仁杰.以硫代碳化学分解石膏制硫酸的可行性分析[J].硫酸工业,2015(2):22-25.
[12] 郑绍聪,宁平,汪帆,等.磷石膏热分解制备二氧化硫和氧化钙研究[J].无机盐工业,2013,49(9):45-47.
[13] 时婷,王新刚,巫建峰,等.磷石膏脱硫钙渣制备轻质碳酸钙[J].化工进展,2015,34(1):178-182.
[14] 陈先勇,唐琴,史伯安,等.多种晶形超细碳酸钙的制备研究[J].化学工程师,2005,19(3):13-15.
[15] NORA H.de L,STEPHEN CP.Surface structure and morphology of calcium carbonate polymorphs calcite,aragonite,and vaterite: an atomistic approach[J].Journal of Physical Chemistry B,1998,102:2914-2922.
[16] HELMUT C.Precipitation of carbonates: recent progress in controlled production of complex shapes[J].Current Opinion in Colloid and Interface Science,2003,8:23-31.
[17] 王勇,赵风云,胡永琪,等.晶型控制剂对沉淀碳酸钙晶型、形态的影响[J].无机盐工业,2006,38(3):5-8.
[18] NICOLE G,HELMUT C,NICOLA P,et al.Superstructures of calcium carbonate crystals by oriented attachment[J].Crystal Growth & Design,2005,5(4):1317-1319.
Effects of impurities in leaching liquid of phosphogypsum desulfurization slag on crystal form of calcium carbonate
CHEN Qiuge,WANG Jian,ZHANG Zhiye,WANG Xinlong,YANG Lin,ZHONG Benhe,YANG Xiushan
(College of Chemical Engineering,Sichuan University,Chengdu 610065,Sichuan China)
Phosphogypsum(PG)desulfurization slag is the residue from chemical decomposition of PG,of which the main component is CaO. Leaching PG desulfurization slag with an ammonium chloride solution and carbonating with CO2to prepare calcium carbonate is an effective way to utilize the calcium in the slag. In this paper,the composition,calcium leaching rate and pH of leaching liquid in different concentrations of ammonium chloride were analyzed. To find out the influence of ions such as ammonia,iron,aluminum and magnesium in the leaching liquid on the crystal form of calcium carbonate,NH4Cl-NH3·H2O solution containing impure ions were prepared and the XRD crystal forms of products were compared with the products obtained by PG desulfurization slag under the same conditions. It turned out that with the increasing of ammonium chloride concentration,pH value and content of aluminum decreased,while the content of iron and magnesium increased. Within the scope of the concentration of ammonium chloride,NH4+has a promoting effect on the formation of vaterite;iron and magnesium facilitate the formation of calcite. Because aluminum's form is different with the increasing of ammonium chloride concentration,aluminum facilitates the formation of vaterite when the concentration of ammonium chloride was 1mol/L,but facilitates the formation of calcite when the concentration of ammonium chloride was up to 1mol/L. The interaction of impurities made the crystalform of vaterite when the concentration of ammonium chloride was below 4mol/L. However,when the concentration of ammonium chloride was 4mol/L,the interaction of impurities made the product a mixture crystal form of vaterite and calcite.
PG desulfurization slag;ammonium chloride;effects of impurities;crystal form of calcium carbonate
TQ 09
A
1000-6613(2016)11-3714-06
10.16085/j.issn.1000-6613.2016.11.049
2016-05-03;修改稿日期:2016-06-28。
国家高技术研究发展计划(2011AA06A106)及四川大学青年教师科研启动基金(2014SCU11020)项目。
陈秋鸽(1991—),女,硕士研究生。E-mail chqiuge@sina.com。联系人:杨秀山,博士,研究方向为化工资源与环保。E-mail yangxs@scu.edu.cn。
