氧化还原条件对城市水体沉积物重金属迁移转化的影响
2016-11-11黄凌霞
张 密, 文 波, 黄凌霞, 杜 璟, 邓 泓,3,4
(1.华东师范大学生态与环境科学学院,上海 200241;2.华东师范大学图书馆,上海 200241;3.华东师范大学上海市城市化生态过程与生态恢复重点实验室,上海 200241;4.华东师范大学浙江天童森林生态系统国家野外科学观测研究站,上海 200241)
氧化还原条件对城市水体沉积物重金属迁移转化的影响
张密1,文波1,黄凌霞1,杜璟2,邓泓1,3,4
(1.华东师范大学生态与环境科学学院,上海200241;2.华东师范大学图书馆,上海200241;3.华东师范大学上海市城市化生态过程与生态恢复重点实验室,上海200241;4.华东师范大学浙江天童森林生态系统国家野外科学观测研究站,上海200241)
以重金属Zn、Fe为研究对象,选取长风公园内的银锄湖和华东师范大学内的丽娃河的沉积物,通过室内模拟水生植物根际泌氧的周期性变化,研究4种不同氧化还原条件:好氧(+O)、厌氧(-O)、好氧后厌氧(+O→-O)和高度厌氧(--O)对沉积物中重金属迁移转化的影响.结果表明,与厌氧处理相比,好氧处理下银锄湖沉积物中可氧化态Fe比例由5.53%下降至4.60%,可还原态Fe比例由13.77%上升至16.20%,残渣态Fe比例由81.08%上升至83.49%,而且Fe向上清液中的释放量减少;弱酸提取态Zn比例由30.14%下降至29.16%,可还原态Zn比例由25.40%下降至23.90%,可氧化态Zn比例由35.73%下降至32.72%,残渣态Zn比例由32.73%上升至35.92%,最终使得上清液中Zn的含量较低.相关性分析结果表明沉积物中可氧化态和可还原态Fe、Zn存在相关性.本研究将对城市富营养化水体生态恢复过程中的风险分析及评价提供科学依据.
城市河流; 沉积物; 氧化还原电位; 充气; Fe; Zn; 迁移转化
0 引 言
在城市化过程中,工业发展、农业生产以及居民活动等向环境中不断排放的重金属污染物逐年增加,并通过灌溉、排污、大气沉降以及河水径流最终汇入河流中,进入河流的重金属在物理沉淀和化学吸附作用下沉积在底泥中,但是在水流冲刷、船舶活动、挖掘活动和水生动物活动等外在因素条件下引起的底泥再悬浮,使被吸附和螯合的重金属再次释放出来,引发“二次污染”,河流的生态系统崩溃,释放的重金属被水生动植物吸收,通过食物链的生物放大作用积累在人体中,重金属污染具有潜伏时间长、毒性危害大以及难去除的特点[1-3].随着对环境质量越来越多地关注在对环境进行修复时,采取物理、化学以及生物修复方法,其中物理、化学修复方法不能从根本上解决问题,反而会引起更严重的污染情况.但是生物修复方法无论从环境效益还是经济效益来看,都能安全有效地修复河流,成为当前国内外研究和开发热点领域[4].有研究表明,大量水生植物对重金属Zn、Cd、Pb、Cr、Ni、Cu、Fe等有很强的吸收积累能力[5].水生植物在生长过程中,由于根系的泌氧作用,在根际周围形成氧化层,一些还原态的重金属被氧化后沉积于根表面,形成氧化物膜,从而影响根际重金属的迁移转化[6-7],但是水生植物修复过程中根系泌氧会改变沉积物氧化还原电位,使沉积物重金属在吸附-解吸、氧化还原等反应下被释放到上层水界面,造成水质的“二次污染”[8-10].还有研究表明在氧化条件下,铁离子和锰离子以氧化难溶物的形式沉积,当土壤风干(通气状况良好)时,土壤吸收氧气的能力增强,氧化环境明显,则难溶性的ZnS会被氧化成可溶性的ZnSO4或S2-被氧化成H2SO4使土壤pH值降低,ZnS的溶解度增加,Zn2+大量游离于土壤溶液中,加重对土壤环境的污染[11],所以随着Eh升高,Zn的淋溶量也会增大[12].在还原条件下,水中的Fe3+被还原成Fe2+再与S2-结合生成FeS沉淀[13].本研究通过室内模拟水生植物生长旺盛期根际氧化状态和水生植物停止生长后的根际缺氧状态,研究不同氧化还原条件变化对城市河流沉积物中重金属Fe和Zn赋存形态及水质的影响,以揭示水生植被恢复的环境效应,为城市河流的生态修复和管理提供科学依据.
1 材料与方法
1.1实验材料
本研究选择了上海普陀区两条富营养化水体(银锄湖和丽娃河)的沉积物作为研究对象.其中银锄湖位于上海市普陀区长风公园,兴建于1956年,面积达3.66×105m2,其中水面积1.43×105m2.在研究中发现(未发表结果),银锄湖水体富含栅藻和小球藻等浮游藻类,栅藻是主要优势种.水体总氮含量约为2.25 mg/L,总磷含量约为0.16 mg/L,根据地表水环境质量评价标准为Ⅲ类—劣Ⅴ类水质.湖内无大型藻类和水生植物,也未曾采用过水生植物进行水体的生态修复.
丽娃河位于华东师范大学中山北路校园内,曾为苏州河的支流,因为长期的富营养化,自2005年起对丽娃河实施以水生植被恢复为重点的生态修复工程,相比银锄湖水质较好,目前水生植物(主要是水盾草)生长良好,浮游藻类以衣藻和小球藻为主,河道的生态环境也相对改善[14].但丽娃河水体总氮含量约为1.88mg/L,总磷含量约0.21 mg/L,根据地表水环境质量评价标准仍为Ⅲ—Ⅳ类水质.
1.2方法
1.2.1样品采集及理化性质分析
2014年4月,用抓斗式采泥器分别采集银锄湖中央和丽娃河南岛附近表层底泥,现场去除贝壳、大块石砾和动植物残体后带回实验室.将采集回实验室的沉积物土样自然条件下风干,研钵研磨过20目尼龙筛,装入自封袋中备用,并用四分法取部分样品磨碎过100目筛,用元素分析仪(vario MICRO cube)测定沉积物中总氮、总磷和总硫的含量,使用火焰原子吸收分光光度法[15]测定沉积物中Zn、Fe含量(分析过程中加入国家标准物质GBW07423和GBW07437进行分析质量控制,回收率均在国家标准参比物质的允许范围内),利用重铬酸钾-硫酸外加热法测定总有机碳[16].其基本理化指标见表1.
1.2.2试验处理
分别称取自丽娃河、银锄湖采集的50 g过20目尼龙筛的风干沉积物样品,置于250 mL锥形瓶中,加蒸馏水250 mL,混匀,锥形瓶上粘贴黑色胶带使之完全避光.采取以下4种方式模拟沉积物的氧化还原状况,并用便携式溶氧仪测定溶液中DO(溶解氧)浓度.
(1)好氧(+O)处理:向培养瓶中通入空气,每天通气12 h,其余时间密封静置,模拟好氧环境(如植物生长时根际泌氧)对沉积物的影响.溶液中DO浓度>5.6~6.7 mg/L.
(2)厌氧(-O)处理:密封静置,不通入任何气体,模拟一般的沉积物水土界面还原环境(如无植物生长)对沉积物的影响.溶液DO浓度为1.6~2.3 mg/L.
(3)高度厌氧(--O)处理:向培养瓶中通纯氮气,每天通气12 h,其余时间密封静置,模拟高度还原环境(如植物死亡后残体分解)对沉积物的影响.溶液中DO浓度为0.05~0.11 mg/L.
(4)好氧后厌氧(+O→-O)处理:先好氧(+O)处理(处理方法同(1))2周,再厌氧(-O)处理(处理方法同(2))2周,模拟植物生长时的根际氧化状态和停止生长后的根际缺氧状态.
每个处理均设置3个重复,实验周期为28 d,培养开始时及开始后每7 d利用便携式测试仪(Eutech Instruments)测定上清液中的pH和Eh,用塑料针筒抽取上清液50 mL(测定和取样时间为通气处理之前),共取样5次.每次取样后补充50mL蒸馏水于培养瓶中.
抽取的水样过0.45 μm滤膜并加酸酸化(pH=2)后使用火焰原子吸收分光光度法测定重金属Zn和Fe.培养结束后,取出底泥,使用冷冻干燥机冻干,研钵研磨过100目尼龙筛,用修正后的BCR连续提取法[17]分析重金属Zn和Fe形态,重金属的形态根据提取步骤的顺序依次分为弱酸提取态(包含水溶态,可交换态和碳酸盐结合态)、可还原态(铁锰氧化物结合态)、可氧化态(有机物和硫化物结合态)和残渣态,提取液中的Zn、Fe也使用原子吸收分光光度法测定.
1.2.3数据处理及统计方法
实验期间,对不同培养条件下上清液中Zn与Fe的释放速率按以下公式换算:
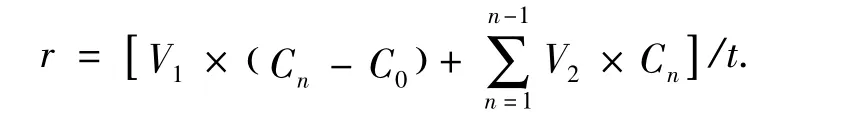
式中r表示释放速率(mg/7d);V1表示处理后样品的总体积(L);Cn,C0分别为处理后第n周和处理前所测的上清液浓度(mg/L);V2表示处理后每次抽取上清液的体积(L);t表示释放时间(7d).
数据用Excel和SPSS 19.0进行相关的统计分析.
2 结果与讨论
2.1银锄湖与丽娃河的沉积物基本特征
银锄湖和丽娃河沉积物中总磷(TP)、总氮(TN)和重金属Fe、Zn的总量及金属主要吸附相有机碳和硫的含量情况见表1.这两种沉积物样品中Fe、Zn含量差异不大,可能是这两个样点的沉积物的地球化学背景较类似.而银锄湖内总有机碳(TOC)和总硫含量高于丽娃河可能是湖泊沉积导致[18],也可能与银锄湖未经过植被恢复有关.
2.2上清液中pH和Eh的变化
由表2可知,丽娃河和银锄湖的泥水混合物的上清液在培养前后pH值发生较大变化,并且在不同的培养条件下有不同的表现.总体来说,pH值有随着氧化还原电位降低而降低的趋势,而且在先通氧后厌氧条件培养下(+O→-O)的pH值略高于高度厌氧处理(--O).通过对丽娃河和银锄湖沉积物培养后的上清液的pH和Eh的相关性分析发现,丽娃河的pH和Eh呈显著正相关(R=0.641,P<0.05),银锄湖的pH和Eh呈极显著正相关(R= 0.835,P<0.01).pH值会随着Eh下降而减小可能是由于丽娃河和银锄湖表层沉积物中沉降了大量的有机质,特别是银锄湖(见表1),在厌氧条件下有机质会在厌氧微生物的作用下发生降解产生酸性物质,而本研究中各培养过程中并不进行定期更新,导致酸性物质大量积累,使溶液pH值下降.石晓勇等[19]在研究东海外海区溶解氧和pH的分布特征中发现受径流影响较小的海水pH值与溶解氧呈显著正相关,而水体氧化还原电位受水体溶解氧的影响,所以海水pH与氧化还原电位呈显著正相关.

表1 本研究中的供试沉积物理化性质Tab.1 Physio-chemical characteristics of sediments in the present study
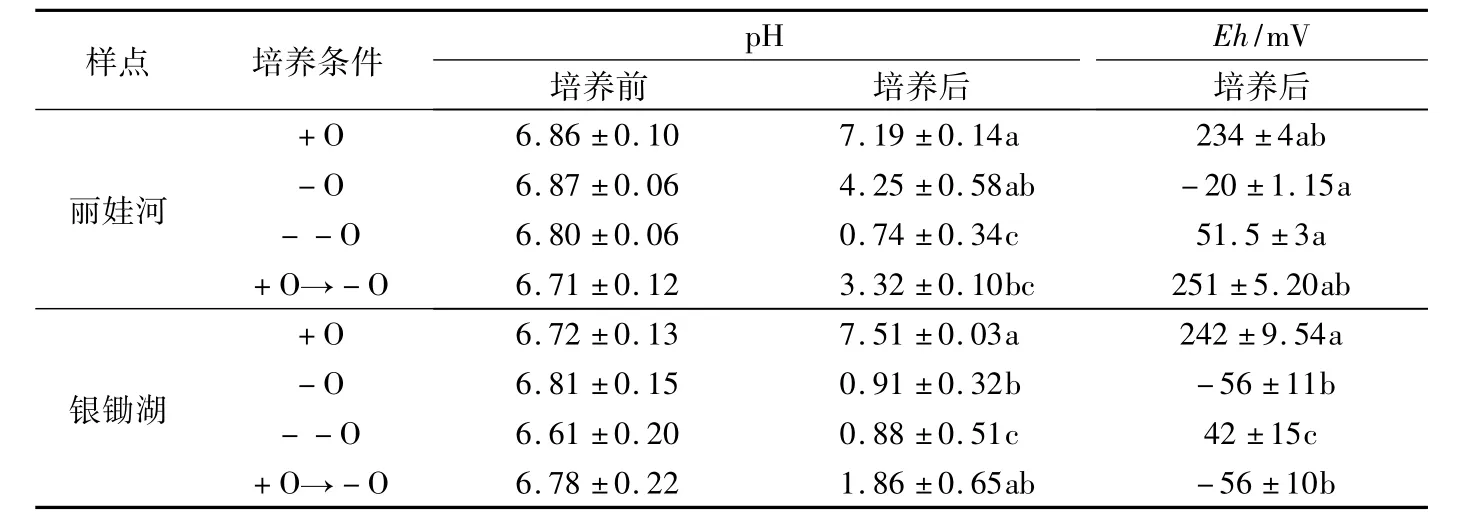
表2 培养前后上清液中pH值及培养后EhTab.2 pH and Eh(only after)of supernatant fluid before and after treatment
2.3不同氧化还原条件培养下上清液和沉积物中Fe的变化
2.3.1上清液中Fe的释放速率变化
由图1可知,丽娃河和银锄湖的沉积物培养初期(0-14 d)各处理条件下向上清液中Fe的释放速率均较低,可能因为沉积物中存在的Fe主要以稳定的残渣态(见图2)形式存在,使得总活性Fe[20]的含量较低,Fe的释放量也较低.培养时间过半(14 d)后,厌氧条件处理(-O)的Fe的释放速率在两个样点都有升高的趋势,在培养至第21天时达到最高值;并且银锄湖沉积物在好氧后厌氧的处理(+O→-O)中,第21天开始上清液中Fe的释放速率也有升高的趋势,可能因为在还原条件下,沉积物中的铁锰氧化物易被还原为Fe2+离子而被释放到上清液中[21].许昆明等[22]研究南海沉积物溶解氧与Fe、Mn浓度的关系中也发现,随着海水深度的增加,溶解氧含量降低导致锰和铁氧化物或氢氧化物被还原成Fe2+和Mn2+.然而在沉积物颗粒再悬浮过程中,部分Fe2+又以铁锰氧化物的形式吸附其他金属沉降而减少[7-8],导致上清液中Fe浓度在培养至第21天后有下降趋势.研究还发现丽娃河和银锄湖中Fe在上清液中的最大释放速率均出现在厌氧处理中,而并非高度厌氧处理或好氧处理,这可能是由于在高度还原条件下,沉积物中铁锰(氢)氧化物易被还原成FeS或FeS2而与金属及有机质结合形成沉淀[20,23],不易被释放到上清液而导致丽娃河的沉积物在高度厌氧条件处理(--O)下上清液的Fe未出现释放.而好氧条件(+O)下即使FeS在短短几分钟内被氧化释放,但Fe2+又会很快被氧化成不溶的铁锰(氢)氧化物与金属再吸附而沉降到沉积物中[7,23],导致上清液中Fe浓度也不会发生太大变化.但因为以硫化铁形式存在的Fe对氧化环境比较敏感,因此与高度厌氧或通氧处理相比,中度的氧化还原条件更能促进Fe的释放.可以预测,如果对银锄湖进行植物修复,由于植物根际造成的泌氧环境,会使Fe以铁锰(氢)氧化物的形式结合其他金属,减少Fe和重金属向上层水体释放的影响.
2.3.2沉积物中Fe形态的变化
丽娃河和银锄湖的沉积物中Fe形态在不同培养条件下的分布规律基本一致(见图2).两个样点的沉积物Fe都主要以残渣态为主,其次为可还原态及可氧化态,弱酸提取态比例最低,其中残渣态Fe比例都高达80%左右,说明其生物有效性低.银锄湖中可氧化态Fe比例相对丽娃河较高,可还原态Fe比例均较低,可能与银锄湖沉积物中TOC及硫的含量相对较高有关(见表1).
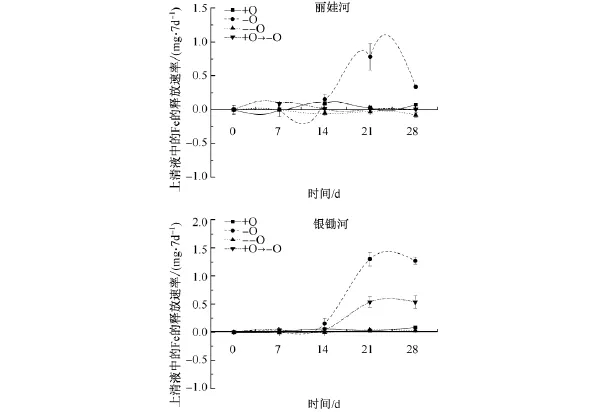
图1 不同氧化还原条件培养下上清液中Fe的释放速率Fig.1 Fe release rates in upernatant fluid during treatment with different redox conditions
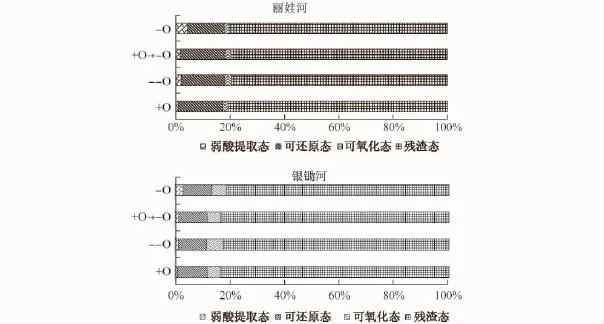
图2 不同氧化还原条件培养后沉积物中各形态Fe百分比Fig.2 Percentage of Fe fraction after treatment with different redox conditions
丽娃河的沉积物在厌氧条件处理与其他处理条件的弱酸提取态Fe比例存在显著性差异(P<0.05),厌氧处理(-O)时弱酸提取态为4.00%,显著高于+O处理(0.83%)、--O处理(1.84%)、+O→-O处理(1.34%);可还原态Fe的比例与厌氧条件处理的也存在显著性差异(P<0.05),厌氧处理(-O)时可还原态Fe为13.77%,低于+O处理(16. 20%)、--O处理(16.10%)、+O→-O处理(16.74%);而可氧化态和残渣态Fe在4种培养条件下不存在显著性差异,比例也没有明显变化.由于沉积物长期处于还原条件,与实验设计的厌氧处理(-O)的情况相似,通过通氧或者极度厌氧处理后,沉积物中易受环境影响的水溶态及可交换态等弱酸提取态Fe发生释放或转移至其他形态而导致比例下降;在对不同培养条件下的4种形态Fe做相关性分析后发现,4种处理条件下弱酸提取态Fe和可还原态Fe之间均存在显著负相关(P<0.05),说明丽娃河的沉积物在好氧或极度厌氧条件下可还原态的Fe与弱酸提取态的Fe可能出现转移.但在高度厌氧条件处理下可还原态Fe比例升高,这可能也与沉积物中铁锰(氢)氧化物在极度缺氧时易被还原成FeS或有关.而各种处理条件下丽娃河中可氧化态Fe比例无显著变化,可能是丽娃河水体经过了水生植被恢复,长期受水生植物根际泌氧的影响导致沉积物中Fe在植物根际形成铁膜等原因而使沉积物中的可氧化态Fe比例较低[4],所以变化不明显.
银锄湖的沉积物各形态Fe的变化趋势与丽娃河的大致相同,各种处理条件后弱酸提取态Fe与厌氧条件处理的相比都较低,可还原态Fe比例都较高.相比较丽娃河,银锄湖在通过好氧处理的沉积物可氧化态Fe比例为4.60%,相比厌氧处理条件的5.53%较低;好氧处理后残渣态Fe比例为83.49%,相比厌氧条件处理的81.08%较高,可以预测如果对银锄湖进行以水生植被恢复为重点的生态修复,沉积物中Fe会受植物根际泌氧的作用以铁锰(氢)氧化物的形式吸附其他金属离子形成沉淀或者形成稳定的残渣态,不会向上层水体释放造成污染.
2.4不同氧化还原条件培养下上清液和沉积物中Zn的变化
2.4.1上清液中Zn的释放速率的变化
如图3所示,不同的培养条件对于沉积物中Zn向上清液中释放含速率的影响不同.丽娃河和银锄湖中沉积物不管是好氧处理(+O)还是先好氧后厌氧处理(+O→-O),在培养至第7天上清液中Zn的释放速率均明显高于全程厌氧(-O)或高度厌氧(--O)的处理,并且表现为显著性差异(P<0.05),这与黄健敏等人的研究相同.他们发现:底泥在氧化条件下会使以有机物或硫化物结合态形式存在的Zn释放到上层水体[24].相对丽娃河,银锄湖的沉积物在培养至第7天的上清液Zn释放速率更高,可能因为银锄湖有机质和硫含量较高,因此以有机质和硫化物结合的可氧化态Zn浓度高于丽娃河(见图3).但随着培养时间的延长,通氧处理后的上清液中Zn释放速率又逐渐下降,一方面可能因为与AVS(酸可挥发性硫化物)结合的Zn在氧化条件下释放达到峰值[16],另一方面可能是好氧环境同时也使溶液中对氧化还原电位敏感的Fe2+被氧化成Fe3+,形成水和氢氧化物,吸附部分释放出的Zn,使溶液中的Zn浓度降低[25],导致上清液中Zn的释放量减少.可以预测如果对银锄湖进行植被修复,由于植物根际泌氧的影响,会改变原来处于还原条件的沉积物Eh、pH和溶解氧等状态[26],使Zn会在短时间内释放.
2.4.2沉积物中Zn形态的变化
从培养前后沉积物中各形态Zn的百分比来看(见图4),虽随着培养条件的改变丽娃河和银锄湖沉积物Zn形态比例有所改变,但仍主要以弱酸提取态、可还原态和残渣态为主,可氧化态比例最低.比较两条富营养化水体中沉积物中各形态的Zn发现,有效态Zn比例都较高,说明沉积物中Zn可能具有较高的生态风险[27].
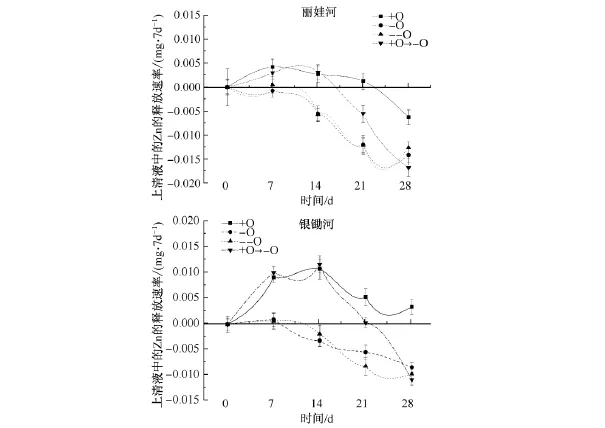
图3 不同氧化还原条件培养下上清液Zn的释放速率Fig.3 Zn release rates in upernatant fluid during treatment with different redox conditions
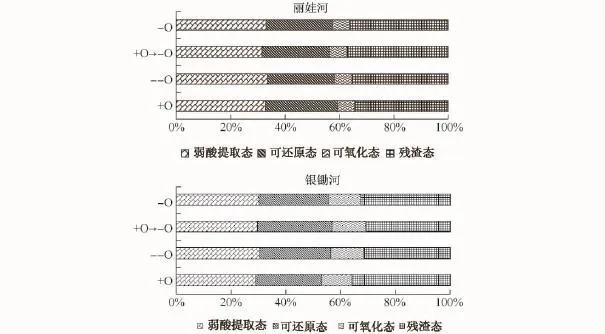
图4 不同氧化还原条件培养后沉积物中各形态Zn百分比Fig.4 Percentage of forms of Zn after treatment with different redox conditions
不同氧化还原条件处理后,相比较厌氧处理条件后银锄湖的沉积物各形态Zn,在好氧处理(+O)后弱酸提取态Zn的比例为29.16%,相比厌氧处理(-O)的30.14%有所降低,可能因为沉积物这部分Zn最不稳定,弱酸提取态Zn中的水溶态和可交换态Zn在中性条件下易释放[28],导致沉积物中弱酸提取态Zn比例下降;可还原态Zn在好氧处理(+O)后为23.90%,相比厌氧处理(-O)的25.40%也降低,可能是因为在氧化条件下酸性腐殖质与被氧化的Fe3+竞争性结合而减少以铁锰氧化态结合的Zn的沉淀[24].可氧化态Zn在好氧处理条件下(+O)比例为32.72%,较厌氧处理(-O)的35.73%显著降低,这与硫化物和有机质结合的Zn在氧化条件下易释放有关[28-29].好氧处理条件下(+O)残渣态Zn比例比厌氧处理条件下(-O)的32.73%升高至35.92%,可以预测如果对银锄湖水体进行以水生植物为基础的生态修复后,沉积物中与有机质和硫化物结合的Zn在植物根际泌氧情况下可以使有效性高的Zn转化成相对稳定的残渣态Zn,实现生态恢复的效果.
而丽娃河的沉积物在好氧处理条件下(+O)可氧化态Zn比例也相对厌氧处理的较低,这与银锄湖处理的结果相一致.残渣态Zn比例稍有降低,弱酸提取态Zn和可还原态Zn比例在4种培养条件都没有显著差异.
2.5沉积物Fe对Zn迁移转化的影响
对丽娃河和银锄湖中沉积物中Zn和Fe的各形态比例进行相关性分析(见表3),丽娃河的沉积物中可氧化态Fe与可氧化态Zn存在极显著正相关,与可还原态Zn存在显著正相关.贾振邦等人也发现,对沉积物进行充气氧化之后,会使水合Fe-Mn氧化物增加,结果导致上清液中Zn浓度增加[30];银锄湖沉积物中可还原态Fe与可还原态Zn和可氧化态Zn都存在显著负相关(见表4),一定程度上可以解释铁锰(氢)氧化物在不同氧化还原条件下对金属Zn的迁移转化的影响.而银锄湖沉积物中弱酸提取态Fe与可还原态Zn、可氧化态Zn都存在极显著正相关,这也说明了弱酸提取态Fe对金属Zn的迁移转化的影响.

表3 丽娃河沉积物不同形态Zn(%)与Fe(%)的Pearson相关关系Tab.3 Pearson correlation coefficient of proportion of Zn(%)forms with Fe(%)forms in sediments of Liwa River
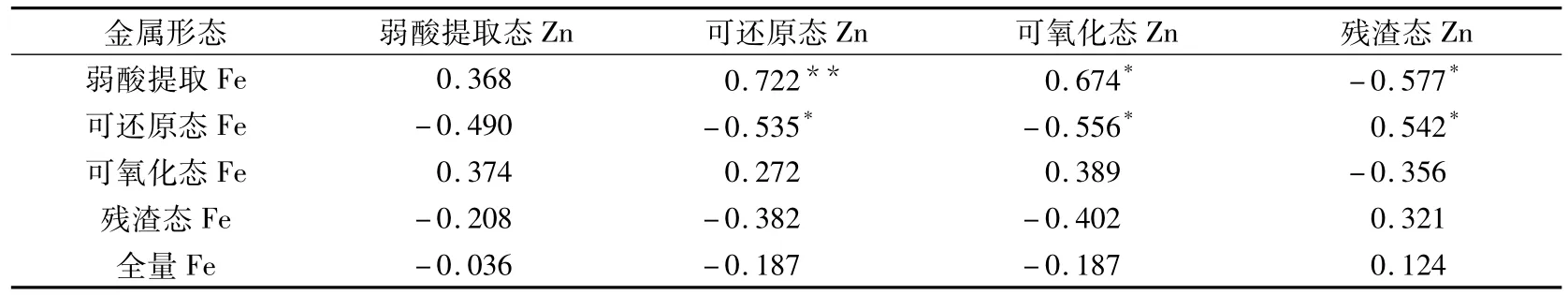
表4 银锄湖沉积物不同形态Zn(%)与Fe(%)的Pearson相关关系Tab.4 Pearson correlation coefficient of proportion of Zn(%)forms with Fe(%)forms in sediments of Yinchu Lake
3 结 论
(1)丽娃河和银锄湖沉积物中Fe的释放速率在培养初期(0~14 d)均较低;培养时间过半(14~21 d)时,厌氧条件处理(-O)下Fe的释放速率均升高.而好氧处理(+O)和先好氧后厌氧处理后沉积物中Zn的释放速率均明显高于厌氧(-O)或高度厌氧(--O)的处理.
(2)丽娃河和银锄湖沉积物中Fe主要以残渣态形态形式存在,其次为可还原态及可氧化态,弱酸提取态比例最低.而沉积物中Zn主要以弱酸提取态、可还原态和残渣态为主,可氧化态比例最低.
(3)丽娃河沉积物中可氧化态Fe与可氧化态和可还原态Zn均存在显著正相关,而银锄湖沉积物中可还原态Fe与可还原态Zn和可氧化态Zn都存在显著负相关.表明Fe在不同氧化还原条件下对金属Zn的迁移转化有一定的影响.
[1]耿雅妮.河流重金属污染研究进展[J].中国农学通报,2012,28(11):262-265.
[2]阳辉,樊贵盛,刘婷.流域底泥重金属分布特征及其生态风险评价[J].水土保持通报,2014,34(2):208-212.
[3]林娜娜,许秋瑾,胡小贞,等.江西崇义县小江流域重金属污染现状及评价[J].环境科学研究,2014,27(9):1051-1060.
[4]杨苏才,南忠仁,曾静静.土壤重金属污染现状与治理途径研究进展[J].安徽农业科学,2006,34(3):549-552.
[5]李飞宇.土壤重金属污染的生物修复技术[J],环境科学与技术,2011,34(12):148-151.
[6]LIU J,DONG Y,XU H,et al.Accumulation of Cd,Pb and Zn by 19 wetland plant species in constructed wetland[J]. Journal of Hazardous Materials,2007,147(3):947-953.
[7]刘文菊,朱永官.湿地植物根表的铁锰氧化物膜[J].生态学报,2005,25(2):358-363.
[8]俞慎,历红波.沉积物再悬浮-重金属释放机制研究进展[J].生态环境学报,2010,19(7):1724-1731.
[9]BEUTEL M W,LEONARD T M,DENT S R,et al.Effects of aerobic and anaerobic conditions on P,N,Fe,Mn and Hg accumulation in waters overlaying profundal sediments of anoligo-mesotrophic lake[J].Water Research,2008,42(8-9):1953-1962.
[10]HWANG K,KIM H,HWANG I.Effect of resuspension on the release of heavy metals and water chemistry in anoxic and oxic[J].Clean-Soil Air Water,2011,39(10):908-915.
[11]李俊莉,宋华明.土壤理化性质对重金属行为的影响分析[J].环境科学动态,2003(1):24-26.
[12]SREEKTISHNAN T R,TYAGI R D.Heavy metal leaching from sewage sludge:A techno-economic evaluation of the process options[J].Environ Technol,1994,15(6):531-543.
[13]顾继光,周启星,王新.土壤重金属污染的治理途径及其研究进展[J].应用基础与工程科学学报,2003,11(2):143-152.
[14]李静文,施文,余丽凡,等.丽娃河受损退化生态系统的近自然恢复工程及效果分析[J].华东师范大学学报:自然科学版,2010(4):35-43.
[15]中华人民共和国国家质量监督检验检疫总局.GB17378.5—2007,海洋监测规范第5部分:沉积物分析部分[S].北京:中国标准出版社,2008.
[16]鲍士旦.土壤农化分析[M].北京:中国农业出版社,2005.
[17]LONG Y Y,HU L F,FANG C R,et al.An evaluation of the modified BCR sequential extraction procedure to assess the potential mobility of copper and zinc in MSW[J].Microchemical Journal,2009,91(1):1-5.
[18]方涛,肖邦定,张晓华,等.曝气对两种不同类型沉积物中重金属释放的影响[J].中国环境科学,2002,22(4):355-359.
[19]石晓勇,王修林,陆茸,等.东海赤潮高发区春季溶解氧和pH分布特征及影响因素探讨[J].海洋与湖沼,2005,36(5):404-412.
[20]吕仁燕,朱茂旭,杨桂朋,等.东海陆架泥质沉积物中固相Fe形态及其对有机质,Fe,S成岩路径的制约意义[J].地球化学,2011,40(4):363-371.
[21]李晓晨,赵丽,王超.玄武湖上覆水间隙水和沉积物中的重金属分布研究[J].环境科学与技术,2008,5(31):4-10.
[22]许昆明,邹文彬,司靖宇.南海越南上升流区沉积物中溶解氧、锰和铁的垂直分布特[J].热带海洋学报,2010,29(5):56-64.
[23]KELDERMAN P,OSMAN A A.Effect of redox potential on heavy metal binding forms in polluted canal sediments in Delft(The Netherlands)[J].Water Research,2007,41(18):4251-4261.
[24]黄健敏,黄润秋.深港西部通道填海区淤泥重金属化学形态分析[J].矿物学报,2007,27(1):83-88.
[25]NEMATI K,BAKAR N K A,SOBHANZADEH E,et al.A modification of the BCR sequential extraction procedure to investigate the potential mobility of copper and zinc in shrimp aquaculturesludge[J].Microchemical Journal,2009,92(2):165-169.
[26]毕春娟,陈振楼,郑祥民,等.根际环境重金属地球化学行为及其生物有效性研究进展[J].地球科学进展,2001,16(3):387-393.
[27]王海,王春霞,王子健,等.太湖表层沉积物中重金属的形态分析[J].环境化学,2002,21(5):430-435.
[28]路永正,董德明,沈秀娥,等.曝气对河流沉积物中重金属Cu、Pb、Zn和Cd释放的影响[J].吉林大学学报:理学版,2005,43(6):877-881.
[29]CAILLE N,TIFFREAU C,LEYVAL C,et al.Solubility of metals in an anoxic sediment during prolonged aeration[J]. Science of the Total Environment,2003,301(1):239-250.
[30]贾振邦,林健枝,吕丰伟.沉积物充气过程对锌的影响[J].环境化学,1999,18(6):507-512.
(责任编辑:张晶)
Effect of redox condition on metal transformation in urban river sediments
ZHANG Mi1, WEN Bo1, HUANG Ling-xia1, DU Jing2, DENG Hong1,3,4
(1.School of Ecological and Environmental Sciences,East China Normal University,Shanghai 200241,China;2.Library of East China Normal University,Shanghai 200241,China;3.Shanghai Key Lab for Urban Ecological Processes and Eco-Restoration,East China Normal University,Shanghai 200241,China;4.Tiantong National Station of Forest Ecosystem,East China Normal University,Shanghai 200241,China)
The sediments from Yinchu Lake and Liwa River were studied for the effects of redox changes on Zn and Fe transformation.A simulated experiment was conducted with 4 different redoxtreatments:aerobic(+O),anaerobic(-O),aerobic then anaerobic(+O→-O)and extensively anaerobic(--O).Compared with anaerobic condition(-O),percentage of oxidizable Fe decreased from 5.53%to 4.60%in the sediment from Yinchu Lake under aerobic condition,while reducible and residual Fe increased from 13.77%to 16.20%and from 81.08%to 83.49%,respectively.Furthermore,the concentration of Fe release in the supernatant was decreased.Percentage of Zn in acid extractable,reducible and Fe-Mn oxides fraction were respectively declined from 30.14% to 29.16%,from 25.40%to 23.90%and from 35.73%to 32.72%in the sediment from Yinchu Lake.However,Zn in residual fraction rose from 32.73%to 35.92%after treated with oxygenenation,which decreased the concentration of Zn release in the supernatant.It indicated that Fe and Zn in Fe-Mn oxides fraction and organic matter fraction had good corrections with each other.Our study would provide scientific basis for risk analysis and evalution on eutrophicated urban river in the process of ecological restoration.
urban river;sedimen;redox potential;aeration;Fe;Zn;migration and transformation
X131
A
10.3969/j.issn.1000-5641.2016.02.018
1000-5641(2016)02-0160-11
2015-03
国家自然科学基金(31400445,41371451)
张密,女,硕士研究生,研究方向污染和恢复生态学.E-mail:hdsdzm@163.com.
邓泓,女,副教授,研究方向污染生态学,生态修复.E-mail:hdeng@des.ecnu.edu.cn.
