阿瑞匹坦预防化疗引起恶心呕吐的疗效及安全性
2016-11-10赵水喜曹京旭
苏 丹,赵水喜,曹京旭
阿瑞匹坦预防化疗引起恶心呕吐的疗效及安全性
苏 丹,赵水喜,曹京旭
目的 观察阿瑞匹坦对减轻化疗所致恶心呕吐的疗效及安全性。方法 将80例接受含顺铂化疗患者随机分为观察组和对照组, 观察组采用阿瑞匹坦与昂丹司琼、地塞米松联合止吐, 对照组采用帕洛诺司琼与昂丹司琼、地塞米松联合止吐, 观察两组疗效及不良反应。结果 观察组呕吐的完全缓解率和恶心控制率分别为80%和77.5%,优于对照组的47.5%和37.5%,皆有统计学意义(P<0.01)。两组中出现最多的不良反应主要有便秘、腹泻、呃逆、食欲减退、疲乏、失眠、转氨酶升高等, 均为轻度。结论 阿瑞匹坦对化疗所致恶心呕吐有明显的预防作用,且不良反应轻,具有临床应用前景。
阿瑞匹坦 ;化疗;呕吐
化疗引起的恶心呕吐(chemotherapy-induced nausea and vomiting,CINV)是最常见的化疗不良反应之一,据统计有70%~80% 的化疗患者有恶心呕吐的经历[1]。如不能有效控制,可产生一系列的相关并发症,如脱水、电解质紊乱、营养不良,严重者可因消化道黏膜损伤而发生出血、感染甚至死亡。因此,预防或减轻CINV对生活质量的维护、延续治疗极其重要[2,3]。NK-1受体阻滞药阿瑞匹坦于2013-10在中国上市,本研究通过对阿瑞匹坦与长效5HT3受体拮抗药帕洛诺司琼预防CINV的疗效、不良反应的比较,为临床提供依据。
1 对象和方法
1.1 对象 我科2013-11至2015-06收治的肺癌患者80例,男40例,女40例,年龄38~69岁,平均(55.21±7.67)岁。入选标准:年龄>18岁,经病理学或细胞学确诊,ECOG<2分,既往未接受过化疗,化疗前心肝肾功能及血常规无异常。排除标准:合并消化道疾病、使用阿片类药物或有颅脑转移瘤等可能出现非化疗原因导致呕吐的患者。80例均使用含高致吐化疗药顺铂的化疗方案,顺铂剂量70 mg/m2,第1天。按随机数字表法分为观察组和对照组各40例,两组患者年龄、性别、化疗方案、病程等方面比较,差异无统计学意义(P<0.05) 。1.2 方法 (1)对照组:盐酸帕洛诺司琼注射液 0. 25 mg 静脉滴入,1次/d,第1天。地塞米松注射液 10 mg 壶入, 1次/d,第1天;5 mg 壶入, 1次/d,第2~4天。盐酸昂丹司琼注射液 8 mg 静脉滴入, 2次/d, 第1~4天。(2)观察组:阿瑞匹坦胶囊 125 mg口服,1次/d,第1天;80 mg 口服, 1次/d,第2~3天。地塞米松注射液 7.5 mg 壶入, 1次/d, 第1天;3.75 mg 壶入, 1次/d, 第2~4天。盐酸昂丹司琼注射液 8 mg 静脉滴入, 2次/d, 第1~4天。
1.3 判定标准
1.3.1 恶心严重程度标准 恶心严重程度分级标准按照视觉模拟量表VAS评定[4]。在纸上面划一条10 cm的横线,横线的一端为0,表示无恶心;另一端为10,表示恶心极其严重;中间部分表示不同程度的恶心症状。无明显恶心为VAS评分<2.5 cm,无明显恶心例数/总例数为恶心完全控制率。
1.3.2 止吐疗效评定标准 止吐疗效评定标准采用中国抗癌协会癌症康复与姑息治疗专业委员会制定的标准[5]:完全缓解(CR),24 h内无呕吐;部分缓解(PR),24 h呕吐1~2 次;轻度缓解(MR),24 h呕吐3~5次;无效(F),24 h呕吐6次以上。连续观察120 h。完全缓解例数/总例数×100%为完全缓解率。
1.3.4 不良反应 按照美国癌症研究所( NCI) 化疗毒性分级标准(CTC3.0版)[6]进行观察和判断,记录两个方案从治疗开始到治疗结束2 周的不良反应发生情况。
1.4 统计学处理 采用SPSS 21. 0 统计分析软件对组中数据进行计算,率的比较采用χ2检验,P<0.01为差异有统计学意义。
2 结 果
在总观察期(顺铂使用后0~120 h),急性期(顺铂使用后0~24 h),延迟期(顺铂使用后25~120 h)对阿瑞匹坦胶囊进行了评价。由表1、2可见,在总观察期,观察组预防呕吐的完全缓解率和恶心控制率改善,皆有统计学意义(P<0.01)。延迟期体现出明显差异,具有统计学意义(P<0.01)。急性期预防呕吐的完全缓解率亦有差异,但是没有统计学意义。由表3可见,两组中出现最多的不良反应主要有便秘、腹泻、呃逆、食欲减退、疲乏、失眠、转氨酶升高等, 均为轻度,两组差别不大。
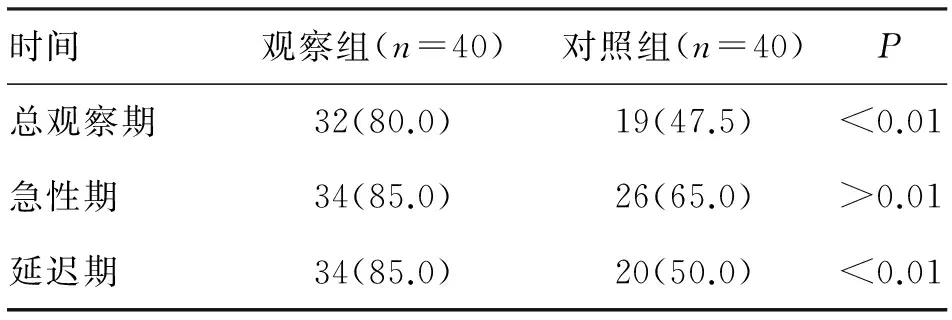
表1 两组方案预防呕吐的完全缓解率对比 (n;%)
注:观察组指阿瑞匹坦胶囊+地塞米松+昂丹司琼。对照组指盐酸帕洛诺司琼+地塞米松+昂丹司琼
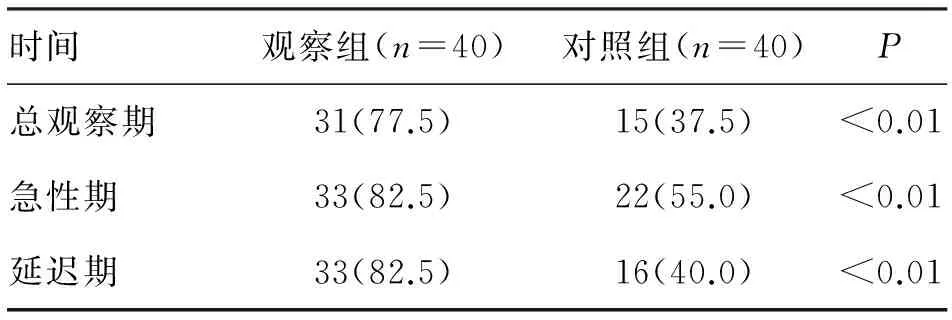
表2 两组方案预防恶心的完全控制率对比 (n;%)
注:观察组指阿瑞匹坦胶囊+地塞米松+昂丹司琼。对照组指盐酸帕洛诺司琼+地塞米松+昂丹司琼
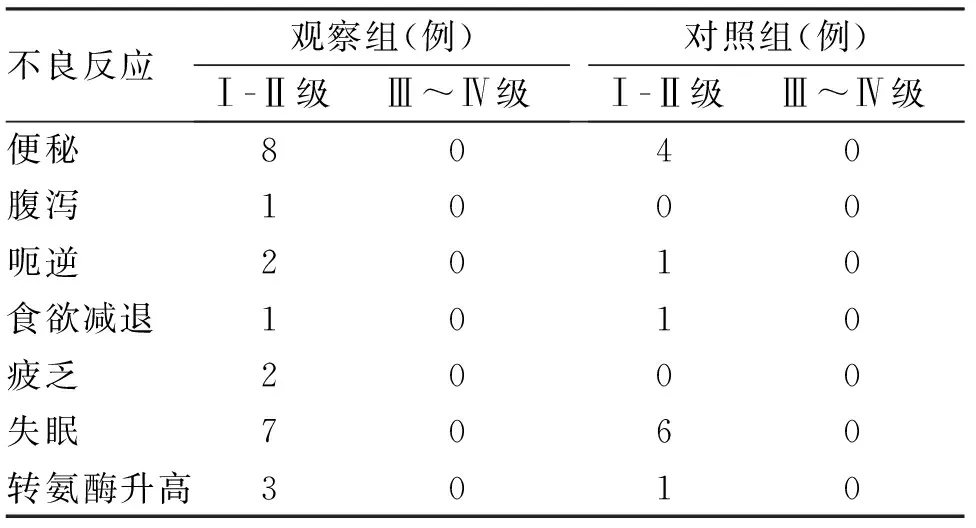
表3 两组方案最常见的临床不良反应
注:观察组指阿瑞匹坦胶囊+地塞米松+昂丹司琼。对照组指盐酸帕洛诺司琼+地塞米松+昂丹司琼
3 讨 论
3.1 CINV的机制及NK-1、5HT3的药理作用 CINV分为两个不同的阶段存在不同的机制[7]。CINV的急性期阶段主要由5HT和5HT3受体系统引起,体内90%的5-HT存在于整个胃肠道的嗜铬细胞中,5HT3受体也在外周神经系统体内分布于交感与副交感节后神经元和纤维中、肠神经系统的感觉神经元中,在中枢神经系统高度集中于最后区和孤束核的迷走神经传入纤维末梢。5-HT通过5HT3受体介导外周和中枢神经系统化疗呕吐反射[8]。延迟期阶段P物质和NK1受体系统对CINV影响更大[7]。P物质主要由神经细胞和胃肠道等周围组织器官中,通过与G蛋白偶联的神经激肽受体结合而发挥生物作用。P物质与5-HT共存于嗜铬细胞以及脑干孤束核和最后区[9]。5HT3受体拮抗药及NK-1受体拮抗药通过选择性结合其相应抗体进而阻断呕吐过程的发生。
3.2 疗效、不良反应分析 顺铂在ASCO、MASCC、NCCN的化疗指南上被定义为高致吐性化疗药,推荐NK-1受体阻滞药+5HT3受体阻滞药+糖皮质激素作为标准止吐方案[10-12]。瑞匹坦是第一个NK-1受体拮抗药,在国外已广泛应用于临床实践预防CINV,中国上市后尚未有任何数据公布。
国外接受含顺铂的抗肿瘤化疗方案中进行的2项随机对照研究汇总中[13],完全缓解率在总观察期、急性期、延迟期方面,阿瑞匹坦组对比观察组分别为60%vs45%(P<0.01),82%vs70%(P<0.01),64%vs47%(P<0.01)。完全缓解率在总观察期、急性期、延迟期方面,恶心控制率在总观察期、急性期、延迟期方面,阿瑞匹坦组对比观察组分别为72%vs65%(P<0.05),91%vs85%(P<0.05),74%vs67%(P<0.05)。本研究中观察组较对照组在总观察期及延迟期阿瑞匹坦组呕吐完全控制率皆明显提高,恶心控制率也明显提高,有统计学意义。这与国外文献报道的结论一致,结果明显好于国外试验数据,这可能与连续、多次使用昂丹司琼配合止吐相关。而在急性期呕吐控制率两组相比却没有差异,提示瑞匹坦主要对延迟期起关键作用。
国外试验中阿瑞匹坦组显著高于对照组的不良反应包括:呃逆(4.6%)、ALT升高(2.8%)、消化不良(2.6%)、便秘(2.4%)、头痛(2.0%)和食欲减退(2.0%)。本组试验中失眠和便秘在两组的发生概率都较高,这与糖皮质激素的使用相关。其余不良反应发生较少。因样本量较少,还需继续观察。
综上所述,阿瑞匹坦能有效预防急性和延迟性化疗所致恶心呕吐,可作为高致吐药物化疗中预防治疗恶心呕吐的首选药物之一,安全性好值得临床推广。为患者顺利治疗、改善生活质量及提高疗效打下基础。
[1] Ettinger D S,Bierman P J,Bradbury B,etal. Antiemesis[J]. J Natl Compr Canc Netw,2007,5(1):12-33.
[2] Richardson J L, Marks G, Levine A .The influence of symptoms of disease and side effects of treatment on compliance with cancer therapy[J]. J Clin Oncol,1988,6(11):1746-1752.
[3] Bloechl-Daum B, Deuson R R, Mavros P,etal.Delayed nausea and vomiting continue to reduce patients’ quality of life after highly and moderately emetogenic chemotherapy despite antiemetic treatment[J].J Clin Oncol,2006,24(27):4472-4478.
[4] Martin A R, Pearson J D, Cai B,etal. Assessing the impact of chemotherapy-induced nausea and vomiting on patients’ daily lives: a modified version of the Functional Living Index-Emesis (FLIE) with 5-day recall[J]. Support Care Cancer,2003,11:522-527.
[5] 中国抗癌协会癌症康复与姑息治疗专业委员会. 肿瘤治疗相关呕吐防治指南[M].北京: 中国协和医科大学出版社,2009: 20-42.
[6] Saito M,Aogi K,Sekine L,etal.Palonosetron plus dexamethasone versus granisetron plus dexamethasone for prevention of nausea and vomiting during chemotherapy: a double-blind, double-dummy, randomised, comparative phase III trial[J]. Lancet Oncol,2009,10(2):115-124.
[7] Cubeddu L X. Serotonin mechanisms in chemotherapy- induced emesis in cancer patients[J].Oncology,1996, 1:18-25 .
[8] Wolf H. Preclinical and clinical pharmacology of the 5- HT3 receptor antagonists[J].Scand J Rheumatol Suppl,2000,113:37-45.
[9] 张晓静,张 频.肿瘤化疗所致恶心呕吐的发生机制和药物治疗的研究进展[J].癌症进展,2006,4(4):348-354.
[10] Roila F, Herrstedt J, Aapro M,etal. Guideline update for MASCC and ESMO in the prevention of chemotherapy- and radiotherapy-induced nausea and vomiting: results of the Perugia consensus conference[J]. Ann Oncol, 2010,21(5):232-243.
[11] Basch E, Prestrud A A, Hesketh P J,etal. Antiemetic American Society Clinical Oncology clinical practice guideline update[J].J Clin Oncol, 2011,29:4189-4198.
[12] NCCN Clinical Practice Guidelines in Oncology version 1 2014. Antiemesis[M]. National Comprehensive Cancer Network (NCCN),2014.
[13] Warr D G,Grunberg S M,Gralla R J,etal. The oral NK(1) antagonist aprepitant for the prevention of acute and delayed chemotherapy-induced nausea andvomiting:Pooled data from 2 randomised, double-blind, placebo controlled trials[J].Eur J Cancer,2013,41(9):1278-1285.
(2016-02-23收稿 2016-06-18修回)
(责任编辑 梁秋野)
Efficacy and safety of aprepitant in patients with nausea and vomiting caused by chemotherapy
SU Dan, ZHAO Shuixi, and CAO Jingxu.
Department of Oncology, the General Hospital of Chinese People’s Armed Police Force, Beijing 100039, China
Objective To observe the curative effect and adverse reaction of aprepitant in alleviating nausea and vomiting caused by chemotherapy. Methods 80 patients with cisplatin chemotherapy were randomly divided into study group and control group. The study group used aprepitant combined with the ondansetron hydrochloride, dexamethasone. The control group received palonosetron hydrochlorid combined with ondansetron hydrochloride, and dexamethasone. The curative effect and adverse reactions in the two groups were observed. Results In the study group, complete remission rate and nausea vomiting control rates were 80% and 77.5% respectively, compared with 47.5% and 37.5% in the control group, there was statistically significant difference (P<0.01). In the two groups, the most adverse reactions mainly included constipation, diarrhea, hiccups, anorexia, fatigue, insomnia, transaminase and elevation, were mild. Conclusions Aprepitant has obvious preventive effect on chemotherapy induced nausea and vomiting, and has clinical application prospects.
aprepitant;chemotherapy;vomiting
苏 丹,本科学历,主治医师。
100039 北京,武警总医院肿瘤一科
赵水喜,E-mail:zhaoshuixi@sina.com
R734.2
