流动注射分光光度法测定红葡萄酒中甲醇
2016-11-04莫腊梅李永生高秀峰
莫腊梅,李永生,高秀峰
(1.四川大学化学工程学院,四川成都610065;2.四川大学基础医学与法医学院,四川成都610064)
流动注射分光光度法测定红葡萄酒中甲醇
莫腊梅1,李永生1,高秀峰2
(1.四川大学化学工程学院,四川成都610065;2.四川大学基础医学与法医学院,四川成都610064)
提出了一种快速自动测定葡萄酒中甲醇的流动注射分析方法。本方法的原理是通过蒸馏从样品中分离甲醇,然后经高锰酸钾氧化成甲醛,过量高锰酸钾与S2O52-脱色,甲醛与品红/亚硫酸反应生成紫色络合物,在最大吸收波长590 nm处进行测定。通过正交实验及单因素优化后,得到了以下最优条件:20 g/L KMnO4,0.3 mol/L H2SO4(15%H3PO4),80 g/L K2S2O5,3 g/L品红-亚硫酸钠,显色反应温度40℃,样品消耗量330 μL,分析速度为24个样/h。对甲醇(500 mg/L)进行11次重复测定,相对标准偏差为0.6%。在优选条件下,用本方法与气相色谱法对5种红葡萄酒进行测定,其测定结果一致。
流动注射;甲醇;显色反应;红葡萄酒
甲醇是酒类的一项非常重要的安全指标,国标[1]中规定葡萄酒中的甲醇含量必须≤400 mg/L。葡萄酒中甲醇主要由原料中果胶物质水解、氨基酸脱氨和发酵原料的霉变产生。甲醇是一种有害物质,人体过量摄入可导致头痛、恶心、视力模糊,严重时可导致失明或死亡[2]。因此,准确、便捷测定酒中甲醇含量,对保证消费者的健康具有重大意义。
目前已经有测定甲醇的各种方法,主要为色谱法(GC、HPLC)及酶法等。色谱法[3-4]往往需要严格的实验条件。酶法[5-6]虽然选择性和灵敏度高,但是酶试剂成本昂贵、不易保存。品红/亚硫酸比色法是目前葡萄酒中甲醇含量测定的常用方法[7],但该法显色不稳定、重现性差、耗时长。Zhang等[8-9]根据在磷酸介质中甲醛对结晶紫与溴酸钾间的氧化还原反应具有催化作用,以及使用二氧化铅固相反应器将甲醇氧化成甲醛,开发了测定甲醇的催化分光光度法,该法灵敏度高,但甲醛催化受阴离子的干扰大,目前还没有用于葡萄酒中甲醇含量测定的报道。因此,开发一个简便、灵敏度高且准确、快速测定红葡萄酒中甲醇的方法仍然是一个需要迫切解决的技术问题。本研究以国标法为依据,利用FIA技术建立了一种能快速测定红葡萄酒中甲醇的自动分析方法。
1 材料与方法
1.1材料、试剂及仪器
葡萄酒样:国产某品牌不同葡萄品种(解百纳、红宝石)的干红葡萄酒;农家自酿(玫瑰香、赤霞珠)的半干红葡萄酒;格鲁吉亚原装进口(老朋友)的半干红葡萄酒。
试剂:碱性品红(天津市大茂化学试剂厂);甲醇,亚硫酸钠,浓盐酸,浓硫酸,浓磷酸,高锰酸钾(成都市科龙化学试剂厂);偏重亚硫酸钾(天津市致远化学试剂有限公司);实验用水为超纯水(电导率0.065 μS/cm)。
仪器设备:FIA3110型流动注射仪;UV-1800PC型紫外/可见分光光度计(上海美谱达);721-P可见分光光度计(上海第三分析仪器厂);ASB-200空气恒温浴(日本分光工业株式会社);艾柯KL-UP-IV-10型纯水仪(成都康宁实验室专用纯水设备厂);XWT-S型有纸记录仪(上海自动化仪表三厂);SC-3000B-011ST型气相色谱仪(附FID检测器,重庆川仪分析仪器有限公司);CH-1型高纯氢气发生器(武汉科林普丰仪器有限公司)。
1.2主要试剂配制
甲醇储备液(1.0 g/L):取630 μL甲醇于500 mL容量瓶中定容,然后移入带盖的棕色瓶中备用。
KMnO4/H3PO4/H2SO4试剂:称取5.0 g KMnO4,溶解于15%(v/v)H3PO4并定容至250 mL,然后与配制的0.6 M H2SO4按1+1比例混合。
品红/亚硫酸钠试剂:称取0.250 g碱性品红,用150 mL、80℃左右的水溶解,冷却后过滤,向滤液中加入25 mL Na2SO3(100 g/L),加入2.5 mL HCl,用水定容至250 mL,置冰箱中4℃低温保存。
1.3样品处理
准确量取50 mL葡萄酒样品于100 mL蒸馏瓶中,加入数粒玻璃珠,加热蒸馏,并将装置连接至真空泵。用50 mL容量瓶收集馏出液至刻度,于20℃水中保温30 min,以超纯水定容至刻度,混匀,备用。
1.4实验装置

图1 测定红葡萄酒中甲醇的流动注射分析系统
设计的FIA系统如图1所示。测定过程:当采样阀处于采样位置时,系统进行定量采样,多余的排除,同时载流(C)和反应试剂(R1、R2、R3)在蠕动泵(P1)作用下进入检测器形成稳定基线;当采样阀处于注入位置时,试样在载流的推动下与R1汇合后进入RC1发生氧化反应;随后与R2汇合后进入RC2发生反应,褪去过量的KMnO4的颜色。褪色反应完成后,反应物与R3汇合并在RC3发生显色反应,生成蓝紫色络合物。通过测量显色产物在最大吸收波长处(590 nm)的吸光度定量甲醇。
2 结果与讨论
2.1还原剂种类的影响
品红/亚硫酸法测定甲醇时,过量的氧化剂KMnO4在580 nm处有最大吸收峰,这将影响显色产物(590 nm)的测定,因此需加入还原剂褪去多余高锰酸钾。由于国标法中KMnO4/H3PO4与H2C2O4/H2SO4反应产生大量CO2,影响FIA系统的重现性,因此,重新筛选了适宜的还原剂。基于文献[7,10-12],考察了草酸、亚硫酸钠、偏重亚硫酸钾以及抗坏血酸4种还原剂对甲醇测定的影响。实验结果表明:还原剂为偏重亚硫酸钾时,产物响应值仅略低于还原剂为草酸时,且反应不产生气体,因此选定偏重亚硫酸钾作为本体系的还原剂。
2.2正交实验
在室温(22℃)下,用1.0 g/L甲醇标液作为测试样品,按4因素5水平的正交实验表进行实验。因素(水平)分别为:KMnO4(5 g/L、10 g/L、15 g/L、20 g/L、30 g/L)、RC1(60 cm、100 cm、150 cm、200 cm、250 cm)、RC3(200 cm、300 cm、400 cm、500 cm、600 cm)、品红浓度(0.5 g/L、1.0 g/L、1.5 g/L、2.0 g/L、3.0 g/L)。由正交实验分析结果知,当KMnO4浓度为20 g/L、品红浓度为3 g/L、RC1长度为60 cm、RC3长度为600 cm时,显色产物响应值最大。
2.3试剂浓度的优化
本研究选取了采样环体积为330 μL,并在正交实验的基础上对各试剂(KMnO4、K2S2O5、显色剂中品红)浓度进行了优化。实验结果表明:测定灵敏度随氧化剂中高锰酸钾浓度增加至20 g/L而上升,超过20 g/L时灵敏度略有下降,选择KMnO4浓度为20 g/L;产物吸光度值随K2S2O5浓度增加呈先增大后迅速降低,最终选择K2S2O5浓度为80 g/L;显色剂(品红/亚硫酸钠)中品红浓度增加,产物吸光度增大,综合考虑显色剂的溶解度和稳定性,选择显色剂中品红浓度为3 g/L。
2.4FIA系统参数的优化
在FIA系统中,各管线的流量大小直接影响系统的灵敏度、分析速度及试剂的消耗量。而在蠕动泵管及其他管线内径一定的前提下,系统的流量可通过调节泵的转速来改变。以0.5 g/L、1.0 g/L甲醇标液作为样品,在10~30 r/min内改变P1的转速,考察甲醇显色对产物峰高的影响。当P1转速高于或低于20 r/min时,产物峰高低、灵敏度低,因此,选择P1转速为20 r/min。
测定甲醇的灵敏度显然取决于氧化反应及显色反应的时间。当流速一定时,可通过RC1、RC3长度改变反应时间。RC1过短导致氧化程度不足,过长则可导致氧化过度;RC2是多余氧化剂褪色的反应器,过短则过量的KMnO4不能完全被还原,过长则造成系统压力及体系分散程度增加;RC3越长显色产物生成量越多,灵敏度越高,低流速和较长的反应盘管长度可以延长停留时间,但反应盘管太长会减缓分析速度、增加产物扩散度。综合考虑灵敏度和分析速率,最佳参数选择如下:RC1、RC2、RC3长度分别为40 cm、100 cm、800 cm;总流速3.2 mL/min(C、R1、R2、R3:0.8 mL/min)。
2.5反应体系影响因素考察
2.5.1系统反应温度的优化
温度影响显色反应与氧化反应的速率及程度。因此,在上述优化条件下,用甲醇作为测试样品,分别考察了氧化反应及显色反应温度对产物吸光度的影响。图2结果表明,氧化反应的温度越高,灵敏度越低;显色反应的温度越高,灵敏度越高。因此,本系统将显色反应盘管温度控制在40℃,氧化反应盘管的温度控制在室温。
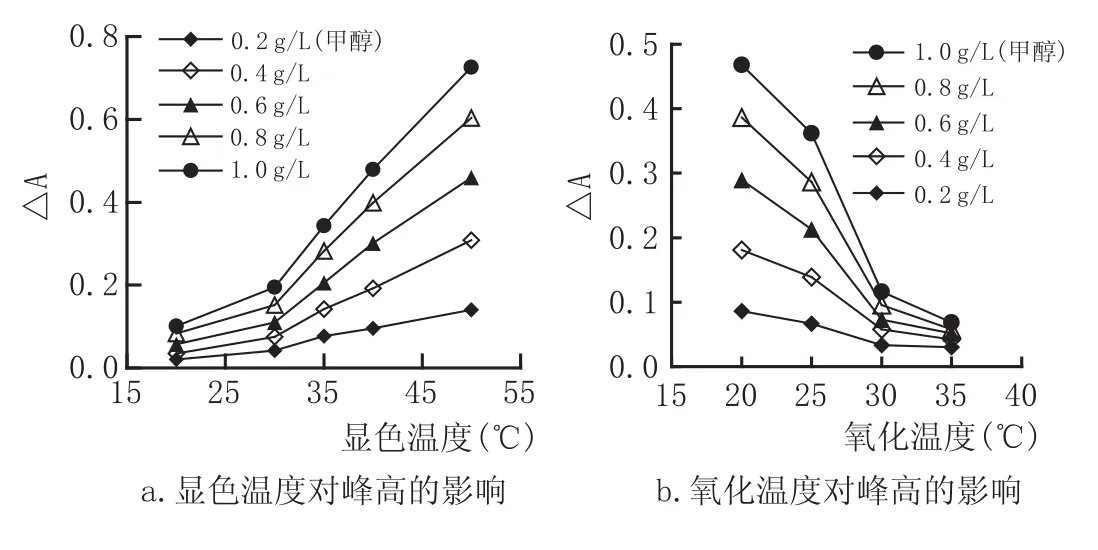
图2 温度对甲醇显色灵敏度的影响
2.5.2系统酸度的考察
葡萄酒中的其他醛类及与高锰酸钾形成的其他醛类与品红/亚硫酸作用也显色,但在一定浓度的硫酸溶液中,除甲醛可形成长时间不褪色的蓝紫色外,其他醛类的显色会消褪,甚至不显色[13]。因此,我们在氧化剂中添加硫酸,一方面可以提高高锰酸钾的氧化性,一方面可以去除其他醛类的干扰。图3结果表明,氧化剂中硫酸浓度增加时,峰高明显增加,方法灵敏度增大;但在实验过程中发现,当硫酸浓度超过0.5 mol/L时系统基线发生漂移。因此,氧化剂为20 g/L高锰酸钾和0.3 mol/L硫酸、15%磷酸的混合物。
2.6干扰物质对甲醇含量测定的影响
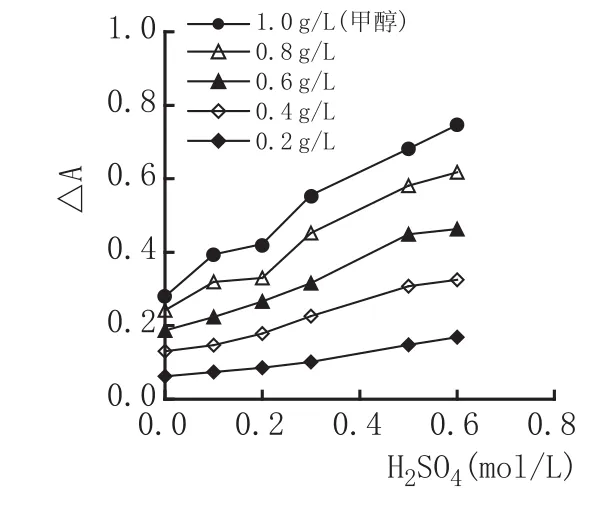
图3 系统酸度对峰高的影响
为了考察葡萄酒中干扰物质对甲醇测定的影响,用1000 mg/L的甲醇标液与不同浓度的干扰物质按1+1比例混合作为试样,用本FIA系统进行测定,计算回收率,控制相对误差在±5%之间。实验结果表明:柠檬酸、乙酸、乙醛、正丙醇、异丁醇、异戊醇、乙酸乙酯、K+、Na+、Mg2+、Mn2+、Ca2+、Br-、PO43-、SO42-、Cl-均不干扰测定;当丙三醇含量超过12 g/L时,将导致甲醇测定结果偏高。从结果看,本方法的选择性较好。
2.7实样中甲醇含量的测定
在优化后的条件下进行操作,考察方法的线性相关系数、线性范围及检出限。在0~1000 mg范围内,线性相关系数r=0.9997,线性关系良好,检出限为8 mg/L。用本方法测定了5种红葡萄酒样品的甲醇含量,并进行了加标回收实验,结果见表1。可以看出,本方法的回收率介于95%~103%,表明本方法准确可靠。
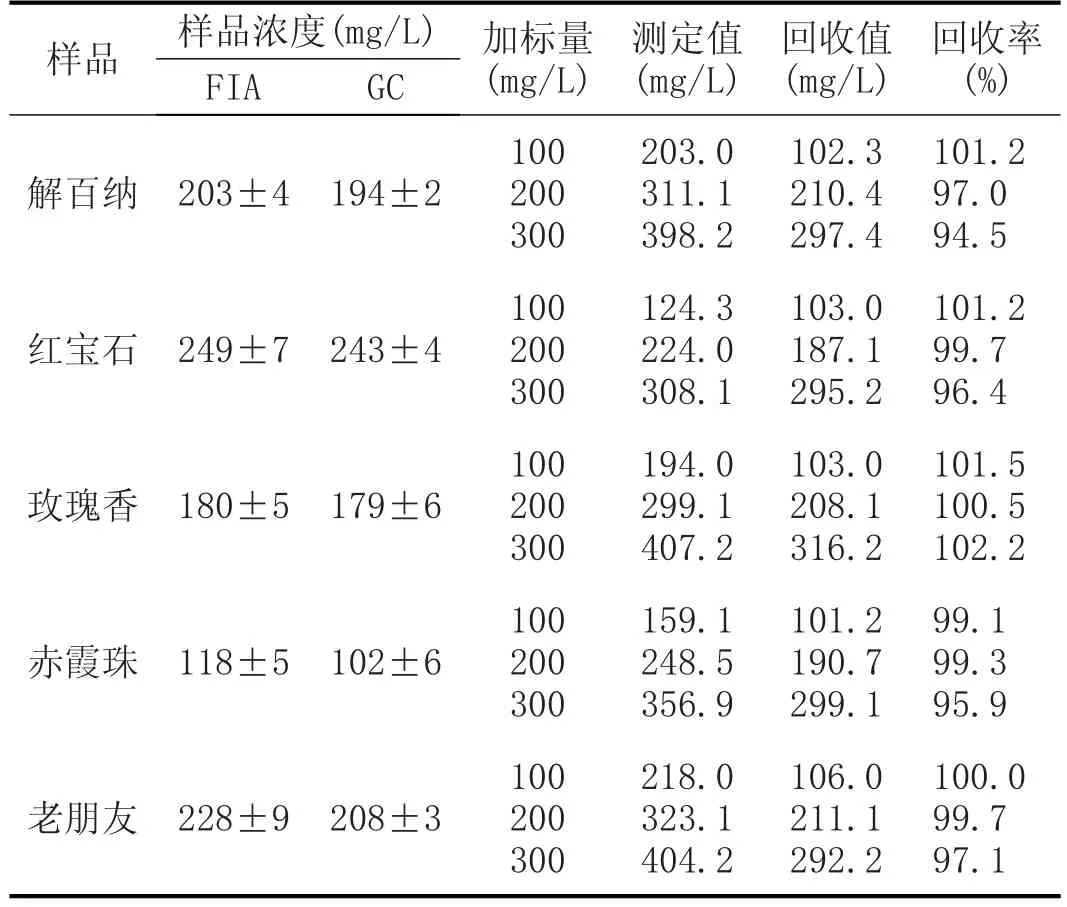
表1 5种酒样的测定及回收率结果
2.8对比实验
为了进一步考察方法的可靠性,对5种商品化的红葡萄酒用本方法与气相色谱法同时进行测试。色谱条件:石英毛细管柱KB1701(30 m×0.32 mm×0.50 μm);载气为氮气;载气、氢气、空气流速分别为15 mL/min、30 mL/min、200 mL/min;检测器、气化室温度为220℃;柱箱温度为50℃;进样体积:1 μL;甲醇含量测定结果见表1。可以看出,气相色谱法得到的结果与本方法一致。
3 结论
本方法自动化程度高、分析速度快、成本低、重现性好、操作简单,可替代甲醇色谱分析法,实现葡萄酒中甲醇的快速连续测定,可用于葡萄酒生产过程的中间及最终质量控制。改变甲醇标液中乙醇的浓度,本方法亦可用于酒精含量不同的其他样品中甲醇含量的测定。
[1]全国食品工业标准化技术委员会酿酒分技术委员会.葡萄酒:GB 15037—2006[S].北京:中国标准出版社,2008.
[2]李永生,齐娇娜,高秀峰.酒中甲醇测定方法的研究进展[J].酿酒科技,2006(1):84-89.
[3]刘兴平,刘火安,张超,等.食用酒中甲醇气相色谱分析方法研究(三)——对所研究方法的综合评价[J].酿酒科技,2001(5):76-79.
[4]Kuo C C,Wen Y H,Wu S S.Determination of methanol by 4-[N-Methyl,N-(1-naphthylmethy1)]-amino-4-oxo-butanoic acid in presence of 4-Dimethylaminopyridine and 1-Ethyl-3-(3-dimethylamino-propyl)carbodiimide hydrochloride as catalysts[J].Anal Letters,2003,36(4):813-825.
[5]Gulce H,GulceA,Kavanoz M,et al.Anew amperometric enzyme electrode for alcohol determination[J].Biosensors and Bioelectronics,2002(17):517-521.
[6]Almuzara C,Cos O,Baeza M,et al.Methanol determination in Pichia pastoris cultures by flow injection analysis[J]. Biotechnology Letters,2002(24):413-417.
[7]全国食品工业标准化技术委员会酿酒分技术委员会.葡萄酒、果酒通用分析方法:GB/T15038—2006[S].北京:中国标准出版社,2008:19-22.
[8]Zhang Z Q,Yan H T,Yue X F.Catalytic determination of trace formaldehyde with a flow injection system using the indicator reaction between crystal violet and bromate[J].Microchim Acta,2004,146(3):259-263.
[9]Yue X F,Zhang Z Q.Simultaneous determination of formaldehyde and methanol by flow-injection catalytic spectrophotometry[J].JAnal Chem,2007,62(10):992-996.
[10]Li Y S,Muo Y,Xie H M.Simultaneous determination of silicate and phosphate in boiler water at power plants based on series flow cells by using flow injection spectrophotometry[J]. Anal ChimActa,2002(455):315-325.
[11]朱昌青,王伦,吴家良.高锰酸钾-抗坏血酸化学发光体系测定抗坏血酸[J].分析试验室,1996,15(1):49-51.
[12]张朝,李永生,高秀峰.基于愈创木酚荧光减量准确测定过氧化物酶活性的新方法[J].食品工业科技,2013,34(12):187-191.
[13]李光,寇志华,丁凤英,等.蒸馏酒中甲醇含量测定的前处理方法的探讨[J].河南预防医学杂志,2005,16(6):332-333.
Determination of Methanol in Red Wine by Flow Injection Spectrophotometry
MO Lamei1,LI Yongsheng1and GAO Xiufeng2
(1.School of Chemical Engineering,Sichuan University,Chengdu,Sichuan 610065;2.West China School of Preclinical and Forensic Medicine,Sichuan University,Chengdu,Sichuan 610064,China)
A rapid and automated determination method of methanol in red wine by flow injection spectrophotometry had been developed.The principles of such method were as follows:methanol separated from wine samples by distillation,then methanol oxidized by permanganate into formaldehyde and excessive permanganate decolorized with withS2O52-,then formaldehyde reacted with magenta-sodium sulfite and a violet reaction product produced,and the determination operated at the maximum absorption wavelength of 590 nm.Through orthogonal experiments and single factor tests,the optimum technical conditions were obtained as follows:20 g/L KMnO4,0.3 mol/L H2SO4(15%H3PO4),80 g/L K2S2O5,3 g/L magenta/sodium sulfite,coloring reaction temperature was at 40℃,sampling volume was 330 μL,and the analytic speed was 24 samples/h.The relative standard deviations for 11 repeated determination of methanol(500 mg/L)was 0.6%.Under the optimum conditions,five commercial wine samples were determined by FIAand GC respectively,and their determination results were the same.
flow-injection;methanol;coloring reaction;red wine
TS262.6;TS261.7;TS261.4
A
1001-9286(2016)10-0108-04
10.13746/j.njkj.2016110
2016-04-01
莫腊梅(1993-),女,四川广安人,硕士研究生,研究方向为食品工业、食品安全技术。
李永生(1958-),男,教授,留日博士,主要从事化学分析自动化、生物传感器等方面的研究,E-mail:lysgxf2005@qq.com。
优先数字出版时间:2016-05-26;地址:http://www.cnki.net/kcms/detail/52.1051.TS.20160526.1123.009.html。
