生物学变异允许总误差在血脂检测中的质量管理
2016-11-04栗秀芳杨悦林曹杰贤
栗秀芳,钱 净,赵 滢,杨悦林,曹杰贤△
(1.云南省昆明市第一人民医院 650000;2.昆明医科大第一附属医院,昆明 650011)
·论著·
生物学变异允许总误差在血脂检测中的质量管理
栗秀芳1,钱净1,赵滢2,杨悦林1,曹杰贤1△
(1.云南省昆明市第一人民医院650000;2.昆明医科大第一附属医院,昆明 650011)
目的探讨生物学变异允许总误差在血脂检测中的质量管理。方法对2015年参加原卫生部脂类正确度验证的胆固醇(CHOL)、三酰甘油(TG)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)进行σ分值、质量目标指数(QGI)、优先改进措施及性能评定等指标进行评价,对成绩不理想的CHOL作原因分析。结果生物学变异设定的质量规范3个层次,当允许总误差处于适当的水平时,TG、HDL-C、LDL-C的σ分值已满足6,无需改进。而CHOL的分析性能为差,需优先改进正确度。当允许总误差处于最佳水平时,4个项目中只有TG的σ分值可达到“良”,可进行精密度改进。当允许总误差处于最低水平时,TG、HDL-C、LDL-C的σ分值远大于6,分析性能达到“优”,CHOL的σ分值(2.9)已接近3σ水平,应从正确度进行纠正。结论6σ质量理论可反映检测项目的性能,且能有效提高分析质量。
血清脂质;生物学变异;总允许误差;准确性;精密度
血脂检测对临床应用作用极大,其发展也相当迅速,准确度是核心要求。因此,客观合理地选择质量目标使临床实验室达到或提高检测水平非常重要。检测系统的方法性能的可接受性,是否达到实验室规定的质量目标,是质量管理的重要内容[1]。生物学变异的质量目标,是依据检验项目个体内生物学变异(CV个体内)和个体间生物学变异(CV个体间)数据,考虑客观医学监测和诊断需要,经统计分析导出临床实验室检测项目不精密度、不准确度和不同水平允许总误差的分析质量规范[2-3]。不同的项目生物学变异不同,达到的分析质量水平也不同。本研究拟运用生物学变异允许总误差,结合该科现行的质量状态,探讨源自生物学变异的允许总误差在血脂检测质量管理中的应用,现报道如下。
1 材料与方法
1.1仪器与试剂Roche Cobas 8000型全自动生化分析仪(昆明医科大第一附属医院检验科)。校准品为罗氏公司产品,室内质控品为英国朗道公司生产,定值质控血清,包括正常和病理2个质控浓度水平,均在有效期内使用。原卫生部临床检验中心脂类正确度验证(TV)计划品:编码NCCL-C-16,批号201511和GBW0178b的2个浓度水平。胆固醇(CHOL)、三酰甘油(TG)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)项目试剂均使用罗氏公司原装试剂。
1.2质量目标对每项试验以允许总误差(TEa)的形式规定质量要求,TEa采用生物学变异允许总误差[4]。
1.3质量水平评估
1.3.1不精密度评价采用变异系数(CV%)表示,2015年1~10月实验室信息系统自动记录生成的8 000个生化分析仪的室内质控结果,每个项目2个浓度水平的质控,取2次CV%均值作为评估依据。
1.3.2不准确度评价偏倚(Bias)表示,该室2015年参加原卫生部临床检验中心血脂正确度验证计划结果数值(以该室测定均值与靶值之间的相对偏差作为实验室偏倚Bias),取2个批号偏倚数据均值。
1.3.3西格玛水平分析按照公式σ值=(TEa-|Bias|)/CV[5]。
1.3.4判断标准将分析性能水平判定为世界级(σ≥6)、优秀(5≤σ<6)、良好(4≤σ<5)、临界(3≤σ<4)、差(2≤σ<3)和不可接受(σ<2)[6],低于3σ性能的检测项目应立即采取措施改进或换用其他检测方法。
1.3.5未达6σ的原因分析计算质量目标指数(QGI)分析性能未达6σ,QGI=Bias/(1.5×CV)。QGI<0.8,提示导致方法性能不佳的主要原因是精密度超出允许范围,优先改进精密度;QGI>1.2提示方法准确度较差,优先改进准确度;QGI为0.8~1.2,提示准确度和精密度均需改进[7]。
2 结 果
2.1各检测项目TEa%最佳水平的优先改进措施当TEa%处于最佳水平时,4个项目只有TG的σ值达到“良”,可优先改进其准确度。其余4项的σ值均小于3σ。见表1。
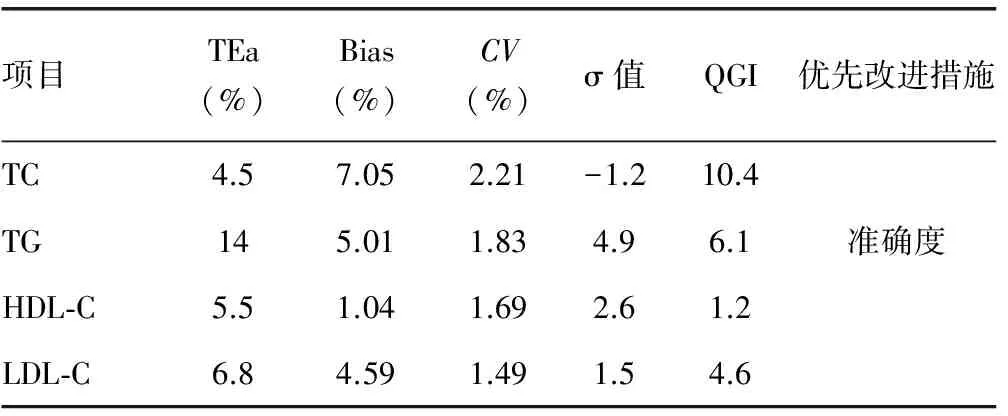
表1 各检测项目TEa%最佳水平的优先改进措施
注:“优先改进措施”未标注者,表明该TEa%目前在该科室要求过高。
2.2各检测项目TEa%适当水平的优先改进措施当TEa%处于适当水平时,TG的σ>6σ;HDL-C、LDL-C的σ值已满足6σ,该3个项目分析性能均达到“优”,无需任何改进,而TC 的σ<2σ,分析性能水平不可接受,应立即采取措施改进或换用其他检测方法。见表2。
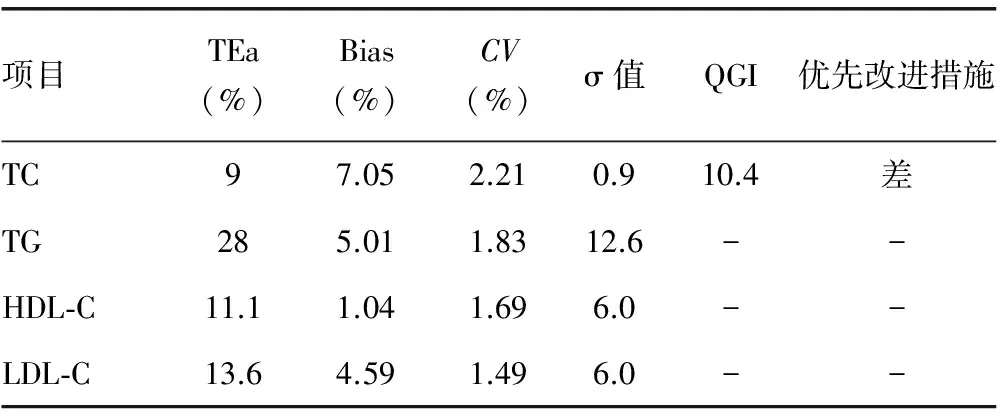
表2 各检测项目TEa%适当水平的优先改进措施
注:“-”分别对应表示σ>6时不用计算QGI及采取纠正措施。
2.3各检测项目TEa%最低水平的优先改进措施当TEa%处于最低水平时,TG、HDL-C、LDL-C 3个项目的σ值均大于6σ,TC的σ达到“差”,需优先改进准确度。见表3。
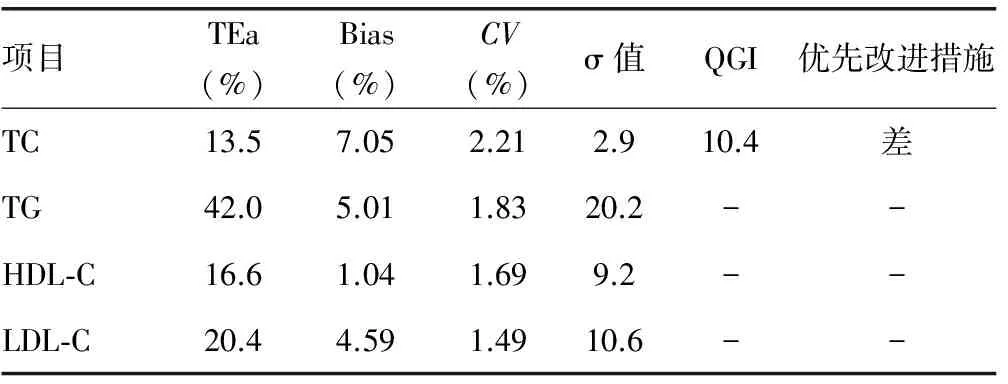
表3 各检测项目TEa%最低水平的优先改进措施
注:“-”分别对应表示σ>6时不用计算QGI及采取纠正措施。
2.4TC项目改进结果采取改进措施后,TC的σ值由2.9上升到4.8,分析性能由“差”提高到“良”,需优先改进其准确度。见表4。
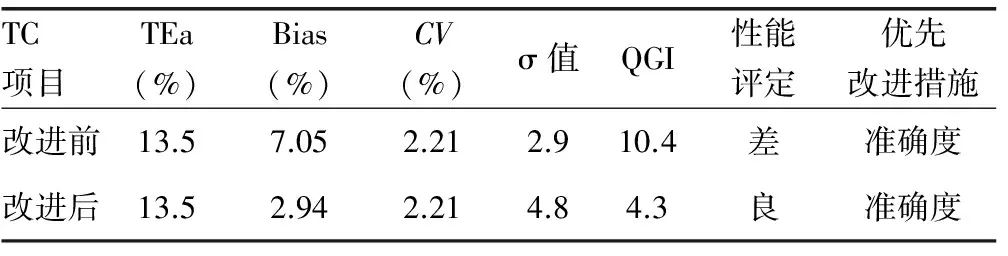
表4 TC改进前后的性能评定
3 讨 论
质量规范(目标)的制定直接影响检验结果的准确性,质量规范过宽,不能提高检测水平,范围过窄不利于整体发展[8]。目前,大多数临床实验室采用美国临床实验室修正法规(CLIA′88)为评判标准,其是基于可通过要求的标准而不是适当的标准,可接受范围就相对较宽,所以以生物学变异为基础的质量规范研究成为关注焦点[2-3,7-9]。国内学者将TEa%进一步分为最佳、适当、最低性能3个层次,以便于实验室根据各项目检测系统的TEa%来评价其能达到质量要求的层次,特别是高度关注那些尚不能达到最低性能的项目。
σ是定量描述实验室分析性能的指标之一,6σ是近年来才开始广泛使用的一个概念,代表新兴的质量管理系统[11]。临床实验室的6σ与全面质量管理(TQM)显著相关,有利于TQM的顺利实施。采用σ评价检验项目性能,适合于已经积累了一定质控数据和室间质量评价数据的常规检验项目的性能评价[12]。6σ质量管理不仅是评价方法性能的工具,也是指导质量改进的工具,为使分析性能达到6σ,有必要了解导致性能不佳的原因——正确度和(或)精密度较差,QGI值可以科学地指导实验室决策优先改进精密度还是正确度。
本研究将血脂4项使用6σ质量管理理论进行性能指标调查。表1结果表明,当TEa%处于最佳水平时,只有TG的σ达到“良”,可优先改进其准确度。表2结果显示,当TEa处于适当水平时,TG的σ>6,HDL-C、LDL-C 已满足6σ,3个项目均无需改进,但TC的σ水平不可接受,必须立即采取措施改进或换用其他检测方法。 表3结果提示,当TEa处于最低水平时,除TC项目的σ水平为“差”,需改进其准确度外,其余均大于6,无需改进。因此,本组对TC项目的优先改进措施进行处理。表4结果说明,TC采取改进措施前后的TEa、Bias、CV%、σ值、QGI、优先改进措施及性能评定的对比。对TC优先改进措施进行原因查找:仪器由有资质的专业人员严格按SOP操作;仪器各部件正常,运行正常;试剂均在有效期内使用,无仪器内试剂开瓶过期等情况;校准品、质控品均无过期,无保存不当、反复冻融等现象;实验室水质合格;方法为胆固醇氧化酶法,各上机参数按厂商提供设定;环境温、湿度均在受控范围;且该实验室在做脂类正确度验证期间,整个分析系统(人、机、料、环、法)未发现异常,室内质控在控。考虑系统误差所致,重新定标后,室内质控值处于2S~3S,和试剂厂家联系后,重新订购新批号校准品,重新定标,室内质控值降至1S以内,重新分析存留的脂类正确度计划品样本后,Bias%从7.05%降至2.94%,σ水平也由2.9升至4.8,分析性能由“差”转为“良”,其优先改进措施仍需提高准确度。对于σ水平为4.8或更高的方法,质控方法的选取就很容易。从构成分析系统的每一个要素认真分析,对不够完善的地方进行后续的改进和研究,以期不断完善。
允许总误差的确定是影响σ值的重要因素,同一试验用不同来源的TEa计算得到的σ值并不相同,甚至差异很大。张路等[13]报道5种不同来源 TEa标准σ值的评价,生物学变异TEa值常被认为是最严格、真实且适当。这和已经发布的行业标准WS/T403-2012及WS/T 406-2012中分析质量指标的设定具有一致性。
综上所述,根据该实验室的血脂检测质量目标、室间质评(正确度验证计划)和室内质控数据,计算σ值和质量目标指数,能准确评价实验室的检测水平,尤其对于方法性能不佳的项目,需持续改进检验质量,以更好地满足临床需求。
[1]王伦善,贾建安,金玉亮,等.6σ标准在临床生化质量管理中的应用[J].临床输血与检验,2014,16(3):269-272.
[2]Ricós C,Alvarez V,Cava F,et al.Current databases on biological variation:pros,cons and progress[J].Scand J Clin Lab Invest,1999,59(7):491-500.
[3]Kallner A,Mcqueen M,Heuck C.The Stockholm consensus conference on quality specifications in laboratory medicine,25-26 April 1999[J].Scand J Clin Lab Invest,1999,59(7):475-476.
[4]王治国.临床检验质量控制技术[M].北京:人民卫生出版社,2004:343-345.
[5]Westgard JO.Six sigma risk analysis[M].Madison:Westgard Qc,2011.
[6]王治国.临床检验方法确认与性能验证[M].北京:人民卫生出版社,2009.
[7]Westgard JO,Westgard SA.The quality of laboratory testing today:an assessment of sigma metrics for analytic quality using performance data from proficiency testing surveys and the CLIA criteria for acceptable performance[J].Am J Clin Pathol,2006,125(3):343-354.
[8]何法霖,白玉,王薇,等.由生物学变异确定的质量规范在常规化学室间质评和室内质控中的应用[J].中华检验医学杂志,2012,35(6):531-537.
[9]王治国.临床检验质量控制技术[M].3版.北京:人民卫生出版,2014:146-150.
[10]冯仁丰.临床检验质量管理技术基础[M].上海:上海科学技术文献出版社,2003.
[11]Mbrowski GS,Anderson PG,Crampton CA,et a1.Pump up your PTIQ[J].MLO Med Lab Obs,1996,28(10):46-51.
[12]赵海建,张传宝,周伟燕,等.应用六西格玛管理方法评价脂类检验项目质量水平[J].中华检验医学杂志,2014,37(4):311-314.
[13]张路,王薇,王治国.允许总误差在西格玛度量用于评价临床化学检测项目分析质量上的应用研究[J].检验医学,2015,30(9):953-957.
Study on the quality management of biological variation allowed total error in detection of serum lipid
LIXiufang1,QIANJing1,ZHAOYing2,YANGYuelin1,CAOJiexian1△
(1.TheFirstPeople′sHospitalofKunming,Kunming,Yunan650000,China;2.TheFirstAffiliatedHospitalofKunmingMedicalUniversity,Kunming,Yunnan650011,China)
ObjectiveTo study on the application of biological variation total allowable error in quality management of serum lipid detection.MethodsThe σ score,quality goal index (QGI),priority improvement measures and performance evaluation of lipid accuracy criteria were evaluated,including cholesterol (CHOL),triglyceride (TG),high density lipoprotein (HDL-C),low density lipoprotein (LDL-C),which included in the standard of accuracy of the Ministry of Health in 2015.The reason for unsatisfactory results of cholesterol (CHOL) test were analyzed.ResultsBased on the three levels of quality specifications derived in biological variation,when the total allowable error was located at an appropriate level,the σ score of TG,HDL-C,LDL-C reached 6,it was not required for improvement.While the score of CHOL performance analysis was poor,accuracy was required to give priority to improving.When the total allowable error reached the best level,only the σ score of TG achieved “good” in the four items,improvement of precision was needed.When the total allowable error was located at the lowest level,the σ score of TG,HDL-C,LDL-C was greater than 6,the score of performance analysis reached the “excellent”.The σ score of CHOL (2.9) had been closen to 3σ,accuracy was required to be corrected.ConclusionThe biological variation derived total allowable error is easy to meet the requirements of the quality management in serum lipid determination by current technologies and methods.The theory of 6σ quality can reflect the performance of detection indexes,and improve the quality of analysis effectively.
serum lipid;biological variation;total allowable error;accuracy;precision
栗秀芳,女,主管技师,主要从事临床生物化学检验研究。
,E-mail:caojiexian2014@163.com。
10.3969/j.issn.1673-4130.2016.19.019
A
1673-4130(2016)19-2708-03
2016-02-24
2016-05-10)
