利用原位红外光谱研究钙钛矿复合半导体CH3NH3PbI3的稳定性
2016-11-03付现伟赵天宇宋思德王琪珑崔得良
刘 阳, 付现伟, 赵天宇, 廉 刚, 董 宁,宋思德, 王琪珑, 崔得良
(山东大学晶体材料国家重点实验室, 济南 250100)
利用原位红外光谱研究钙钛矿复合半导体CH3NH3PbI3的稳定性
刘阳, 付现伟, 赵天宇, 廉刚, 董宁,宋思德, 王琪珑, 崔得良
(山东大学晶体材料国家重点实验室, 济南 250100)
利用高压原位红外光谱法实时跟踪监测了CH3NH3PbI3在高压氮气以及不同含量氧气气氛中加热时的变化规律. 发现CH3NH3PbI3对氧气十分敏感, 当氮气中含有1%(体积分数)的氧气时, CH3NH3PbI3加热到150 ℃发生分解; 继续提高氧气含量到21%, 温度升高到100 ℃时CH3NH3PbI3即发生分解; 若在常压高纯氮气中加热, 其分解温度则能提高到250 ℃; 若将氮气压力提高到4.0 MPa, CH3NH3PbI3的分解温度进一步提高到270 ℃. 实验结果表明, 提高压力和减少环境中的氧含量是改善钙钛矿复合半导体稳定性的有效方法. 相应地, 复合半导体光电子器件的热处理过程可以在更高的温度下进行, 从而有希望获得性能更加优良的钙钛矿复合半导体光电子器件.
钙钛矿; 复合半导体; 稳定性; 原位红外光谱
太阳能具有清洁、 成本低和可再生的优点, 是解决目前能源危机和环境污染问题的理想能源, 因此与光伏材料和器件相关的研究已成为近年来的研究热点. 钙钛矿复合半导体CH3NH3PbX3(X=Cl, Br, I)具有大的光吸收系数[1,2]、 高的载流子迁移率以及超长的载流子寿命和扩散长度[3,4], 已经在光伏器件[5,6]、 光电二极管和探测器[7]以及传感器等的研制中得到广泛应用. 自2009年钙钛矿复合半导体光伏器件被首次提出以来[8], 人们做了大量系统的工作, 并于近几年取得了一系列突破性成果. 迄今, 钙钛矿复合半导体光伏器件的能量转换效率已经达到了22.1%[9]. 尽管如此, 这类材料和器件的应用仍面临一系列难题:如难于大面积制备、 含有重金属铅以及器件稳定性差等. 针对前两个问题, 科研人员进行了系统的探索并取得了较大进展. 例如, Liu等[10]在大于1 cm2的柔性衬底上制备了转换效率达到10.2%的钙钛矿复合半导体光伏器件. 另外, 用无铅的CH3NH3SnI3和CH3NH3SnI3-xBrx取代CH3NH3PbX3也得到了较好的结果[11,12].
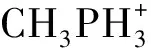
1 实验部分
1.1试剂与仪器
碘甲胺(CH3NH3I, 纯度98.0%, 日本TCI公司), 碘化铅(PbI2, 纯度98.0%, 上海Aladdin公司);N,N-二甲基甲酰胺(DMF, A. R. 级, 天津大茂化学试剂厂). 所有试剂均为购置后直接使用, 未做进一步纯化.
样品的漫反射原位红外光谱使用Thermo Nicolet公司Nexus 670型傅里叶变换红外光谱仪加漫反射附件采集, 测定时设定波数分辨率为4 cm-1, 扫描次数为32次, 波数范围650~4000 cm-1. 加热样品时产生的气态产物的原位红外光谱则利用高温高压分解池(HTHP cell)中的透过模式采集, 测试时波数分辨率为4 cm-1, 扫描次数为50次, 波数范围650~4000 cm-1. 样品的X射线衍射分析使用Bruker公司D8 Advance型多功能X射线衍射仪, 扫描速度为0.1 s/step, 扫描范围:10°~50°.
1.2实验过程
依次将PbI2(0.47 g)和CH3NH3I(0.1621 g)加入到1 mL DMF中, 再将得到的溶液加热到70 ℃后恒温, 并持续搅拌12 h, 得到前驱体溶液. 将前驱体溶液继续加热到120 ℃使溶剂挥发, 即得到复合半导体CH3NH3PbI3. 在采集样品的原位红外光谱时, 将合成的CH3NH3PbI3与KBr按照1∶100的质量比混合均匀后放入漫反射附件的样品槽中[图1(A)]. 开始加热前, 先向样品室内反复通入高纯氮气, 以便排空其中的空气. 再向样品室内通入高纯氮气(常压和高压氮气), 然后将样品池加热到一系列设定温度值, 并同时采集样品的红外光谱. 测试过程中以纯KBr作为背景. 监测样品分解产生的气态产物时, 将一定量的CH3NH3PbI3放在高温高压分解池[图1(B)]的样品槽中, 并向样品室内反复通入高纯氮气以排除其中的空气, 最后再分别通入含氧量(体积分数)为1%, 5%, 10%, 15%以及21%的氮气, 并在加热过程中实时采集气态产物的红外光谱. 采集红外光谱时以室温下的空气为背景. 图1为原位红外光谱采集系统的示意图.
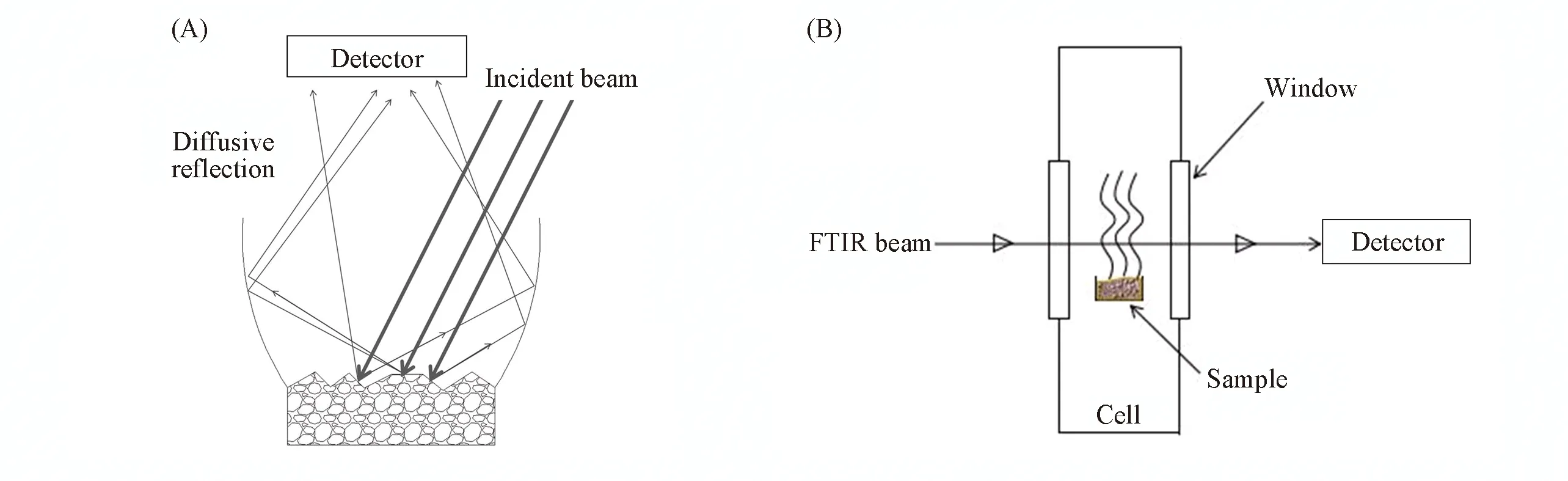
Fig.1 Schematic diagram of in situ FTIR spectroscopy equipment(A) Diffusive reflection cell; (B) high temperature high pressure(HTHP) cell.
2 结果与讨论
2.1氧气对CH3NH3PbI3稳定性的影响
除了水蒸汽外, 氧气是促使钙钛矿复合半导体分解的另一个重要因素. 研究发现, 将CH3NH3PbI3在氧气中于85 ℃加热24 h后, 会有PbI2固体生成[20]. 但是, 对CH3NH3PbI3钙钛矿复合半导体材料在较低氧含量的环境(封装后的器件在长时间工作后就会有少量氧气渗入钙钛矿复合半导体层)中的稳定性研究较少. 图2给出了在氧含量分别为1%, 5%, 10%, 15% 和21%的常压氮气中加热CH3NH3PbI3时采集的气态产物的原位红外光谱. 其中, 2930和3224 cm-1处的吸收峰分别对应于CH3NH2中饱和C—H键的伸缩振动和N—H键伸缩振动. 很明显, 如果在气态产物中检测到CH3NH2, 则可以直接证实CH3NH3PbI3已经发生分解. 从图2(A)可以看出, 当氮气中含有1%的氧气时, 随着温度的升高, 在150℃附近出现了CH3NH2的2个吸收峰(2930和3223 cm-1), 表明HI和CH3NH2在此温度下已经脱离CH3NH3PbI3晶体, 即CH3NH3PbI3的起始分解温度为150 ℃. 从图2(B)~(E)可以看出, 当氧气的含量分别为5%, 10%, 15%和21%时, CH3NH3PbI3的起始分解温度分别为140, 125, 110和100 ℃. 这表明氧气含量的增加会明显促进CH3NH3PbI3的分解, 而降低氧含量则可大幅度提高钙钛矿复合半导体的稳定性[20].
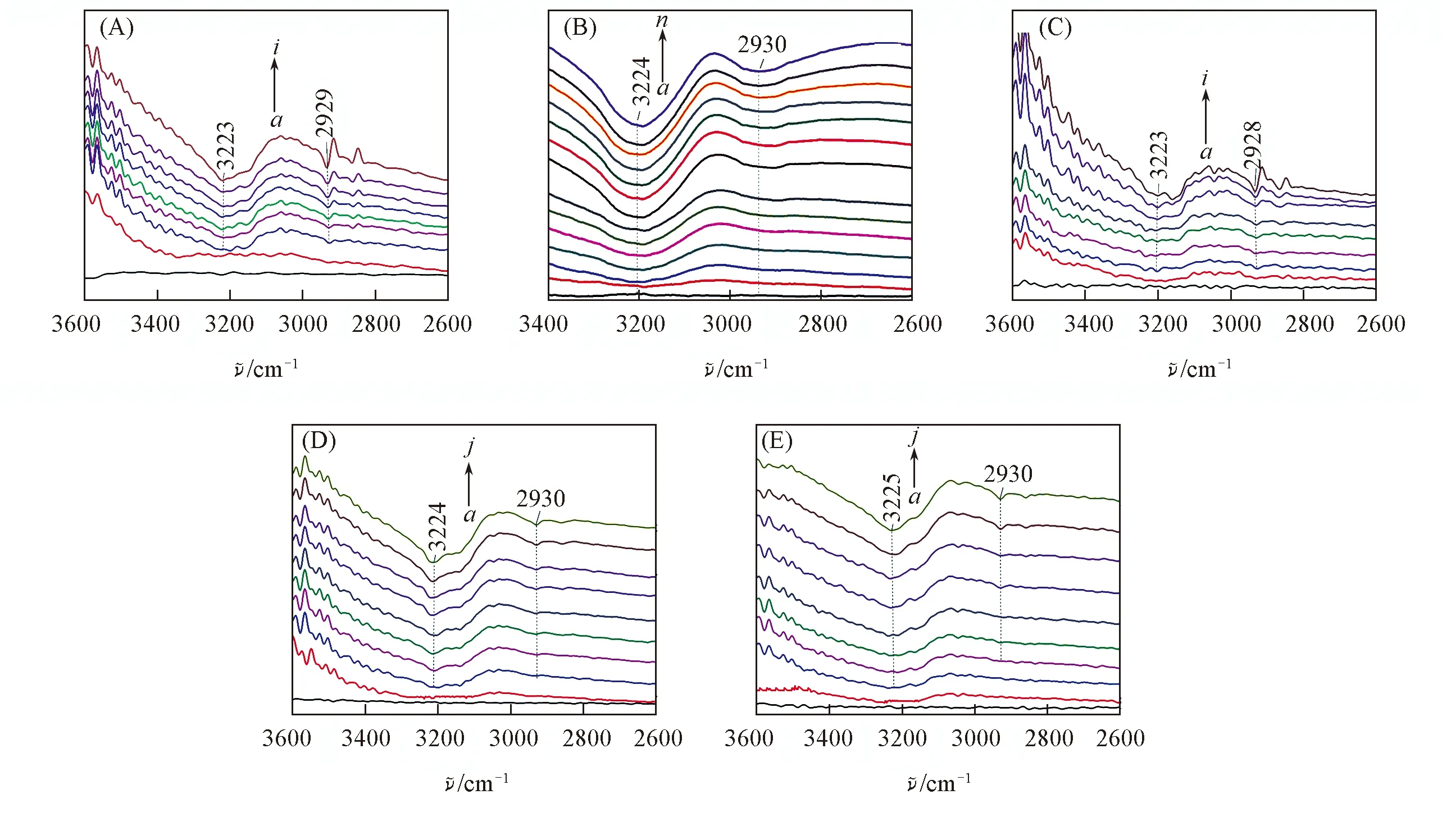
Fig.2 In situ FTIR spectra collected when heating CH3NH3PbI3 in nitrogen containing 1%(A), 5%(B), 10%(C), 15%(D) and 21%(E) O2Temperature/℃:(A) a—i:30, 140, 150, 160, 170, 180, 190, 200, 250; (B) a—n:22, 120, 140, 150, 160, 180, 190, 200, 210, 220, 230, 240, 250, 260; (C) a—i:30, 120, 125, 130, 140, 150, 160, 200, 250; (D) a—j:30, 100, 110, 120, 130, 140, 150, 160, 200, 250; (E) a—j:30, 80, 100, 110, 120, 130, 140, 150, 180, 200.
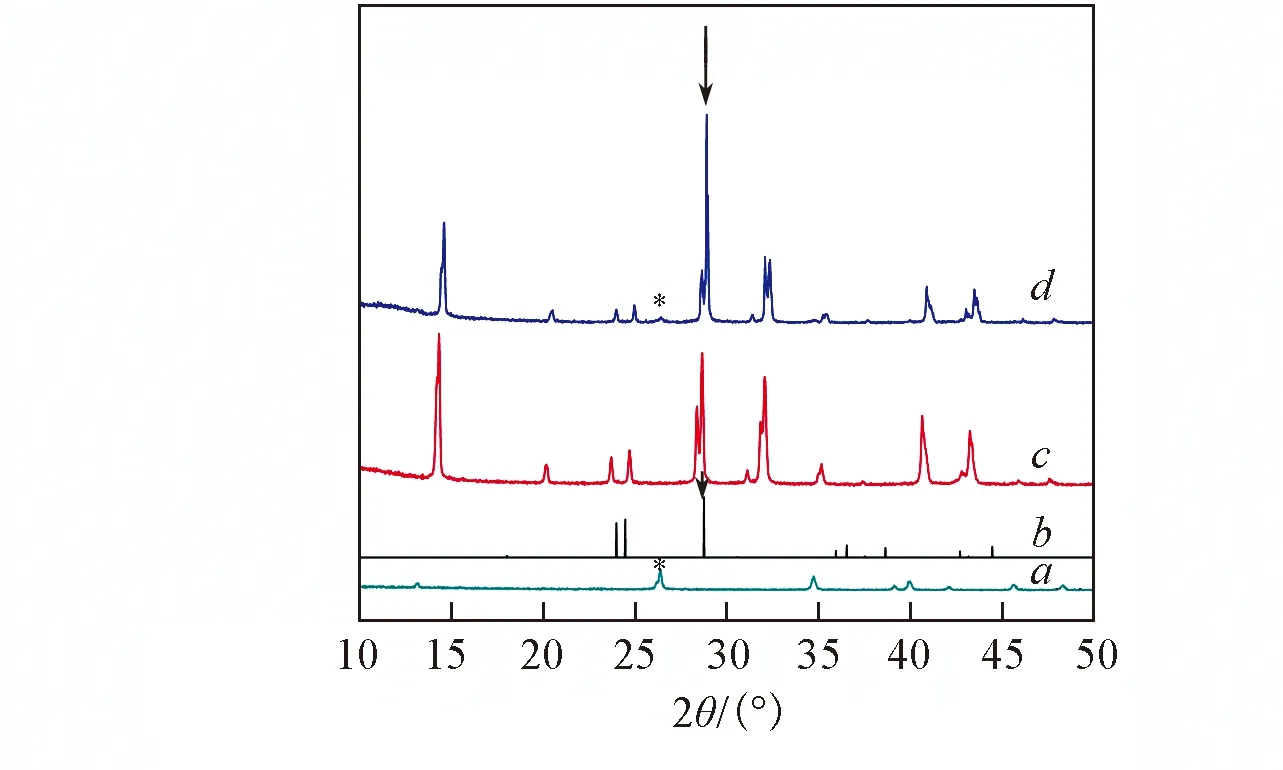
Fig.3 XRD patterns of PbI2(a), I2(b), CH3NH3PbI3(c) and the sample prepared by heating CH3NH3PbI3 at 110 ℃ in synthetic air(d)
样品的X射线衍射(XRD)谱同样可以证实上述结论. 图3给出了钙钛矿复合半导体CH3NH3PbI3在氧含量为21%的常压氮气(合成空气)中于110 ℃加热8 h后所得样品的XRD谱图. 可以看出, 经过上述加热处理后, 在25.9°出现的新衍射峰(图中用星号标出)来源于PbI2, 表明此时样品已经分解; 另一方面, 经过上述加热处理后, 与CH3NH3PbI3对应的衍射峰强度整体上减弱, 但位于28.5°的峰(图中用箭头标出)强度却大幅增加(图3谱线c), 这实际上是由钙钛矿CH3NH3PbI3的衍射峰与I2的主峰相互叠加引起的. 图3表明CH3NH3PbI3在较高氧含量的气氛中加热时, 产物中含有PbI2和I2.
根据上述结果, 推测在含有一定量氧气的氮气中加热CH3NH3PbI3时, 会发生如下分解反应:
(1)
(2)
(3)
在分解过程中, CH3NH3I, CH3NH2和HI作为中间产物同时存在. 在上述几个反应步骤中, 氧气与HI间发生的反应(3)快且不可逆, 它会消耗HI从而促使反应(1)和(2)的平衡向右进行, 使CH3NH3PbI3更容易发生分解. 环境气氛中存在的氧气会大大促进反应过程(1)和(2), 因此CH3NH3I不再是一个稳定产物, 其吸收峰(1407 cm-1)未出现在固态样品的红外谱图上.
2.2常压氮气中CH3NH3PbI3的稳定性

Fig.4 In situ FTIR spectra collected when heating CH3NH3PbI3 in N2 under atmospheric pressure Temperature/℃:a—i:30, 200, 230, 250, 260, 270, 280, 300, 30(CH3NH3I).
既然降低氧含量可以提高CH3NH3PbI3的稳定性, 那么如果能够完全排除环境中的氧气, 则CH3NH3PbI3的稳定性应该能够得到大幅改善. 图4是在常压高纯氮气中加热CH3NH3PbI3时样品表面的漫反射红外光谱. 其中, 在CH3NH3PbI3的吸收谱上, 1578, 1468.7和1421.3 cm-1处的吸收峰分别对应于N—H键弯曲振动、 C—N键伸缩振动和C—H键弯曲振动. 考虑到在CH3NH3PbI3中, 有机胺分子与Pb-I无机骨架之间主要通过N—H…I氢键结合[21], 因此N—H键对应的吸收峰的变化可以直接反映出晶体结构的变化. 在原位测试过程中, 主要是通过将CH3NH3PbI3中N—H键的弯曲振动对应的吸收峰(1578 cm-1)与CH3NH3I对应的吸收峰(1407 cm-1)的变化趋势结合起来分析CH3NH3PbI3的分解过程.
图4表明, 随着温度的逐渐升高, 1578 cm-1处的吸收峰相对强度不断变弱, 而且在250 ℃达到最小值. 温度超过250 ℃后, 该峰强度又逐渐增强且峰位向低波数移动(红移); 与此同时, CH3NH3I的吸收峰(1407 cm-1)在250 ℃附近开始出现. 该现象说明, 在常压氮气中加热CH3NH3PbI3时, 样品从250 ℃开始按照下面的方式分解[22]:
(4)
(5)
2.3高压氮气中CH3NH3PbI3的稳定性
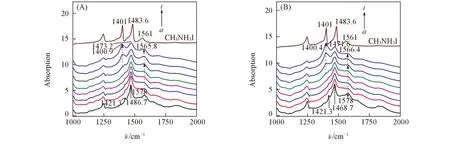
Fig.5 In situ FTIR spectra collected when heating CH3NH3PbI3 in N2 under pressure of 2.0 MPa(A) and 4.0 MPa(B)Temperature/℃:(A) a—i:30, 150, 200, 230, 250, 260, 280, 300, 30(CH3NH3I); (B) a—i:30, 200, 250, 260, 270, 280, 290, 300, 30(CH3NH3I).
比较上面的结果发现, 当环境气氛中的氧气被排除后, CH3NH3PbI3的分解温度得到大幅提高. 再考虑到有气体产物的分解反应一般会对压力比较敏感, 那么增大氮气的压力可进一步提高CH3NH3PbI3的分解温度.
图5是氮气压力分别为2.0 MPa和4.0 MPa时, 加热CH3NH3PbI3原位采集的漫反射红外谱图. 由图可见, 当氮气压力为2.0 MPa时, CH3NH3I对应的位于1401 cm-1的吸收峰在260 ℃附近开始出现, 而在4.0 MPa氮气中加热CH3NH3PbI3时, 该峰直到270 ℃才变得比较明显. 说明当氮气压力从常压逐渐升高到4.0 MPa时, CH3NH3PbI3的分解温度从250 ℃提高到了270 ℃. 事实上, 在高压作用下, 材料分子之间的距离会被压缩, 相互作用增强, 从而使分解过程被抑制[23].
3 结 论
通过利用原位红外光谱方法监测钙钛矿复合半导体CH3NH3PbI3的分解过程, 发现排除环境气氛中的氧气以及提高压力都可以明显改善其稳定性. 该结果不但对钙钛矿复合半导体光电器件制备工艺的优化具有指导作用, 而且有可能在此基础上探索出单晶薄膜的制备方法, 从而获得性能更加优异的光伏器件和光电探测器件.
在钙钛矿复合半导体CH3NH3PbI3的合成过程中, 清华大学化学系王立铎教授给予很多具体指导和帮助, 在此表示衷心感谢.
[1]Tanaka K., Takahashi T., Ban T., Kondo T., Uchida K., Miura N.,SolidStateCommun., 2003, 127(9), 619—623
[2]Ball J. M., Stranks S. D., Hörantner M. T., Hüttner S., Zhang W., Crossland E. J., Ramirez I., Reide M., Johnston M. B., Friend R. H.,EnergyEnviron.Sci., 2015, 8, 602—609
[3]Zhao Y. Q., Wu L. J., Liu B., Wang L. Z., He P. B., Cai M. Q.,J.PowerSources, 2016, 313, 96—103
[4]Leijtens T., Stranks S. D., Eperon G. E., Lindblad R., Johansson E. M., McPherson I. J., Rensmo H., Ball J. M., Lee M. M., Snaith H. J.,ACSNano, 2014, 8(7), 7147—7155
[5]Boix P. P., Agarwala S., Koh T. M., Mathews N., Mhaisalkar S. G.,J.Phys.Chem.Lett., 2015, 6, 898—907
[6]Qian L., Ding L. M.,Chem.J.ChineseUniversities, 2015, 36(4), 595—607(钱柳, 丁黎明. 高等学校化学学报, 2015, 36(4), 595—607)
[8]Akihiro K., Kenjiro T., Yasuo S., Tsutomu M.,J.Am.Chem.Soc., 2009, 17(131), 6050—6051
[9]NREL Chart, http://www.nrel.gov/ncpv/images/efficiency_chart.jpg, Accessed 13.03.2016, 2016
[10]Liu D., Kelly T. L.,Nat.Photonics, 2014, 8(2), 133—138
[11]Zhang Y. Y., Chen S., Xu P., Xiang H., Gong X. G., Walsh A., Wei S. H.,arXivpreprintarXiv:1506.01301, 2015
[12]Savage L.,Opt.PhotonicsNews, 2014, 25(11), 26—33
[13]Mor G. K., Varghese O. K., Paulose M., Shankar K., Grimes C. A.,Sol.EnergyMater.Sol.Cells, 2006, 90(14), 2011—2075
[14]Niu G., Guo X., Wang L.,J.Mater.Chem.A, 2015, 2(17), 8970—8980
[16]Ito S., Tanaka S., Manabe K., Nishino H.,J.Phys.Chem.C, 2014, 118, 16995—17000
[17]Pathak S. K., Abate A., Leijtens T., Hollman D. J., Teuscher J., Pazos L., Docampo P., Steiner U., Snaith H. J.,Adv.EnergyMater., 2014, 4, 1301667
[18]Misra R. K., Ciammaruchi L., Aharon S., Mogilyansky D., Etgar L., Visoly-Fisher I., Katz E. A.,arXivpreprintarXiv:1603.08683, 2016
[19]El-Mellouhi F., Bentria E. T., Rashkeev S. N., Kais S., Alharbi F. H.,arXivpreprintarXiv:1604.06875, 2016
[20]Conings B., Drijkoningen J., Gauquelin N., Babayigit A., D’Haen J., D’Olieslaeger L., Ethirajan A., Verbeeck J., Manca J., Mosconi E., Angelis F. D., Boyen H.,Adv.EnergyMater., 2015, 5, 1500477
[21]Geng W., Zhang L., Zhang Y. N., Lau W. M., Liu L. M.,J.Phys.Chem.C, 2014, 118, 19565—19571
[22]Dualeh A., Gao P., Seok S. I., Nazeeruddin M. K., Grätzel M.,Chem.Mater., 2014, 26(21), 6160—6164
[23]Wang Y., Lü X., Yang W., Wen T., Yang L., Ren X., Wang L., Lin Z., Zhao Y.,J.Am.Chem.Soc., 2015, 137(34), 11144—11149
(Ed.:F, K, M)
† Supported by the National Natural Science Foundation of China(Nos.51102151, 51372143).
Investigation on Stability of Perovskite Semiconductor CH3NH3PbI3byIn-situFTIR Spectroscopy†
LIU Yang, FU Xianwei, ZHAO Tianyu, LIAN Gang, DONG Ning,SONG Side, WANG Qilong, CUI Deliang*
(State Key Lab of Crystal Materials, Shandong University, Jinan 250100, China)
Perovskite hybrid semiconductors CH3NH3PbX3(X=Cl, Br, I) have attracted much interests of the chemists and material scientists due to their advantages including facile preparation, low cost and excellent optoelectronic properties. However, the poor stability of these hybrid semiconductors severely frustrated their practical applications, thus it is very important to investigate their decomposition process and explore the new route to improve their stability. Here we investigated the thermal decomposition process of CH3NH3PbI3using anin-situFourier transformation infrared(FTIR) spectrometer. It was found that the stability of CH3NH3PbI3was rather sensitive to the existence of oxygen, it began to decompose at 150 ℃ when 1%(volume fraction) oxygen was introduced into the nitrogen atmosphere. In comparison, its decomposition temperature strikingly increased to 250 ℃ when it was heated in pure nitrogen of atmospheric pressure. It was rather surprising that the decomposition temperature of CH3NH3PbI3further increased to 270 ℃ when the pressure of nitrogen increased to 4.0 MPa. This phenomenon reveals that the thermal stability of CH3NH3PbX3should be greatly improved by applying an even high pressure, thus the post-treatment of photovoltaic devices could be performed at much higher temperature and even better performance can be anticipated.
Perovskite; Hybrid semiconductor; Stability;In-situFourier transformation infrared spectroscopy
10.7503/cjcu20160179
2016-03-23. 网络出版日期:2016-08-18.
国家自然科学基金(批准号:51102151, 51372143)资助.
O614; O641; O657.61
A
联系人简介:崔得良, 男, 博士, 教授, 主要从事复合半导体材料方面的研究. E-mail:cuidl@sdu.edu.cn
