中高温条件下铝镁锂与水反应的热重分析①
2016-11-03杨卫娟刘晓伟张天佑刘建忠周俊虎
杨卫娟,刘晓伟,张天佑,施 伟,刘建忠,周俊虎
(浙江大学 能源清洁利用国家重点实验室,杭州 310027)
中高温条件下铝镁锂与水反应的热重分析①
杨卫娟,刘晓伟,张天佑,施伟,刘建忠,周俊虎
(浙江大学 能源清洁利用国家重点实验室,杭州310027)
为了探究中高温条件下促进铝水反应的有效方法,利用热重分析仪研究了从室温到1 030 ℃范围内Al-Mg-Li三元金属合金(Al含量85%)与水蒸气反应时的燃烧特性。实结果表明,700 ℃通水后TG曲线出现2个明显的质量增加阶。第1阶段从700 ℃开始,持续时间和增重比例均随着Li含量增加而增加,最高增重速率出现在740 ℃附近,第2阶段起始温度随着Li含量的增加而升高;样品增重效率随Li含量变化呈现S形变化规律。在11%Li工况时,最大反应速度和燃烧效率都达到峰值。
铝水反应;镁;锂;热重分析
0 引言
金属基燃料因为具有高能量密度的特点,成为下一代水下推进系统的首选燃料[1-3]。一般的金属基燃料由金属或者金属合金(铝、镁、铝镁合金等)及添加物组成,反应系统通过金属与水直接反应放出大量热来提供动力[4-5]。铝金属燃料因具有更好的能量特性而受到了广泛关注[6]。
铝水反应需要解决的一个重要问题是,当铝与水反应时,其表面会生成一层致密的氧化铝薄膜(α-Al2O3),阻止反应的进一步进行[7]。如何消除氧化铝薄膜的阻碍作用,成为研究者的首要工作目标,一般方法包括通过机械球磨破坏氧化层,添加其他金属形成合金,或者使用小粒径金属粉末等[8-11]。Moore等[12]研究了不同Li含量(从100%Li到26%Li)的铝锂合金燃烧特性,样品在坩埚中加热到1 000~1 400 K与水蒸气反应,在产物中检测到Li2O、γ-LiAlO2、β-Li5AlO4和部分固体LiOH,实验结果表明Li以气相形式与水反应,而Al则以固相参与反应。Ivanov和Grant等[11,13]通过实验研究发现,铝水反应的热力学参数受多种因素影响,燃烧速率随压力增加呈现线性变化,添加剂能够影响点火温度和绝热燃烧温度。Gorbunov等[14]研究Al和Mg等高能量金属在水中的燃烧,结果表明燃烧性能取决于金属粉末的氧化程度,氧化程度取决于金属基燃料与水的比例,且水的相态改变并不影响金属的氧化程度。Richard等[15]发现,金属的熔点越低,则着火点越低;纳米级金属颗粒的燃烧速度要远大于微米级的燃烧速度,主要原因就是金属颗粒表面钝化的氧化膜影响了反应的进行。Yang等[16]利用热天平测量了铝镁锂合金在连续通水条件下升温至1 030 ℃时的热重变化曲线,发现了“三阶段”变化规律,即升温过程中有3个明显的质量增加阶段。
本文以铝基金属燃料的二次燃烧为应用背景,利用热重分析方法探究了室温到1 030 ℃铝镁锂三元金属合金与水蒸气的反应特性,探索了不同镁锂比例对铝水反应的影响,并计算分析了其化学动力学特性。
1 实验
如图1所示,铝粉平均粒径为10 μm,纯度为99.9%;镁粉平均粒径为100 μm,纯度为99.9%;铝锂合金粉末平均粒径为45 μm,纯度为99.99%,合金中铝含量为80%,锂含量为20%。按照各种金属粉末比例不同,样品共分7组,每组中Al的含量都保持85%不变,从第1组到第7组,Li的含量分别为0%、2%、5%、7.5%、10%、13%、15%,相应Mg的比例则从15%下降到0%。实验开始前,将准备好的金属粉按照各组不同比例进行调配,并使之混合均匀。
本实验是在热重分析仪(THERMO CAHN's Thermax500,最高工作温度1 100 ℃)上进行,该热重分析仪内部是一个圆柱形的反应室,样品置于悬挂于反应室中部的石英坩埚中与周围的气体进行反应。因为氮气(N2)在高温条件下可与铝反应生成氮化铝干扰实验结果,所以实验中选择氩气(Ar)作为反应保护气,N2被用来作为热重分析仪的平衡气和炉气。
实验开始前,通入Ar进行扫气,清除反应室内部残余的空气,并保持反应室内部干燥。试验中,温度从室温增加到1 030 ℃,升温速率为25 ℃/min。当温度增加到700 ℃时,向反应室中通入180 ℃的水蒸气。温度增加到1 030 ℃时,保持该温度10 min,使得样品能够充分反应。实验蒸气来自加热管道,通过Ar携带进入反应室内部。用来生成蒸气的水流量为0.1 ml/min,Ar流量为500 ml/min,N2流量为500 ml/min,每组样品的质量均为10 mg。实验原理见图2,表1给出了主要热重实验的结果。

(a) 铝粉 (b) 镁粉 (c) 铝锂合金粉末

图2 实验原理图

表1 热重实验结果
2 实验结果与讨论
几种不同比例样品实验TG和DTG曲线见图3。图3中的TG和DTG曲线表明该反应主要有3个阶段:首先是反应开始前的失重阶段;其次是700 ℃通水蒸汽后3种金属与水迅速反应的第1增重阶段;最后是1 000 ℃附近铝和水反应使得质量增加的第2增重阶段。
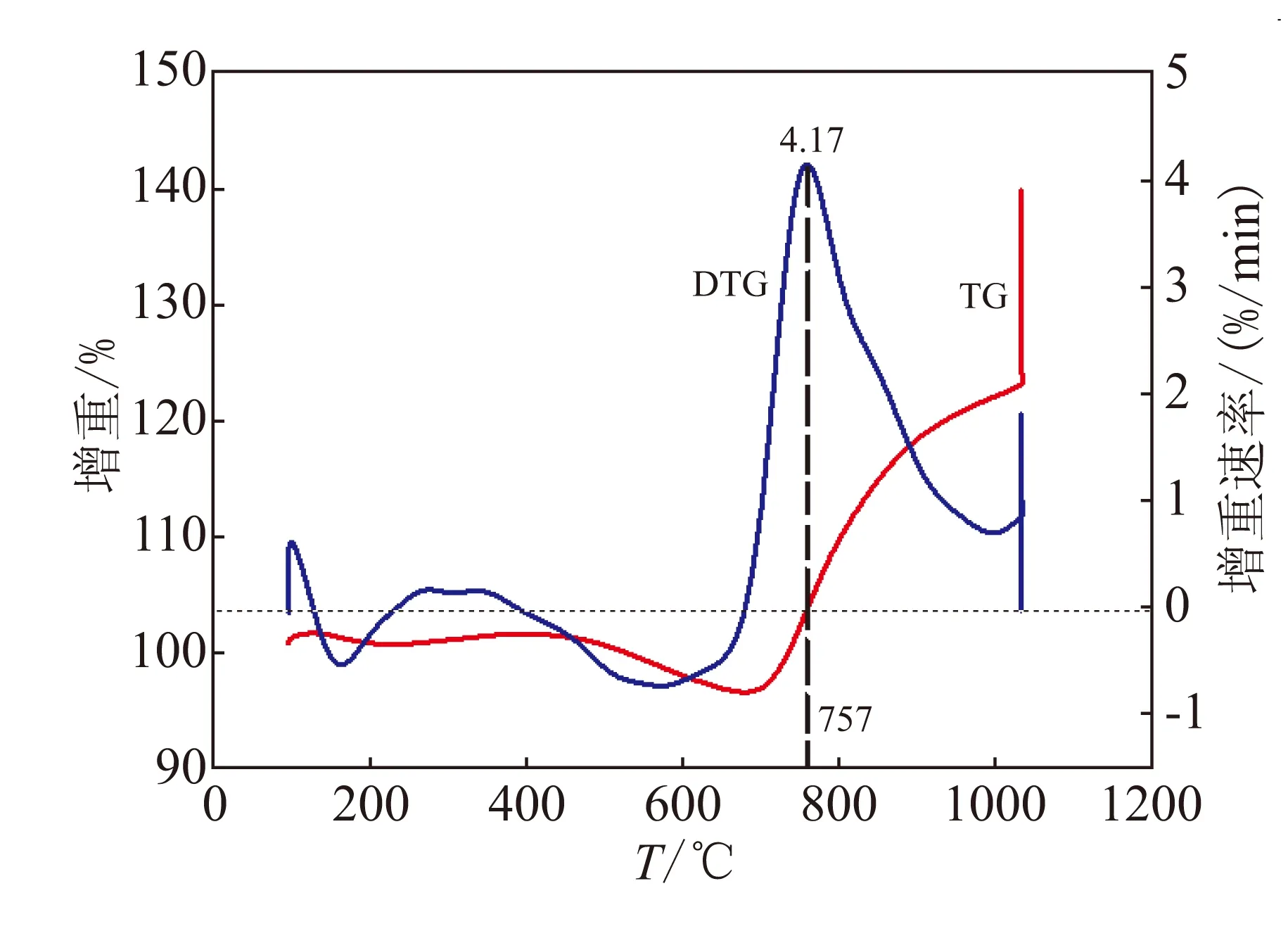
(a)15%Li
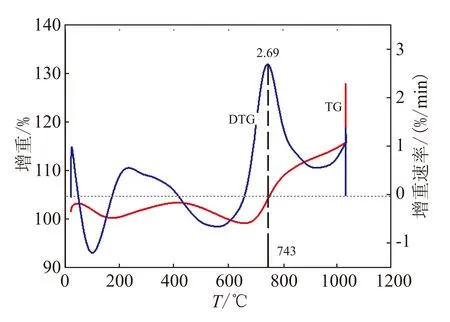
(b) 7.5%Li

(c) 0%Li
TG和DTG曲线显示,随着温度升高,开始样品质量基本保持不变,从410 ℃附近到700 ℃为失重阶段:样品质量出现明显下降,失重比例最高可达3.2%,这是因为金属混合物中Mg和Li的蒸发。由表2可知[17],对于铝镁锂3种金属在600 ℃时, Mg和Li具有相对较高的蒸气压和蒸发速率。铝在600 ℃时蒸发速率只有5.14×10-9g/(cm2·h),与镁锂相比仍相差近十个数量级,所以此时铝的蒸发量可忽略不计。因此,在这一温度区间可能是Mg和Li蒸发导致样品质量出现下降。另一方面,结合表1数据可发现,当Li和Mg的质量比接近1时(7.5%Li工况),样品的失重率很小,说明金属镁和锂的相对含量对前期失重有着很大影响,其机理有待今后深入研究。
研究表明,加热阶段会导致添加剂如镁锂的蒸发损失。这一现象将在金属燃料的一次燃烧中发生。虽然失重比例较小,但蒸发物几乎全部来自镁锂,其对金属燃料的燃烧效果的影响不可忽视,这也是金属燃烧器的设计过程中必须考虑到的因素。

表2 600 ℃时各金属蒸气压及在真空中的蒸发速率
700 ℃通入水蒸气后,样品质量出现了一个迅速增加的阶段,锂含量增加时,这一阶段持续时间延长,增重幅度变大。通过进一步计算发现,在这一阶段增重比例明显高于当Mg和Li完全参与反应时的样品增重,说明该段有部分铝同样参与了反应,但参与反应的铝比例有限。根据张天佑等[18]的实验结果,只有温度达到950 ℃以上时,纯铝才能与水发生较明显的反应,而且总的增重效率只能达到12%。推测在第一阶段镁锂与水的反应放热形成了局部高温(>950 ℃),处于局部高温区的铝能够提前与水发生反应。
当温度达到1 000 ℃附近时,TG曲线再次出现明显增长。在这第2阶段的反应中,铝与水蒸气直接发生反应生成氧化铝,使得质量继续增加。镁和锂的氧化物(Li2O和MgO等)促进了铝水反应的进行。研究结果[12,16]表明,铝锂共同与水反应时会生成LiAlO2和Li5Al·O4等物质,铝锂化合物的形成使得铝水反应平衡向正方向移动,提高了铝与水的反应效率。而这一结果由Li2O和Al的混合粉末热重实验得到证实。采用Li2O和Al的混合粉末(Al和Li2O的质量比为85/32)在相同的实验条件下获得了17.18%的增重,高于纯铝与水反应时的增重比例,这说明Li2O粉末促进了铝水反应。
达到1 030 ℃后,由于热重天平工作条件限制,温度无法继续升高,系统温度在1 030 ℃维持了10 min,此时反应仍在继续,样品质量仍持续增加(TG和DTG重合段)。从实验结果上来看,总的增重比例不高正是因为反应温度较低造成的。
从DTG曲线变化来看,第一增重阶段波峰最大值出现在10%Li工况,表明最大反应速度和最大增重比例并不处于相同的比例条件下,说明Mg的存在提升了金属合金与水的反应速度,而对反应效率的影响则小于Li。在有Li参加反应时,最高反应速度对应的温度点随Li含量增加而升高(726~757 ℃)。
分别比较Mg和Li对铝水反应的促进效果(0%Li和15%Li),发现Li在第一阶段增重、总增重和最高反应速率方面的提升效果均好于Mg。但反应开始前Li容易出现较高的蒸发损失现象,添加部分Mg则能减少这种蒸发损失,同时能够提高最高反应速率。另一方面,锂具有毒性且价格较高,添加少量的Mg可降低经济成本,同时能获得与Al-Li合金接近的增重比例。
表1表明,随Li含量的减少,样品的总增重比例和第一阶段失重出现下降。由于每组样品中各种金属比例不同,增重量的变化并不能代表金属反应效率。为了比较不同Li含量对促进铝水反应效果的影响,定义燃烧效率φ为样品实际放热与完全反应时理论放热的比值,计算如式(1)~式(8):
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)

Moore等[12]利用X射线检测了Al-Li合金与水反应的产物(反应温度为1 000~1 400 K),在燃烧产物中并没有检测到Li单质的存在。Mg和Li都属于较活泼的金属,因此计算时假定镁和锂已与水完全反应,从而计算参加反应的铝的总量,进而得到实际反应放热。
不同Li含量燃烧效率变化曲线见图4。图4显示,随锂含量的增加,刚开始时,铝水反应燃烧效率变化不明显;当Li的比例在5%~10%之间时,铝水反应的燃烧效率呈现明显上升的趋势;当Li含量高于10%时,此时随Li的增加,对铝水反应的促进效果变化减弱。从图4可看出,Li含量对于铝与水反应的促进效果呈现S型规律,Li含量低、Mg含量高时,对铝水反应结果几乎没有影响,而Mg含量低、Li含量高时,可大量的促进Al与水的反应(Al的反应程度从14.6%增加到52%,表示实际反应的铝和总的铝的比例,可根据式(1)、式(4)、式(5)计算得到),且当Li含量达到一定比例后,促进效果增加缓慢。从Mg含量变化的角度来看,增重效率变化表明,Mg含量的增加并不能促进该条件下Al水反应效率的提高,Li对于铝水反应的促进效果明显好于Mg。

图4 不同Li含量燃烧效率变化曲线
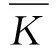

图5 第1增重阶段部分动力学参数随Li含量变化
3 结论
(1)通入水蒸气前,在410~700 ℃之间时,由于Mg和Li的蒸发导致了TG曲线上样品质量出现下降的现象,在该阶段内,Al几乎不发生蒸发。
(2)增加Li的含量,能提升总的燃烧效率,但燃烧效率的提升存在一个敏感段(5%Li到10%Li),在此阶段内,燃烧效率提升很快,而在此阶段外,燃烧效率则增加缓慢。
(3)反应动力学分析结果表明,在第1阶段合适的Al-Mg-Li比例能同时获得最高的反应速度和较高的燃烧效率。
[1]郑邯勇. 铝水推进系统的现状与发展前景[J]. 舰船科学技术, 2003, 25(5):24-25.
[2]刘冠鹏, 李凤生, 郭效德. 铝粉燃料与水反应的研究进展[J]. 固体火箭技术, 2007, 30(2):138-141.
[3]李上文, 赵凤起, 袁潮, 等. 国外固体推进剂研究与开发的趋势[J]. 固体火箭技术, 2002, 25(2):36-42.
[4]邹美帅, 杨荣杰, 郭晓燕,等. Al/H2O推进剂的研究进展[J].含能材料, 2007, 15(4):421-424.
[5]Sun Y L. Research progress on aluminum-water propulsion system[C]//44th AIAA/ASME/SAE/ASEE Joint Propulsion Conference & Exhibit, AIAA, 2008: 5038.
[6]张运刚, 庞爱民, 张文刚, 等. 金属基燃料与水反应研究现状及应用前景[J]. 固体火箭技术, 2006, 29(1):52-55.[7]慕伟意, 杜继红, 李争显, 等. 铝在高温水蒸气中表面氧化膜的性能[J]. 表面技术, 2004, 33(2): 55-57.
[8]Wang H Z, Leung D Y C, Leung M K H, et al. A review on hydrogen production using aluminum and aluminum alloys[J]. Renewable and Sustainable Energy Reviews, 2009, 13: 845-853.
[9]Dupiano P, Stamatis D, Dreizin E L. Hydrogen production by reacting water with mechanically milled composite aluminum-metal oxide powders[J]. International Journal of Hydrogen Energy, 2011, 36: 4781-4791.
[10]赵卫兵, 史小峰, 伊寅, 等. 水反应金属燃料在超高速鱼雷推进系统中的应用[J]. 火炸药学报, 2006, 29(5):53-56.
[11]Ivanov V G, Gavrilyuk O V, Glazkov O V, et al. Specific Features of the Reaction between Ultrafine Aluminum and Water in a Combustion Regime[J]. Combustion, Explosion, and Shock Waves, 2000, 36(2): 213-219.
[12]Moore J T, Turns S R, Yetter R A. Combustion of lithium-aluminum alloys[J]. Combustion Science and Technology, 2005, 177(4): 627-669.
[13]Grant A Risha, Ying Huang, Richard A Yetter, et al. Combustion of aluminum particles with steam and liquid water[J]. AIAA Journal, 2000.
[14]Gorbunov V V. Combustion of mixtures high-calorific metal powders and water[R]. Army Foreign Science and Technology Center Charlottesville Va, 1973.
[15]Richard A Yetter, Grant A Risha, Steven F son. Metal particle combustion and nanotechnology[J]. Proceeding of the Combustion Institute, 2009(32): 1819-1838.
[16]Yang Wei-juan, Liu Xiao-wei, Liu Jian-zhong, et al. Thermogravimetric analysis of hydrogen production from Al-Mg-Li particles and water[C]//6th International Conference on Hydrogen Production, 2015: 3.
[17]戴永年, 杨斌. 有色金属真空冶金(第二版)[M]. 北京: 冶金工业出版社, 2009: 8-9.
[18]张天佑, 杨卫娟, 周俊虎, 等. 水蒸气气氛下铝锂合金反应特性及动力学分析[J]. 固体火箭技术, 2015, 38(1): 79-82.
(编辑:刘红利)
Thermogravimetric analysis of the reaction of Al-Mg-Li and water at medium-high temperature
YANG Wei-juan, LIU Xiao-wei,ZHANG Tian-you, SHI Wei, LIU Jian-zhong, ZHOU Jun-hu
(State Key Laboratory of Clean Energy Utilization, Zhejiang University, Hangzhou310027,China)
To find effective methods promoting aluminum-water reaction at medium-high temperature, the combustion characteristic of Al-Mg-Li alloy (85% Al ) in water vapor from room temperature to 1 030 ℃ was studied by THERMO CAHN's Thermax500 pressurized thermogravimetric. The results show that two weight gain stages occur after water vapor feeding beginning at 700 ℃. The first stage starts from 700 ℃, the duration time and weight gain ratio were increased with the lithium content increasing, and the peak of weight gain rate appears at about 740 ℃. As for the second stage, the start temperature was raised with Li content increasing. The weight gain efficiency shows an S-shape tendency with the Li content from 0% to 15%. In the case of 11% of Li content, reaction rate as well as combustion efficiency reach at the peak.
aluminum-water reaction;magnesium;lithium;thermogravimetric analysis
2015-05-22;
2015-07-16。
杨卫娟(1976—),女,副教授,主要从事金属燃料利用、微燃烧等研究。E-mail:yangwj@zju.edu.cn
V438
A
1006-2793(2016)03-0364-05
10.7673/j.issn.1006-2793.2016.03.013
