镉-铀纳米孔洞金属-有机配位聚合物的合成、结构及光学性能研究
2016-10-14吴红燕林武滔王仁章
吴红燕,林武滔,王仁章
(三明学院 资源与化工学院,福建 三明 365004)
镉-铀纳米孔洞金属-有机配位聚合物的合成、结构及光学性能研究
吴红燕,林武滔,王仁章
(三明学院 资源与化工学院,福建 三明 365004)
利用镉金属络合物离子和芳香有机二羧酸配体与铀酰离子在水热条件下反应,合成了d-5f异金属有机配位聚合物,通过X-射线单晶衍射方法确定其晶体结构,并对其红外、紫外-可见和荧光光谱进行了经验归属。晶体结构解析表明:化合物为蜂窝状主-客体型结构的化合物,其中主体框架为蜂窝平面的网络结构,客体是八面体构型的金属络合物,紫外-可见光谱表明此化合物具有半导体性质,荧光光谱表明此化合物具有典型的铀酰离子发射峰。这些实验结果可为新型d-5f异金属有机配位聚合物的设计合成与应用提供有价值的理论与实验依据。
d-5f异金属配位聚合物;水热合成;荧光;铀酰
锕系元素杂化材料,尤其是那些由六价铀构成的材料,已经引起人们极大的兴趣,因为他们的结构多样性和功能性应用[1-2]。六价铀通常以线性铀酰离子(UO22+)存在,铀酰离子可以与有机配体配位形成铀酰有机配合物的拓展结构(一维链,二维层,三维网状结构),有机配体通常是多羧酸盐,磷酸盐,锗酸盐,砷酸盐、钼酸盐等[3-9]。在通用的桥接配体中,多羧酸如噻吩-2,5-二羧酸[10-11],对苯二甲酸[12-13],萘酚-1,4-二羧酸[14]是在组装铀酰-有机框架化合物中最常用的桥联配体。
铀酰-有机框架化合物表现出许多有趣的物理或化学特性,包括光致发光[15-17],光催化[3-4,17],光电转换[18]和非线性光学效应[19],其中可见光激发光催化行为仍处于起步阶段。过渡金属配合物因为有各种各样的电学行为已被广泛应用于生物探针、电化学和光化学领域[20]。所以如果把铀酰离子和过渡金属离子配合物同时引入一个反应体系中,一方面可以大大增加化合物结构的多样性。另一方面过渡金属有不同于铀酰离子的光、电、磁及催化性能,得到的铀酰-过渡混合金属化合物将可能产生新颖的物理化学性质。正因为这样一个充满诱惑的应用前景存在,所以在单纯的铀酰配合物合成的基础上,人们开始设计和合成铀酰-过渡混合金属配位聚合物。目前,已经有大量的磷酸铀酰[21],硼酸铀酰[22],异金属铀酰[23-24]化合物被合成出来。
本文将具有特定功能的有机配体和金属离子或金属簇按照预先设想的方式排列起来,设计出具有预期结构和功能的新化合物,从而达到设计和合成配位聚合物的目的。
1 实验部分
1.1实验主要化学试剂和仪器
化学试剂:四水合硝酸镉(Cd(NO3)2·4H2O),1,10-菲啰啉,一水(C12H8N2·H2O),噻吩-2,5-二羧酸(C6H6O4S),硝酸双氧铀(UO2(NO3)2·6H2O),水,无水乙醇,无水乙醚。
仪器:DF-101B集热式控温磁力搅拌器,DHG-9076A型真空干燥箱,TG328G型分析天平,XTS20体视变倍显微镜,SP2000型傅立叶红外光谱仪,FL900/FS920型稳态和瞬态荧光光谱仪,Lambda-800型UV/VIS光谱仪,Rigaku Weissenberg IP衍射仪,X-Ray MINIFLEX2型粉末衍射仪,SX series马弗炉。
1.2{[Cd(phen)3][(UO2)2(Tda)3](Tda)·6H2O}n(A)的合成
称取四水合硝酸镉0.0308 g(0.1 mmol)置于装有10 mL水的25 mL聚四氟乙烯內衬中,向其中加入1,10-邻菲罗啉0.0600 g(0.3 mmol),搅拌变成白色浑浊溶液,然后依次加入六水合硝酸双氧铀0.1078 g(0.2 mmol),噻吩-2,5-二羧酸0.0688 g(0.4 mmol),常温搅拌半小时后将其置于不锈钢套中,程序控温过程如下:常温下经300min加热升温至160℃,恒温4 d,然后经2 d降到常温。产品用水、无水乙醇、无水乙醚分别洗涤3次,室温下真空干燥,得到红色块状晶体0.0732 g。产率为37.1%(以UO2(NO3)2·6H2O计算)。
2 结果与分析
2.1化合物{[Cd(phen)3][(UO2)2(Tda)3](Tda)·6H2O}n(A)结构解析
化合物A(CCDC号为886784)属于三斜晶系,P-1空间群,其晶体学数据见表1。重要的键长、键角值见表2。化合物A在晶体学上含有99个独立的非氢原子,其中2个U原子,1个Cd原子,4 个S原子,60个C原子,6个N原子和26个O原子。

表1 化合物A的晶体学数据

续表1
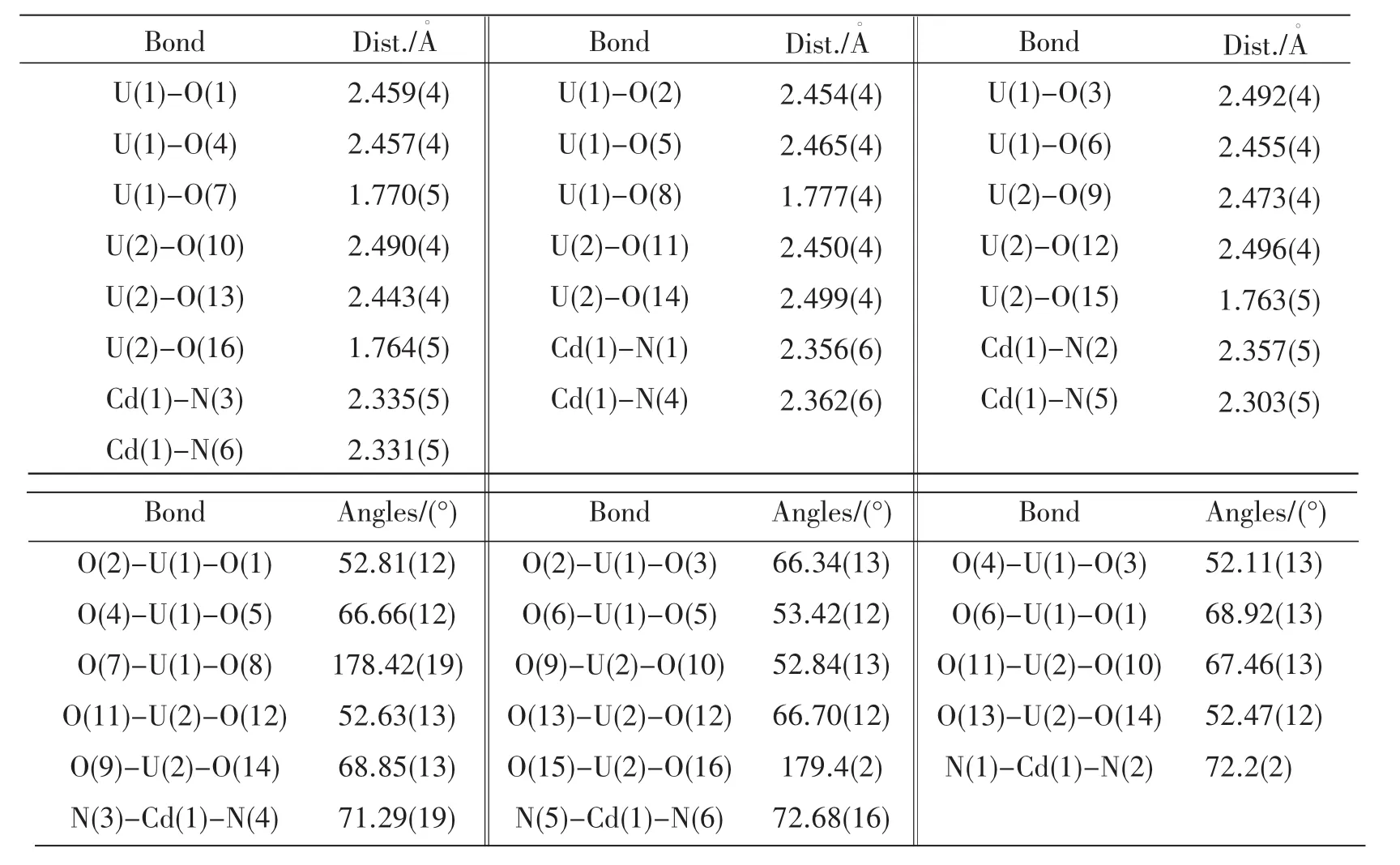
表2 化合物A重要的键长、键角值
晶体结构解析结果表明:化合物A整个结构由金属配合物阳离子、2-D聚阴离子、一个Tda分子以及6个游离的H2O分子组成。
化合物A聚阴离子主体框架主要由相邻的铀酰离子通过与噻吩-2,5-二羧酸桥连,形成由6个铀酰和6个噻吩-2,5-二羧酸构成的六边形蜂窝孔结构,孔洞直径为10.87~16.03(图2),从图3可以看出,这个形成六边形结构并不是平面型的,而是采用了169.18°弯角的椅式构象。
在化合物A中,主体框架层之间没有相互作用,但是主体框架层与金属配合物阳离子客体之间不仅存在静电引力作用,而且还存在氢键作用。即两个金属配合物上的氢能分别与相邻主体框架层上的羧基氧形成氢键。具体是无机阳离子簇[Cd(phen)3]2+中的H37与主体框架层中的O6间形成一个独立的C-H···O分子内氢键(图4)。而无机阳离子簇[Cd(phen)3]2+中的H26和另一层主体框架中的O7之间形成分子间氢键作用(图5)。整个化合物就是通过镉金属配合物客体上的不同氢原子分别与相邻层的氧形成氢键(表3)结合为3-D蜂窝状结构的主-客体化合物(图6)
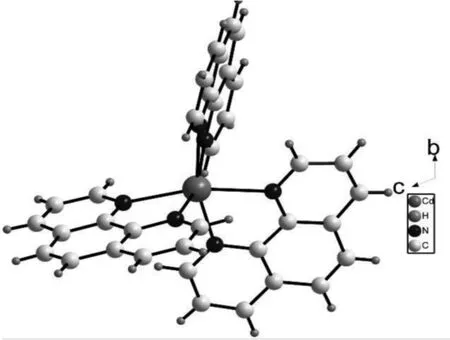
图1 化合物中的无机阳离子簇
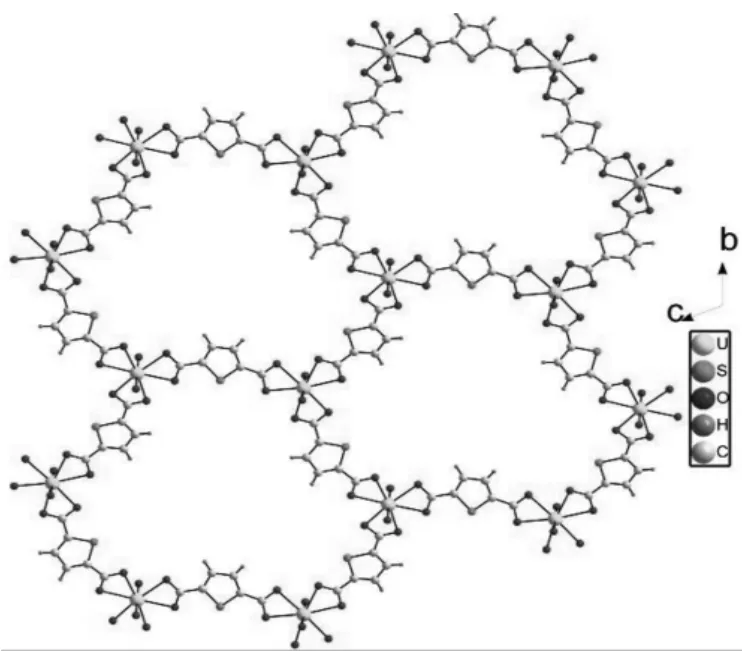
图2 化合物中蜂窝平面主体框架在ab面的结构图
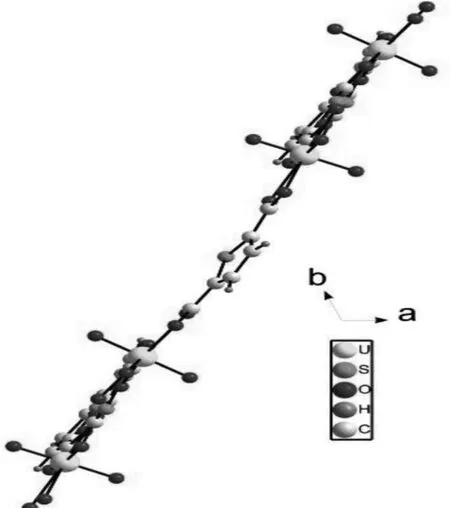
图3 化合物中的阴离子
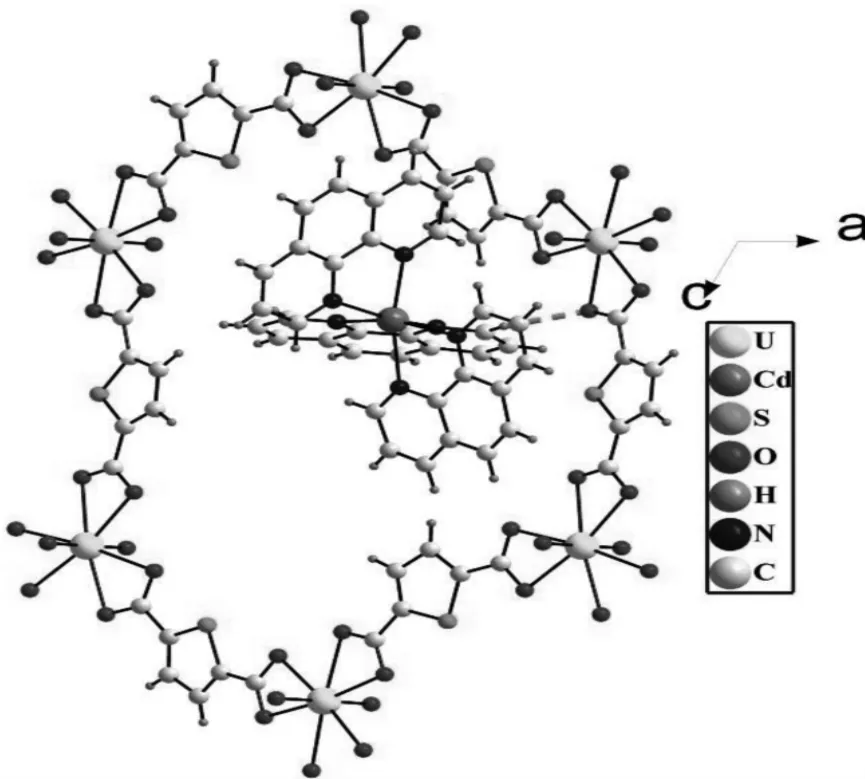
图4 化合物A中阴阳离子通过分子内氢键作用图
表3 化合物A中的氢键作用(长度用键角用(°)表示

表3 化合物A中的氢键作用(长度用键角用(°)表示
D-H C(26)--H(26)C(37)--H(37)d(D-H)0.93 0.93 d(H···A)2.49 2.44 ∠DHA 125 138 d(D···A)3.1143 3.1949 A O(7)O(6)
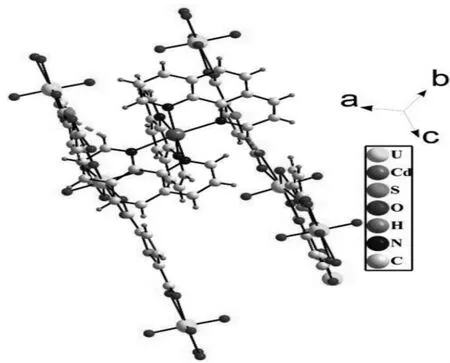
图5 化合物A中阴阳离子通过分子间氢键作用图

图6 化合物A中阴阳离子通过氢键作用形成3-D结构投影图
2.2化合物的红外光谱
使用样品与KBr混合压片的方法,对该化合物进行红外光谱表征,获得了化合物A的红外光谱,如图7所示。这个化合物的特点是3350 cm-1处的吸收峰对应于结构中水分子的伸缩振动;在3094,1103,820以及770 cm-1的吸收峰对应芳环上C-H面内弯曲振动和面外弯曲振动;在1396 cm-1以及1523cm-1的吸收峰对应羧基的对称和反对称伸缩振动;在927 cm-1有明显的强吸收峰,对应于化合物中铀酰基团O= U=O的特征反对称伸缩振动;在 724 cm-1出现吸收峰对应于化合物中C-S-C伸缩振动,在482 cm-1出现吸收峰对应于化合物中Cd-N伸缩振动,这与单晶X射线衍射分析的结果一致。
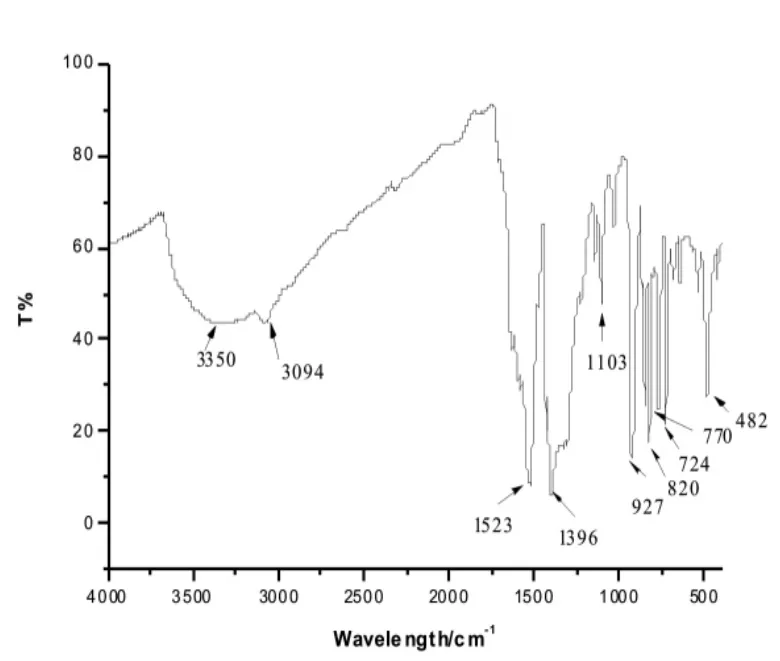
图7 化合物A的红外振动吸收图
2.3化合物的UV-Vis谱和吸收谱
图8(a)为化合物A的紫外-可见光谱图,图8(b)为化合物A转化后的吸收光谱图。化合物A在264、303、405、453 nm处有吸收峰,其中264、303 nm处的吸收峰可归属为Cd与菲啰啉配位形成的Cd→N的荷移跃迁或菲啰啉的π—π*电子跃迁,405 nm处的吸收峰归属为铀酰基团的电子吸收,453 nm处可归属为U(VI)中心的空轨道与配体之间的LMCT跃迁。由转换谱图8(b)可以看到,化合物A的吸收边为3.35 eV,表明此化合物具有半导体性质。
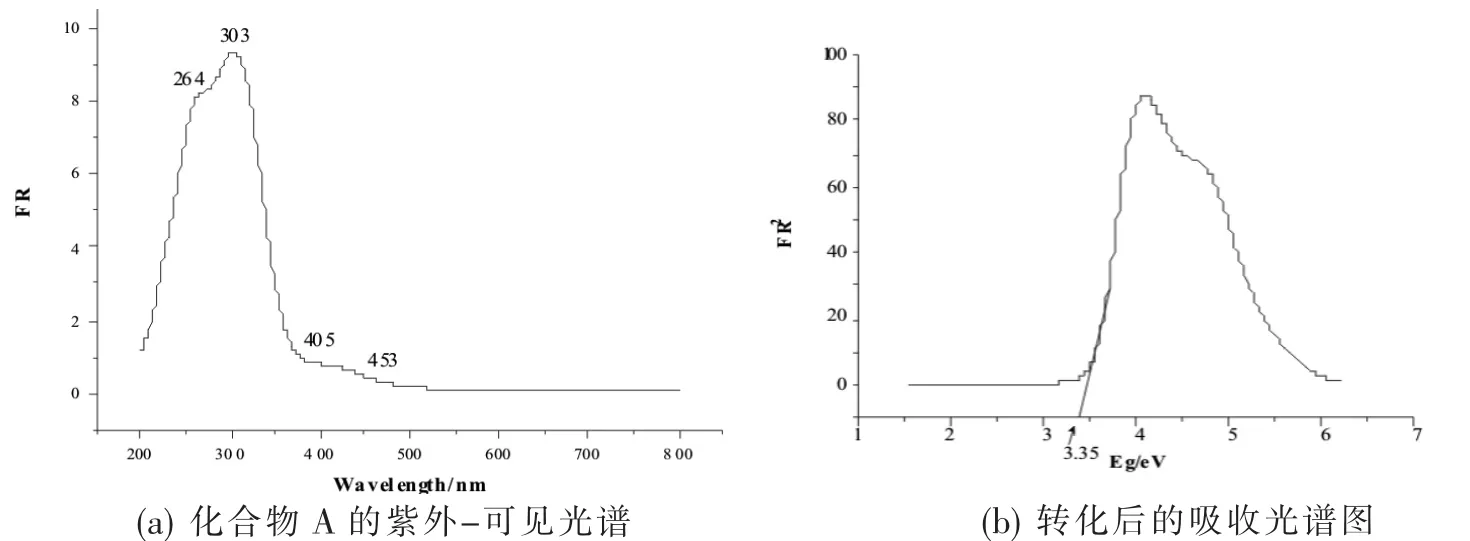
图8 化合物A的紫外-可见光谱图和转化后的吸收光谱图
2.4化合物的固体荧光光谱
图9是化合物A的荧光光谱,激发谱 374,482,542 nm处有3个峰,分别用这3个波长作激发波长,得到的发射谱在380到600 nm表现6个发射峰,分别为在380、480、498、519、540、596nm处的峰。380 nm归属为菲啰啉到镉的L→M的跃迁。480 nm处的发射峰归属为铀酰离子的三线态到单线态电荷转移。498、519、540、596 nm 4个发射峰归属为电子从第一激发到基态的跃迁。

图9 化合物A的固体荧光光谱图
3 结论
选择镉金属络合物离子和芳香有机二羧酸配体与铀酰离子在水热条件下反应,合成了d-5f纳米孔洞异金属有机配位聚合物,此化合物新颖的结构特点对进一步了解铀酰配合物的配位方式,具有一定的指导意义。紫外-可见光谱表明此化合物具有半导体性质,荧光光谱表明此化合物具有典型的铀酰离子发射峰。这些结果表明此化合物具有潜在的应用价值。
[1]ANDREWS M B,CAHILL C L.Uranyl bearing hybrid materials synthesis,speciation,and solid-state structures[J]. Chem Rev,2013,113:1121-1136.
[2]SADAKIYO M,YAMADA T,KITAGAWA H.Rational designs for highly proton-conductive metal-organic frameworks[J].Journal of the American Chemical Society,2009,131:9906-9907.
[3]YU Z T,LIAO Z L,JIANG Y S,et al.Water-insoluble Ag-U-organic assemblies with photocatalytic activity[J]. Eur J,2005(11):2642-2650.
[4]LIAO Z L,LI G D,BI M H,et al.Preparation,structures,and photocatalytic properties of three new uranyl-organic assembly compounds[J].Inorg Chem,2008,47:4844-4853.
[5]LIN C H,LII K H.A3(U2O4)(Ge2O7)(A=Rb,Cs):mixed-valence uranium(V,VI)germanates[J].Angew Chem Int Ed,2008,47:8711-8713.
[6]CHEN C S,LEE S F,LII K H.K(UO)Si2O6:A pentavalent uranium silicate[J].J Am Chem Soc,2005,127:12208-12209.
[7]MIHALCEA I,HENRY N,VOLKRINGER C,et al.Uranyl-pyromellitate coordination polymers:toward threedimensional open frameworks with large channel systems[J].Cryst Growth Des,2012,12(1):526-535.
[8]THANGAVELU S G,ANDREWS M B,POPE S J A,et al.Synthesis,structures,and luminescent properties of uranyl terpyridine aromatic carboxylate coordination polymers[J].Inorg Chem,2013,52(4):2060-2069.
[9]THUERY P.Sulfonate complexes of actinide ions:structural diversity in uranyl complexes with 2-sulfobenzoate[J]. Inorg Chem,2013,52:435-447.
[10]HUANG W,WU D,ZHOU P,et al.Luminescent and magnetic properties of lanthanide-thiophene-2,5-dicarboxylate hybrid materials[J].Cryst Growth Des,2009,9(3):1361-1369.
[11]SUN Y G,JIANG B,CUI T F,et al.Solvothermal synthesis,crystal structure,and properties of lanthanide-organic frameworks based on thiophene-2,5-dicarboxylic acid[J].Dalton Trans,2011,40:11581-11590.
[12]REINEKE T M,EDDAOUDIM,FEHR M,et al.From condensed lanthanide coordination solids to microporous frameworks having accessible metal sites[J].J Am Chem Soc,1999,121(8):1651-1657.
[13]DAIGUEBONNE C,KERBELLEC N,GUILLOU O,et al.Structural and luminescent properties of micro-and nanosized particles of lanthanide terephthalate coordination polymers[J].Inorg Chem,2008,47:3700-3708.
[14]YANG J,YUE Q,LI G D,et al.Structures,photoluminescence,up-conversion,and magnetism of 2D and 3D rareearth coordination polymers with multicarboxylate linkages[J].Inorg Chem,2006,45:2857-2865.
[15]MIHALCEA I,HENRY N,BOUSQUET T,et al.Six-fold coordinated uranyl cations in extended coordination polymers[J].Cryst Growth Des,2012,12:4641-4648.
[16]SONIA G,THANGAVELU,SIMON J A.Pope and christopher l cahill synthetic,structural,and luminescence study of uranyl coordination polymers containing chelatingterpyridineandtrispyridyltriazineligands[J].CrystEngComm,2015,17:6236-6247.
[17]YANG WEITING,TIAN WAN GUO,LIU XIAO XIAO,et al.Syntheses,structures,luminescence,and photocatalytic properties of a series of uranyl coordination polymers[J].Cryst Growth Des,2014,14(11):5904-5911.
[18]CHEN W,YUAN H M,WANG J Y,et al.Synthesis,structure,and photoelectronic effects of a uranium zinc organic coordination polymer containing infinite metal oxide sheets[J].J Am Chem Soc,2003,125(31):9266-9267.
[19]WANG YAN LONG,LI YUXIANG,BAI ZHUANLING.Design and synthesis of a chiral uranium-based microporous metalorganicframeworkwithhighSHGefficiencyandsequestrationpotentialforlow-valentactinides[J].DaltonTrans,2015,44:18810-18814.
[20]FERNA NDEZ MOREIRA V,THORP GREENWOOD F L,COOGAN M P.Application of d6transition metal complexes in fluorescence cell imaging[J].Chem Commun,2010,46:186-202.
[21]DANIEL GROHOL,ABRAHAM CLEARFIELD.Solid-State water-catalyzed transformation at room temperature of a nonluminescent linear-chain uranyl phenylphosphonate into a luminescent one[J].J Am Chem Soc,1997,119(20):4662-4668.
[22]WANG SHUAO,EVGENY V,ALEKSEEV,et al.Crystal chemistry of the potassium and rubidium uranyl borate families derived from boric acid fluxes[J].Inorg Chem,2010,49:6690-6696.
[23]PIUS O,THOMAS E,ALBRECHT SCHMITT.Heterobimetallic copper(II)uranyl carboxyphenylphosphonates[J]. Cryst Growth Des,2011(11):4676-4683.
[24]PIERRE THU RY.Two uranyl-organic frameworks with pyridinecarboxylate ligands,a novel heterometallic uranyl -copper(II)complex with a cation-cation interaction[J].Inorganic Chemistry Communications,2009,12:800-803.
(责任编辑:朱联九)
Synthesis,Structure and Optical Properties Research of Cadmium-Uranium Nano Holes of Metal-Organic Coordination Polymer
WU Hong-yan,LIN Wu-tao,WANG Ren-zhang
(School of Resource and Chemical Engineering,Sanming University,Sanming 365004,China)
Based on the reaction of Cadmium metallic complexes ions,aromatic organic dicarboxylic acid and uranyl ions under hydrothermal conditions,heterometallic organic coordination polymers was obtained and its crystal structure was determined by X-ray single crystal diffraction method.The empirical assignments of infrared,ultraviolet-visible and fluorescence spectra of these coordination polymers were given.Crystal structure analysis shows that it is host-guest type structure of the compound;the main framework is honeycomb-like flat network structure;the object is octahedral configuration of metal complexes;Uv-vis spectra shows that the compound has semiconductor properties;fluorescence spectrum indicates that this compound has a typical emission peak of uranyl ion.The results of these experiments will provide valuable theoretical and experimental basis for the synthesis and application of new d-5f heterometallic-organic coordination polymers.
d-5f heterometallic coordination polymers;hydrothermal synthesis;fluorescence;uranyl
O631
A
1673-4343(2016)02-0014-07
10.14098/j.cn35-1288/z.2016.02.004
2015-12-08
三明学院科学研究发展基金项目(B201406/Q);福建省中青年教师教育科研项目(JA15480)
吴红燕,女,江西东乡人,助理实验师。主要研究方向:有机功能材料。
