全直肠系膜切除术对低位直肠癌患者局部复发率及生活质量的影响
2016-09-23王建军
王建军
临床与基础研究
全直肠系膜切除术对低位直肠癌患者局部复发率及生活质量的影响
王建军
目的探讨全直肠系膜切除手术(total mesorectal excision,TME)对直肠癌患者近远期疗效及生存质量的影响。方法选取2008年1月至2011年12月期间徐州市贾汪区人民医院收治的低位直肠癌患者为研究对象,根据术式分为TME组60例及传统手术组66例。随访5年,对比分析两组患者近远期疗效及生存质量。结果两组手术时间差异无统计学意义(P>0.05),TEM组术中出血量住院时间、总并发症发生率均低于传统手术组,差异有统计学意义(均P<0.05)。两组1、3年复发率及1、3年生存率相比差异均无统计学意义(均P>0.05),而5年局部复发率及5年生存率相比,差异均有统计学意义(均P<0.05)。结论TME手术能提高直肠癌患者治疗效果,降低患者局部复发率,提高患者生存率及生存质量。
直肠肿瘤;全直肠系膜切除术;复发率;生存率;
直肠癌(rectal cancer,RC)是危害人类健康的常见的恶性肿瘤之一,发病率位于恶性肿瘤的第5位,占成年人恶性肿瘤的5%。欧洲每年约有200 000直肠癌新发病例。我国结直肠癌的发病率约为3.1/10万~10.7/10万,直肠癌所占比例约为70%,估计每年直肠癌的新发病例约10万。其中,中低位直肠癌的比例在70%~80%[1]。目前临床上较为常用的低位直肠癌根治手术是miles手术(即造口手术治疗),造口手术虽然挽救了患者,但此种术式对患者生理影响较大,且复发率高[2]。局部复发通常是无法治愈的,并常引起全身性转移。为此,我们对本院低位直肠癌患者应用全直肠系膜切除术(total mesorectal excision,TME)及传统手术治疗,术后对患者随访5年,观察不同手术方法对患者生存状况的影响,旨在为临床结直肠癌治疗提供指导。
1 资料及方法
1.1临床资料选取2008年1月至2011年12月期间本院收治的低位直肠癌患者为研究对象,所有患者经肠镜及病理学确诊;排除肝肾功能不全者,两处以上肿瘤者,姑息性切除者,联合盆腔脏器切除者,共110例入组。根据患者术式分为TME组60例及传统手术组50例。TME组:男34例,女26例,年龄34~80岁,平均(57.6±4.9)岁;肿瘤直径1.5~10.6 cm,平均(6.8±1.9) cm;病理类型:低分化腺癌28例,中分化腺癌19例,高分化腺癌11例,黏液腺癌2例;Dukes分期:A期18例,B期21例,C期21例,其中淋巴结转移19例。传统手术组:男28例,女22例,患者年龄36~79岁,平均年龄为(56.8±5.4)岁。肿瘤直径1.3~11.6 cm,平均(6.7±1.5)cm;病理类型:低分化腺癌24例,中分化腺癌15例,高分化腺癌10例,黏液腺癌1例;Dukes分期:A期14例,B期19例,C期17例,其中淋巴结转移16例。两组患者性别、年龄、肿瘤直径、病理类型、Dukes分期、淋巴结转移比较差异无统计学意义(P>0.05),具有可比性。
1.2手术方法两组患者均全麻进行手术,传统手术组常规开腹探查,判断肿瘤情况,钝性分离直肠,在距离肿瘤大约2 cm处部位将直肠系膜进行切除。TME组开腹探查后游离乙状结肠,在肠系膜下动脉根部无神经区游离出肠系膜下动脉,保留腹主动脉神经丛。在分离直肠系膜时保留上腹下丛和腹下神经丛,同时在处理直肠侧韧带时,注意保留下腹神经丛和盆内神经丛。距脾静脉及主动脉间1 cm处将肠系膜下动静脉结扎,对肠系膜淋巴与血管周围部位进行清扫。随后采用电刀或剪刀沿着壁层筋膜、盆腔脏层间筋膜切断,并将病灶及其周围系膜完全切除,保持脏层筋膜完整性。强调环绕剥离直肠系膜,对患者的腹下神经、盆内神经进行保护。肿瘤远端的直肠系膜切除应达5 cm,以免系膜脏层受损,出现癌细胞扩散现象或残留现象。如肿瘤切除后,切线与齿状线距离超过2 cm,可行保肛手术。若无法保肛,则需行单吻合器左下腹结肠造瘘。
1.3随访方法通过电话或门诊的方式对患者进行随访。随访以患者出院为起点,5年或患者死亡为终点。
1.4统计学分析采用SPSS16.0统计软件进行数据分析,计量资料采用均数±标准差表示,组间采用t检验,计数资料采用率表示,组间比较采用χ2或确切概率法检验,P<0.05为差异有统计学意义。
2 结果
2.1两组患者临床效果分析两组手术时间差异无统计学意义(P>0.05),TME组术中出血量、住院时间、总并发症发生率均低于传统手术组,差异有统计学意义(均P<0.05)(表1)。

表1 两组患者术中出血量、手术时间、住院时间及术后并发症的比较
2.2两组远期治疗效果分析随访过程中,两组术后1、3年复发率及1、3年生存率相比差异均无统计学意义(P>0.05),而5年局部复发率及5年生存率相比,差异均有统计学意义(P<0.05)(表2,表3)。
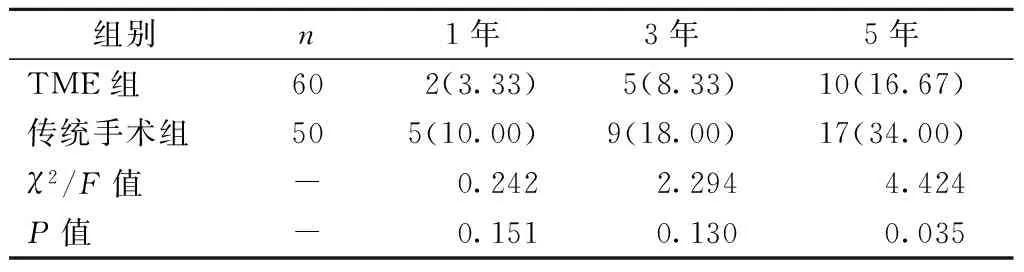
表2 两组术后1、3、5年复发率对比[例(%)]

表3 两组术后1、3、5年生存率对比[例(%)]
3 讨论
直肠系膜是一个由疏松结缔组织构成的独立结构,富含淋巴、血管组织,外表覆盖一层盆腔筋膜,其位于直肠的后方,从直肠两侧及后方三个方向包绕直肠,并在侧方与环绕血管和腹下丛的结缔组织及“侧韧带”融合。直肠和直肠系膜被盆腔筋膜的脏层包裹,直肠癌的局部播散一般不超过此范围。而直肠系膜内即使无淋巴结转移存在也隐藏着癌细胞巢[3]。直肠系膜的播散比腔内播散危害性更大,若不完全切除直肠系膜术后易于局部复发[4]。
传统手术治疗低位直肠癌的操作是钝性分离肠系膜后切除肿瘤。这种方式容易引起直肠固有筋膜的撕裂,从而引起肿瘤细胞脱落、转移[5]。再者直肠系膜切断水平与肿瘤远端肠壁的切断水平在同一平面,肿瘤细胞可能残留于未被切除的直肠系膜中,增加了局部复发风险。本组随访中,传统手术组第5年肿瘤的局部复发率高于TME组,差异有统计学意义(P<0.05)。
TME以人体的胚胎发育过程为手术的解剖基础[6],TME要求[7]:(1)直视下直肠周围间隙锐性分离;(2)保持盆筋膜脏层的完整性;(3)肿瘤远端直肠系膜的切除不少于5 cm。确切地讲TME并非是一种术式,而是直肠中、下段癌所应当遵循的一项原则。沿胚胎发育的先天层面锐性分离,精细解剖,将直肠癌及其相关转移病灶、局部浸润组织完全切除,保证包裹肿瘤系膜的完整性,有效避免了结肠系膜破裂造成的肿瘤播散,从而达到根治肿瘤的目的[8-9]。TME强调保留腹主动脉神经丛、上腹下丛和腹下神经丛、下腹神经丛和盆内神经丛,术后能很好地保留患者排尿及性功能,提高了患者生存质量,这也是TME的优势[10]。相较于传统根治术,TME更加准确、精细,有效避免了手术部位以外脏器受到不必要的干扰,从而在很大程度上降低了吻合口水肿、吻合口瘘、切口处腹腔粘连和肠梗阻等并发症的发生[8],有利于患者的康复。王红军[11]总结了92例中低位直肠癌患者应用全直肠系膜切除联合单吻合器技术,结果术后吻合口瘘发生率仅1.1%,全部患者1年后肛门控便、排便功能接近正常,3年局部复发率4.4%。本研究显示,TME组患者术中出血量、术后并发症发生率及住院时间均优于传统手术组,差异有统计学意义(P<0.05)。
TME出血量少、恢复快、并发症少,局部复发率低,能大大提高患者的生存率,值得临床推广应用。
[1]彭开勤.努力降低直肠癌术后复发率[J].腹部外科,2014,27(4):233-235.
[2]MAURER C A, RENZULLI P, Kull C, et al. The impact of the introduction of total mesorectal excision on local recurrence rate and survival in rectal cancer: long-term results[J]. Ann Surg Oncol, 2011, 18(7): 1899-1906.
[3]MACFARLANE J K, RYALL R D, HEALD R J. Mesorectal excision for rectal cancer [J].Lancet, 1993,341(8843):457-460.
[4]姚君良,唐建伟,顾超.腹腔镜下全直肠系膜切除术治疗低位直肠癌的疗效分析[J].中国临床医学,2013,20(2):143-144.
[5]BUCHS N C, NICHOLSON G A, RIS F, et al. Transanal total mesorectal excision: A valid option for rectal cancer[J]. World J Gastroenterol, 2015, 21(41):11700-11708.
[6]WU Y, WU Y Y, LI S, et al. TEM and conventional rectal surgery for T1 rectal cancer: a meta-analysis[J]. Hepatogastroenterology, 2011, 58(106):364-368.
[7]LU J Y, LIN G L, QIU H Z, et al. Comparison of Transanal Endoscopic Microsurgery and Total Mesorectal Excision in the Treatment of T1 Rectal Cancer: A Meta-Analysis[J]. PLVS One, 2015, 10(10):e0141427.
[8]PALMA P, HORISBERGER K, Joos A, et al. Local excision of early rectal cancer: is transanal endoscopic microsurgery an alternative to radical surgery[J]. Rev Esp Enferm Dig, 2009, 101(3):172-178.
[9]ZIEREN J, PAUL M, MENENAKOS C. Transanal endoscopic microsurgery (TEM) vs. radical surgery (RS) in the treatment of rectal cancer: indications, limitations, prospectives. A review[J]. Acta Gastroenterol Belg, 2007, 70(4):374-380.
[10]LEE D K, JO M K, SONG K, et al. Voiding and sexual function after autonomic-nerve-preserving surgery for rectal cancer in disease-free male patients [J] . Korean J Urol, 2010, 51(12):858-862.
[11]王红军.单吻合器在低位直肠癌保肛术中应用的临床研究[J].中国肿瘤外科杂志,2011,3(5):257-259.
221011江苏徐州,徐州市贾汪区人民医院普外科
/
王建军,男,副主任医师,研究方向:普外科临床诊治及科研工作,E-mail:tougao136@163.com
10.3969/j.issn.1674-4136.2016.03.012
1674-4136(2016)03-0188-03
2016-01-01][本文编辑:李庆]
