雷迪帕韦-索非布韦治疗丙肝肝硬化的疗效与安全性研究
2016-09-22龙云铸谭英征李丹赵斌傅金球周青傅京力赵韵华
龙云铸 谭英征 李丹 赵斌 傅金球 周青 傅京力 赵韵华
雷迪帕韦-索非布韦治疗丙肝肝硬化的疗效与安全性研究
龙云铸谭英征李丹赵斌傅金球周青傅京力赵韵华
目的探究雷迪帕韦(Ledipasvir)-索非布韦(Sofosbuvir)治疗丙肝肝硬化的疗效与安全性。方法选择株洲市中心医院自购药物治疗的80例株洲市丙型肝硬化患者,HCV-RNA水平≥80 IU/mL,肝硬化Child-Pugh分级属于A级,将患者分为肝硬化代偿期组和肝硬化失代偿期组,给与雷迪帕韦-索非布韦治疗,定量分析患者血清中HCV-RNA水平,检测患者病毒学应答情况。分析肝纤维化标志物水平,记录治疗过程中出现不良反应情况。结果接受雷迪帕韦-索非布韦治疗后肝硬化代偿期组和肝硬化失代偿期组有效率均为100%,其中肝硬化代偿期组HCV-RNA转阴率(71.05%)高于肝硬化失代偿期组(66.67%),代偿期组和肝硬化失代偿期组EVR、ETVR和SVR均发生改变,比例均高于85%,治疗后两组PC III和HA水平均显著低于治疗前。治疗后两组患者中出现不良反应的概率分别为4.76%和7.89%,包括2例疲乏,1例头痛,1例恶心和1例腹泻。结论雷迪帕韦-索非布韦治疗丙肝肝硬化具有更好的疗效,且安全性较高。
索非布韦;雷迪帕韦;联合用药;丙肝肝硬化;慢性丙型肝炎病毒治疗
慢性丙型肝炎病毒(Hepatitis C virus,HCV)感染是全球性的公共卫生问题,HCV患者极易发生肝硬化甚至肝癌,造成患者生存率降低,预后较差[1]。目前临床中治疗慢性丙型肝炎(chronic hepatitis C,CHC)的标准疗法是聚乙二醇干扰素(pegylated interferon,Peg-IFN)联合利巴韦林(ribavirin,RBV)注射治疗,但是皮下注射干扰素可导致患者产生多种不良反应,且不便于临床处理,目前已被禁止用于肝硬化治疗[2]。2014年10月10日美国食品药品监督管理局(Food and Drug Administration,FDA)批准了美国吉利德Gilead公司的药品雷迪帕韦-索非布韦(Ledipasvir and Sofosbuvir,商品名Harvoni片剂)上市,在临床Ⅲ期试验中,本药品对于治疗基因1型慢性丙型肝炎HCV成年患者具有良好的治疗效果[3],本文中主要研究其治疗丙肝肝硬化的疗效与安全性。
材料与方法
一、一般资料
选择2015年3月至2015年9月我院自购药物治疗的80例株洲市丙型肝炎肝硬化患者,诊断符合中华医学会肝病学分会及传染病与寄生虫病学分会2004年修订的《丙型肝炎防治指南》[4]诊断标准,其中男性44例,女性36例,年龄18 ~63岁,平均(36.74±13.03)岁,病程5~22年。所有患者血清HCV抗体阳性>6个月且HCV-RNA水平≥80 IU/mL,病毒分型均为基因1型,肝硬化Child-Pugh分级属于A级为肝硬化代偿期组,肝硬化Child-Pugh分级属于B、C级为肝硬化失代偿期组,其他并发病控制良好至少3个月以上。其中肝硬化代偿期患者38例,其中男性22例,女性16例,年龄18~60岁,平均(33.49±15.61)岁,病程7~22年。肝硬化失代偿期患者42例,其中男性22例,女性20例,年龄20 ~63岁,平均(33.99±13.86)岁,病程5~21年。排除其他肝炎病毒重叠感染、重症肝炎、自身免疫性肝病、药物性肝炎、寄生虫肝病、酒精性肝病等患者。
结果
一、两组HCV-RNA改变情况
通过分析HCV-RNA水平发现,接受雷迪帕韦-索非布韦治疗后第4周肝硬化代偿期组和失代偿期组的HCVRNA转阴率分别为71.05%和66.67%,接受治疗后第12周HCV-RNA转阴率分别为84.21%和85.71%,接受治疗后第24周HCV-RNA转阴率均为100%,见表1。

表1 两组HCV-RNA转阴情况比较[n(%)]
二、两组病毒学应答情况的变化
通过分析两组病毒学应答情况,发现雷迪帕韦-索非布韦治疗可以促进肝硬化代偿期组EVR(86.84%)、ETVR (100%)和SVR(94.74%)和肝硬化失代偿期组的EVR (100%)、ETVR(95.24%)和SVR(90.48%)的改善情况,随着治疗结束,两组患者均出现病毒学应答减弱情况,见表2。
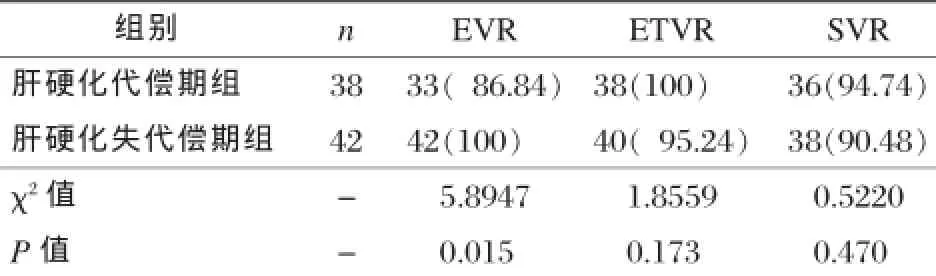
表2 两组病毒学应答情况比较[n(%)]
三、两组肝纤维化标志物的变化
通过比较血清中Ⅲ型前胶原(PCⅢ)和透明质酸(HA)发现,治疗前肝硬化失代偿期组和肝硬化代偿期组的PCⅢ和HA水平无显著差异,治疗后PCⅢ和HA水平均显著低于治疗前。并且肝硬化失代偿期组治疗后PCⅢ和HA水平显著低于肝硬化代偿期组(P<0.001),见表3。
四、两组出现不良反应情况
肝硬化失代偿期组出现不良反应的概率为4.76%,包括1例疲乏和1例头痛。肝硬化代偿期组出现不良反应的概率为7.89%,包括1例疲乏,1例恶心和1例腹泻。两组不良反应发生率无明显差异(P>0.05),见表4。
讨论
表3 两组肝纤维化标志物的变化(±s,μg/L)

表3 两组肝纤维化标志物的变化(±s,μg/L)
注:*与治疗前相比,P<0.001,#与肝硬化代偿期组相比,P<0.001。
组别nPCⅢt值P值HAt值P值治疗前治疗后治疗前治疗后肝硬化代偿期组38105.3±5.649.8±3.7*50.97<0.001327.9±44.8141.6±23.1*22.78<0.001肝硬化失代偿期组42107.5±3.932.4±3.6*#91.70<0.001324.6±37.494.7±8.5*#38.85<0.001 t值-1.120821.27--0.558812.35--P值-0.2658<0.001--0.7207<0.001--
丙型病毒肝炎是严重危害患者的健康和生命的疾病,我国HCV感染率高达3%,其中约1/3的患者可能恶化发展为肝硬化甚至肝癌。发生肝硬化的患者中,每年将有3%~5%患者癌变,即使是代偿期患者,每年有10%的患者肝功能恶化为失代偿,10年内死亡率高达80%[6]。
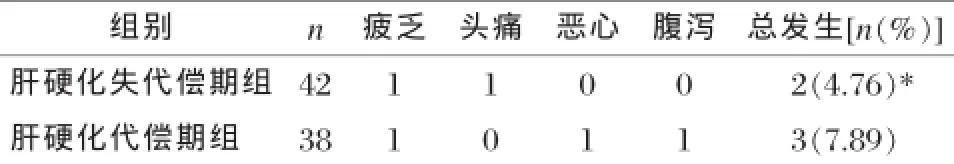
表4 两组不良反应情况比较(n)
HCV感染肝细胞后,依赖HCV特异性NS5B聚合酶产生子代RNA,在宿主细胞内扩增,而HCV蛋白则被HCV特异性的NS5A蛋白酶剪切并活化[7]。因副作用太大,标准的治疗方案干扰素+利巴韦林是禁用的,而双环醇加病毒唑疗法的疗效则不够理想,因此丙肝肝硬化患者迫切需要得到积极安全有效的治疗,新型抗丙肝病毒治疗的药物也亟需研究[8]。目前针对丙肝病毒治疗的靶点主要存在于丙肝病毒RNA的非结构蛋白编码区域,在丙肝病毒复制过程中,N3解旋酶、NS5A和NS5B发挥重要作用,因此目前治疗药物主要是通过抑制这三种酶的活性达到抗病毒效果。
2014年10月10日,美国FDA批准的吉利德Gilead公司的Harvoni片剂上市用于成年患者治疗基因1型慢性丙型肝炎HCV,其主要成分是索非布韦(Sofosbuvir)和雷迪帕韦(Ledipasvir)。其中索菲布韦已经被多次应用于临床治疗丙型肝炎,它是一种核苷聚合酶抑制剂,口服制剂,可有效避免皮下注射引发的不良反应如皮疹等。研究发现索菲布韦可以用于治疗慢性丙型肝炎,联合利巴韦林治疗时可有效缓解HCV基因型1、2、3型患者症状[9]。雷迪帕韦是针对HCV特异性NS5A蛋白酶的抑制剂,旨在通过抑制HCV蛋白的活化治疗慢性丙型肝炎[10]。但是在美国,索非布韦联合雷迪帕韦治疗的费用高达16.8万美元。2015年3月吉立德公司授权的仿制品开始销售,Sovaldi的药价已经开始暴跌。在东南亚国家的价格相当于12周疗程900美元,与将要上市的获得吉列德授权的印度仿制药的计划定价相同。一些印度大型仿制药公司与吉列德签署了授权协议,吉列德允许他们在91个最穷国家销售低价的Sovaldi仿制药,但中国不在此列。然而“格列卫”事件为国内患者提供了转机,株洲市的丙肝肝硬化患者通过多种渠道,从印度等东南亚国家购得该药。因此本文中主要研究2015年3月至2015年9月自购药物治疗的丙型肝硬化患者的治疗疗效。
通过分析HCV-RNA水平发现,接受雷迪帕韦-索非布韦治疗后24周肝硬化代偿期组和肝硬化失代偿期组HCVRNA转阴率均可达到100%,说明索非布韦-雷迪帕韦治疗可以更有效的抑制HCV的复制,可以用于治疗不同时期的肝硬化,且对肝硬化代偿期患者疗效更好。进而我们分析了两组患者病毒学应答情况,发现肝硬化代偿期组和肝硬化失代偿期组EVR、ETVR和SVR均发生改变,比例均高于85%,持续的病毒学应答减弱就意味着临床治愈,因此这个结果进一步说明雷迪帕韦-索非布韦治疗可以更有效的抑制HCV病毒的活力。此外,雷迪帕韦-索非布韦治疗对肝硬化代偿期组(86.84%)和肝硬化失代偿期组(100%)早期病毒学应答的疗效具有显著性差异(P<0.05),有助于临床中对肝硬化患者进行较好的分型治疗。肝硬化过程中伴随着严重的组织纤维化过程,血清中Ⅲ型胶原增加而Ⅱ型胶原减少。本文中通过比较血清中Ⅲ型前胶原(PCⅢ)和透明质酸(HA)发现,治疗前肝硬化失代偿期组和肝硬化代偿期组的PCⅢ和HA水平无显著差异,治疗后PCⅢ和HA水平均显著低于治疗前,说明雷迪帕韦-索非布韦治疗可以缓解丙肝肝硬化情况。通过统计两组患者中出现不良反应的情况发现雷迪帕韦-索非布韦治疗肝硬化失代偿期组出现不良反应的概率为4.76%,包括1例疲乏和1例头痛。肝硬化代偿期组出现不良反应的概率为7.89%,包括1例疲乏,1例恶心和1例腹泻。不良反应概率较低,因此雷迪帕韦-索非布韦治疗肝硬化相较于传统治疗方案不良反应较少,安全性相对较高。
总之,与传统疗法相比,雷迪帕韦-索非布韦治疗丙肝肝硬化具有更好的疗效,且安全性较高。
[1]Halfon P,Goldiner I,Zelber-Sagi S,et al.Hepatitis C Virus[J].J Viral Hepat,2013,20(S3):16-42.
[2]Noel N,Michot JM,Besson C,et al.Distinct efficacy of pegylatedinterferon α2a and α2b during treatment of essential thrombocythemia[J].Int J Hematol,2013,97(3):438-439.
[3]Afdhal N,Zeuzem S,Kwo P,et al.Ledipasvir and sofosbuvir for untreated HCV genotype 1 infection[J].N Engl J Med,2014,370 (20):1889-1898.
[4]中华医学会肝病学分会中华医学会传染病与寄生虫病学分会.丙型肝炎防治指南[J].中华传染病杂志,2004,22(2):131-136.
[5]中华肝脏病学会肝纤维化学组.肝纤维化诊断及疗效评估共识[J].中华肝脏病杂志,2002,10(5):327-328.
[6]Jacobson IM,McHutchison JG,Dusheiko G,et al.Telaprevir for previously untreated chronic hepatitis C virus infection[J].N Engl J Med,2011,364(25):2405-2416.
[7]Sarrazin C,Hézode C,Zeuzem S,et al.Antiviral strategies in hepatitis C virus infection[J].J Hepatol,2012,56(Suppl 1):S88-S100.
[8]Poordad F,Hezode C,Trinh R,et al.ABT-450/r-ombitasvir and dasabuvir with ribavirin for hepatitis C with cirrhosis[J].N Engl J Med,2014,370(21):1973-1982.
[9]Lawitz E,Mangia A,Wyles D,et al.Sofosbuvir for previously untreated chronic hepatitis C infection[J].N Engl J Med,2013,368 (20):1878-1887.
[10]Kowdley KV,Gordon SC,Reddy KR,et al.Ledipasvir and sofosbuvir for 8 or 12 weeks for chronic HCV without cirrhosis[J].N Engl J Med,2014,370(20):1879-1888.
(本文编辑:李跃)
10.3969/j.issn.1672-2159.2016.03.022
412007株洲市中心医院
二、治疗方案
根据病人病情分为肝硬化代偿期组(38例)和肝硬化失代偿期(42例)。两组均进行雷迪帕韦-索非布韦治疗,商品名Harvoni片剂(美国吉利德公司)400 mg(1片),1次/d。疗程24周。
三、检测指标
实验开始前分别检测患者的肝肾功能、血常规、甲状腺功能、肝抗原谱、腹部超声心电图等,各项目均采用全自动分析仪进行,育龄女性排除妊娠,治疗过程中每2周检查一次,并对患者不良反应进行记录。各组患者治疗前在年龄性别和常规检测结果中不存在显著性差异。另外,分别于治疗前、治疗后第4、12、24周收集患者血液样品,利用HCV-RNA定量试剂盒检测血液中HCV-RNA表达情况。
四、疗效评估
参照《肝纤维化诊断及疗效评估共识》[5]中的有关标准拟定:①HCV-RNA(-)为转阴,说明疗效显著,明显下降为好转;②肝纤维化标志物下降>40%;③生化项目好转或恢复正常;④超声下门静脉主干内径及脾脏厚度缩小。以上4项均符合为有效。
五、病毒学应答评估
早期病毒学应答(early virus response,EVR):治疗12周时血清HCV-RNA呈阴性;治疗结束时病毒学应答(endtreatment virusre response,ETVR):治疗结束时血清HCVRNA含量小于检测小于80 IU/mL;持续病毒学应答(sustained virological response,SVR):治疗结束后至少随访24周时血清HCV-RNA定量检测小于80 IU/mL。
六、统计方法
2015-09-09)
