非结核分枝杆菌肺病临床特征及其影像学特点
2016-09-20张静波褚海青
张静波, 褚海青
非结核分枝杆菌肺病临床特征及其影像学特点
张静波, 褚海青
非结核分枝杆菌; 肺病; 临床特征; 影像学
近年来,非结核分枝杆菌(NTM)病疫情呈现上升趋势,其中NTM肺病因为无典型临床特异性,且耐药率高,致病菌种繁多,对临床诊断及治疗造成极大的困难,成为重要的公共卫生问题。因此,关注国内外NTM 病的流行趋势,了解NTM病的临床特征及影像学特征,以期做到早期诊断早期治疗,以适应实际工作的需要,成为国内外研究的热点。本文就NTM肺病临床特征及其影像学特点展开综述。
1 流行病学
NTM肺病呈逐年增长趋势[1-10](见表1),特别是在老年人及获得性免疫缺陷综合征(AIDS)患者中,NTM肺病的流行更为普遍。由于NTM肺病与肺结核不同,不需要向公共卫生机构报告,因此,无法得出NTM肺病的发病率、患病率的精确数据,实际情况可能远高于目前的研究报道。我国NTM研究工作起步较晚,1979年全国第1次结核病流行病学抽样调查显示,8省市(52万人)抽样调查结果痰分枝杆菌培养阳性681份,经菌种鉴定29株为NTM,分离率4.3%。1990年第3次全国结核病流行病学抽样调查结果显示:NTM感染率为15.35%,最高为浙江省(44.89%),最低为西藏自治区(1.94%)。2000年我国第4次全国流行病学调查结果NTM感染率为11.1%。而近年来尚无全国范围内大样本的流行病学调查数据,但根据国内相关文献报道,NTM感染在分枝杆菌培养阳性患者中约占1.6%~6.7%。吴龙章等[11]对1998—2002年广州地区4 129例分枝杆菌培养阳性的病例中,经菌型鉴定而确诊为NTM肺病66例(1.6%);上海市肺科医院2011年1月—2014年1月首诊初治痰抗酸染色(AFB)涂片阳性患者4 167例,4 043例患者经过菌种鉴定诊断为肺结核,124例(3.0%)患者经过菌种鉴定诊断为NTM感染,其中52例脓肿分枝杆菌肺病,72例非脓肿分枝杆菌肺病,分别为胞内分枝杆菌42例(33.9%)、鸟分枝杆菌8例(6.4%)、堪萨斯分枝杆菌7例(5.6%)、戈登分枝杆菌6例(4.8%)、偶发分枝杆菌5例(4.0%)、龟分枝杆菌2例(1.6%)、苏加尔维斯分枝杆菌1例(0.8%)、石蜡分枝杆菌1例(0.8%)。分枝杆菌属除结核分枝杆菌复合群(包括结核分枝杆菌、牛分枝杆菌、非洲分枝杆菌、田鼠分枝杆菌)和麻风分枝杆菌外统称为非结核分枝杆菌。目前已知分枝杆菌属种类超过150种,其中有许多可能引起疾病[12]。NTM可分为缓慢生长和快速生长两类[13]。缓慢生长类主要包括鸟分枝杆菌、胞内分枝杆菌和堪萨斯分枝杆菌;快速生长包括脓肿分枝杆菌、偶发分枝杆菌和龟分枝杆菌。缓慢生长和快速生长NTM对药物的敏感性不同,缓慢生长NTM易引起肺部和淋巴结病变,快速生长NTM易导致皮肤、骨和关节病变[14]。不同NTM种类在各个地区的分布不尽相同,宿主的影响因素及所致NTM肺病的临床表现也有所差异。在美国,NTM肺病约80%由鸟胞内分枝杆菌复合群(Mycobacterium avium-intracellulare complex,MAC)引起[3],英国的比例为 43%,在亚洲MAC的比例占56%,其次为脓肿分枝杆菌占35%[4],而我国的相关研究较少。国内有学者报道63例NTM肺病患者,经菌型鉴定龟分枝杆菌最多,占总量的 44%。另有报道648株NTM鉴定结果,MAC为149例、戈登分枝杆菌98株、龟分枝杆菌90株、脓肿分枝杆菌90株、不产色分枝杆菌62株、瘰疬分枝杆菌3l株、偶发分枝杆菌30株、耻垢分枝杆菌30株、次要分枝杆菌12株和其他非结核分枝杆菌56株。
某些宿主因素,如免疫缺陷或已存在的肺部疾病可导致NTM易感性。与结核分枝杆菌相比,NTM毒力和致病性均较低,通常属于机会性致病菌,引起人体疾病常为继发性的,患者大多有慢性基础疾病或免疫损害。NTM细胞壁中的脂阿拉伯甘露聚糖可结合巨噬细胞释放的Toll样受体2 (TLR-2),产生白介素12(IL-12)、肿瘤坏死因子(TNF),并导致一系列的炎性反应。这些细胞因子调节肉芽肿的形成,是免疫级联反应的主要成分[15]。先前存在的肺部疾病,如支气管扩张、慢性阻塞性肺病、囊性肺纤维化、肺结核、尘肺,导致局部防御体系的破坏,因此更易感染NTM。结核分枝杆菌可黏附于正常黏膜,而NTM更易通过纤连蛋白介导反应黏附于受损黏膜[16-17]。人类免疫缺陷病毒(HIV)感染所致的细胞免疫下降也是NTM的易感因素。
2 NTM肺病的临床表现
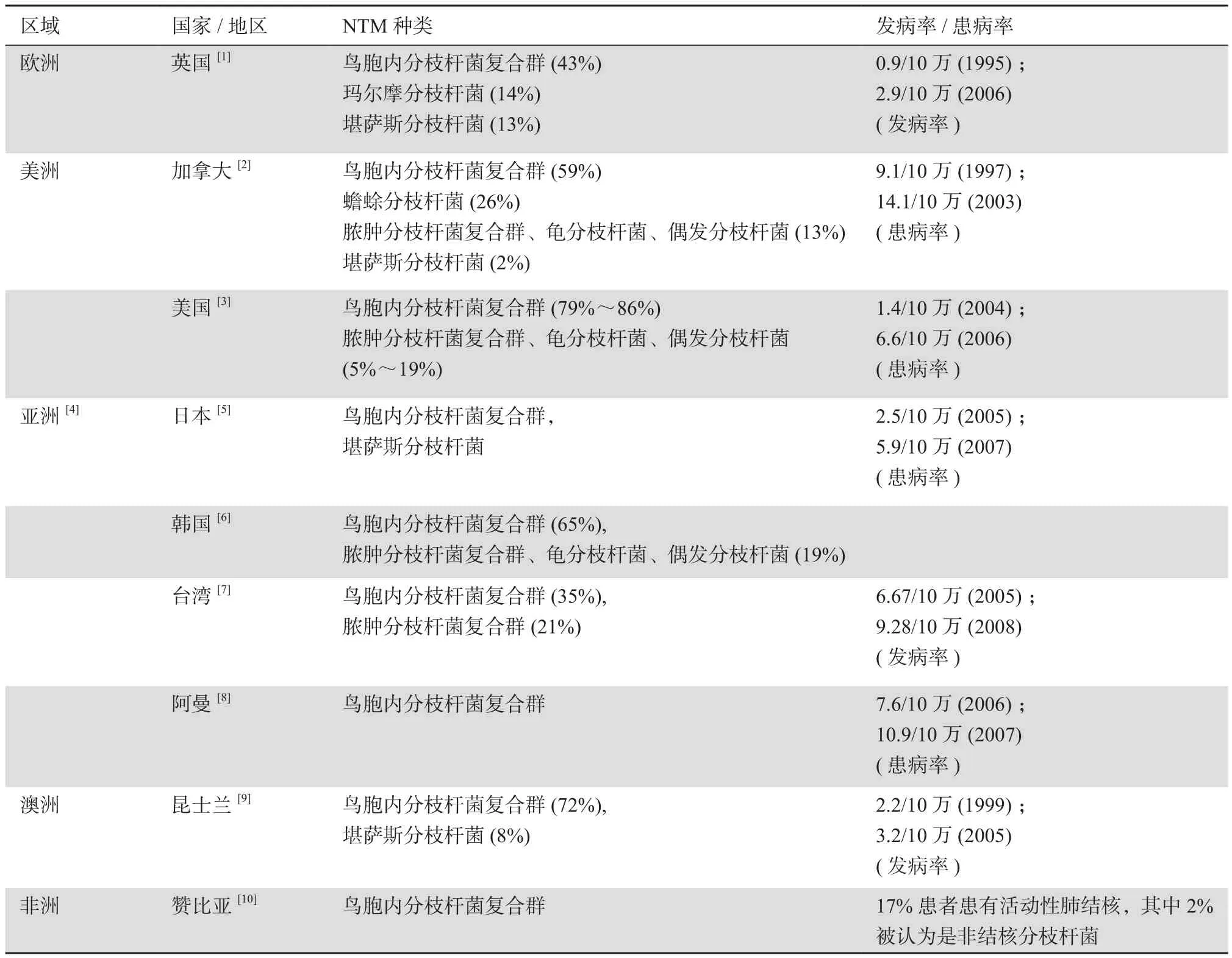
表1 不同区域非结核分枝杆菌流行病学特点
NTM肺病通常表现为非特异性症状,如发热、乏力、盗汗,部分患者可出现咳嗽或呼吸困难,而胸痛和咯血比较少见。SIMONS等[4]分析了亚洲各地区报道的NTM肺病的特点,见表2。
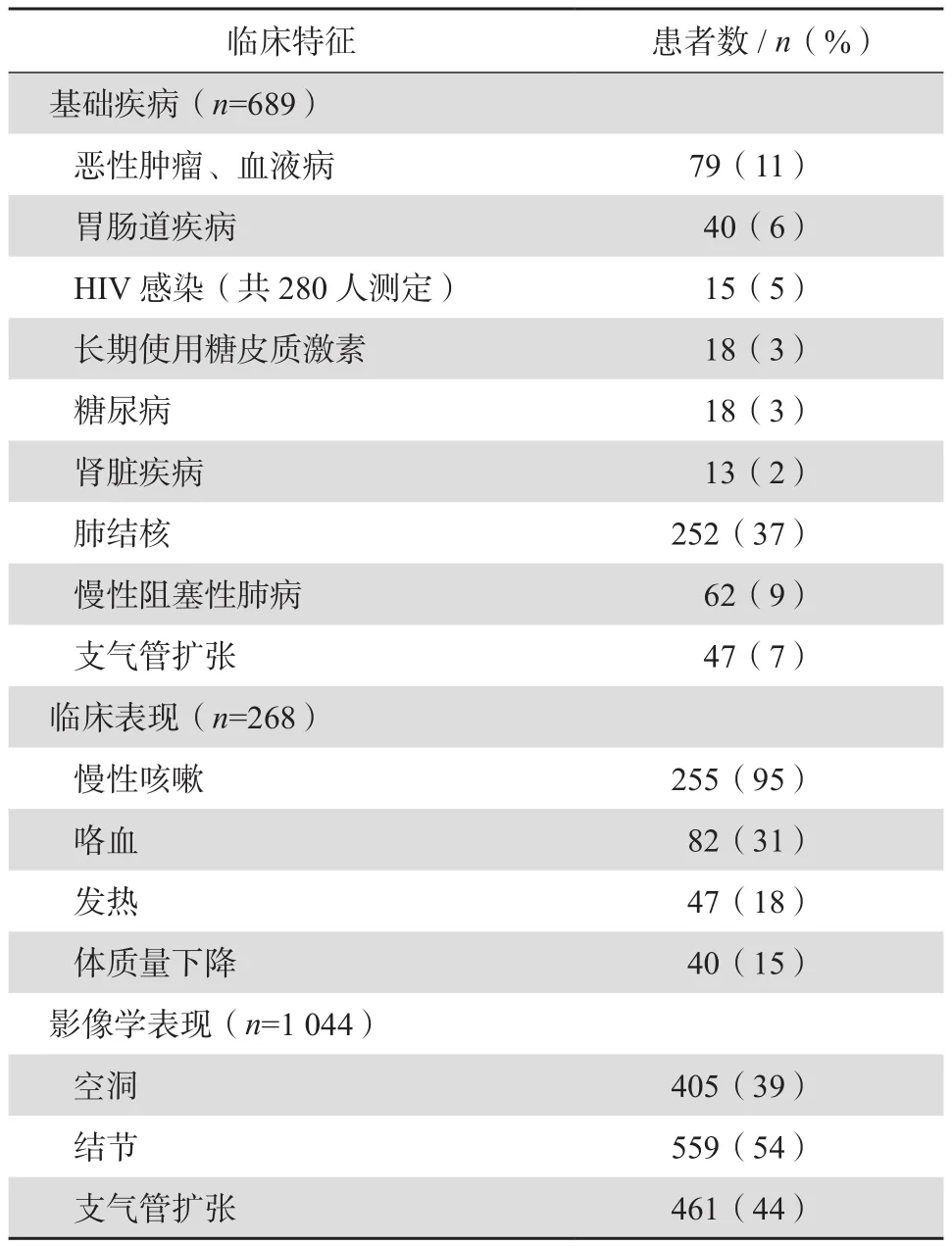
表2 亚洲地区NTM肺病特点
3 NTM肺病的CT表现
NTM肺病的主要影像学表现为支气管扩张、肺结节、小叶中心结节及空洞,通常累及双肺等,常常需要与肺结核鉴别。肺结核确诊可依据下呼吸道标本结核菌培养及PCR结果,但临床症状及胸部影像在肺结核的诊断中也有重要地位[18]。典型肺结核的CT特点包括空洞、肺实变、斑片影、肺结节、纵隔淋巴结肿大、淋巴结钙化、胸腔积液等。由于生物学特性的不同,肺结核与NTM感染的临床表现和CT影像学特点存在一定的差异[19-20]。而由于CT检查的快速、普遍及密度分辨率高等优点,通过胸部CT表现的比较以帮助早期鉴别NTM肺病和肺结核便有了良好的可行性[21-22]。传统观点认为,没有任何影像学工具能可靠地将NTM肺病与肺结核区分开,但NTM与结节性支气管扩张可以一起出现,尤其是进行高分辨CT(HRCT)检查。另外,HRCT中NTM常见的表现是成群出现的直径<5 mm的结节,也被称为树芽征。较大的结节可伴或不伴有空洞[23]。
近年来的研究提示我们CT其实可以成为
NTM肺病及肺结核鉴别的有用工具。有研究者总结NTM肺病的胸部影像学特点[24]:①肺部病变可持续数年无变化,或抗结核治疗无明显吸收甚至呈缓慢进展病。②两肺多叶或单叶均可受累且一般多叶多于单叶、上叶多于下叶,以右肺上叶受累最多见[25]。③肺部病灶形态复杂,斑片状或大片状浸润影、纤维条索影、空洞及结节影均可见,并常为数种病变形态同时多发混杂存在。④可继发支气管扩张和支气管播散。⑤可伴有肺毁损、肺气肿或肺大泡、胸膜粘连肥厚及纵隔内淋巴结肿大等征象。⑥病灶干酪样坏死和钙化少见。NTM肺病CT表现多样,与肺结核类似,国内外文献报道主要有结节、斑片、斑块实变影、空洞、支气管扩张、“树芽征”、磨玻璃影等,肺部多种形态病变通常合并出现,累及各肺叶,并且多合并胸膜增厚粘连[26]。本文结合目前报道的NTM肺病较为可靠的主要CT表现展开讨论。
3.1支气管扩张
支气管扩张与NTM的相关性已有报道,尤其是支气管扩张与鸟分枝杆菌、胞内分枝杆菌复合群感染的关系,发现NTM支气管扩张好发于双侧、右中叶及左舌段[27],而MOORE[28]报道支气管扩张是NTM肺病最常见表现,通常发生于右肺中叶及左肺上叶舌段。之后的陆续报道支气管扩张分布更为广泛,涉及各肺叶。YUAN等[29]比较了75例肺结核与20例NTM肺病患者的胸部CT表现,发现支气管扩张、胸腔积液以及肺结节对于区分肺结核及NTM存在统计学意义。
3.2空洞
空洞是肺结核和NTM病非常典型影像学特征,KIM等[30]认为空洞型AFB涂片阳性的肺结核和NTM肺病有相当相似的临床特征,这导致空洞型肺部分枝杆菌感染患者的经验性治疗更加困难,因此对于空洞的细化描述来区分结核和NTM是很有必要的。KAHKOUEE等[31]发现厚壁空洞、淋巴结钙化提示结核可能;而支气管扩张,同一肺段和相邻肺叶的小结节是NTM的独立预测因子,但是空洞的偏侧及分布NTM肺病与肺结核没有差别。TADESSE等[32]的研究结果显示,空洞如果伴有淋巴结肿大,淋巴结抽吸物AFB镜检将会有更高的灵敏度和特异度,因此如果肿大的淋巴结能够进行支气管内超声波检查法(EBUS)针吸活检等检查对于鉴别诊断可能更有帮助。ALBELDA等[33]发现与肺结核比较,NTM肺病中的空洞比较小(平均直径2.5 cm;范围0.5~7 cm)、壁比较薄(壁厚≤1 mm),而肺结核者较大(空洞平均直径6 cm;范围2~10 cm)。MOORE[28]的CT研究则认为NTM肺病的空洞壁较厚,空洞直径1.5~3 cm。
3.3树芽征“树芽征”可见于多种疾病,如肺结核、弥漫性泛细支气管炎等,“树芽征”通常可导致肺功能慢性严重进行性受损。NTM肺病也可出现该种比较有特征性的影像改变,多见于右中叶和左舌段[17]。
KOH等[34]报道36例NTM肺病中24例表现有“树芽征”,并且在薄层CT上观察更加普遍。
3.4结节
结节是NTM肺病常见表现,国内贺伟等[35]报道22例均有结节,且多数(9 例) 直径<1 cm。TAKADA等[36]报道50例中44例为小结节,分布以上叶、下叶为多。
3.5磨玻璃影
磨玻璃影文献报道较少,发生率相对较低,TAKADA等[36]报道50例中有4例磨玻璃影。磨玻璃影一种是由于NTM肺病直接引起,另一种是患者出现咯血形成的肺泡内积血。
3.6斑片、片样实变
HAN等[37]发现NTM肺病中偶见斑片、片样实变:以炎性渗出为主密度较淡,实变为主则密度较高,有时见“支气管充气征”。
4 NTM肺病诊断
相对于结核分枝杆菌,NTM的致病性较低,而且容易被认为是标本污染,因此NTM感染常被低估。而常用于结核病的诊断方法并不适用于NTM感染,然而,我们对这些微生物侵犯机体并导致细支气管炎、支气管扩张、肉芽肿性炎的认识在不断深入[38-39],也探索了一些新的、较快捷的诊断方法。但也有观点认为,对于分离出NTM的患者,不应考虑为标本污染,应立即给予治疗[39-40]。美国胸科学会/美国传染病学会2007年发布了NTM肺病的诊断标准[41],诊断的关键是:排除其他疾病,特别是结核和肿瘤;微生物结果;影像学证据。
对于NTM肺病的诊断,病原学结果与临床、影像资料必不可少[42]。NTM肺病患者胸部CT检查中,HRCT应为常规检查。NTM肺病肺部病变分布于各个肺叶,并且多种形态病变共存。KOH等[34]认为CT发现细支气管炎超过5个肺叶,合并支气管扩张、小叶实变、空洞,应考虑NTM肺病。NTM肺病表现多样,有结节、片样实变、空洞、支气管扩张、“树芽征”等,多种病变经常合并出现,主要与肺结核鉴别。肺内病变表现为支气管扩张,主要发生在右肺中叶、左肺上叶舌段,并且合并其他病变如空洞、结节等,应考虑NTM肺病。肺内病变为多发薄壁空洞,并且干酪坏死少,亦要考虑NTM肺病。“树芽征”表现需与弥漫性泛细支气管炎鉴别,NTM肺病一般合并结节、空洞等,而弥漫性泛细支气管炎很少见空洞,鉴别不难。
从呼吸道分泌物中反复进行微生物培养对于NTM肺病的诊断非常重要,虽然一次阳性结果并不充分,但若临床表现、影像学表现,尤其是CT表现符合NTM肺病的特点,那么还是需要考虑诊断为NTM肺病。
5 结论
人类接触NTM不可避免,而且在不断增加,并且在某些情况下会导致肺部疾病。虽然分子生物学技术的进步使得实验室快速鉴定NTM成为可能,但仍需加强对NTM肺病的发病机制、临床过程和流行病学研究,进一步提升早期诊断NTM肺病的能力,减少误诊及其带来的非必要的抗结核治疗及药物不良反应。
[1]MOORE JE, KRUIJSHAAR ME, ORMEROD LP, et al. Increasing reports of non-tuberculous mycobacteria in England,Wales and Northern Ireland, 1995-2006[J]. BMC Public Health,2010, 10(1): 612.
[2]MARRAS TK, CHEDORE P, YING AM, et al. Isolation prevalence of pulmonary non-tuberculous mycobacteria in Ontario, 1997-2003[J]. Thorax, 2007, 62(8): 661-666.
[3]PREVOTS DR, SHAW PA, STRICKLAND D, et al. Nontuberculous mycobacterial lung disease prevalence at four integrated health care delivery systems[J]. Am J Respir Crit Care Med, 2010, 182(7): 970-976.
[4]SIMONS S, VAN INGEN J, HSUEH PR, et al.Nontuberculous mycobacteria in respiratory tract infections, eastern Asia[J]. Emerg Infecti Dis, 2011, 17(3): 343-349.
[5]KAJIKI A. Non-tuberculous mycobacteriosis. What has been coming out [J]. Kekkaku, 2011, 86(2): 113-125.
[6]RYOO SW, SHIN S, SHIM MS, et al. Spread of nontuberculous mycobacteria from 1993 to 2006 in Koreans[J]. Clin Lab Anal,2008, 22(6): 415-420.
[7]CHEN CY, CHEN HY, CHOU CH, et al. Pulmonary infection caused by nontuberculous mycobacteria in a medical center inTaiwan, 2005-2008[J]. Diagn Microbiol Infec Dis, 2012, 72 (1): 47-51.
[8]AL-MAHRUQI SH, van INGEN J, AL-BUSAIDY S, et al. Clinical relevance of nontuberculous mycobacteria, Oman[J]. Emerg Infect Dis, 2009, 15(2): 292-294.
[9]THOMSON RM. Changing epidemiology of pulmonary nontuberculous mycobacteria infections[J]. Emerg Infect Dis,2010, 16(10): 1576-1583.
[10]BUIJTELS PC, VAN DER SANDEMA, DE-GRAAFFCS, et al. Nontuberculous mycobacteria, Zambia[J]. Emerg Infect Dis,2009, 15(2): 242-249.
[11]吴龙章,蔡杏珊,关玉华,等.66例非结核分支杆菌肺病的临床分析[J].中国防痨杂志,2003,25(4):257-259.
[12]YUAN MK, CHANG CY, TSAI PH, et al. Comparative chest computed tomography findings of non-tuberculous mycobacterial lung diseases and pulmonary tuberculosis in patients with afb smear-positive sputum[J]. BMC Pulm Med, 2014, 14(1): 65.
[13]NGUYEN VX. Diagnosis and treatment of disease caused by nontuberculous mycobacteria. This official statement of the American Thoracic Society was approved by the Board of Directors, March 1997. Medical Section of the American Lung Association[J]. Am J Respir Crit Care Med, 1997, 156(2pt2):s1-s25.
[14]TORTOLI E. Impact of genotypic studies on mycobacterial taxonomy: the new mycobacteria of the 1990s[J]. Clina Microbiol Revi, 2003, 16(2): 319-354.
[15]SEXTON P, HARRISON AC. Susceptibility to nontuberculous mycobacterial lung disease[J]. Eur Respir J, 2008, 31(6):1322-1333.
[16]MIDDLETON AM, CHADWICK MV, NICHOLSON AG, et al. Inhibition of adherence of Mycobacterium avium complex and Mycobacterium tuberculosis to fibronectin on the respiratory mucosa[J]. Respir Med, 2004, 98(12): 1203-1206.
[17]MIDDLETON AM, CHADWICK MV, NICHOLSON AG,et al. The role of Mycobacterium avium complex fibronectin attachment protein in adherence to the human respiratory mucosa[J]. Mol Microbiol, 2000, 38(2): 381-391.
[18]AHSAN MJ, ANSARI MY, YASMIN S, et al. Tuberculosis:current treatment, tiagnostics, and newer antitubercular agents in clinical trials[J]. Infect Disord Drug Targets, 2015,15(1):32-41.
[19]WOODRING JH, VANDIVIERE MH. Pulmonary disease caused by nontuberculous mycobacteria[J]. J Thorac Imaging,1990, 5(2): 64-76.
[20]DAMARAJU D, JAMIESON F, CHEDORE P, et al. Isolation of non-tuberculous mycobacteria among patients with pulmonary tuberculosis in Ontario, Canada[J]. Int J Tuberc Lung Dis,2013, 17(5): 676-681.
[21]JEONG YJ, LEE KS, KOH WJ, et al. Nontuberculous mycobacterial pulmonary infection in immunocompetent Patients: comparison of thin-Section CT and histopathologic findings 1[J]. Radiology, 2004, 231(3): 880-886.
[22]LEE Y, SONG JW, CHAE EJ, et al. CT findings of pulmonary non-tuberculous mycobacterial infection in non-AIDS immunocompromised patients: a case-controlled comparison with immunocompetent patients[J]. Br J Radiol, 2013, 86 (1024):20120209.
[23]JOHNSON MM, ODELL JA. Nontuberculous mycobacterial pulmonary infections[J]. J Thoraci Dis, 2014, 6(3): 210-220.
[24]尤正千,朱晓华.肺非结核分支杆菌病的CT影像表现[J].中国临床医学影像杂志,2005,16(3):141-143.
[25]ERASMUS JJ, McADAMS HP, FARRELL MA, et al. Pulmonary nontuberculous mycobacterial infection: radiologic manifestations 1[J]. Radiographics, 1999, 19(6): 1487-1503.
[26] WITTRAM C, WEISBROD GL.Mycobacterium avium complex lung disease in immunocompetent patients: radiography-CT correlation[J]. Br J Radiol, 2002, 75(892): 340-344.
[27]CHUNG MJ, LEE KS, KOH WJ, et al. Thin-section CT findings of nontuberculous mycobacterial pulmonary diseases:comparison between Mycobacterium avium-intracellulare complex and Mycobacterium abscessus infection[J]. J Korean Med Sci, 2005, 20(5): 777-783.
[28]MOORE EH. Atypical mycobacterial infection in the lung: CT appearance[J]. Radiology, 1993, 187(3): 777-782.
[29]YUAN MK, CHANG CY, TSAI PH, et al. Comparative chest computed tomography findings of non-tuberculous mycobacterial lung diseases and pulmonary tuberculosis in patients with acid fast baciui smear-positive sputum[J]. BMC Pulmonary Medicine,2014, 14(1): 65.
[30]KIM YK, HAHN S, UH Y, et al. Comparable characteristics of tuberculous and non-tuberculous mycobacterial cavitary lung diseases[J]. Int J Tuberc Lung Dis, 2014, 18(6): 725-729.
[31]KAHKOUEE S, ESMI E, MOGHADAM A, et al. Multidrug resistant tuberculosis versus non-tuberculous mycobacterial infections: a CT-scan challenge[J]. Braz J Infect Dis, 2013, 17 (2): 137-142.
[32]TADESSE M, ABEBE G, ABDISSA K, et al. Concentration of lymph node aspirate improves the sensitivity of acid fast smear microscopy for the diagnosis of tuberculous lymphadenitis in jimma, southwest ethiopia[J]. PloS One, 2014, 9(9):e106726.
[33]ALBELDA SM, KERN JA, MARINELLI DL, et al. Expanding spectrum of pulmonary disease caused by nontuberculous mycobacteria[J]. Radiology, 1985, 157(2): 289-296.
[34]KOH W J, LEE K S, KWON O J, et al. Bilateral bronchiectasis and bronchiolitis at thin-section CT: diagnostic implications in nontuberculous mycobacterial pulmonary infection 1[J]. Radiology, 2005, 235(1): 282-288.
[35]贺伟,潘纪戍.肺非结核性分支杆菌病的X线和CT表现[J].中华放射学杂志,2004,38(1):1789-1791.
[36]TAKADA Y, SAKAI F, SUZUKI K, et al. CT features of pulmonary nontuberculous mycobacterial infection: effects of underlying pulmonary disease[J]. Radiat Med, 1999, 18(3):167-175.
[37]HAN D, LEE KS, KOH WJ, et al. Radiographic and CT findings of nontuberculous mycobacterial pulmonary infectioncaused by Mycobacterium abscessus[J]. AJR AM J Roentgenol,2003, 181(2): 513-517.
[38]FUJITA J, OHTSUKI Y, SUEMITSU I, et al. Pathological and radiological changes in resected lung specimens in Mycobacterium avium intracellulare complex disease[J]. Eur Respir J, 1999, 13(3): 535-540.
[39] ROSSMAN MD. Colonization withMycobacterium avium complex—an outdated concept[J]. Eur Respir J, 1999, 13(3):479-479.
[40]OLIVIER KN, YANKASKAS JR, KNOWLES MR. Nontuberculous mycobacterial pulmonary disease in cystic fibrosis[J]. Semin Respir Infect, 1996, 11(4): 272-284.
[41]GRIFFITH DE, AKSAMIT T, BROWN-ELLIOTT BA, et al. An official ATS/IDSA statement: diagnosis, treatment, and prevention of nontuberculous mycobacterial diseases[J]. Am J Respir Crit Care Med, 2007, 175(4): 367-416.
[42]MEHTA M, MARRAS TK. Impaired health-related quality of life in pulmonary nontuberculous mycobacterial disease[J]. Respir Med, 2011, 105(11): 1718-1725.
Clinical and imaging features of non-tuberculous mycobacterial lung diseases
ZHNG Jingbo, CHU Haiqing. (Department of Respiratory Medicine, Shanghai Pulmonary Hospital, Tongji University School of Medicine, Shanghai 200433, China)
·信息交流·
R521
A
1009-7708(2016)01-0086-06
10.16718/j.1009-7708.2016.01.020
上海同济大学附属上海市肺科医院呼吸科,上海 200433。
张静波(1979—),男,硕士,主治医师,主要从事呼吸病学研究。
褚海青,E-mail:chu_haiqing@126.com。
2015-02-25
2015-06-17
