采用微波消解-ICP-AES法分析不同产地大枣中无机元素的组成及其含量
2016-09-12段金廒钱大玮唐晓清
郭 盛,段金廒,*,严 辉,钱大玮,唐晓清
(1.南京中医药大学,江苏省中药资源产业化过程协同创新中心/中药资源产业化与方剂创新药物国家地方联合工程研究中心,江苏南京 210023;2.南京农业大学,园艺学院,江苏南京 210095)
采用微波消解-ICP-AES法分析不同产地大枣中无机元素的组成及其含量
郭盛1,段金廒1,*,严辉1,钱大玮1,唐晓清2
(1.南京中医药大学,江苏省中药资源产业化过程协同创新中心/中药资源产业化与方剂创新药物国家地方联合工程研究中心,江苏南京 210023;2.南京农业大学,园艺学院,江苏南京 210095)
采用微波消解-ICP-AES法探索不同产地、不同栽培品种大枣中无机元素的组成及含量,结果表明在所测定的19种无机元素中,不同产地、不同栽培品种大枣中普遍含有元素K、Ca、Mg、Na、Fe、B、Sr、Al、Zn、Mn、Mo、Cu;在所检测的37批样品中,有36批样品中检出有害重金属元素Pb,其平均含量可达2.62 μg/g;所有样品均未检出有害元素As、Cd、Cr、Hg。依据各样品中测定元素的含量,采用主成分分析法,选择前4个因子(F1~F4)对大枣营养保健价值进行了综合评价,其综合评价函数为F=0.19936F1+0.18240F2+0.17396F3+0.10946F4。结果显示,产自陕西彬县的晋枣品种、河南内黄的扁核酸枣品种以及山东荷泽的核桃纹品种综合排序分列1、2和3位,表明从无机元素角度考虑以上三个产地所产大枣品质较好。本研究为药食两用大枣资源营养及保健价值的进一步发现及安全性评价提供了一定的数据支撑,为大枣适宜栽培区域、栽培品种的选择提供了借鉴。
大枣,无机元素,微波消解,ICP-AES
大枣为鼠李科枣属植物枣(ZiziphusjujubaMill.)的干燥成熟果实,亦称红枣,为我国第一大干果,是一种美味可口,营养极其丰富的食品。大枣也广泛用于中医临床,为药食同源之品,具有补中益气、养血安神之功,常用于脾虚食少、乏力便溏、妇人脏躁等症。现代研究显示,大枣传统药用功效的发挥与其含有丰富的糖类、三萜类、核苷及碱基类、氨基酸类、无机元素类等化学成分关系密切[1-2]。无机元素在人体内不仅具有促进机体合成生命活动所需的物质,提高生命质量的作用,而且还可提高相关生物酶的活性,增强机体的免疫功能[3]。中药材的药效及食品的营养价值也与其所含无机元素的组成及含量密切相关[4]。此外,食品中的砷、镉、铅、汞、硒等重金属元素可以通过生物富集作用最终到达人体造成慢性中毒,引发癌症、呼吸系统疾病、心血管疾病、生殖发育疾病等,重金属超标不仅严重危害人体的身心健康,而且会严重阻碍商品进出口贸易,造成巨大经济损失[5]。因此,开展具有药食两用价值的大枣中无机元素的研究对于阐释其药效作用机理、评定其营养价值及安全性具有重要意义。

表1 样品信息表
据统计,我国现有大枣栽培品种及类型近1000种,广布于除黑龙江外的全国广大地区[6]。而现有大枣中无机元素的分析报道多仅以某一栽培区域或少数几个栽培品种为研究对象[7-11],并未对我国大枣各主产地及主栽品种样品进行综合分析,较难反映我国目前大枣资源整体无机元素分布特征。据此,本研究选取我国目前栽培面积较大,或已形成商品规模的27个栽培产地的31个栽培品种,共计37批次样品,采用微波消解-ICP-AES法分析其19种无机元素的组成及含量差异性,以期为我国大枣资源营养价值的评定及其营养功能的开发提供依据,为其安全性的评定提供理论数据,也为其保健功效的阐释提供借鉴。
1 材料与方法
1.1材料与仪器
元素标准溶液K(GSB 04-1733-2004)、Na(GSB 04-1738-2004)、Ca(GSB 04-1720-2004)、Se(GSB 04-1751-2004)、B(GSB 04-1716-2004)、Mo(GSB 04-1737-2004)、Sr(GSB 04-1754-2004)、Hg(GSB 04-1729-2004)、Pb(GSB 04-1742-2004)、Mg(GSB 04-1735-2004)(质量浓度均为1000 μg/mL),混合元素(Al、As、Cd、Co、Cr、Cu、Fe、Mg、Mn、Zn、)标准溶液(GSB 04-1766-2004)(质量浓度为100 μg/mL)购自国家标准物质中心;超纯水(18.2 MΩ·cm)自制;硝酸(优级纯)、过氧化氢(分析纯)购自上海国药化学试剂公司。
大枣样品采自河北、山东、新疆、宁夏等省区,经南京中医药大学段金廒教授鉴定为鼠李科植物枣ZiziphusjujubaMill.的成熟果实。标本存于南京中医药大学标本馆。样品采集后,去离子水清洗表面,45 ℃烘干,取果肉粉碎过40目筛,备用。样品信息见表1。
Milestone Ethos T微波消解系统意大利Milestone公司;Optima 2100DV型电感耦合等离子发射光谱仪美国Perkin Elmer公司;BT125型电子天平赛多利斯科学仪器有限公司;EPED超纯水系统南京易普达易科技发展有限公司。
1.2实验方法
1.2.1供试品溶液的制备准确称取样品粉末(40目)1.0 g于聚四氟乙烯消解罐中,加入7 mL HNO3和1 mL 30% H2O2,密闭后置入微波消解炉中,10 min升至200 ℃,保持10 min,微波功率1000 W,待消解完全后,冷却,转移至50 mL量瓶中,加去离子水至刻度,摇匀,即得供试品溶液。同步以硝酸7 mL和30% H2O21 mL做空白实验。
1.2.2ICP-AES测定条件的选择射频功率1.3 kW,雾化气流量0.8 L/min,辅助气流量0.2 L/min,冷却气流量15 L/min,观测方向Axial,溶液提升量1.5 mL/min。
1.2.3分析谱线的选择及仪器检出限测定依据光谱仪对每个元素的测定均可以同时选择多条特征谱线的特点,同时考虑到共存元素的相互干扰,在本研究中每个元素首先选取2~3条谱线进行测定,综合分析强度、干扰情况及稳定性,最终选择干扰少、精密度和信噪比均较高的谱线作为被测元素的分析谱线。取空白溶液测量10次,以标准偏差3倍时所对应的分析浓度为该元素的仪器检出限。

表2 各元素分析波长、线性方程、相关系数、检出限实验结果
1.2.3工作曲线绘制取标准物质K元素母液,加去离子水配制成浓度分别为0、20、50、100、200、400 μg/mL的系列标准品溶液;Ca、Mg元素母液加去离子水配制浓度分别为0、5.0、10.0、20.0、40.0、60.0 μg/mL的系列标准品溶液;B、Al、As、Cd、Co、Cr、Cu、Fe、Hg、Mn、Mo、Na、Pb、Se、Sr、Zn、元素母液加去离子水配制浓度分别为0、0.5、1.0、2.0、4.0、8.0 μg/mL的系列标准品混合溶液。上述各标准溶液在选定的工作条件下经ICP-AES测定后,仪器给出各元素的工作曲线及线性关系。
2 结果与分析
2.1元素分析谱线的选择及检出限的测定
进行ICP-AES法测定时,元素分析谱线选择是否恰当,直接影响到测定方法的可信度及测定结果的准确性。遵照“1.2.2”项下实验方法进行分析谱线选择和仪器检出限测定,结果见表2。19种元素选定的分析谱线受到的干扰小,且信噪比高。各元素的检出限在0.001~0.066 μg/mL,检出限较低,均可满足本实验测试要求。
2.2工作曲线
19种元素工作曲线线性回归方程、相关系数(r)测定结果见表2,结果显示各元素标准曲线线性相关系数为0.9995~0.9999,表明该方法线性关系均良好。
2.3精密度及重复性实验
在选定的测试条件下,取山东沾化产冬枣样品为供试品,精密称取1.0 g粉末,按“1.2.1”项下方法进行消解,制备供试品溶液,在选定条件下采用ICP-AES法重复测定6次,得供试品溶液精密度实验结果;另取混合对照品溶液,在相同条件下重测定6次,得对照品溶液精密度实验结果(见表3)。取山东沾化产冬枣样品为供试品,精密称取1.0 g粉末,平行6份,按“1.2.1”项下方法分别进行消解,制备供试品溶液,在选定条件下测定各元素质量分数,得重复性实验结果(见表3)。由表3可知,精密度RSD在0.43%~2.11%,重复性RSD在0.99%~2.54%,表明该方法精密度及重复性均良好,可满足测定要求。
2.4加样回收率实验
取山东沾化产冬枣样品,采用标准加入法进行加样回收率实验。准确称取6份样品各0.5 g,分别加入适量已知质量浓度的各元素标准溶液。按“1.2.1”项下方法进行微波消解制备供试品溶液,在选定的测试条件下分别测定,结果(见表4)显示其回收率为91.9%~107.6%,RSD<4%,表明该方法准确可靠。
2.5样品测定结果
在上述方法学考察的基础上,按照选定的最佳仪器测试参数,采用标准曲线法测定各样品溶液中无机元素的含量,结果见表5。比较不同产地及栽培品种大枣样品中常量元素含量,发现所有样品K含量均较高,其平均值可达11.01 mg/g,其中山东荷泽产核桃纹样品K含量最高(24.81 mg/g),最低的为河南新郑产的灰枣样品(5.46 mg/g);Ca平均含量为0.87 mg/g,其中含量最高的为河南新郑产的鸡心枣样品(1.43 mg/g),最低的为新疆若羌产的若羌大枣样品(0.49 mg/g);Mg平均含量为0.48 mg/g,其中含量最高的为陕西彬县产的晋枣样品(0.69 mg/g),最低的为河北赞皇产的赞皇大枣样品(0.23 mg/g);Na含量相对较低(0.14 mg/g),且各样品间差异较大,最高者可达0.63 mg/g(新疆和田产骏枣样品),而在山西稷山产的板枣样品中却未检测到。微量元素比较结果显示:Fe和B平均含量相对较高,分别为23.26 μg/g和22.91 μg/g,其次为Sr(8.58)、Al(7.80 μg/g)和Zn(6.23 μg/g),Mn、Mo相对含量较低,其平均值分别为2.81 μg/g和2.72μg/g,Co和Se未检出。其中,Fe含量相对较高的为山东茌平产圆铃枣样品(43.46 μg/g),B含量相对较高的为河南内黄产扁核酸枣样品(36.92 μg/g),Al含量相对较高的为山西柳林产牙枣样品(22.75 μg/g),Zn含量相对较高的为安徽芜湖产菱枣样品(18.23 μg/g)。

表3 各元素的精密度、重复性实验测定结果
所有样品中均未检出国家食品安全卫生标准《食品中污染物限量》(GB2762-2012)及现行版《药用植物及制剂进出口绿色行业标准》规定重点检测的有害元素As、Cd、Cr及Hg;Cu元素含量除产自河南内黄的扁核酸样品(20.09 μg/g)超过《药用植物及制剂进出口绿色行业标准》规定的小于等于20 mg/kg限量外,其余样品均符合要求;有83.8%的样品其Pb元素含量超过《食品安全卫生标准-食品中污染物限量》规定的小于等于1 mg/kg限量标准,其中河南新郑产鸡心枣品种(9.54 μg/g)、江苏泗洪产泗洪大枣品种(8.00 μg/g)、河北沧县产无核枣品种(11.78 μg/g)Pb元素含量均超过了《药用植物及制剂进出口绿色行业标准》规定的小于等于5 mg/kg的限量标准。
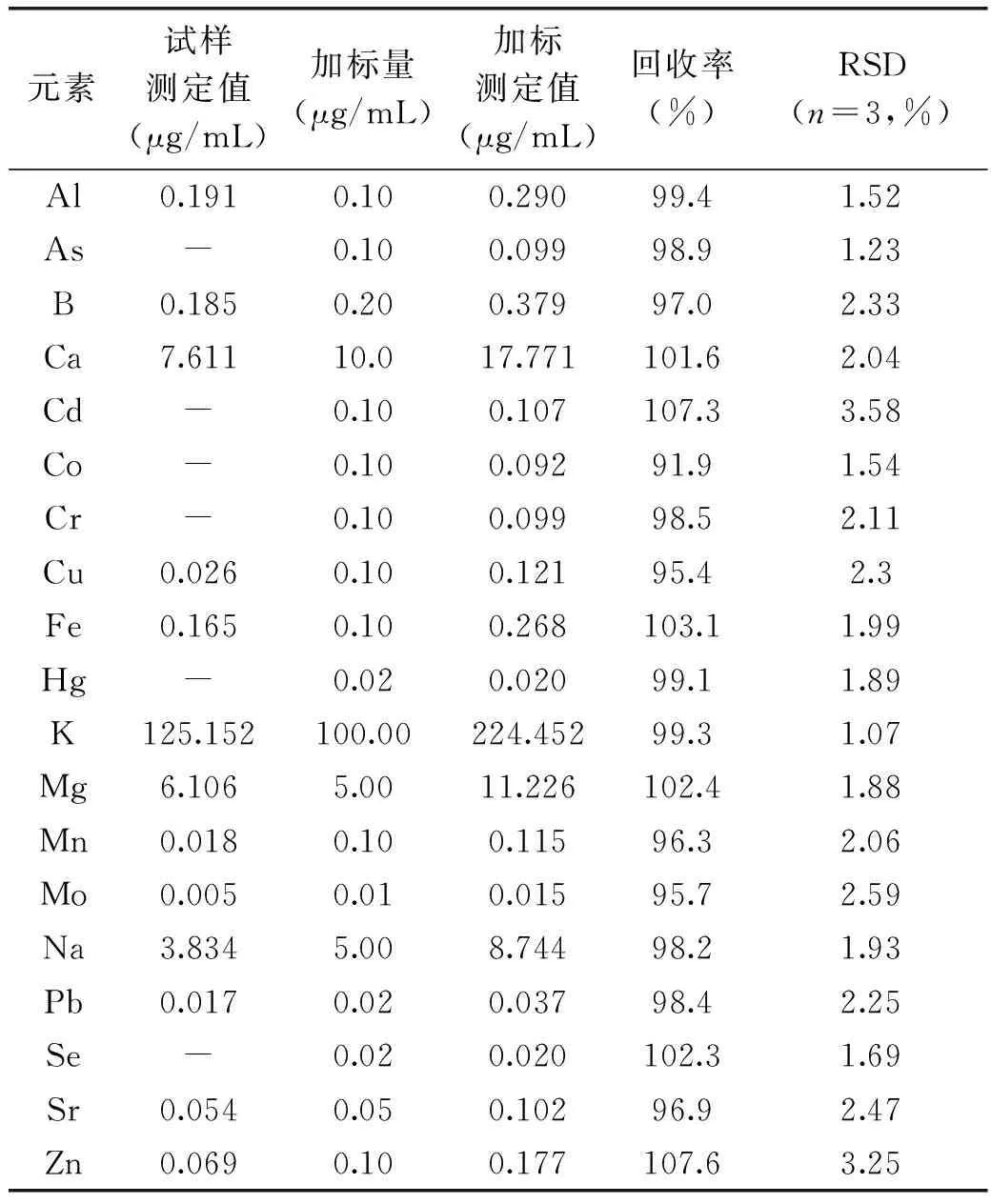
表4 各元素的加样回收率实验测定结果
本研究样品基本涵盖了我国目前已形成商品规模的大枣主产地及主栽品种,研究样品具有代表性,可基本反映我国目前大枣中无机元素含量的基本状况。研究结果显示:所有大枣样品均呈现出高K低Na的分布特点,且Ca和Mg含量丰富;微量元素中以Fe、B、Sr、Al、Zn含量较为丰富。其中K是机体中重要的电解质,可加强肌肉的韧性和心脏的运动力,具有促进蛋白质、碳水化合物和热能代谢的作用;Ca和Mg可参与神经及免疫信息传导,Mg还具有抑制神经兴奋性的作用;Fe和人体免疫防御功能关系密切,可协调多种元素的体内代谢,同时Fe也是构成血红蛋白、肌红蛋白、细胞色素和其它酶系统的主要成分,与造血功能关系密切[3];B可显著提高细胞中超氧化物歧化酶和谷胱甘肽过氧化物酶的水平,在保护细胞膜的完整性、防止脂质氧化以及清除自由基等生理反应中都起着重要作用[12];Sr可参与人体骨造髓的生理过程[13];Zn是人体中含金属酶的成份,可参与核酸和蛋白质代谢作用,与人体生长发育及免疫功能密切相关[14]。上述元素所表现出的生理功能与大枣具有补中益气、养血安神的功效相一致,因此可认为大枣所含有的这些无机元素为大枣营养价值体现及功效的发挥密切相关。此外,97.3%的样品检出有害元素Pb,其引入途径值得进一步研究。
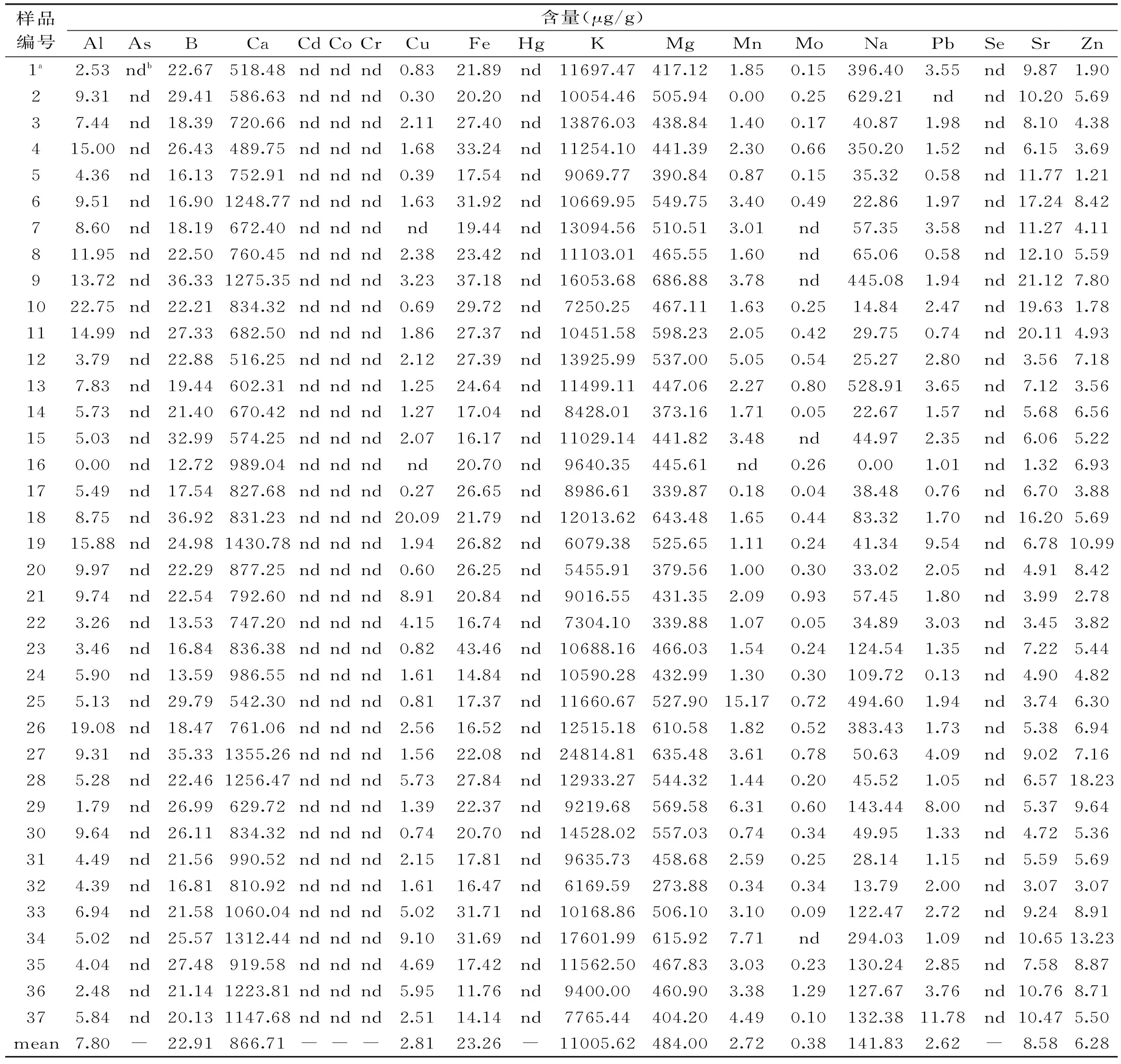
表5 不同样品中无机元素分析结果
注:a样品序号同表1;b未检测到。
2.6大枣果实无机元素含量相关性分析
采用SPSS16.0软件对大枣样品中检测到的各元素进行相关性分析,因多数变量不服从正态分布,故采用Spearman等级相关系数法,统计结果见表6。相关矩阵分析显示,大枣样品中有7对元素呈现极显著正相关(p<0.01),分别为Mg与B、K、Mn、Zn,Mn与B、Pb,Ca与Zn;有12对元素呈显著正相关(p<0.05),分别为Cu与Ca、Mn、Zn,K与B、Mn、Na,Sr与Al、Fe、Mg,Na与B、Mn,Fe与Mg。特别是Mg、Mn分别与6种元素显著相关,K与4种元素显著相关,表现出这些元素间具有相互协同、促进吸收的关系。其余各元素之间多存在相关趋势,但均未达到显著性水平。

表6 大枣果实中无机元素相关性分析结果
注:ap<0.05;bp<0.01。
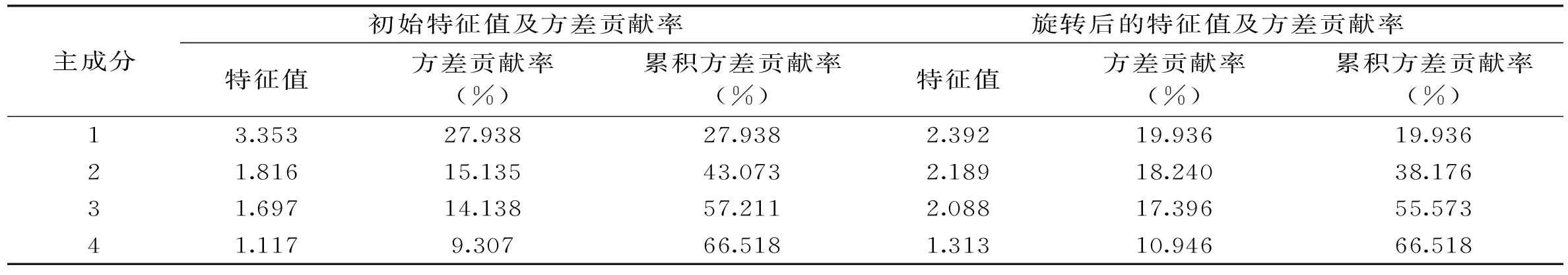
表7 主成分的特征值及贡献率
Rotation Method:Varimax with Kaiser Normalization.

表8 旋转后的因子载荷矩阵
Rotation Method:Varimax with Kaiser Normalization.
2.7不同产地及品种大枣样品营养及保健价值综合评价
因大枣中含有的多种无机元素与其保健、药用价值密切相关,因此可基于无机元素组成及含量对不同产地及不同栽培品种大枣样品的保健及营养价值进行评价。因各样品中所含无机元素种类较多,且不同元素间数据差异较大,故选择主成分分析法对所测定数据进行降维处理后再行评价,以增加评判结果的科学性。以37批次大枣样品中含有的除有害元素Pb外的12种元素组成的37×12矩阵进行主成分分析,结果显示前4个主成分特征值均大于1,说明前4个因子在影响大枣质量评价的指标中起着主导作用,4个主成分的累积贡献率达66.5%,能够较客观地反映大枣的内在质量,故选取前4个主成分进行分析。同时为各主成分因子更好地解释各变量,分析中对特征值及因子载荷矩阵采用了方差最大化正交旋转,结果见表7。各元素在4个主成分上的载荷值见表8,其中B、K等元素在第1主成分上有较高载荷,说明第1主成分主要反映了B、K、Mg、Mn和Na元素指标的信息;同理,第2主成分主要反映了Al和Sr元素指标的信息;第3主成分主要反映了Ca、Zn元素指标的信息;第4主成分主要反映了Cu、Mo和Fe元素指标的信息。即前4个主成分基本可包含12种无机元素的全部信息。
选取上述个主成分因子,以其得分与方差贡献率乘积之和相加,得出各个大枣样品的无机元素总因子得分值F,以F大小评价大枣样品保健及营养价值高低[15-16],其综合评价函数为:
F=0.19936F1+0.18240F2+0.17396F3+0.10946F4
按综合评价函数计算出的不同样品综合得分(F)及得分排名见表9。陕西彬县产晋枣样品、河南内黄产扁核酸枣样品以及山东荷泽产核桃纹枣样品综合排序分列1、2和3位,表明就无机元素角度而言以上大枣样品品质较好。
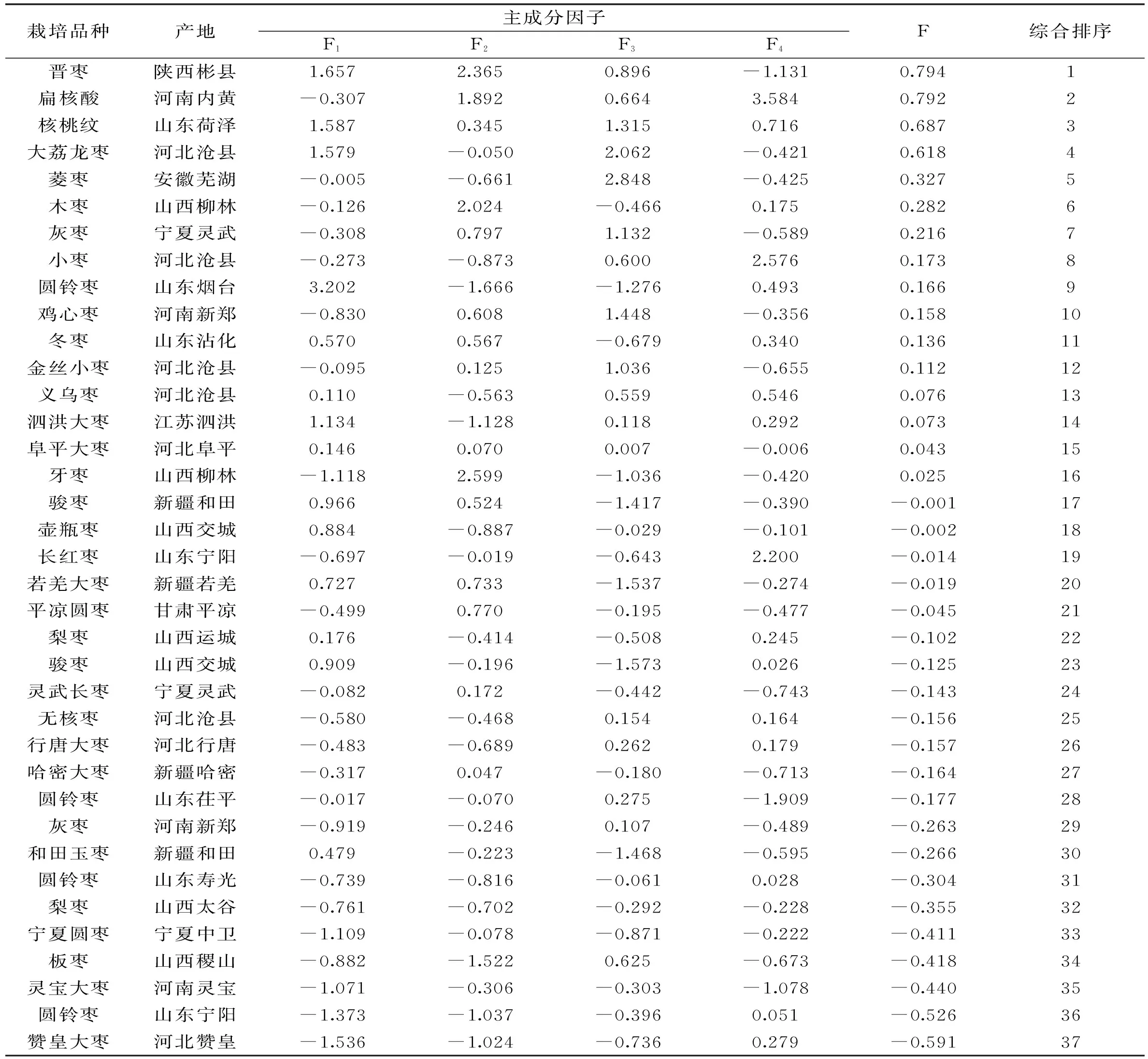
表9 不同大枣样品中无机元素主成分因子及其综合评价结果
3 结论
本文采用微波消解结合ICP-AES法建立了大枣中包含营养元素及有害重金属共计19种无机元素的分析方法,并通过37批次样品验证表明该方法简便、准确可靠。不同产地、不同品种大枣样品中含量较高的无机元素有K、Ca、Mg、Na、Fe、B、Sr、Al、Zn,不同样品间含量差异较大;多数样品中均检出有害重金属元素Pb,其平均含量高于国家食品安全卫生标准《食品中污染物限量》(GB2762-2012)的相关限量标准。基于主成分分析法,通过对不同样品中的无机元素含量进行降维分析,将所测到的12种无机元素指标简化为4个主成分,建立了基于无机元素角度客观评价大枣保健营养价值的综合评价方法。该方法中各主成分的贡献率(综合评价函数中的权重)是经分析原始数据计算而得,克服了其他综合评价方法中人为确定各指标权重的问题,其评价结果更为客观公正。评价结果为药食两用大枣栽培区域及品种选择提供了一定的理论数据。
[1]郭盛,段金廒,钱大玮,等. 枣属植物化学成分研究进展[J]. 国际药学研究杂志,2013,40(6):702-710.
[2]Gao QH,Wu CS,Wang M. The jujube(Ziziphus Jujuba Mill.)fruit:A review of current knowledge of fruit composition and health benefits[J]. Journal of Agricultural and Food Chemistry,2013,61:3351-3363.
[3]丛涛,赵霖. 微量元素锌铜铁硒锰的检测及临床营养学意义[J]. 微量元素与健康研究,2006,23(6):59-61.
[4]陈文,王湘君,赵阳,等. 微波消解-ICP-AES法测定蜂胶中营养元素[J]. 食品工业科技,2013,34(20):56-59.
[5]李莉,李伟青,申德省,等. 食品中重金属总量及形态分析研究进展[J]. 食品工业科技,2013,34(7):387-391.
[6]刘孟军,汪民. 中国枣种质资源[M]. 北京:中国林业出版社,2009.
[7]陈恺,李瑾瑜,李琼,等. ICP-AES法同时测定新疆红枣中的12种元素[J]. 食品与机械,2015,31(1):78-81.
[8]芮玉奎,申琳,生吉萍. 冬枣果实中微量元素和重金属含量研究[J]. 光谱学与光谱分析,2008,28(8):1928-1930.
[9]南海娟,马汉军,杨永慧. 3 种枣果中主要营养成分和元素比较[J]. 食品与发酵工业,2014,40(5):161-165.
[10]刘一兵,范增民. 大枣和小枣中微量元素含量的比较研究[J]. 微量元素与健康研究,2007,24(1):20-21.
[11]陈秋生,张强,殷萍,等. 电感耦合等离子体质谱法同时测定冬枣中多种元素的含量[J]. 天津农业科学,2015,21(2):5-8.
[12]谢伟,徐国茂,叶琴. 微量元素硼与人体健康[J]. 微量元素与健康研究,2010,27(1):65-66.
[13]王建科,任永全,陈惠玲,等. 怀牛膝及其不同炮制品中10种微量元素的含量[J]. 微量元素与健康研究,2003,20(6):28.
[14]曹继华,王正益,王勤. 中药微量元素与健康[J]. 广东微量元素科学,1999,6(10):10-12.
[15]严辉,段金廒,钱大玮,等. 不同产地当归药材及其土壤无机元素的关联分析与探讨[J]. 中药材,2011,34(4):512-516.
[16]姚鑫,周桂生,唐于平,等. 采用微波消解-ICP-AES法对不同产地果用银杏叶无机元素分析与评价[J]. 光谱学与光谱分析,2013(3):808-812.
Determination of the inorganic elements in jujube fruits cultivated in different regions by microwave digestion and ICP-AES method
GUO Sheng1,DUAN Jin-ao1,*,YAN Hui1,QIAN Da-wei1,TANG Xiao-qing2
(1.Jiangsu Collaborative Innovation Center of Chinese Medicinal Resources Industrialization,and National and Local Collaborative Engineering Center of Chinese Medicinal Resources Industrialization and Formulae Innovative Medicine,Nanjing University of Chinese Medicine,Nanjing 210023,China 2.College of Horticulture,Nanjing Agricultural University,Nanjing 210095,China)
Inorganic elements in jujube fruits collected from different regions were determined by microwave digestion coupled with ICP-AES method. The results showed that in the 19 kinds of inorganic elements determined in the assay,almost all of the samples contain the elements of K,Ca,Mg,Na,Fe,B,Sr,Al,Zn,Mn,Mo and Cu. The harmful heavy metal element of Pb was detected in most of samples,and its average content could get up to 2.62 μg/g.The harmful elements of As,Cd,Cr and Hg were not detected in all the samples. Based on the contents of elements in different samples,principal component analysis method was performed and 4 factors(F1-F4)were selected to evaluate the jujube nutrition and health value. The evaluation function is F=0.19936F1+0.18240F2+0.17396F3+0.10946F4. The results showed that the cultivars from Shaanxi Binxian,Henan Neihuang and Shandong Heze ranked in the top three in the terms of inorganic elements,which indicated that the qualities of above samples are better than those of other samples. This study provided the data of nutritional value and safety for the jujube resources,and also provided the reference for selecting the cultivation regions and cultivars of jujube.
Ziziphusjujuba,inorganic element,microwave digestion,ICP-AES
2015-04-29
郭盛(1977-),男,博士,主要从事中药资源化学研究及教学工作,E-mail:gsh916@163.com。
段金廒(1956-),男,博士,教授,研究方向:中药资源及中药化学,E-mail:dja@njutcm.edu.cn。
国家自然科学基金面上项目(81473538);教育部霍英东教育基金会高等院校青年教师基金项目(141040);江苏高校优势学科建设工程资助项目(ysxk-2014)。
TS
A
1002-0306(2016)01-0000-00
10.13386/j.issn1002-0306.2016.01.000
