在盐酸溶液中[HMIM]BF4对70高碳钢的缓蚀作用和吸附行为
2016-09-01王威淳
王威淳
(湖南工业大学包装新材料与技术重点实验室,湖南 株洲 412007)
在盐酸溶液中[HMIM]BF4对70高碳钢的缓蚀作用和吸附行为
王威淳
(湖南工业大学包装新材料与技术重点实验室,湖南株洲412007)
合成了咪唑类离子液体1-己基-3-甲基咪唑四氟硼酸盐([HMIM]BF4),采用失重法与电化学方法研究了在1 mol/L HCl溶液中对高碳钢(70钢)的缓蚀性能、吸附行为及缓蚀机理。结果表明,[HMIM]BF4具有明显的缓蚀作用,属于混合型缓蚀剂,缓蚀效率随着浓度的增加而增大,随着温度升高而下降。该离子液体在碳钢表面的吸附反应为自发放热过程,且该吸附符合Langmuir吸附等温式,属于同时具有物理吸附和化学吸附的混合吸附。
缓蚀剂;咪唑离子液体;高碳钢;吸附特性;电化学技术
金属材料在现代工农业中占有非常重要的地位。机械、交通、运输、国防和科学技术等各部门都需要大量的金属材料。然而,金属材料在其使用过程中,由于周围环境影响会遭到不同形式的破坏,腐蚀是其中最常见的破坏之一。据统计,每年由于金属腐蚀造成的钢铁损失约占当年钢产量的10%~20%。金属腐蚀事故引起的停产、停电等间接损失就更无法计算[1]。为了解决金属腐蚀的问题,加入缓蚀剂是常用的一种简单有效的方法。相比较于常规的缓蚀剂,离子液体缓蚀剂具有良好的导电性、相对较宽的电化学窗口[2]、生物毒性低、低温活性高、非易燃性、良好的化学和热稳定性[3-4]以及缓蚀效果显著等优良的理化性能,作为新型环保高效缓蚀剂越来越引起人们的关注及研究。离子液体用于碳钢的缓蚀剂研究也取得了很多成果[5-7],不过对于优质碳素钢高碳钢的缓蚀研究相对较少。
1 实 验
1.11-己基-3-甲基咪唑四氟硼酸盐([HMIM]BF4)的合成与表征
离子液体1-己基-3-甲基咪唑四氟硼酸盐([HMIM]BF4)参照文献[8]合成,采用傅里叶变换红外光谱仪(型号Nicolet iS10,美国热电-仪器公司生产)表征。
1.2失重法测量
依次使用800-2400目的金相砂纸将70碳钢试样(3.0 cm×2.0 cm×0.15 cm)打磨至表面呈镜而光泽,再分别经去离子水、丙酮及无水乙醇清洗,干燥,称量。腐蚀介质为1 mol/L HCl溶液,实验前向溶液中通入氮气30 min以除去溶液中的氧气。然后在(298±1)K下,将片状试样静态悬挂于腐蚀介质中,浸泡72 h,取出后用硬毛刷轻轻擦除腐蚀产物,再由去离子水、丙酮及无水乙醇清洗,干燥至恒重后称重。
1.3电化学测试
电化学测试使用仪器为CHI 660B电化学工作站,采用三电极体系,工作电极为碳钢电极,采用环氧树脂封装,工作面积为1 cm2,铂电极及饱和甘汞电极分别为辅助电极与参比电极。测量极化曲线时,在开路电位(OCP)±150 mV的电位范围内,进行动电位扫描测试,扫描频率为1.0 mV·s-1;测量电化学阻抗测试时,电化学扰动信号的幅值为5 mV,频率变化范围为100 kHz~10 mHz。
2 结果与讨论
2.1离子液体的红外光谱
图1为[HMIM]BF4离子液体的红外光谱图。如图1所示,3160 cm-1和3121 cm-1处是咪唑环上 C-H的伸缩振动吸收峰,2933 cm-1和2861 cm-1是侧链上烷基 C-H 的伸缩振动吸收峰,1574 cm-1和1468 cm-1是咪唑环骨架的振动峰,1060 cm-1是BF4-的吸收峰[9]。因此,根据以上特征峰可判断,所合成的产物为[HMIM]BF4离子液体。

图1 [HMIM]BF4的红外光谱Fig.1 FT-IR spectrum (KBr) of [HMIM]BF4
2.2失重法
根据式(1)计算腐蚀速率V(mg·m-2·h-1)[10]。
(1)
式中:ΔW——70碳钢试样在腐蚀介质中的减少的重量,mg
S——试样的表面积,m2
t——试样在腐蚀介质中浸泡的时间,h
再根据式(2)计算腐蚀剂的缓蚀效率ηw(%)[11]。
(2)
式中:V0和V——试样在HCl介质中未加和加有缓蚀剂时的腐蚀速率

表1 (298±1) K下,1.0 M HCl中70碳钢在未加及加有 不同浓度[HMIM]BF4的失重测试结果及缓蚀效率Table 1 Weight loss measurements data and inhibition efficiencies for 70 high-carbon steel immersed in 1.0 M HCl solution without and with various concentrations of [HMIM]BF4 at (298±1) K for 72 h
1.0 mol/L HCl溶液中,70碳钢在未加及加有不同浓度[HMIM]BF4的失重测试结果如表1所示。从表1可知,当[HMIM]BF4的浓度从2 mM增加到10 mM时,腐蚀速率均逐渐降低,缓蚀效率增加。当离子液体的浓度达到10 mM时,缓蚀效率可达82.4%。
2.3极化曲线法
图2为在1 mol/L HCl中,分别加入不同浓度的离子液体([HMIM]BF4)所测定的极化曲线,相关参数如表2所示,结果表明,随着[HMIM]BF4的加入,其对应的腐蚀电流密度(icorr)减小,而腐蚀电位(Ecorr)的变化不明显,说明HCl介质中[HMIM]BF4对70碳钢表现为混合型缓蚀剂。此外,阴极极化曲线的斜率(bc)变化不大,而阳极极化曲线的斜率(ba)值有较大变化,表明缓蚀剂的加入并没有影响70碳钢的阴极的析氢反应机理[12],而是对其阳极腐蚀过程产生了影响。
由表2还可以看出,随着腐蚀介质中加入离子液体([HMIM]BF4)浓度的增加,对应的腐蚀电流密度减小,缓蚀效率增加,缓蚀能力强弱顺序以及对应的缓蚀效率结果与失重测试的结论一致。
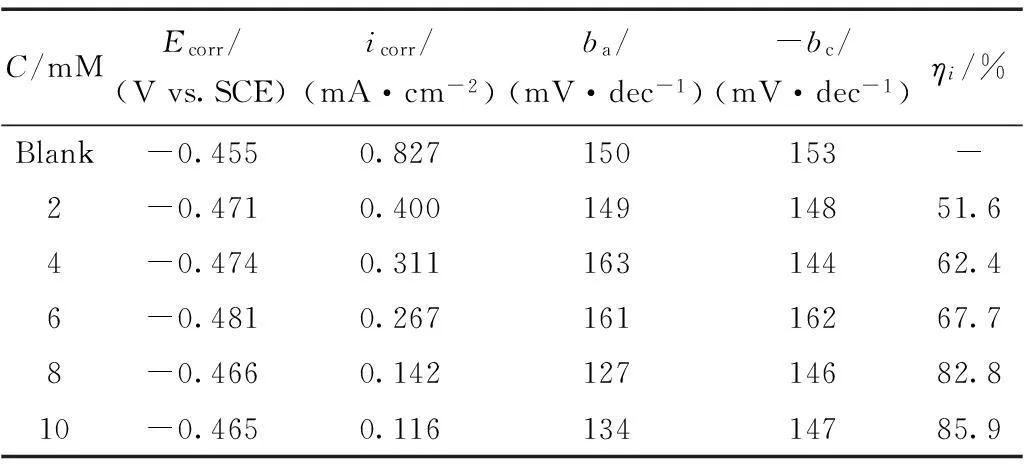
表2 1.0 M HCl中70碳钢在未加和加有不同浓度的 [HMIM]BF4的极化曲线参数及缓蚀效率Table 2 Polarization parameters and inhibition efficiencies for 70 high-carbon steel in 1.0 M HCl solution without and with various concentrations of [HMIM]BF4

图2 1.0 M HCl中70碳钢在未加和加有不同浓度的[HMIM]BF4的极化曲线Fig.2 Polarization curves of 70 high-carbon steel in 1.0 M HCl solution without and with various concentrations of [HMIM]BF4
2.4电化学阻抗法
1.0 mol/L HCl溶液中,70碳钢试样在未加及加有不同浓度的 [HMIM]BF4的交流阻抗曲线如图3所示。采用图4所示的等效电路对交流阻抗图进行拟合分析,相关的参数及缓蚀效率的结果如表3所示。
由Nyquist图(图3a)可知HCl介质中70碳钢在未加和加有不同浓度的[HMIM]BF4的腐蚀反应特征为非标准的容抗弧,且容抗弧的半径随着[HMIM]BF4浓度的增加而增大,表明体系腐蚀电阻增大,意味着腐蚀速率减小。从Bode图(图3b和c)也可以看出,随着离子液体的加入,模值和相位角都随之增大,表明这种离子液体在70碳钢表面的覆盖率随之增加,缓蚀效率增加。
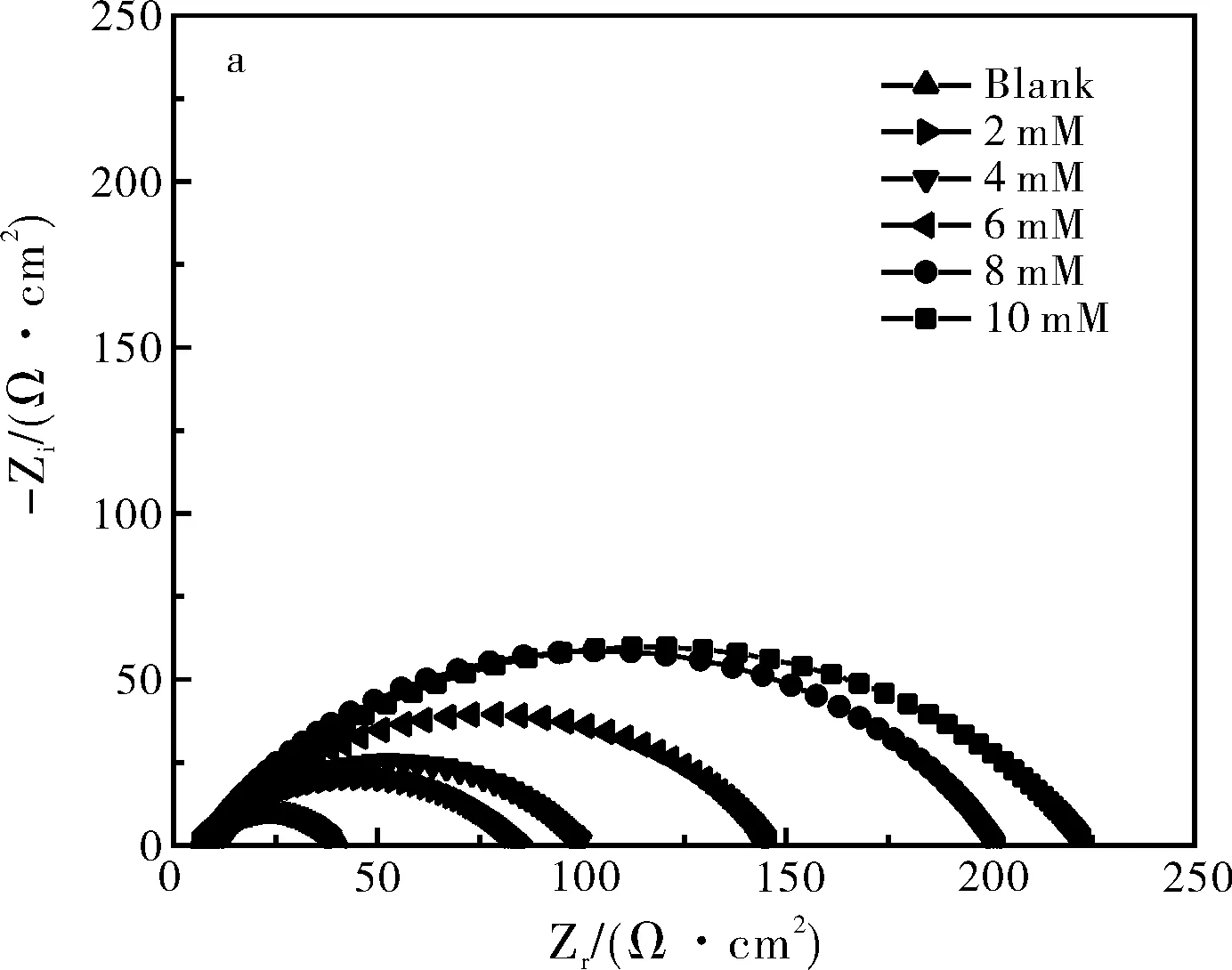
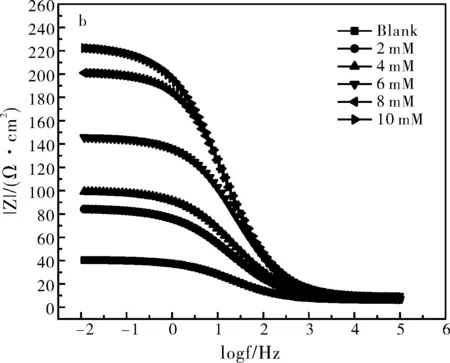

图3 1.0 M HCl中70碳钢在未加和加有不同浓度的[HMIM]BF4的Nyquist图(a),Bode-模值图(b)及Bode-幅值图(c)Fig.3 Nyquist plots of 70 high-carbon steel in 1.0 M HCl solution without and with various concentrations of [HMIM]BF4(a), Bode-magnitude plots (b) and Bode-phase plots (c)
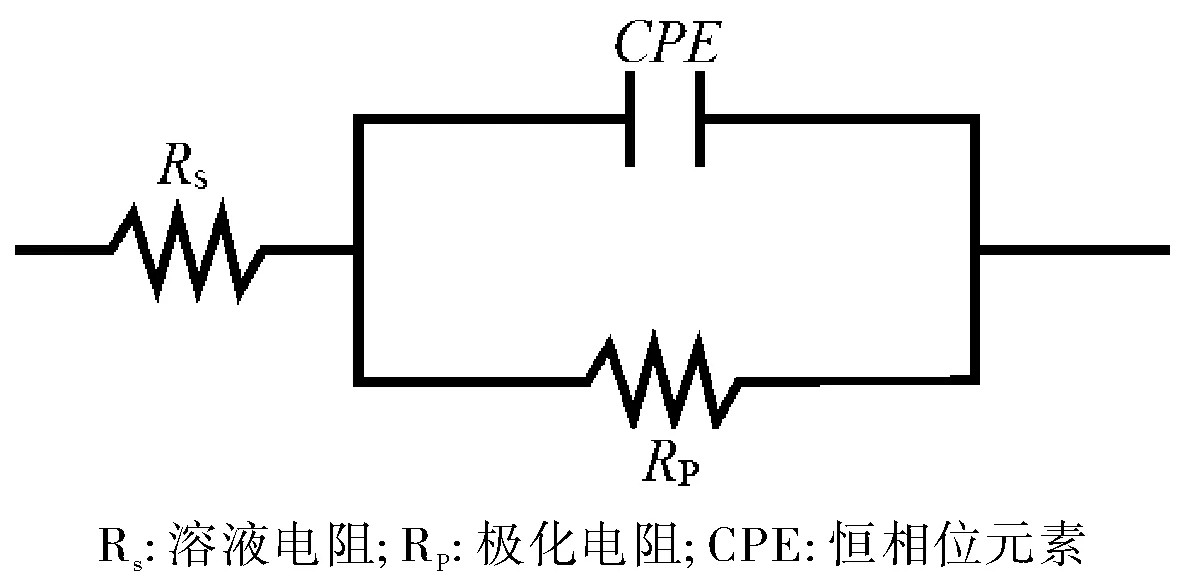
图4 等效电路图Fig.4 Equivalent circuit model
此外,由表3也可以看出,随着离子液体浓度的增加,Rp值变大,表明体系发生腐蚀反应的难度增加,缓蚀效果越好。缓蚀效率与失重及极化曲线测试结果一致。同时双电层电容Cdl值随着离子液体浓度的增加而逐渐减小,是由于缓蚀剂分子的介电常数较低,吸附在70碳钢表面取代了原本吸附在其表面的水分子,使得双电层电容Cdl值减小。在一定范围内,缓蚀剂浓度越高,吸附的缓蚀剂分子越多,Cdl值越小[13]。
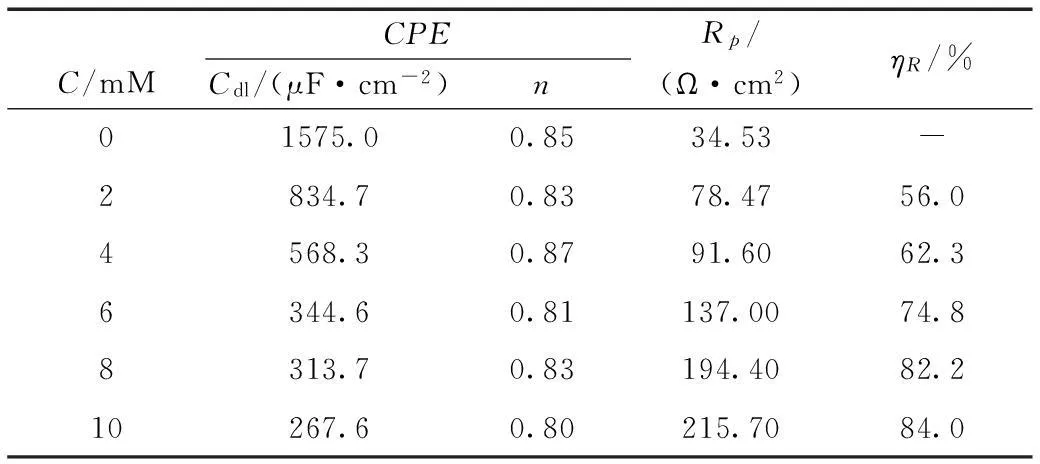
表3 1.0 M HCl中70碳钢在未加和加有不同浓度的 [HMIM]BF4的EIS参数及缓蚀效率Table 3 EIS parameters and inhibition efficiencies for 70 high-carbon steel in 1.0 M HCl solution without and with various concentrations of [HMIM]BF4
2.5离子液体在碳钢表面的吸附行为
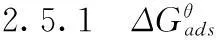
结合表2得到的实验数据,离子液体在70碳钢表面上的覆盖率(θ)可用缓蚀效率(ηi)来近似表示,通过作图拟合,发现C/θ与C之间呈现出如图5所示良好的直线关系。通过与各吸附等温式比较,发现该吸附符合Langmuir吸附等温式[13-14]。
(3)
式中:C——离子液体浓度
θ——离子液体在70碳钢表面的覆盖率
Kads——缓蚀剂分子在70碳钢表面吸附反应的吸附平衡常数
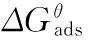
(4)
式中:R——理想气体常数
T——绝对温度
55.5——溶液中水的浓度,mol·L-1
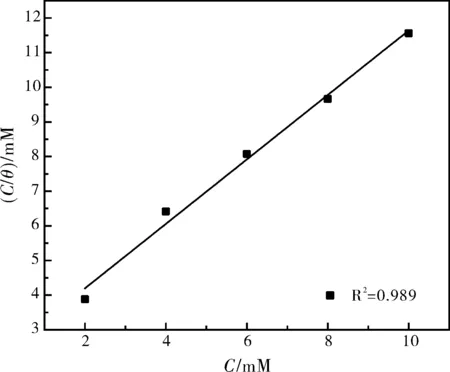
图5 [HMIM]BF4在70碳钢表面的Langmuir吸附等温模型Fig.5 Langmuir adsorption isotherm of [HMIM]BF4 on the 70 high-carbon steel surface in 1.0 M HCl solution at (298±1) K
在不同的温度(303、313、323、333 K)下,1.0 mol/L HCl溶液中,70碳钢在未加和加入10 mM的[HMIM]BF4利用极化曲线所得腐蚀电流密度及对应的缓蚀效率如表4所示。
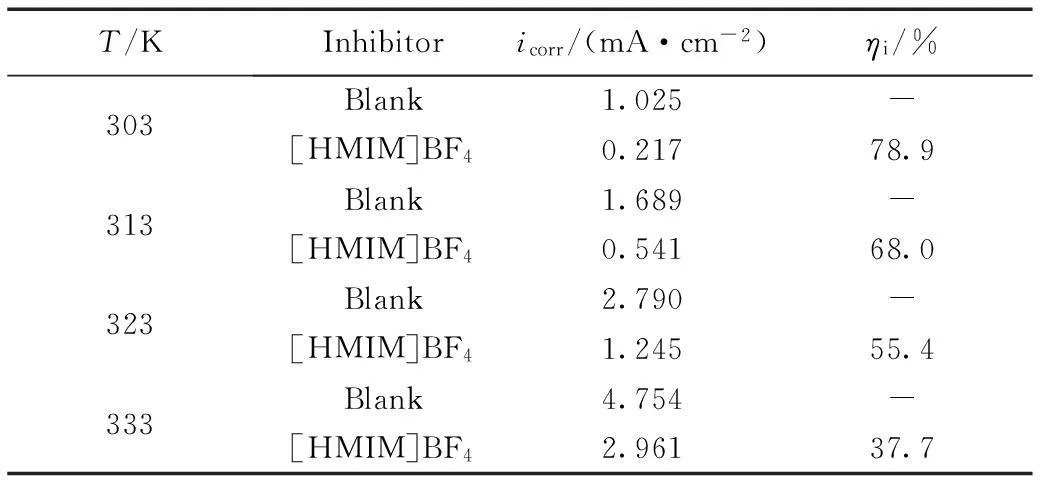
表4 不同温度下1.0 M HCl中70碳钢在未加及加有10 mM [HMIM]BF4的极化曲线参数及缓蚀效率Table 4 Polarization parameters and inhibition efficiency for 70 high-carbon steel in 1.0 M HCl solution without and with 10 mM [HMIM]BF4 at different temperatures
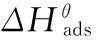
(5)
式中:θ——缓蚀剂在70碳钢表面的覆盖率(θ=ηi)
A1——与温度无关的常数
C——缓蚀剂浓度
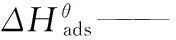
R——理想气体常数
T——绝对温度
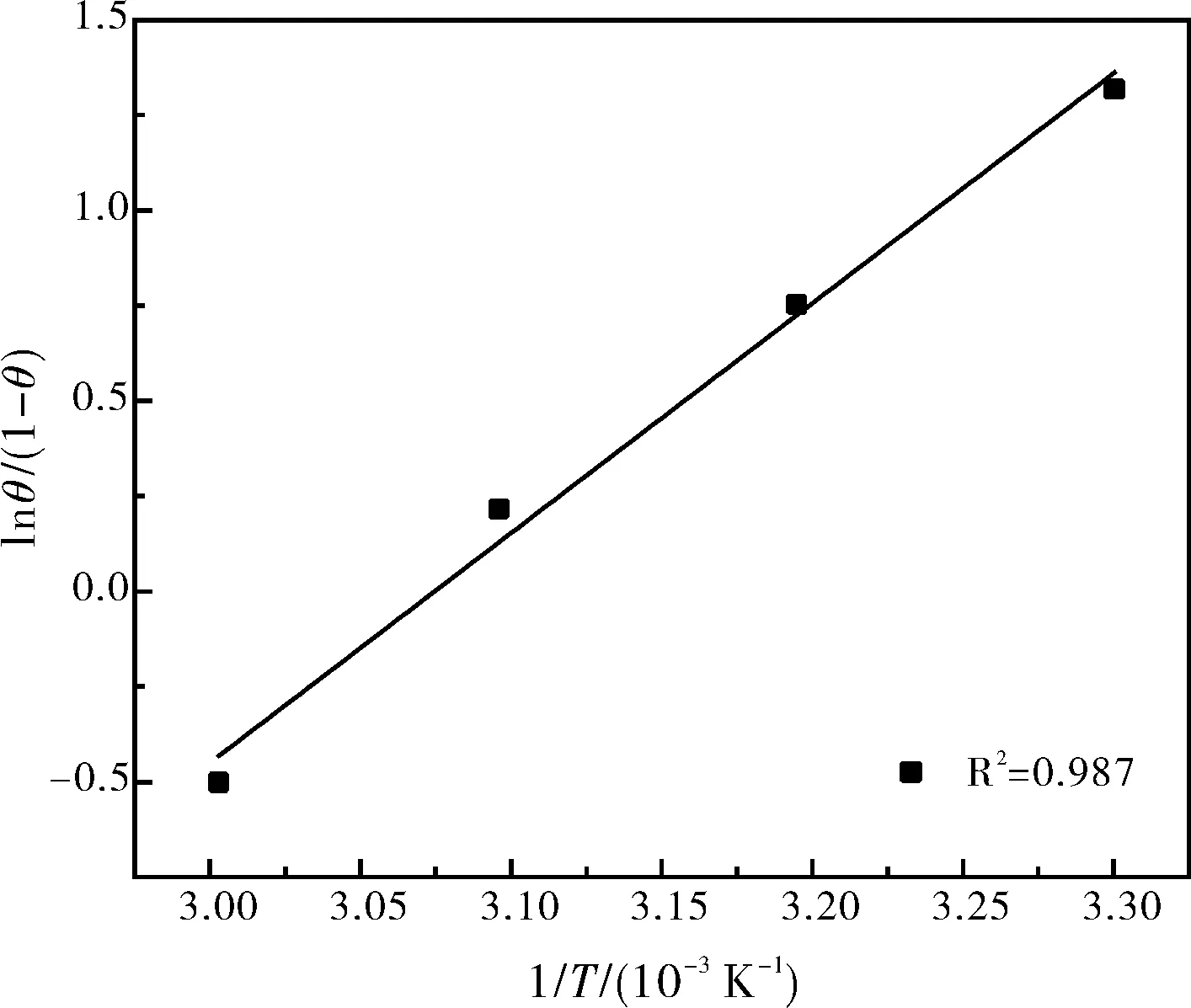
图6 1.0 M HCl中 [HMIM]BF4在70碳钢表面吸附的ln[θ/(1-θ)]与1/T函数关系图Fig.6 Plots of ln[θ/(1-θ)] versus 1/T of 10 mM [HMIM]BF4on the 70 high-carbon steel surface in 1.0 M HCl solution
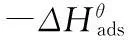
(6)
3 结 论
在1.0 mol/L的HCl溶液中,离子液体[HMIM]BF4对高碳钢70碳钢具有良好的缓蚀作用,属于混合型缓蚀剂,[HMIM]BF4在70碳钢表面的吸附属于同时具有物理吸附和化学吸附的混合吸附,且该吸附满足Lagmuir吸附等温式。吸附过程为自发的放热反应。
[1]张天胜等.缓蚀剂[M].北京:化学工业出版社,2008.
[2]Tsuda T,Hussey C L.Electrochemical applications of room-temperature ionic liquids[J].Electrochemical Society Interface,2007,16(1):42-49.
[3]Zhang Q B,Hua Y X.Corrosion inhibition of mild steel by alkylimidazolium ionic liquids in hydrochloric acid[J].Electrochimica Acta,2009,54(6):1881-1887.
[4]Asefi D,Mahmoodi N M,Arami M.Effect of nonionic co-surfactants on corrosion inhibition effect of cationic gemini surfactant[J].Colloids & Surfaces A Physicochemical & Engineering Aspects,2010,355(s1-3):183-186.
[5]王明,刘静,赵寿典,等.离子液体作为金属缓蚀剂的研究进展[J].煤炭与化工, 2015(2):32-34.
[6]李俊莉,刘世川,卢永斌,等.离子液体对碳钢的缓蚀行为研究进展[J].应用化工, 2015(3):544-548.
[7]屈冠伟,刘静,崔云,等.离子液体缓蚀剂的研究进展[J].煤炭与化工,2014(1):43-45.
[8]王丽华.四氟硼酸盐的合成研究[J].齐齐哈尔大学学报:自然科学版,2008, 24(1):22-24.
[9]冷菁.新型离子液体的缓蚀性能研究[D].南京理工大学,2012.
[10]Bobina M, Kellenberger A,Millet J P, et al.Corrosion resistance of carbon steel in weak acid solutions in the presence of L-histidine as corrosion inhibitor[J]. Corrosion Science,2013,69(4):389-395.
[11]Tian H, Li W,Cao K, et al.Potent inhibition of copper corrosion in neutral chloride media by novel non-toxic thiadiazole derivatives[J].Corrosion Science, 2013,73(73):281-291.
[12]He X,Jiang Y,Li C, et al.Inhibition properties and adsorption behavior of imidazole and 2-phenyl-2-imidazoline on AA5052 in 1.0 M HCl solution[J].Corrosion Science,2014,83(7):124-136.
[13]陈国浩.二氧化碳腐蚀体系缓蚀剂的缓蚀机理及缓蚀协同效应研究[D].北京化工大学, 2012.
[14]齐连惠,张继群.基于神经网络的酰洗缓蚀构效关系研究[J].腐蚀科学与防护技术, 2001(1):24-28.
[15]Zhang F,Tang Y,Cao Z, et al.Performance and theoretical study on corrosion inhibition of 2-(4-pyridyl)-benzimidazole for mild steel in hydrochloric acid[J]. Corrosion Science, 2012, 61(8):1-9.
[16]Atkins,P.W.Atkins' Physical chemistry/[M].Oxford University Press,2006.
[17]徐效陵,黄宝华,刘军,等.盐酸溶液中吡咯烷酮离子液体对碳钢的缓蚀性能[J].中国腐蚀与防护学报,2011,31(5):336-340.
[18]何新快,侯柏龙,江雨妹,等.在H2SO4溶液中咪唑和2-苯基-2-咪唑啉对Cu的缓蚀性能和吸附行为[J].金属学报,2013(8):1017-1024.
Inhibition Property and Adsorption Behavior of [HMIM]BF4on 70 High-carbon Steel in HCl Solution
WANG Wei-chun
(Key Laboratory of New Materials and Technology for Packaging, Hunan UniversityofTechnology,HunanZhuzhou412007,China)
Imidazole ionic liquid 1-hexyl-3-methylimidazolium tetrafluoroborate([HMIM]BF4) was synthesized. Using weight loss method and electrochemical methods, inhibition properties, adsorption behavior and inhibition mechanism of 70 high-carbon steel in 1 mol/L HCl solution were studied. The results showed that [HMIM]BF4had significant inhibition effect, belonged to mixed inhibitor, inhibition efficiency increased with increasing concentration, decreased with increasing temperature. The adsorption reaction of ionic liquid on steel surface was a spontaneous exothermic process, and the adsorption isotherm comply Langmuir belonged simultaneously with mixed physical adsorption and chemical adsorption.
corrosion inhibitor; alkylimidazolium ionic liquid; high-carbon steel; adsorption property; electrochemistry techniques
TG174.42
A
1001-9677(2016)09-0079-04
