高效液相色谱法测定左炔诺孕酮片的溶出度
2016-09-01孙秋商丽丽孙晶晶吉林省白城市食品药品检验所吉林白城37000吉林省药品检验所吉林长春30033
孙秋,商丽丽,孙晶晶.吉林省白城市食品药品检验所,吉林白城 37000;.吉林省药品检验所,吉林长春 30033
高效液相色谱法测定左炔诺孕酮片的溶出度
孙秋1,商丽丽1,孙晶晶2
1.吉林省白城市食品药品检验所,吉林白城137000;2.吉林省药品检验所,吉林长春130033
目的 建立高效液相色谱法测定左炔诺孕酮片的溶出度方法。方法 采用 《中国药典》2015年版四部溶出度测定法第三法,以0.8%十二烷基硫酸钠(SDS)溶液250 mL为溶出介质,转速为75 r/min,取样时间为45 min。采用以Agilent ZORBAX 300-SCX C18为色谱柱,以乙腈-水(60∶40)为流动相,检测波长为240 nm的高效液相色谱法检测溶出量。结果 左炔诺孕酮在0.375~2.625 μg,范围内线性关系良好(r2=1.0);平均回收率为99.53%,RSD为0.85%(n=9);3批样品45 min内的溶出度依次为:100.6%、100.2%和100.5%。结论 该方法符合溶出度方法的建立原则,可控制左炔诺孕酮片的内在质量。
左炔诺孕酮片;高效液相色谱;溶出度;测定
[Abstract]Objective To establish the method of high efficiency liquid chromatography in detecting the dissolution rate of levonorgestrel tabelts.Methods 0.8%lauryl sodium sulfate solution(SDS)were used as the dissolution medium with 75r/ min revolving speed and 45min sampling time according to the third law in the four dissolution spectrophotometry in Chinese pharmacopoeia in 2015,and the dissolution amount was detected by the high efficiency liquid chromatography with the Agilent ZORBAX 300-SCX C18 chromatographic column,acetonitrile-water(60:40)mobile phase and 240nm detection wavelength.Results The linear correlation of levonorgestrel between 0.375-2.625μg was good,r2=1.0,the average recycle rate was 99.53%and RSD was 0.85%,(n=9),the dissolution rates of three batches of samples within 45min were in turn 100.6%,100.2%and 100.5%.Conclusion The method meets the establishment principle of the dissolution method,and it can control the inner quality of levonorgestrel tabelts.
[Key words]Levonorgestrel tabelts;High efficiency liquid chromatography;Dissolution rate;Measurement
左炔诺孕酮片为常用女性口服避孕药,具有较强抑制垂体分泌促性腺激素的作用而抑制排卵;它能使宫颈黏液变稠,阻碍精子穿透,并能使子宫内膜萎缩不利于孕卵着床,从而起到避孕作用。左炔诺孕酮片的现行质量标准收载于《中国药典》2015年版二部。鉴于左炔诺孕酮为难溶性药物,且《中国药典》2015年版二部收载的本品质量标准尚未建立其溶出度检测方法[1]。为了更好地控制该产品质量,该文通过优化色谱条件和溶出介质等研究,建立了左炔诺孕酮片溶出度的HPLC测定方法,并对3批上市产品进行了溶出度的测定。该方法简单、准确、可行,可用于评价该药品质量。
1 材料与方法
1.1材料
1.1.1仪器 RCZ-8M智能溶出仪(天大天发仪器厂),Agilent 1200高效液相色谱仪(美国Agilent公司),SARTORLUS-BP211D型电子分析天平 (赛多利斯公司),KH-700V型超声波清洗器(昆山禾创)等。
1.1.2药品与试剂①对照品:左炔诺孕酮(批号:100083-201510)购于中国药品生物制品检定所;②药品:某厂家生产的左炔诺孕酮片(规格:0.75 mg)3批(批号:140903、141209和150110)③试剂:乙腈:色谱纯(美国),超纯水(自制),其他试剂均为分析纯。
2 方法与结果
2.1溶出条件的选择
2.1.1溶出度测定方法的选择由于本品规格较小,每片仅含0.75 mg左炔诺孕酮,故采用溶出度测定法第三法进行溶出度的检查,采用高效液相色谱法测定其溶出量。
2.1.2溶出介质的筛选本品溶于丙酮,微溶于甲醇和乙醇,不溶于水,该研究参照《中国药典》2015年版二部左炔诺孕酮炔雌醚片项下溶出度测定方法[1],选用0.8%十二烷基硫酸钠溶液250 mL为溶出介质。
2.1.3转速筛选取140903批产品6片,以0.8%十二烷基硫酸钠溶液250 mL为溶出介质,测定时间为45 min,考察本品在转速为75 r/min和100r/min条件下的溶出情况,结果见表1。

表1 样品在不同转速下溶出度比较结果
结果表明:样品在75 r/min与100 r/min的溶出度无明显差异,所以选择75 r/min。
2.2色谱方法的建立
2.2.1检测波长的筛选取本品细粉适量,加流动相制成每1 mL约含左炔诺孕酮7 μg的溶液,在190 nm~400 nm波长范围进行扫描,图谱显示,最大吸收在240 nm处(图1),故选择240 nm为测定波长。
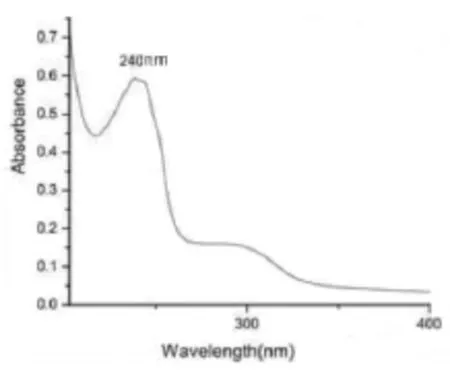
图1 全波长扫描
2.2.2色谱条件及系统适应性色谱柱:Agilent ZORBAX Eclipse XDB-C 18,(250 mm×4.6 mm×5 μm);检测波长:240 nm;柱温:30℃;进样量:20 μL;流动相:乙腈-水(60∶40);流速:1.0 mL/min。理论板数:按左炔诺孕酮峰计算应不低于2000,与相邻峰的分离度不低于1.5,系统适应性色谱图见图2。
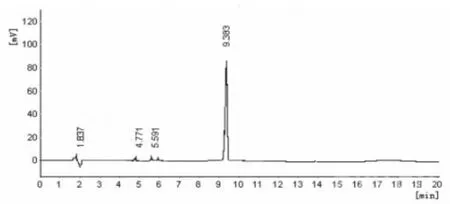
图2 左炔诺孕酮片溶出度测定系统适用性HPLC图
2.3溶液的配制
2.3.1供试品溶液的制备取本品,照溶出度测定法(《中国药典》2015年版四部通则0931第三法),以0.8%十二烷基硫酸钠溶液250 mL为溶出介质,转速为75 r/ min,依法操作,经45 min时,取溶液适量,滤过,取续滤液作为供试品溶液。
2.3.2对照品溶液的制备精密称取左炔诺孕酮对照品适量,加流动相制成每1 mL约含0.075 mg左炔诺孕酮的溶液,摇匀,临用前过0.45 μm的微孔滤膜,即得。
2.3.3溶出介质的制备称取十二烷基硫酸钠8.001 9 g锥形瓶中,加适量水,加热搅拌至溶解,放凉后,用水定容至1 000 mL,摇匀,即得。
2.4专属性试验
取供试品溶液、对照品溶液及溶出介质,按“2.2.2”项下方法分别进样。专属性考察结果见图3。
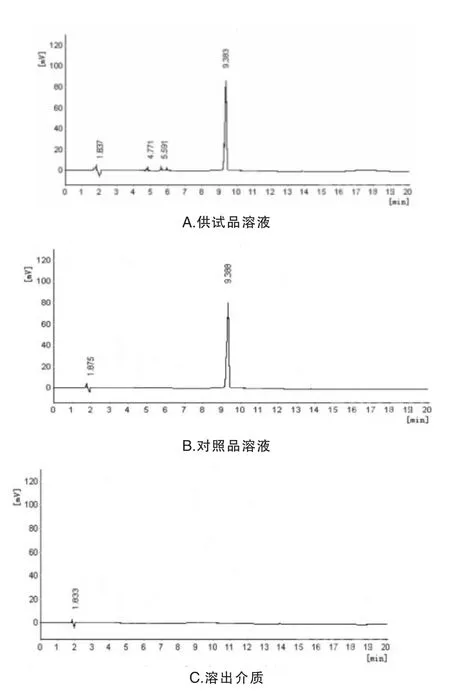
图3 专属性考察色谱图
结果表明,检测波长240 nm,供试品溶液和对照品溶液在相同位置出现主成分色谱峰,溶出介质在主成分位置无色谱峰出现,方法专属性良好。
2.5线性试验
分别精密吸取 “2.3.2”项下对照品溶液5、10、15、20、25、30、35 μL,依次按 “2.2.2”项下色谱条件进行测定,记录色谱图,以进样量(x)为横坐标。峰面积(y)为纵坐标,进行线性回归,得回归方程:y=22248x+56.22,(R2=1)在0.375~2.625 μg范围内,进样量和峰面积呈良好的线性关系。如图4。

图4 左炔诺孕酮含量线性图
2.6精密度试验
精密量取线性试验项下的对照品溶液适量,连续进样6次,每次20 μL,记录色谱图,计算RSD为0.69%,结果表明,本测定精密度良好。
2.7溶液的稳定性试验
取含量线性下的样品溶液,分别于0、5、7、8 h进样20 μL,测定左炔诺孕酮峰面积,计算RSD为0.95%,结果表明:供试品溶液在8 h内稳定性良好。
2.8重复性试验
精密称取样品细粉(批号110401)适量,共6份,加流动相溶解制成每1 μL约含0.075 mg左炔诺孕酮的溶液,摇匀,离心,取上层澄清液,作为供试品溶液。分别精密量取20 μL注入液相色谱仪,记录色谱图,计算RSD为0.77%,结果表明,本方法重复性良好。
2.9回收率试验
根据企业提供的处方,精密称取适量空白辅料,分别加入适量左炔诺孕酮原料,加流动相制成浓度为测定浓度80%、100%和120%的供试品溶液。每个浓度配制样品3份,按 “2.2.2”项下色谱条件进行测定,计算左炔诺孕酮的回收率为99.53%、RSD为0.85%,结果见表2。表明本方法准确度较高。
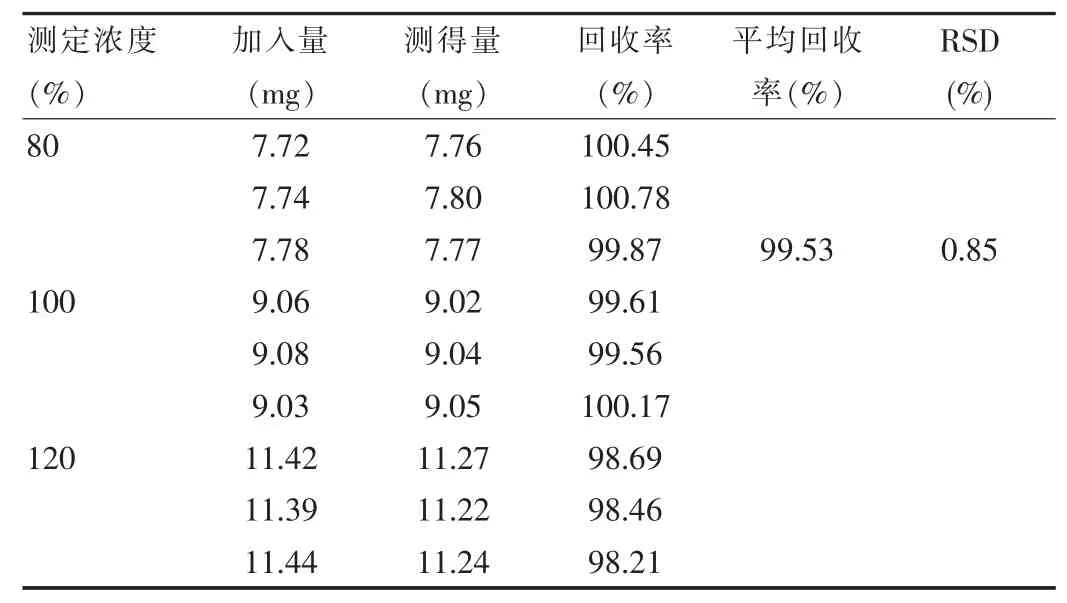
表2 含量测定回收率试验结果
2.10耐用性试验取供试品溶液,按“2.2.2”项下色谱条件,考察供试品溶液在改变色谱柱(Diamonsil C18)、色谱柱温度(25℃、35℃)和流动相比例(55∶45)对分析结果的影响。结果表明,在上述不同条件下,左炔诺孕酮峰面积的RSD为1.46%。
2.11样品溶出度测定取上述3批样品,按“2.3.1”项下方法分别制备供试品溶液,按 “2.2.2”项下色谱条件进行溶出度测定。结果见表3。

表3 三批样品溶出度测定结果
3 讨论
本品规格较小,为0.75 mg,考虑到检测灵敏度,在该研究中,实验者选择小杯法进行溶出度考察,溶剂量为250 mL,能够满足漏槽条件。
由于《中国药典》2015年版二部的左炔诺孕酮片的质量标准中没收载溶出度检查项,而对于口服固体制剂,溶出度是评价药物质量的一个内在指标。作为制剂质量控制的一种手段[2]。该文建立的溶出度测定方法,经方法学验证,此方法可行,回收率良好,对评价该药物制剂的安全和有效性提供了有效的手段。
[1]国家药典委员会编.中华人民共和国药典 (二部)[S].2015年版.中国医药科技出版社,2015:152-153.
[2]李先红.复方左炔诺孕酮片溶出度试验方法的研究[J].襄樊学院学报,2001,22(5):49-52.
High Efficiency Liquid Chromatography in Detecting the Dissolution Rate of Levonorgestrel Tabelts
SUN Qiu1,SHANG Li-li1,SUN Jing-jing2
1.Baicheng Food and Drug Inspection Institute,Baicheng,Jilin Province,137000 China;2.Drug Inspection Institute of Jilin Province,Changchun,Jilin Province,130033 China
R927
A
1672-5654(2016)06(c)-0117-03
10.16659/j.cnki.1672-5654.2016.18.117
孙秋(1983.9-),女,吉林乾安人,本科,主管药师,主要从事药品检验工作。
(2016-04-01)
