135例氟喹诺酮类抗菌药物致不良反应
2016-08-15张益钦谢根英辜雅莉吴小红
张益钦,谢根英,辜雅莉,吴小红
(1.厦门市海沧医院药剂科,福建 厦门 361026; 2.厦门长庚医院药剂科,福建 厦门 361028)
135例氟喹诺酮类抗菌药物致不良反应
张益钦1*,谢根英1,辜雅莉2,吴小红1
(1.厦门市海沧医院药剂科,福建 厦门361026; 2.厦门长庚医院药剂科,福建 厦门361028)
目的:了解氟喹诺酮类抗菌药物在临床应用中的不良反应发生情况,提醒临床警惕该类药物的不良反应,促进合理用药。方法:对厦门市海沧医院2012—2015年药品不良反应监测中心收到的氟喹诺酮类抗菌药物所致的不良反应进行整理和分析。结果:135例发生药品不良反应的患者中,≥60岁36例,占26.67%;涉及3种氟喹诺酮类抗菌药物,主要为莫西沙星,其次为左氧氟沙星,再次为环丙沙星;口服给药73例,静脉给药62例;氟喹诺酮类抗菌药物的主要不良反应为中枢神经系统症状,其次为消化道症状及过敏反应等。结论:氟喹诺酮类抗菌药物引起的不良反应较多,临床应严格根据药品的用法与用量、禁忌证、注意事项、不良反应、联合用药、特殊人群用药等信息使用氟喹诺酮类抗菌药物,密切观察患者病情变化,发现不良反应后及时停药或更换药物并对症处理,提高用药合理性。
氟喹诺酮类; 抗菌药物; 药品不良反应
氟喹诺酮类抗菌药物可选择性地抑制敏感革兰阴性菌DNA回旋酶A亚单位的切割封口活性,同时也能阻断革兰阳性菌的拓扑异构酶Ⅳ的解旋活性,导致细菌死亡而发挥杀菌作用[1]。其具有抗菌谱广、抗菌力强、口服吸收好、组织浓度高、与其他抗菌药物无交叉耐药性、不良反应相对较少等特点,已成为治疗细菌感染性疾病的主要药物。2013年我国抗感染药致严重不良反应报告中,氟喹诺酮类抗菌药物致不良反应报告数排序居第4位,而在国家基本药物致不良反应/事件报告中,左氧氟沙星致不良反应/事件报告数排序居第1位[2]。2014年4月,世界卫生组织发布的《抗生素耐药:全球监测报告》指出,大肠埃希菌对氟喹诺酮类抗菌药物在全球范围内广泛耐药且耐药率高[3]。现对厦门市海沧医院(以下简称“我院”)2012—2015年氟喹诺酮类抗菌药物致不良反应报告进行回顾性统计分析,报告如下。
1 资料与方法
资料来源于2012—2015年我院1 078例药品不良反应报告,其中,抗菌药物引起的不良反应369例,占药品不良反应报告总数的比例最高,为34.23%;氟喹诺酮类抗菌药物致不良反应135例,占药品不良反应报告总数的12.52%,占抗菌药物不良反应报告数的比例最高,为36.59%。根据世界卫生组织乌普萨拉监测中心方法[4]、诺氏评估量表[5],按患者性别、年龄,给药时间、药品种类、给药途径、不良反应症状、处置措施、转归等,对135例氟喹诺酮类抗菌药物致不良反应进行统计分析。
2 结果
2.1氟喹诺酮类抗菌药物致不良反应报告的基本情况
135例使用氟喹诺酮类抗菌药物发生不良反应的患者中,女性73例,男性62例;年龄22~93岁,平均47岁。其中60岁以上患者36例,占氟喹诺酮类抗菌药物致不良反应报告数的26.67%。报告来源方面,门诊82例,住院病房52例,急诊1例。其中113例报告来自呼吸内科,占83.70%,其余来自泌尿外科、消化科等。
2.23种氟喹诺酮类抗菌药物引发不良反应的给药途径分布
我院现有3种氟喹诺酮类抗菌药物,6个品规(左氧氟沙星片及左氧氟沙星注射液、环丙沙星片及环丙沙星注射液、莫西沙星片及莫西沙星注射液)。引发不良反应的氟喹诺酮类抗菌药物主要为莫西沙星和左氧氟沙星,口服给药的病例数稍多于静脉给药,见表1。

表1 3种氟喹诺酮类抗菌药物引发不良反应的给药途径分布Tab 1 Distribution of route of administration of three kinds of fluoroquinolones that induce ADR
2.3氟喹诺酮类抗菌药物各品种致不良反应累及器官和(或)系统分布
135例氟喹诺酮类抗菌药物致不良反应中,轻度109例,中度25例,重度1例。大部分不良反应表现为单一症状,少数表现为多种症状,累及2~3个器官和(或)系统,见表2。其中,神经系统反应最多,以头晕、头痛、失眠、手抖、胡言乱语多见,严重者表现为谵妄、癫痫;其次为消化系统反应,以胃肠道不适(恶心、呕吐、腹痛、腹泻)及氨基转移酶升高多见;再次为变态反应,以全身皮疹、瘙痒为主;另外,心血管系统反应表现为高血压、胸闷、室性心动过速、心悸等,呼吸系统反应表现为气喘、胸闷,血液系统反应表现为血小板减少症、静脉炎,亦有伴随跟腱疼痛。
2.4氟喹诺酮类抗菌药物致不良反应的处理
135例氟喹诺酮类抗菌药物致不良反应中,可耐受的有24例;停药的有49例;更换药物的有43例;减慢给药速度的有4例(滴注速度控制在20~40滴/min以下);对症处理的有15例,如给予双八面体蒙脱石散缓解腹泻、比索洛尔降压、甲泼尼龙缓解皮肤过敏症状等。报告中氟喹诺酮类抗菌药物的用量均为常规治疗剂量。莫西沙星临床1日给药1次;因感染性疾病而接受左氧氟沙星片治疗的患者一般使用剂量为250~750 mg、1日1次,常规500 mg、1日1次,疗程3~7 d,平均疗程5 d。其中1例患者因右下肺炎使用左氧氟沙星注射液750 mg、100 ml/h、静脉滴注,患者出现静脉炎,局部皮肤发红明显,无明显疼痛和瘙痒,减慢滴注速度至60 ml/h后,患者症状消失,可耐受。可见,单次大剂量、快速静脉滴注可引起不良反应,改变给药速度可减少不良反应发生。
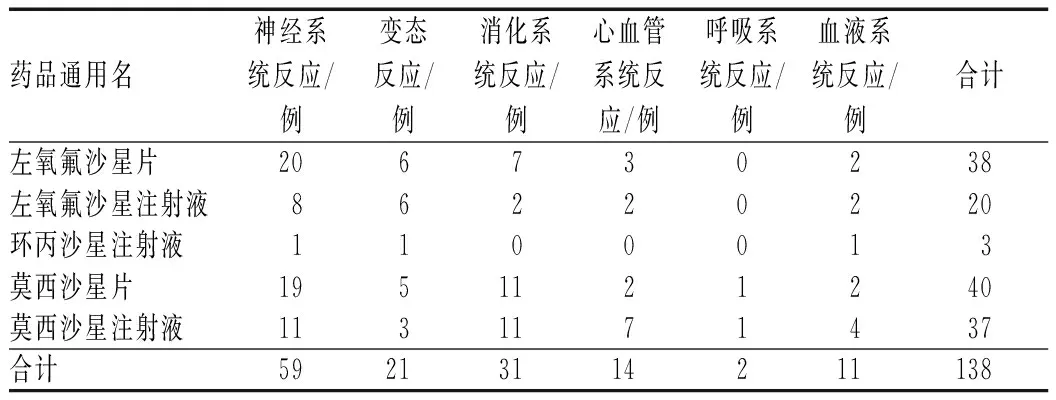
表2 氟喹诺酮类抗菌药物各品种致不良反应累及器官和 (或)系统分布Tab 2 Distribution of ADR induced by different kinds of fluoroquinolones involved organs and(or) system
3 讨论
氟喹诺酮类抗菌药物在临床上主要用于治疗泌尿生殖道、胃肠道、呼吸道及皮肤软组织感染等。近年来,随着临床研究的深入,其临床应用也不断拓宽,但也使对该类药物耐药的菌株产生。根据《抗菌药物临床应用指导原则(2015版)》,左氧氟沙星、莫西沙星等可用于肺炎链球菌和溶血性链球菌所致的急性咽炎和扁桃体炎、中耳炎等,以及肺炎链球菌、支原体、衣原体等所致的社区获得性肺炎(community acquired pneumonia,CAP)。氟喹诺酮类抗菌药物治疗CAP有以下优势:(1)可同时覆盖CAP常见细菌及非典型致病原(肺炎链球菌、肺炎支原体、肺炎衣原体、嗜肺军团菌);(2)单用与β-内酰胺类+大环内酯类抗菌药物的疗效相似,并可降低重症CAP患者的病死率;(3)其药动学/药效学特性允许1日给药1次,更方便施行序贯疗法,如莫西沙星静脉滴注/口服序贯疗法治疗CAP,其效果与头孢曲松+左氧氟沙星相当[6-7]。此外,亦可用于革兰阴性杆菌所致的下呼吸道感染。氟喹诺酮类抗菌药物在尿液或泌尿生殖系统组织中的浓度较高、有效浓度持续时间较长,故可广泛用于泌尿、生殖系统感染;其对志贺菌属所致的肠道感染疗效好,对细菌性腹泻、重症痢疾的治疗效果优于氨基糖苷类及头孢菌素类抗菌药物,是治疗伤寒沙门菌感染的首选药物[8]。
3.1氟喹诺酮类抗菌药物致中枢神经系统不良反应
本调查结果显示,中枢神经系统反应为氟喹诺酮类抗菌药物主要的不良反应,主要表现为头痛、头晕、失眠、手抖,严重者表现为癫痫、谵妄。该类药物因氟原子的引入,脂溶性较强,能透过血-脑脊液屏障进入脑组织,容易引起神经系统不良反应,个别可导致痉挛和癫痫发作。本调查中,引发癫痫2例,其中需急救者1例。该患者既往有癫痫病史,此次因肺部感染给予左氧氟沙星片口服治疗,用药当晚出现癫痫大发作,口吐白沫,并出现深度昏迷,“120”急诊入院给予抗癫痫治疗后好转。另一例患者为80岁老年男性,有脑部外伤史,因肺部感染给予左氧氟沙星注射液0.6 g、静脉滴注,后患者出现精神异常亢奋、胡言乱语,第2日继续静脉滴注仍出现类似情况,故停药并更换药物治疗。氟喹诺酮类抗菌药物可抑制神经递质γ-氨基丁酸与受体结合而使中枢神经兴奋性增高,可导致痉挛和癫痫发作,特别是与茶碱或非甾体抗炎药联用更为常见。临床有脑部外伤、癫痫病史等患者应避免使用氟喹诺酮类抗菌药物。
3.2氟喹诺酮类抗菌药物致消化系统不良反应
本调查中,氟喹诺酮类抗菌药物致胃肠道不良反应及肝肾损害的发生率为22.46%。一般的胃肠道反应为氟喹诺酮类抗菌药物最常见的不良反应,表现为上腹不适、食欲缺乏、嗳气、恶心、呕吐、腹泻及血清氨基转移酶、尿素氮、肌酐升高等[9]。症状一般较轻,停药后可消失。本调查中,中度消化系统反应5例,其中氨基转移酶升高3例,给予硫普罗宁治疗后症状好转,其余2例表现为呕吐、腹泻,对症治疗后好转。
3.3氟喹诺酮类抗菌药物致变态反应
氟喹诺酮类抗菌药物致变态反应主要表现为皮肤损害,瘙痒、皮疹等过敏症状,发生率为15.22%。其中,中度变态反应11例,给予抗过敏药等对症处理后好转。与其他抗菌药物相比,氟喹诺酮类抗菌药物引起的过敏反应发生率较低,且一般不会引起过敏性休克等严重过敏症状。几乎所有氟喹诺酮类抗菌药物都有光毒性,表现为暴露在太阳光下的皮肤区域出现从中度红斑到严重大疱疹,因此,患者服药期间应避免直接暴露于阳光下,一旦发生类似不良反应,停药或更换药物及对症处理后可缓解。
3.4氟喹诺酮类抗菌药物致其他不良反应
(1)药品说明书“警告”项中提示,氟喹诺酮类抗菌药物有致跟腱断裂风险,文献报道强调对>60岁患者、联合应用皮质激素患者以及肾脏、心脏和肺移植患者,该类药物相关跟腱炎和跟腱断裂的风险将进一步增加。患者若出现相关跟腱红肿、疼痛等,应立即停药并就诊。氟喹诺酮类抗菌药物可使QT间期延长,也使QTC延长,进而引发心律失常,表现为血压升高或降低、心动过速,严重者可致心肌梗死等。因此,心脏病及高血压病患者应慎用氟喹诺酮类药物。(2)静脉注射氟喹诺酮类抗菌药物还有可能导致注射部位疼痛及静脉炎。国家食品药品监督管理总局在2013年11月25日发布的第58期药品不良反应信息通报《关于氟喹诺酮类药品的严重不良反应》中提出,应用氟喹诺酮类抗菌药物时应注意以下不良反应的发生:重症肌无力加重、不可逆转的周围神经病变、影响糖尿病患者的血糖控制水平[10]。Chou等[11]共调查了2006—2007年11月78 433例接受抗菌药物治疗的糖尿病患者的相关情况,结果显示,糖尿病患者口服氟喹诺酮类抗菌药物可能是出现血糖异常的原因,其中莫西沙星导致血糖异常的风险最高。(3)新的不良反应:文献报道,氟喹诺酮类抗菌药物有可能引发青光眼[12]、视网膜脱离的风险[13]。
综上所述,氟喹诺酮类抗菌药物虽广泛应用于临床,其致细菌性耐药已被经常报道[14]。临床应加强对抗菌药物合理应用的监管,药师需严格按照药品的用法与用量、禁忌证、注意事项、不良反应、联合用药、特殊人群用药等信息审核处方,临床用药过程中需密切观察患者病情变化,发现不良反应后及时停药或更换药物并对症处理,保障患者安全用药。
[1]李端,殷明.药理学[M].6版.北京,人民卫生出版社,2007:388-389.
[2]国家食品药品监督管理总局.国家药品不良反应监测年度报告(2013年)[EB/OL].[2014-05-14].http://www.sfda.gov.cn/WS01/CL0078/99794.html.
[3]World Health Organization.Drug resistance[EB/OL].[2014-04-30].http://www.who.int/topics/drug_resistance/en.
[4]Uppsala Monitoring Centre of World Health Organization.The use of WHO-UMC system for standardised case causality assessment[EB/OL].http://www.who.int/medicines/areas/quality_safety/safety_efficacy/WHOcausality_assessment.pdf.
[5]Naranjo CA,Busto U,Sellers EM,et al.A method for estimating the probability of adverse drug reactions[J].Clin Pharmacol Ther,1981,30(2):239-245.
[6]Torres A,Garau J,Arvis P,et al.Moxifloxacin monotherapy is effective in hospitalized Patients with community acquired pneumonia: the MOTIV study—a randomized clinical trial[J].Clin Infect Dis,2008,46(10):1499-1509.
[7]彭堃,刘又宁.氟喹诺酮治疗社区获得性肺炎的临床评价[J].中国社区医师,2006,22(2):17-18.
[8]汪复,朱德妹,胡付品,等.2012年中国CHINET细菌耐药性监测[J].中国感染与化疗杂志,2013,13(5):321-330.
[9]杨世杰.药理学[M].2版.北京:人民卫生出版社,2010:421-422.
[10]国家食品药品监督管理总局.药品不良反应信息通报(第58期)关注氟喹诺酮类药品的严重不良反应[EB/OL].[2013-11-25].http://www.sda.gov.cn/WS01/CL0078/94324.html.
[11]Chou HW,Wang JL,Chang CH,et al.Risk of Severe dysglycemia among diabetic patients receiving levofloxacin ciprofloxacin or moxifloxacin in Taiwan[J].Clin Infect Dis,2013,57(7):971-980.
[12]Yang L,Etminan M,Mikelberg FS.Oral fluoroquinolones and risk of glaucoma[J].J Glaucoma,2013,23(7):464-466.
[13]Etminan M,Forooghian F,Brophy JM,et al.Oral fluoroquinolones and the risk of retinal detachment[J].JAMA,2012,307(13):1414-1419.
[14]汪复,张婴元.实用抗感染治疗学[M].2版.北京:人民卫生出版社,2012:397-398.
135 Cases of Adverse Drug Reactions Induced by Fluoroquinolones Antibiotics
ZHANG Yiqin1, XIE Genying1, GU Yali2, WU Xiaohong1
(1.Dept.of Pharmacy, Xiamen Haicang Hospital, Fujian Xiamen 361026, China; 2.Dept.of Pharmacy, Xiamen Changgeng Hospital, Fujian Xiamen 361028, China)
OBJECTIVE:To investigate the occurrence of adverse drug reactions(ADR) induced by fluoroquinolones antibiotics in clinic, so as to provide some tips for the clinic to attach more importance to the adverse drug reactions and promote the rational drug use. METHODS: ADR cases induced by fluoroquinolones antibiotics
by ADR monitoring center of Xiamen Haicang Hospital during 2012-2015 were statistically analyzed. RESULTS: Of the 135 cases, 36 cases were ≥60 years old, accounting for 26.67%; including three kinds of fluoroquinolones antibiotics, and moxifloxacin dominated the first place, followed by levofloxacin and ciprofloxacin. 73 cases were induced by oral administration, and 62 cases were induced by intravenous administration. The main manifestations of ADR induced by fluoroquinolones antibiotics were central nervous system symptoms, followed by gastrointestinal symptoms and anaphylactic reactions, etc.. CONCLUSIONS: The incidence of ADR induced by fluoroquinolones antibiotics is relatively high, the clinic should strictly apply fluoroquinolones antibiotics according to the information of usage and dosage, contraindications, matters need attention, ADR, drug combination and medication of special crowd. Meanwhile, the clinic should closely observe the changes of patients’ conditions, timely withdrawal drugs and give symptomatic treatment to the patients, so as to improve the rationality of drug use.
Fluoroquinolones; Antibiotics; ADR
2016-02-16)
R969.3;R978.1
A
1672-2124(2016)07-0986-03
10.14009/j.issn.1672-2124.2016.07.045
*主管药师。研究方向:临床药学、药物咨询。E-mail:56939071@qq.com
