QuEChERS-GC-MS/MS测定饮料中邻苯二甲酸酯
2016-08-06曹慧陈小珍张东雷郑军科浙江省质量检测科学研究院浙江杭州310018
曹慧,陈小珍,张东雷,郑军科(浙江省质量检测科学研究院,浙江杭州310018)
QuEChERS-GC-MS/MS测定饮料中邻苯二甲酸酯
曹慧,陈小珍,张东雷,郑军科
(浙江省质量检测科学研究院,浙江杭州310018)
采用QuEChERS-气相色谱/三重四极杆质谱(GC/MS/MS)同时测定饮料中17种邻苯二甲酸酯类塑化剂。样品经正己烷提取,基质分散固相萃取净化,采用气相色谱-质谱/质谱法测定,外标法定量。17种邻苯二甲酸酯在各自的线性范围内(5 μg/L~1 000 μg/L)线性关系良好,线性相关系数在0.99以上,添加10、50和200 μg/kg 3个不同浓度水平,含乳饮料中17种邻苯二甲酸酯的平均回收率在80.9%~108.7%,相对标准偏差在0.2%~14.2%,果汁饮料中17种邻苯二甲酸酯的平均回收率在81.4%~110.2%,相对标准偏差在1.3%~13.0%,检出限和定量下限分别为1.5 μg/kg~3.0 μg/kg 和5.0μg/kg~10.0μg/kg。该方法灵敏度高、重现性好、结果准确可靠,适合饮料中邻苯二甲酸酯类塑化剂的检测。
QuEChERS;邻苯二甲酸酯类;塑化剂;气相色谱/三重四极杆质谱;饮料
邻苯二甲酸酯类塑化剂是一类重要的化工产品添加剂,被广泛应用于包装材料中[1]。邻苯二甲酸酯分子结构与激素类似并可以模拟雌激素效应,会干扰神经、免疫和内分泌系统的正常调节,对人体健康造成危害,具有致突变、致癌和致畸性。
目前,文献报道关于邻苯二甲酸酯类塑化剂测定的方法有微生物法[2]、气相色谱[3-5]和气相色谱-质谱法[6-9]、液相色谱[10-12]和液相色谱-串联质谱法[13-15],而国家标准的测定方法为气相色谱-质谱法。上述方法存在着较多弊端,微生物法、气相色谱和液相色谱法存在着假阳性确诊困难等缺点;气相色谱-单四极杆质谱的选择性较差,结果仍存在着假阳性等风险;液相色谱串联质谱法具有定性准确、灵敏度高等优点,但是液相系统的管路本底较高,很难准确定量。另外,国家标准的前处理方法较简单,采用质谱检测时,基质效应强,定量困难。本文采用QuEChERS(快速quick、简单easy、便宜cheap、有效effective、可靠rugged、安全safe)-气相色谱-三重四极杆串联质谱技术建立饮料中17种邻苯二甲酸酯类塑化剂的检测方法,通过串联质谱的高选择性反应监测技术,实现17种邻苯二甲酸酯类塑化剂二级质谱同时分析。
1 材料与方法
1.1材料与试剂
17种邻苯二甲酸酯混合标准品:邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二异丁酯(DIBP)、邻苯二甲酸二(2-甲氧基)乙酯(DMEP)、邻苯二甲酸二(4-甲基-2-戊基)酯(BMPP)、邻苯二甲酸二(2-乙氧基)乙酯(DEEP)、邻苯二甲酸丁基苄基酯(BBP)、邻苯二甲酸二己酯(DHXP)、邻苯二甲酸二戊酯(DPP)、邻苯二甲酸二(2-丁氧基)乙酯(DBEP)、邻苯二甲酸二环己酯(DCHP)、邻苯二甲酸二(2-乙基)己酯(DEHP)、邻苯二甲酸二苯酯(DPhP)、邻苯二甲酸二正辛酯(DNOP)、邻苯二甲酸二异壬酯(DINP)、邻苯二甲酸二壬酯(DNP):浓度均为1 000 μg/mL,迪马科技有限公司。
邻苯二甲酸酯混合标准溶液的配制:吸取液体标样100μL,用正己烷稀释定容到10mL,配制成10μg/mL的储备液,密封储存于4℃冰箱中,备用,再用正己烷稀释成混合标准使用液。
正己烷:色谱纯,美国TEDIA公司产品;PSA吸附剂:上海安谱科学仪器有限公司;无水硫酸镁:分析纯,国药集团化学试剂有限公司,使用前马弗炉内进行高温烘烤。
1.2仪器设备
TSQ Quantum GC气相色谱-质谱/质谱联用仪:美国Thermo Fisher Scientific公司。
1.3样品预处理
1.3.1提取
取5.0 mL试样于玻璃离心管中,加入5 mL正己烷,振荡摇匀,静置后在4 000 r/min离心5 min,移取上清液待净化处理。
1.3.2净化
将上清液转移至另一根玻璃试管中,加入50 mgPSA(乙二胺-N-丙基)和200mg无水MgSO4,涡旋2 min,静置后取上清液进行气相色谱-质谱/质谱分析测定。
1.4气相色谱-质谱/质谱分析
1.4.1色谱条件
色谱柱:DB-5石英毛细管色谱柱(30 m×0.25 mm× 0.25 μm);升温程序:60℃保持1 min,以20℃/min升至220℃,保持1 min,再以3℃/min升至280℃,保持4 min;进样口温度为280℃;载气为高纯氦气(99.999%),氦气流速为1.0 mL/min。
1.4.2质谱条件
电子轰击(EI)离子源,离子源温度为250℃,电离能量为70 eV;GC-MS传输线温度为280℃;灯丝电流为50 μA;Q2碰撞气为Ar(1.5 mTorr)。
2 结果与讨论
2.1母离子和子离子的选择
在EI离子化模式下,通过全扫描方式找出各种目标化合物的碎片离子,根据丰度比确定母离子。选择子离子扫描方式,调节碰撞能量,选取碰撞后丰度较高的两个子离子分别作为定量和定性离子,并确定其最佳碰撞能量的电压值。表1为最终确定的母离子、子离子和碰撞能量等参数。
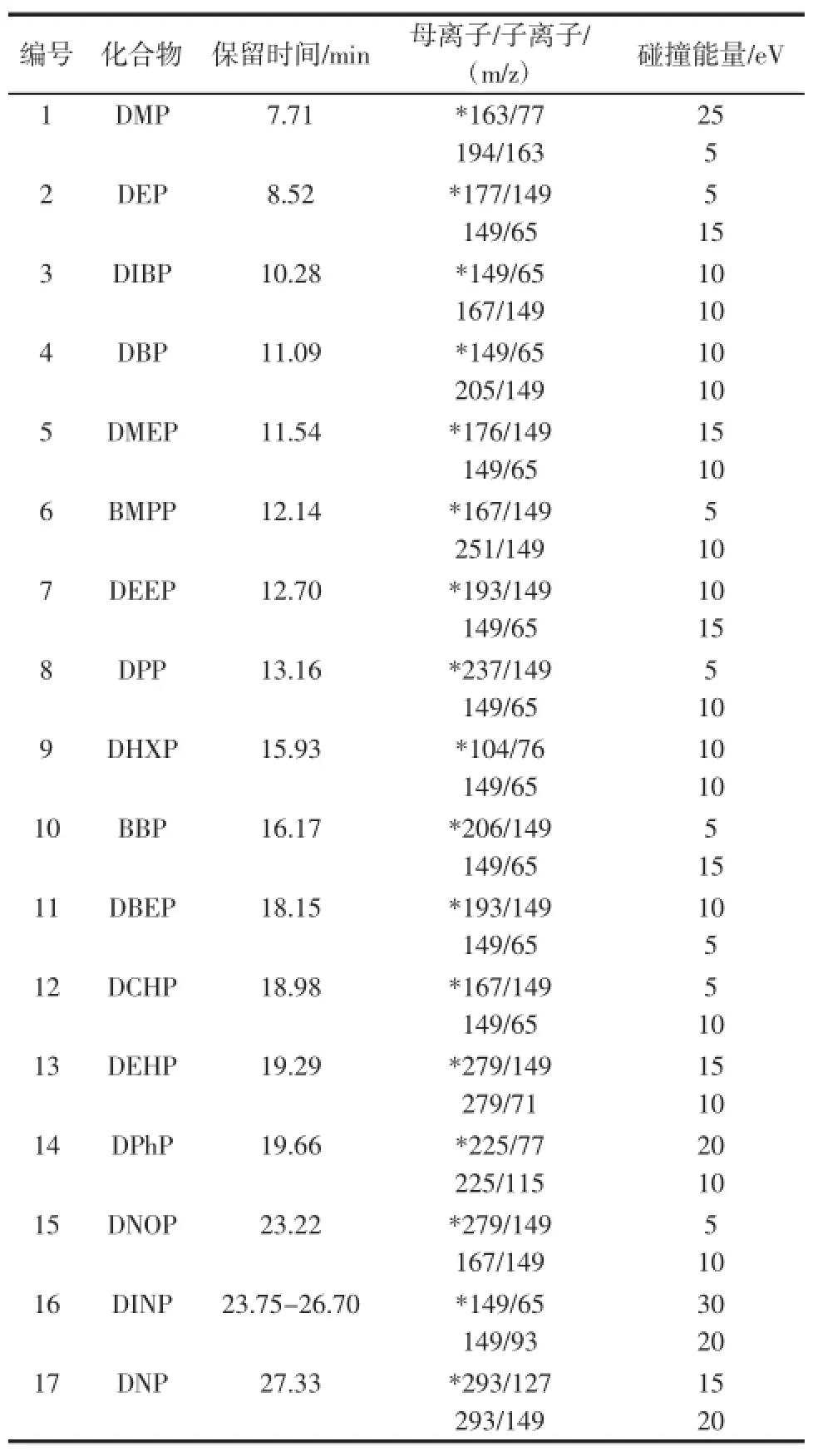
表1 17种邻苯二甲酸酯的保留时间、母离子、子离子和碰撞能量Table 1 Retention time,precursorion,production and collision energy of 17 phthalate esters
2.2基质效应
质谱分析中,基质效应普遍存在,且串联质谱的基质效应一般强于单四极杆质谱。为了研究净化处理后17种邻苯二甲酸酯的基质效应,分别用正己烷和含乳饮料空白样品处理液稀释了一系列的标准溶液,分别进行气相色谱-质谱/质谱测定。以基质标准曲线斜率与正己烷标准曲线的斜率比值评估基质效应。试验结果表明:17种邻苯二甲酸酯的斜率比值在0.81~ 1.04,说明样品经基质分散固相萃取净化后,基质效应已基本消除。但是考虑到样品间的基质差异较大,本试验采用空白基质提取液配制标样以进行定量分析。
2.3线性范围、检出限和定量限
取浓度分别为5、10、50、100、250、500、1 000 μg/L系列标准溶液曲线,经气相色谱-质谱/质谱测试得到标准曲线、相应的线性回归方程和相关系数,见表2。
结果表明:17种邻苯二甲酸酯在5μg/L~1000μg/L的浓度范围内具有良好的线性关系,相关系数r2为0.9902~0.998 1。分别按3倍信噪比和10倍信噪比计算得到17种邻苯二甲酸酯化合物的检出限和定量限。2.4方法的回收率和精密度
在空白的含乳饮料和果汁饮料基质中添加10、50、200 μg/kg 3个浓度水平的混合标准溶液,按1.3试验方法进行前处理,结果如表3所示。
结果表明:含乳饮料中17种邻苯二甲酸酯的回收率为80.9%~108.7%,相对标准偏差为0.2%~14.2%;果汁饮料中17种邻苯二甲酸酯的回收率为81.4%~110.2%,相对标准偏差为1.3%~13.0%。
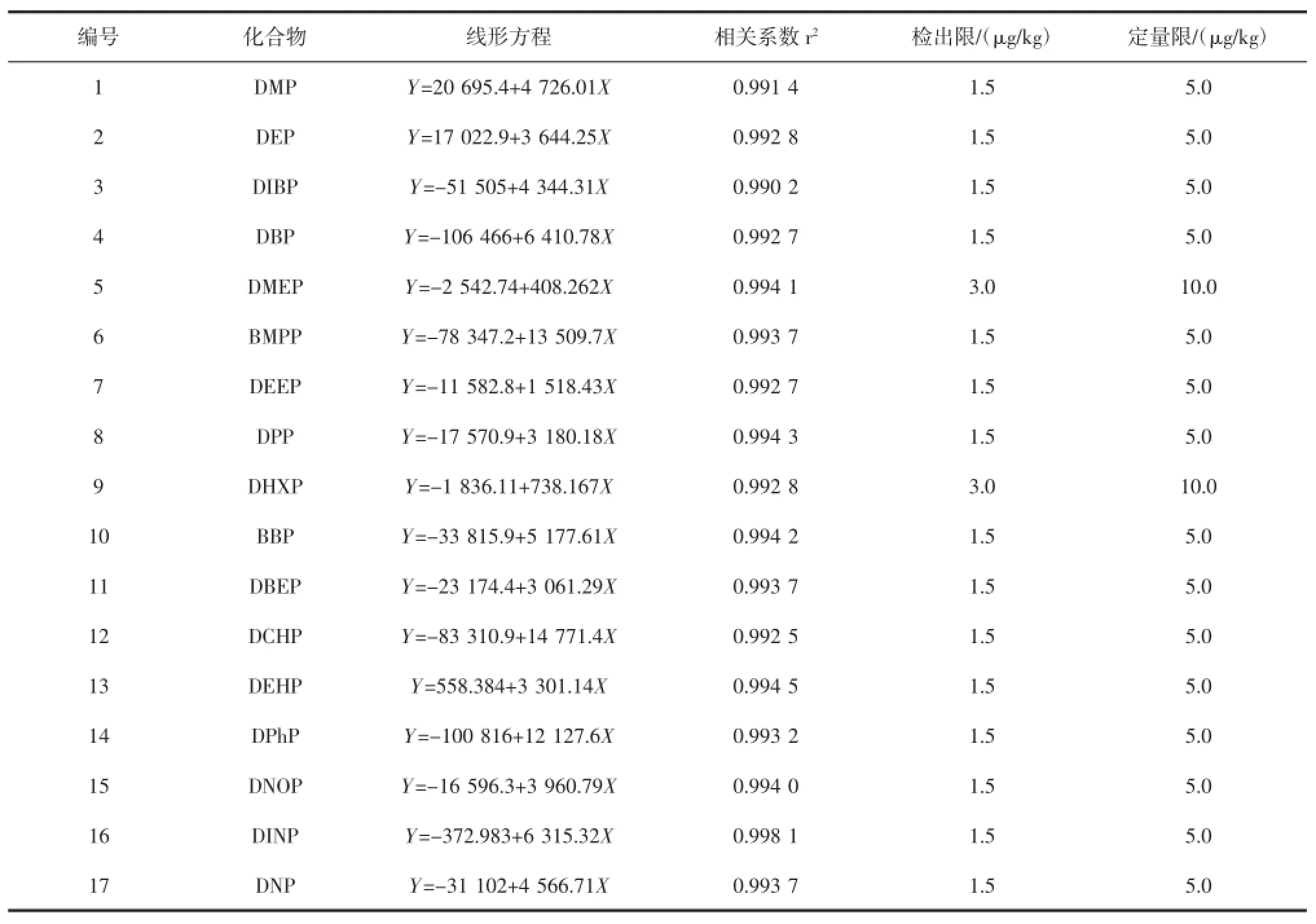
表2 17种邻苯二甲酸酯的线性方程、相关系数、检出限和定量限Table 2 Linear equations,correlation coefficients,LOD and LOQ of 17 phthalate esters
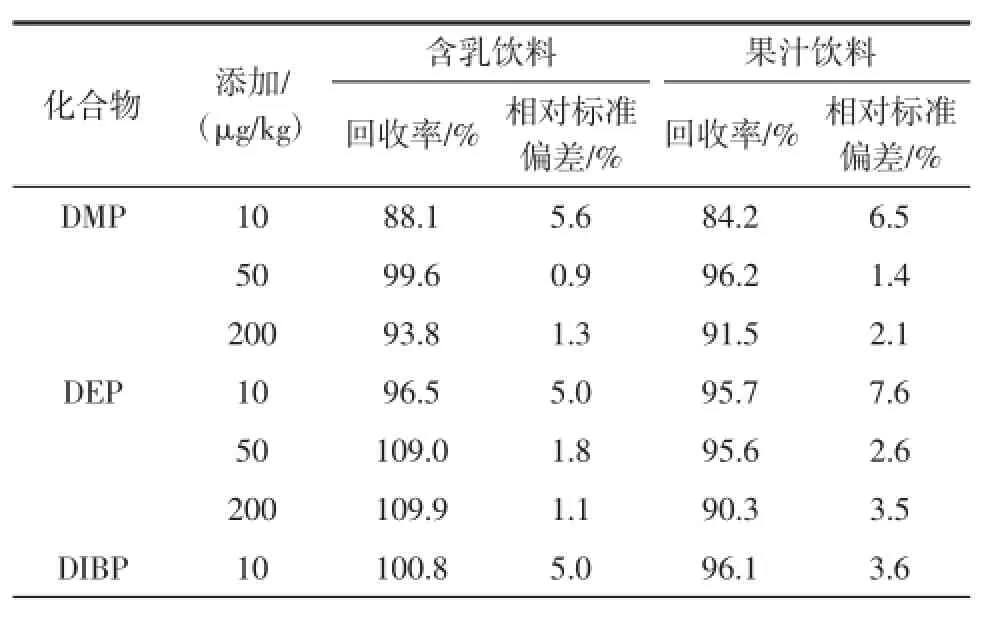
表3 17种邻苯二甲酸酯的回收率和相对标准偏差Table 3 The recoveries and RSD of 17 phthalate esters

续表3 17种邻苯二甲酸酯的回收率和相对标准偏差Continue table 3 The recoveries and RSD of 17 phthalate esters
3 结论
本研究利用QuEChERS-气相色谱-三重四极杆质谱仪,对含乳饮料和果汁饮料中的17种邻苯二甲酸酯同时进行分析。该方法前处理简单,净化效果好,回收率稳定,适合饮料中邻苯二甲酸酯的分析测试。与传统的标准检测方法相比,由于串联质谱选择性强,有效地避免了假阳性的可能,有效地保证了定性和定量结果的可靠性;由于串联质谱具有高选择性反应监测的特点,灵敏度高,定量结果能完全满足现有检测标准的要求。
[1]宋继霞,杨正慧,陈乐群.食品中邻苯二甲酸酯类塑化剂的测定及迁移研究进展[J].化学分析计量,2013,22(1):100-102
[2]万宇平,陶光灿,李勇,等.邻苯二甲酸二丁酯(塑化剂)ELISA检测方法的研究[J].食品工业,2013,34(9):194-196
[3]周宜斌,周庆.气相色谱法快速测定白酒中邻苯二甲酸酯残留量[J].中国药师,2013,16(9):1362-1363
[4]廖艳,余煜棉,赖子尼,等.气相色谱法测定6种邻苯二甲酸酯痕量组分的固相萃取条件研究[J].化学试剂,2010,32(3):239-242
[5]戚文炜,朱培瑜,吴薇.液液萃取/气相色谱法测定环境水样中邻苯二甲酸酯类化合物[J].干旱环境检测,2006,20(4):196-198
[6]邓莉,郝学财.分散固相萃取技术分析油脂类食品中塑化剂含量[J].分析化学,2013,41(7):1037-1043
[7]苗宏健,梁栋,鲁杰,等.气相色谱-串联质谱法测定白酒中18种邻苯二甲酸酯[J].中国食品卫生杂志,2014,26(3):249-254
[8]石凤琼,柯常亮,林钦,等.气相色谱-质谱法测定水产品中15种邻苯二甲酸酯类塑化剂的残留量[J].分析测试学报,2013,32 (8):915-922
[9]薛亮,梅雯芳.气相质谱法测定食品中塑化剂DPRP和HEP[J].食品工业,2014,35(6):266-269
[10]佟晓波,李莹,娇筱曼,等.HPLC法测定化妆品中十六种邻苯二甲酸酯类化合物[J].香料香精化妆品,2012,6(3):33-35
[11]马燕玲,陈令新.超声辅助分散液液微萃取-高效液相色谱测定水样中的4种邻苯二甲酸酯类增塑剂[J].色谱,2013,31(2):155-161
[12]张会军,张敬轩,李辉,等.凝胶渗透色谱-高效液相色谱法对辣椒酱中14种邻苯二甲酸酯的同时检测[J].食品科学,2011,32 (4):152-154
[13]刘红河,黄晓群,王晖,等.高效液相色谱-串联质谱法测定食品中邻苯二甲酸酯[J].现代预防医学,2008,35(1):119-121
[14]李拥军,熊文明,陈坚文,等.固相萃取/高效液相色谱-串联质谱法测定罗非鱼中9种邻苯二甲酸酯[J].分析测试学报,2012,31(3):278-283
[15]徐敦明,郑向华,杨黎忠,等.液相色谱-串联质谱法测定饮料中邻苯二甲酸二(2-乙基)己酯和邻苯二甲酸二异壬酯[J].分析化学,2012,40(2):304-308
Determination of 17 PAEs in Drinks by QuEChERS and GC-MS/MS
CAO Hui,CHEN Xiao-zhen,ZHANG Dong-lei,ZHENG Jun-ke
(Zhejiang Institute of Quality Inspection Science,Hangzhou 310018,Zhejiang,China)
A method was developed for determination of 17 phthalate esters residues in drinks using QuEChERS and gas chromatography-tandem mass spectrometry(GC/MS/MS).The samples were extracted with n-hexane and cleaned up with dispersive-solid phase extraction.The extracts were determined by GC/MS/MS using external standard method.The linearity of the method was good between 5 μg/L and 1000 μg/L.In milk beverage,the mean recoveries at the three spiked levels of 10,50,200 μg/kg were 80.9%-108.7%,the relative standard deviation(RSD)were 0.2%-14.2%.In fruit drink,the mean recoveries at the three spiked levels of 10,50,200 μg/kg were 81.4%-110.2%,the relative standard deviation(RSD)were 1.3%-13.0%.The detection limits and quantitation limits were 1.5 μg/kg-3.0 μg/kg and 5.0 μg/kg-10.0 μg/kg respectively.The simplicity,sensitivity and good precision of the method made it be well suitable for determination of phthalate esters residues in drinks.
QuEChERS;phthalate esters;plasticizer;gas chromatography-tandem mass spectrometry(GC/ MS/MS);drinks
10.3969/j.issn.1005-6521.2016.10.030
浙江省质量技术监督系统科研计划资助(20150204)
曹慧(1980—),女(汉),高级工程师,博士,主要从事食品检测和科研工作。
2015-04-10
