环孢素软胶囊溶出度H PLC检测方法改进研究
2016-08-04刘虹赵海鹏李源陈燕
刘虹 赵海鹏 李源 陈燕
(潍坊市食品药品检验检测中心,山东 潍坊 261205)
环孢素软胶囊溶出度H PLC检测方法改进研究
刘虹赵海鹏李源陈燕
(潍坊市食品药品检验检测中心,山东 潍坊 261205)
目的:对环孢素软胶囊溶出度检测高效液相色谱(HPLC)方法进行改进。方法:采用浆法,含0.1 mol/L HCl的0.5%十二烷基磺酸钠为溶出介质,转速75 rpm,分别于第15,30,45,60,75,90 min取样,测定4个厂家产品的溶出度,绘制溶出曲线。HPLC色谱条件为:C8(2)柱(4.6 mm×250 mm,5 μm);0.1%三氟乙酸∶四氢呋喃∶乙腈∶0.5%三乙胺(磷酸调pH为2.4)(20∶25∶40∶15)为流动相,柱温60℃,流速1.0 mL/min;检测波长210 nm。结果:本方法线性范围为5~ 100 μg/mL,定量限、检测限分别为2.6,0.86 μg/mL。4个厂家的样品在90 min内溶出度均超过标示量的80%,但溶出曲线存在明显差别。结论:本方法准确、可靠,灵敏度高,能够区分不同厂家产品的溶出特征,适用于环孢素软胶囊溶出度的检测。
环孢素软胶囊;溶出度;高效液相色谱法
环孢素是一种环肽类免疫抑制剂,主要用于预防组织器官移植的排斥反应及自身免疫性疾病。根据国家食品药品监督管理总局网站查询结果,目前国内批准上市的环孢素制剂已达14家,剂型主要为软胶囊制剂。环孢素存在环孢素H、异环孢素A等多种杂质,且环孢素在高效液相色谱(HPLC)系统中存在构象异构体变换。其软胶囊则含有表面活性剂及中长链油脂等亲油性内容物。上述杂质、构象异构体及内容物的存在对其溶出度的测定均存在干扰,影响检测结果的准确性。
《中国药典》未收录环孢素软胶囊质量标准,部颁标准WS1-(-144)2004Z[1]未对其溶出度检测作出规定。目前国内尚缺乏关于环孢素软胶囊溶出度检测方法的文献报道,本文参考国内外质量标准[2]及文献方法[3-4]对环孢素软胶囊溶出度测定的HPLC检测方法进行了研究,建立的HPLC方法专属性强、灵敏度高、准确度和重复性好、方法简便,有利于环孢素软胶囊的质量控制和监管。
1仪器和试药
1.1仪器
美国Agilent1200型高效液相色谱仪(G1310A泵,G1316A柱温箱,G1329A自动进样器,G1314 BVWD紫外检测器),XS-205型电子分析天平(Mettler-Toledo公司),ZRS-6G药物溶出实验仪(天津市天大天发科技有限公司),PHS-3C型精密pH计(上海精密科学仪器有限公司)。
1.2试药
环孢素对照品(中国食品药品检定研究院,批号:130495-200202);环孢素软胶囊(规格:25 mg)由N、H、C、S 4家公司提供(批号:S057,140502HB,110902201,11171023)。三氟乙酸、四氢呋喃、乙腈、三乙胺为色谱纯,水为超纯水。其余试剂为分析纯。
2色谱条件与方法
2.1色谱条件与系统适用性
色谱柱:Phenomenex LunaC8(2)色谱柱(4.6 mm×250 mm,5 μm);流动相:0.1%三氟乙酸∶四氢呋喃∶乙腈∶0.5%三乙胺(磷酸调pH为2.4)(20∶25∶40∶15);柱温:60℃;流速:1.0 mL/min;检测波长:210 nm;进样量:10 μL。理论塔板数按环孢素峰计算不低于2 000,环孢素峰与相邻峰的分离度不低于1.7,重复进样的相对标准偏差不大于2.0%[3]。
2.2溶液制备
2.2.1供试品溶液制备取本品,照溶出度与释放度测定法(《中国药典》2015年版四部通则 0931第二法),以含 0.1 mol/L HCl的0.5%十二烷基磺酸钠(sodium dodecyl sulfonate,SDS)水溶液1 000 mL为溶出介质,转速为75 rpm,依法操作,经45 min取溶液适量,滤过,取续滤液作为供试品溶液。
2.2.2对照品溶液制备精密称取环孢素对照品,加“2.2.1”项下溶出介质溶解,分别稀释制成2,5,15,30,60,100,140 μg/mL浓度的溶液。
2.2.3空白辅料溶液制备各厂家辅料存在差异,因此以4个厂家的常见辅料:明胶、无水乙醇、玉米油、1,2-丙二醇、甘油、聚氧乙烯氢化蓖麻油、单硬脂酸甘油酯、山梨醇等为辅料,依处方量按“2.1.1”项供试品溶液制备方法配制空白辅料溶液。
2.3样品测定
精密量取供试品溶液及对照品溶液各10 μL注入液相色谱仪,记录色谱图,按外标法以峰面积计算出对应时间点每粒胶囊的溶出度,绘制溶出曲线。
3方法学考察
3.1检测条件考察
3.1.1色谱柱的选择《中国药典》2015年版[5]、《美国药典》[2]HPLC测定环孢素软胶囊含量的色谱柱为C18柱,柱温需要达到70~ 80℃。试验中发现,按照《美国药典》[2]色谱条件测定环孢素软胶囊溶出度时,主峰与共洗脱峰无法有效分离;采用C8柱可将主峰与共洗脱峰有效分离。结果见图1。3.1.2柱温的选择试验中对不同温度下(55,60,65,70℃)环孢素软胶囊的峰形进行了考察,结果见图2。环孢素主峰峰形随温度升高趋于尖锐。65,70℃下,主峰与共洗脱峰未能有效分离;55℃下主峰与共洗脱峰分离效果较好,但理论塔板数低于700,分离效率较低。因此本实验选用60℃柱温进行溶出度测定。
3.1.3流动相的选择国内外药品标准[1,2,5]及文献[3-4]用于环孢素含量测定的流动相包括乙腈-水-叔丁基甲醚-磷酸(430∶520∶50∶1)、四氢呋喃-水(80∶20)等。试验中发现采用上述流动相普遍存在环孢素峰出峰晚(12~ 15 min)及峰形拖尾问题。因此本文对流动相组成进行调整,加入三乙胺作为扫尾剂,并对流动相配比进行了考察,结果表明,采用“2.1”项下流动相可使环孢素主峰出峰时间缩短至7.2 min(见图1~ 2),平均峰宽为0.55,环孢素主峰与相邻峰的分离度为(1.7± 0.2);平均拖尾因子为1.04。

图1 溶出介质中环孢素软胶囊的HPLC色谱图
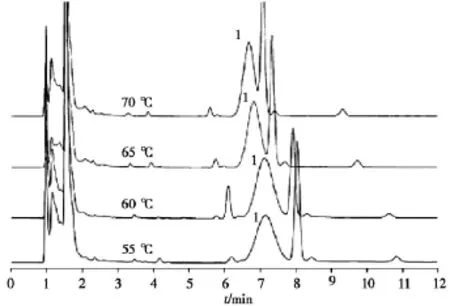
图2 不同温度下溶出介质中环孢素软胶囊的HPLC色谱图
3.1.4溶出介质的选择《美国药典》[2]中环孢素胶囊剂溶出度测定所用介质为水或含 0.1 mol/L HCl的0.5%SDS水溶液。试验中比较了环孢素软胶囊在超纯水和含0.1 mol/L HCl的0.5%SDS水溶液两种介质中的色谱分离行为。结果见图3。在超纯水中,环孢素主峰与共洗脱峰未能有效分离;在含0.1 mol/L HCl的0.5%SDS水溶液中,环孢素主峰与共洗脱峰可有效分离,因此选用含0.1 mol/L HCl的0.5%SDS水溶液作为溶出介质。
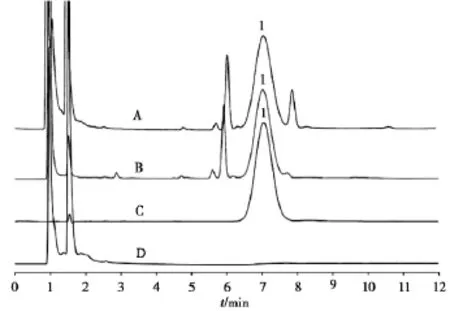
图3 环孢素及软胶囊在不同溶出介质中的色谱图
3.1.5溶出方法及转速的选择《美国药典》[2]中环孢素软胶囊溶出度测定采用浆法,转速为50 rpm。试验中考察了蓝法(50,75 rpm)和浆法(50,75 rpm)的溶出曲线,结果见图4。4种条件下,环孢素软胶囊在45 min内均可达到溶出平台。其中浆法75 rpm溶出曲线更为理想且能够区分不同厂家产品的溶出曲线。
3.2方法学考察
3.2.1专属性试验分别依次取对照品溶液、供试品溶液和空白辅料溶液按“2.1”项下色谱条件进样分析,色谱图见图5,可见空白辅料不干扰环孢素的测定。

图4 不同溶出方法和转速下环孢素软胶囊的溶出曲线

图5 对照品(A)、供试品(B)及空白辅料(C)HPLC色谱图
3.2.2线性范围及标准曲线取“2.2.2”项下不同浓度的对照品溶液,注入液相色谱,以环孢素浓度(μg/mL)对峰面积进行线性回归(图6)。线性方程为:
Y=35.75X+185(R2=0.999 9),
线性范围为5~ 100 μg/mL。
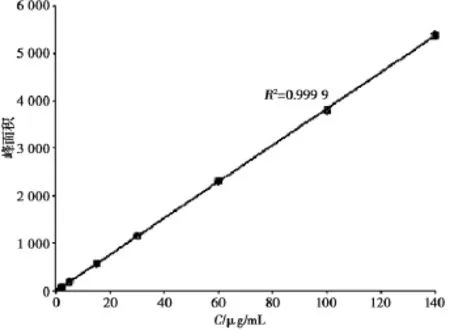
图6 环孢素含量测定标准曲线
3.2.3精密度试验日内精密度:取对照品适量,按“2.2.2”项下方法配成 20,40,80 μg/mL的溶液,每隔2 h测定一次,连续测定5次,记录峰面积并计算5次峰面积的 RSD;日间精密度:取上述溶液,每日同一时间测定1次,连续测定3天,记录峰面积并计算3次峰面积的RSD。结果见表1。
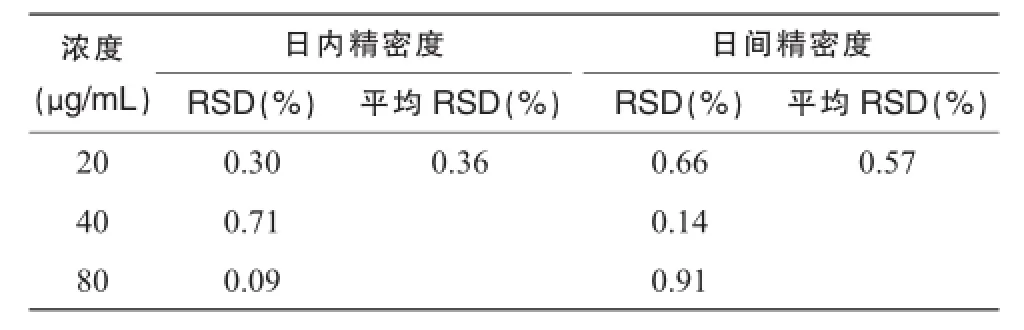
表1 环孢素在流动相中的日内及日间精密度
3.2.4稳定性试验取“2.2.1”项下供试品溶液1份,依法分别于0,3,6,9,12,24 h进样分析,结果环孢素峰面积的RSD为0.26% (n=6),表明环孢素溶液在24 h内稳定。
3.2.5回收率试验按处方量的 80%,100%,120%精密称取环孢素对照品20,25,30 mg各 3份,加入处方量辅料,溶出介质溶解,容量瓶中定容至500 mL,摇匀、静置。精密吸取上清液 1 mL 于 10 mL容量瓶中,溶出介质稀释至刻度,过滤,取续滤液 10 μL注入液相色谱仪,记录色谱图,测定峰面积,计算回收率及 RSD。结果见表2。
3.2.6定量限和检测限取“2.2.1”项下对照品,配成系列浓度的溶液,取上述溶液各10 μL注入液相色谱仪,依法测定。信噪比S/N=10时,环孢素浓度为2.6 μg/mL,当信噪比S/N=3时,环孢素浓度为0.86 μg/mL。因此该法的定量限和检测限分别为2.6 μg/mL和0.86 μg/mL。
4结果与结论
取4个厂家的环孢素软胶囊样品,照溶出度与释放度测定法(《中国药典》2015年版四部通则0931第二法),以“2.2.1”项下溶出介质1 000 mL为介质,转速为75 rpm,依法操作,分别于第15,30,45,60,75,90 min取溶液适量,滤过,取续滤液作为供试品溶液。另精密称取环孢素对照品适量,加溶出介质溶解并稀释制成与供试品溶液相同浓度的溶液,作为对照品溶液。分别精密量取上述两种溶液各 10 μL,照“2.1”项下色谱条件测定,并按外标法以峰面积计算每粒的溶出量。限度为90 min内溶出度不低于标示量的80%[2]。
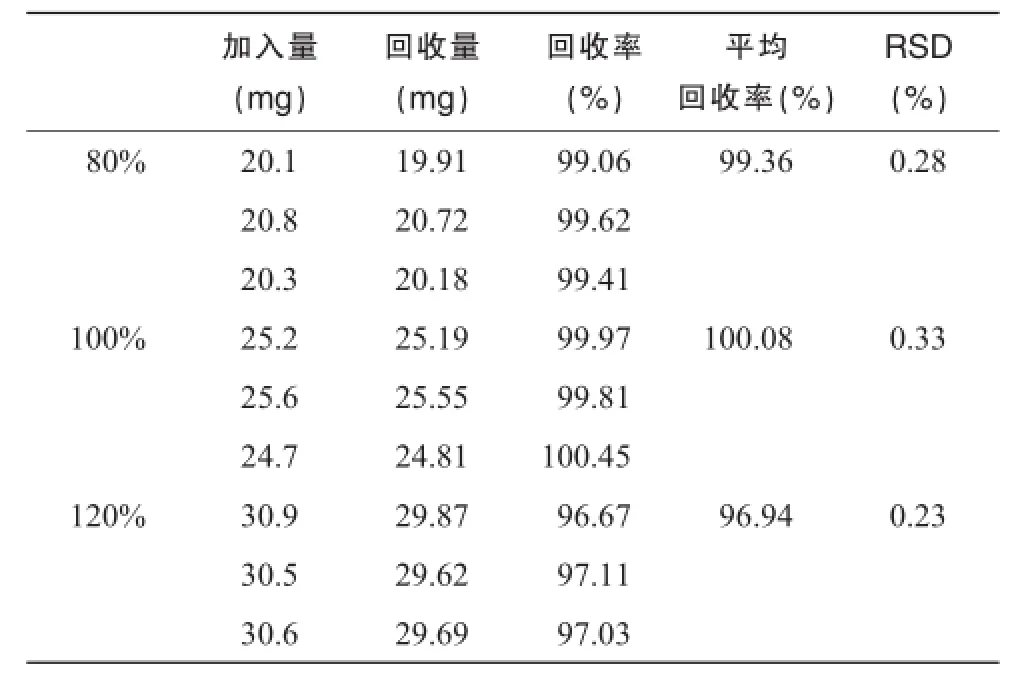
表2 环孢素回收率试验结果
依法测定,同批次样品均测定6次(n=6),计算各时间点的溶出度(%),结果见图7。
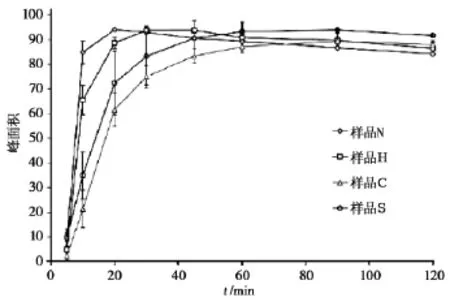
图7 不同样品的溶出曲线
由图可见,4种样品在90 min内的溶出度均超过标示量的80%,符合《美国药典》[2]标准要求,但4种样品溶出速度存在显著差异,样品达到标示量80%的速度依次为N>H>S>C。通过溶出曲线可见,4种样品溶出度达到最值后其曲线均存在轻微下行趋势,可能是由于环孢素降解所致。
5讨论
环孢素治疗指数较窄[6],治疗剂量与毒性剂量接近。其体外溶出行为的差异对药物体内吸收、药效及毒性造成的影响相比其他药物更为显著。由于我国尚缺乏环孢素制剂的溶出度测定法定标准,本文参考国外药典标准[2]及文献对环孢素软胶囊的溶出度测定方法进行了改进研究,并对不同厂家环孢素软胶囊的溶出曲线进行了比较研究。
《美国药典》[2]中环孢素胶囊含量测定常用 C18柱,柱温普遍高于70℃,导致色谱柱寿命缩短,仅能维持2~ 4周[7]。本文比较了C18与C8两种色谱柱对环孢素软胶囊主药及辅料的分离效果。结果表明,C8在较低温度下仍能够实现主药及辅料的有效分离,且在本色谱条件下主药出峰时间较快,有利于延长色谱柱寿命,缩短分析时间。《美国药典》环孢素胶囊溶出度测定转速为 50 rpm,指标为90 min内药物溶出度,本次实验研究表明,所测样品在45 min内溶出度均可超过标示量的80%,因此上述标准存在偏低的问题。
仿制药质量一致性评价是目前我国药品监管的主要工作之一。我国已发布《普通口服固体制剂溶出曲线测定与比较指导原则》,旨在通过体外溶出度试验确认药品质量和疗效的一致性。本研究采用建立的HPLC方法对不同厂家产品的溶出度进行了测定,虽然所测样品的溶出度均符合要求,但其溶出曲线存在明显差异,原研厂家产品(N)的溶出速度快于国产品种(C、H、S),而国产品种之间的溶出速度也存在明显差别。上述溶出速度的差异可能是导致临床疗效差异的原因之一。
由于不同厂家环孢素软胶囊辅料配方及配比可能存在不同,进而导致溶出度产生差异。而本研究的HPLC方法中,空白辅料溶液的选取可能无法反映不同厂家产品辅料的差异,因此,本HPLC方法的专属性试验可能存在一定的局限。
综上,本实验建立的环孢素软胶囊溶出度HPLC检测方法能够有效解决环孢素主峰展宽及辅料干扰问题,主峰出峰时间快,方法准确、精密、具有较宽的线性范围,相比现有方法,能够在较低温度下实现环孢素软胶囊溶出度测定,且能够区分不同厂家产品的溶出曲线,适用于环孢素软胶囊溶出度检查和评价。
[1] 国家药典委员会.新药转正标准(55册)[M].北京:人民卫生出版社,2008:53.
[2] 美国药典委员会.美国药典[S].VSP35-NF30.北京:化学工业出版社,2011:2794-2795.
[3] 刘浩,仇士林.HPLC法测定环孢素胶囊中环孢素及降解产物的含量[J].中国抗生素杂志,2002,27(4):227-231.
[4]庞文哲,宋更申,王茉莉.HPLC法同时测定环孢素注射液的含量和有关物质[J].中国药房,2015,26(3):399-401.
[5]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2015:583-584.
[6] 孟金薇,司继刚,袁姜.高效液相色谱法测定环孢素A血药浓度的方法改进[J].中国药业,2003,12(9):38.
Improvement of HPLC Method for Determination of Dissolution of Ciclospor in Soft Capsules
Liu Hong,Zhao Haipeng,Li Yuan,Chen Yan
(Weifang Institute for Food and Drug Control,Shandong Weifang 261205,China)
Objective:To improve the HPLC method for determination of dissolution of ciclosporin soft capsules.Methods:The paddle method was adopted using 0.5%sodium dodecyl sulfonate containing 0.1 mol/L HCl as a media at a rotation rate of 75 rpm.Samples were taken from the products of manufacturers at time points(15,30,45,60,75 and 90 min)and determined for dissolution,based on which a dissolution curve was plotted.HPLC was performed with C8(2)column(4.6 mm×250 mm,5 μm)at a column temperature of 60℃,using the mixture of 0.1%trifluoroacetic acid,tetrahydrofuran,acetonitrile and 0.5%triethylamine(20∶25∶40∶15,adjusted to pH 2.4 using phosphoric acid)as mobile phase at a flow rate of 1.0 mL/min.The wavelength for detection was 210 nm.Results:The linear range of the method was 5~ 100 μg/mL,while the quantitation and detection limits were 2.6 and 0.86 μg/mL,respectively.All the dissolutions of samples from four manufacturers within 90 min were more than 80%of the stated amount.However,the dissolution curves of the samples showed significant difference.Conclusion:The HPLC method was accurate,reliable and highly sensitive,which distinguished the dissolution characters of products from various manufacturers,and was suitable for the determination of dissolution of ciclosporin soft capsules.
Ciclosporin Soft Capsules;Dissolution;HPLC
10.3969/j.issn.1672-5433.2016.04.003
刘虹,女,主管药师。研究方向:药品检验。通讯作者E-mail:liuhong1969@163.com
2016-01-07)
