关于硫酸性质与应用的系列问题(3)
——硫酸应用中的一些问题释疑
2016-07-28北京王笃年
◇ 北京 王笃年
笃年老师问与答
关于硫酸性质与应用的系列问题(3)
——硫酸应用中的一些问题释疑
◇北京王笃年
8) 用浓硫酸与NaCl反应可以制得HCl,这是否说明H2SO4酸性比盐酸强?
实验室制取HCl的方法之一是利用浓硫酸与固体食盐混合加热:
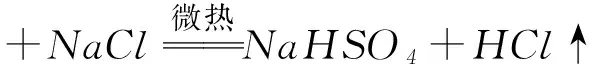
或

并不能依据该反应说硫酸的酸性比盐酸强.因为该反应的推动力是熵增(固体与液体反应产生气体物质),硫酸所表现的性质只是酸性和难挥发性.如果这个说法不能令人信服,可以接着看下面的反应:
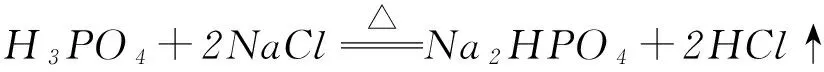
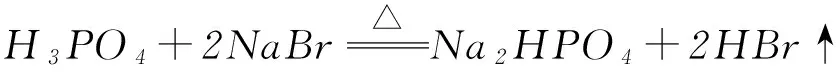
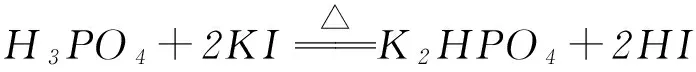
盐酸、氢溴酸、氢碘酸都属于典型的强酸,而磷酸只是一种中等强度的酸,我们不能根据这些反应就说磷酸的酸性比盐酸、氢溴酸、氢碘酸都强,上述反应的推动力也是熵增效应,磷酸所表现的性质是酸性与难挥发性.
9) 为什么用浓硫酸制取HNO3时只能微热生成NaHSO4而不能生成Na2SO4?
用浓硫酸制取HCl、HF等物质时,可以通过加热使硫酸分子中的2个H都转化为挥发性酸:
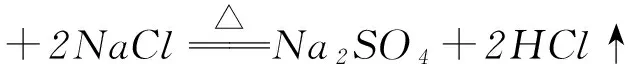
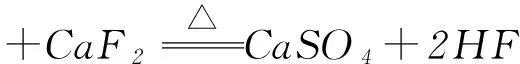
而实验室里用硫酸与NaNO3反应制取HNO3时,化学方程式却只能写成

这与硝酸的不稳定性有关,硝酸受热易分解,而若要使硫酸的第2个氢电离发挥作用,温度要达到500℃以上,这样的温度下硝酸就会分解殆尽,最终得不到HNO3.
10) 浓硫酸具有强氧化性,为什么却能用来干燥还原性气体H2、CO和SO2?
浓硫酸是常用的气体干燥剂,然而它具有强氧化性,所以不能用浓硫酸干燥H2S、HI、HBr等还原性气体.然而H2、CO、SO2气体都是广泛使用的气体还原剂,为什么却可以用浓硫酸干燥呢?
观察总结H2、CO作为还原剂时的反应条件可知,它们都是在加热或高温状态下发挥其还原性的.这是为什么呢?这与H2、CO的分子结构比较牢固有关.我们知道,分子参加化学反应的前提是旧的化学键被破坏,CO分子内2个原子通过三键连接,键能很大(1076kJ·mol-1),故分子不易拆开;氢气分子内2个原子间虽然只是共价单键连接,但是这个单键键长太短,导致键能很大(436kJ·mol-1),分子结构也非常稳定.所以常温下,H2、CO都不容易被氧化,故而可以用浓硫酸干燥.SO2虽然具有强还原性,但因为硫元素常见价态有-2、0、+4、+6价,假设硫酸将SO2氧化,则只能是SO2氧化为H2SO4而H2SO4还原为SO2,最终结果是反应物和产物都没有变化.自然界里,这样的“反应”实际上是不会发生的.所以说,硫酸并不能氧化SO2气体.
11) 硫酸能不能干燥NO、乙烯?
都不能.实验事实表明,NO通入浓硫酸后会全部被吸收.目前尚没有找到明确的文献说明,但根据NO分子结构及有关化合物(亚硝酰硫酸NOHSO4)存在的资料可以猜测,吸收原理无非有如下2个方面:一是简单的溶解吸收,因为NO是极性分子,根据相似相溶原理,它应该可以溶解于极性溶剂硫酸之中;二是化学反应,NO具有很强的还原性而硫酸具有强氧化性,二者相遇发生反应:2NO+3H2SO4=2NOHSO4(亚硝酰硫酸)+SO2+2H2O.
常温下乙烯与浓硫酸的反应在历史上曾有重要的应用——乙烯水化法制乙醇.具体步骤如下:
第1步,乙烯通入浓硫酸中,发生如下加成反应:
CH2=CH2+H-OSO3H(浓硫酸) →
C2H5-OSO3H(硫酸氢乙酯).
第2步,硫酸氢乙酯水解得乙醇,然后通过蒸馏把乙醇分离.
C2H5-OSO3H+H-OH→
C2H5-OH+H2SO4.
此法第1步并不需要什么催化剂,乙烯通入浓硫酸即可发生.该法理论上看非常合适,硫酸可以循环利用,完全符合绿色化学思想.但实践中发现,该法把大量的浓硫酸转化为稀硫酸,而稀硫酸的浓缩需要耗费很多的能量,所以早已被新的工艺取代.
所以,虽然乙烯气体可以用浓硫酸与乙醇在170℃下反应制备,但由于常温下乙烯与浓硫酸发生加成反应,不可用浓硫酸干燥乙烯气体.
12) 为什么酸化高锰酸钾溶液总是用硫酸,而很少用盐酸、硝酸?
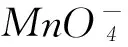
(作者单位:北京十一学校)
