2015年欧洲心脏病协会关于室性心律失常患者治疗和心脏性猝死预防指南的解读
2016-07-21胡大一沈珠军
梁 峰,胡大一,沈珠军,姚 远
(1.首都医科大学大兴医院心内科,北京 102600; 2.北京大学人民医院心脏中心,北京 100044; 3.中国协和医科大学北京协和医院心内科,北京 100730; 4.首都医科大学平谷教学医院心内科,北京 101200)
·热点关注·
2015年欧洲心脏病协会关于室性心律失常患者治疗和心脏性猝死预防指南的解读
梁峰1*,胡大一2,沈珠军3,姚远4#
(1.首都医科大学大兴医院心内科,北京102600; 2.北京大学人民医院心脏中心,北京100044; 3.中国协和医科大学北京协和医院心内科,北京100730; 4.首都医科大学平谷教学医院心内科,北京101200)
2015年欧洲心脏病协会(european society of cardiology,ESC)关于室性心律失常(ventricular arrhythmias,VA)患者治疗和心脏性猝死(sudden cardiac death,SCD)预防指南为2006年美国心脏病学院(america cardiology college,ACC)/美国心脏协会(american heart association,AHA)/ESC关于VA患者治疗和SCD预防指南的更新版[1-2]。其内容重点聚焦于SCD的预防,及时更新是由于SCD疾病自然病史的新认识以及影响心力衰竭(heart failure,HF)的药物、器械及治疗策略的重要研究成果[3]。本文主要解读VA和SCD总体风险评价和治疗,不包含特定心脏病患者VA和SCD的评价和治疗。
1SCD的定义、流行病学和预防的展望
猝死:明显健康的个体,症状发作1 h内发生的非创伤性、意外致命事件;如果死亡未被见证,而事件前24 h受害者健康状况良好,则适合该定义。SCD:当某种先天性或后天性可能致命性心脏病在生存期已存在,或尸检确诊某种心脏或血管异常可能为猝死事件的原因,或验尸后未确定明显的心脏外原因,因此心律失常事件可能是死亡的原因,此时适用SCD。
1.1SCD的流行病学
过去20年间通过采用各种预防措施降低了冠心病(coronary heart disease,CAD)和HF负担,降低了高收入国家心血管死亡率[4]。但全世界每年仍有约1 700万人死于心血管疾病,其中约25%为SCD。预计女性SCD的年发生率为1.40/10万人,男性为6.68/10万人。
年轻人与老年人发生SCD相关心脏病的原因不同。年轻个体发病原因主要为离子通道病和心肌病、心肌炎和药物滥用[5],而老年人群则以慢性退行性疾病为主(CAD、瓣膜性心脏病和HF)。多种困惑减弱了2组人群对SCD原因的识别,如老年患者可能患多种慢性心血管疾病,但难以确定哪种疾病最易于发生SCD;年轻个体SCD原因即使在事件发生后仍可能模糊不清,某些疾病缺乏结构异常,只是在流行病学方面具有相关性。
1.2猝死者尸检和分子解剖
猝死患者的尸检和分子解剖的适应证:推荐进行尸检检查猝死原因并明确SCD是否继发于心律失常或非心律失常机制(如主动脉瘤破裂)(Ⅰ类推荐,证据级别C,简称ⅠC)。每当进行尸检时,推荐标准的心脏组织学检查以及含有代表两个心室横向切片的定位标记心肌组织块(ⅠC)。所有不明原因猝死者推荐进行血液和其他收集体液的毒理学与分子病理学分析(ⅠC)。疑似某种特定遗传性离子通道病和心肌病的所有猝死者,应考虑潜在致病基因的针对性死后遗传分析(ⅡaC)[6]。
1.3SCD风险预测
SCD的预测是心律失常学的“点金石”,尝试预测SCD的可靠指标是最近几十年心律失常学研究最活跃的领域之一[7]。现在可以明确,猝死的特性是起源于“完美风暴”—脆弱基础(心脏电或机械特性的遗传性或获得性变化)与多种瞬态因素相互作用触发致命事件。下面简单回顾正常人、缺血性心脏病、离子通道病和心肌病患者SCD危险分层方案的不足。
1.3.1无明确心脏病个体:约50%的心脏骤停发生于无明确心脏病的个体,但多数患有隐匿缺血性心脏病。因此预防一般人群SCD最有效的方法为缺血性心脏病个体风险因素的量化评分,随后控制风险因素如总胆固醇、血糖、血压、吸烟和体质量指数。目前观察到约40% SCD下降的原因与CAD和其他心脏病发病率的降低相关。
多项研究提供证据,猝死具有遗传倾向,即使不出现孟德尔遗传疾病,猝死的倾向性也刻写在基因上,并促进分子生物学检查,以明确预测一般人群SCD的脱氧核糖核酸(DNA)标志。搜索易于发生SCD单核苷酸多态性的研究,结果发现2项全基因组关联研究(GWAS)有意义: AGNES研究涉及首次心肌梗死和心室颤动(ventricular fibrillation,VF)的患者,与首次心肌梗死无VF的患者人群进行比较。位于21q21基因位点的一个单核苷酸多态性获得全基因组学意义(OR=1.78);第2项极大规模的研究结果确定2q24.2基因位点的强烈信号,其中包含3个功能未知基因,全部表达于心脏。该基因位点增加SCD风险1.92,但是该项研究未复制出AGNES的结果。这些遗传数据虽未用于临床实践,但其提示遗传学可能演变成一种有前途的方法,量化生命早期SCD的风险。新技术可更快、更低成本进行基因分型,快速提供大量人口的数据,并可提高这些研究的统计学效力。
1.3.2缺血性心脏病患者:20多年来,全世界的研究者设想缺血性心脏病发生SCD的一种广谱的“指标”。结果仅一项指标显示与心肌梗死和左室功能障碍的猝死风险增加相关,即左室射血分数(LVEF)。十多年来其用于指导植入式心律转复除颤器(implantable cardioverter defibrillator,ICD)对SCD的一级预防,常与纽约心功能分级(new york heart association,NYHA)合用。预测SCD有希望的新型指标中,生化指标如B型尿钠肽和氨基末端B型尿钠肽的初步结果研究令人鼓舞[8]。
1.3.3遗传性致心律失常性疾病患者:各种离子通道病和心肌病危险分层方案存在高度异质性,虽然校正的QT间期是长QT综合征(long QT syndrome,LQTS)心脏事件风险的可靠指标,间隔肥厚可预测肥厚型心肌病(hypertrophic cardiomyopathy,HCM)的预后;其他疾病,如Brugada综合征和短QT综合征风险分层指标不健全,如何预防性使用ICD具有不确定性。迄今遗传信息可用于指导风险分层仅限于少数几种疾病,如LQTS和核纤层蛋白A/C扩张型心肌病。
1.4特定情况SCD的预防
1.4.1一般人群SCD风险的筛查:警惕遗传性致心律失常性疾病心电图和超声心动图的迹象,是临床实践的重要部分,可有助于早期识别患者是否处于SCD的风险。这种严谨的方法是否应该扩大规模筛查,如用于有猝死风险的人群,现在仍不清楚。虽然欧洲和美国有专家共识,支持运动员参赛前进行筛查,但最近研究报道,以色列竞技运动员实施筛查后的SCD发生率无变化。
总体来说,由于探查到未知数量 “假阳性”和遗漏百分比不清患者(“假阴性”)的筛选策略后果还不明确,故目前还不能提供人群筛选的推荐方案。相反,当个体剧烈体力运动时心律失常风险较高和结构或基因疾病恶化时,指南不支持现有运动员参赛前筛查的推荐;欧洲已有共识,这种人群应进行临床评价、个人和家族史采集和基础12导联心电图检查[9]。
1.4.2筛查猝死者家族成员:多达50%的心律失常性猝死综合征(sudden arrhythmic death syndrome,SADS)者家属确诊为遗传性心律失常疾病,尤其是离子通道病、偶尔轻微型心肌病或家族性高胆固醇血症。因此,当尸检不可行和(或)验尸未检查出异常、毒理学检查结果正常,死者第1代亲属应告知类似事件的潜在风险,并应进行心脏检查评价。早年不明原因猝死综合征反复发作或遗传性心脏病家族史代表危险警告,强烈推荐进行家族成员评价。猝死者第1代亲属的筛查是一种重要干预,以确定处于风险状态的个体,建议使用现有的治疗并预防猝死。应该评价这些患者和家属的社会心理需求,并于专业中心进行多学科干预,这种干预方法具有临床价值。
建议猝死家族成员应用多种方案进行筛选,通常采取遵循渐进的方法,依据初始发现和家族史,从低成本和高效检查开始,并进一步转向昂贵检查。每当出现疑似诊断,应依据结构和心电异常,遵循疑似疾病的标准诊断过程进行。应对家庭成员的积极询问,准确的病史采集是确立尸检诊断的第一步。年轻猝死者应侧重于心肌病和离子通道病,包括对有预兆心脏症状(包括晕厥或癫痫)的评价及对死亡情况的详尽询问和死前心脏临床检查的搜集。当猝死者>40岁,应评价CAD的危险因素。另外应建立3代家谱,记录所有猝死和心脏疾病。应尽力查找过去医疗记录和(或)验尸检查。应优先评价具有心脏病症状的家族成员,如晕厥、心悸或胸痛。猝死者第1代亲属评价方法见表1。家族成员中没有疾病诊断,则儿童应至少筛查基线心电图(ECG)和超声心动图。

表1 不明原因猝死综合征或SADS家族成员的诊断检查方法
由于许多遗传性心律失常性疾病呈现年龄相关外显率和不完全表达,年轻个体应定期随访。无症状和生长良好的成人不必监护治疗, 除非症状出现或从家庭成员获得新信息。
当疑似遗传性心律失常性疾病,进行分子尸检时,猝死者DNA取样是最好的信息来源。如果检查结果阳性,家族成员应提供机会,以级联方式进行预测基因筛选。死者无生物取样,当疑似家族成员患遗传性疾病时,可以考虑对第1代亲属进行针对性分子筛查。相反,对临床评价后无某种特殊疾病线索的不明原因猝死综合征或SADS亲属,不应进行大组基因的遗传筛选,尤其婴儿猝死综合征者。
1.4.3既往明确或疑似VA患者的筛选:(1)病史:心悸、先兆晕厥和晕厥是3种最重要的症状,需要全面病史采集和可能的进一步检查,排除与VA的关联性。室性心动过速(ventricular tachycardia,VT)相关的心悸通常突然发作或开始,可能导致先兆晕厥和(或)晕厥。无任何先兆突然晕倒伴意识丧失,必定考虑缓慢性心律失常或VA。剧烈运动中发生的晕厥,呈坐位或仰卧位时晕厥发作应考虑心脏原因,而其他情境事件可能提示血管迷走性晕厥或体位性低血压。应该追问患者与内在结构心脏病相关的症状,如胸部不适、呼吸困难和疲劳。对疑似VA患者的评价,必须包括对其SCD家族史和药物的全面了解,包括药物剂量。SCD的阳性家族史是易患VA和SCD的强烈独立预测因素。虽然体格检查极少发现阳性体征,但有时会提示有价值的线索。
(2)疑似或已知VA患者的无创性评价:①静息12导联ECG:评价所有VA患者推荐静息12导联ECG检查(ⅠA)。②ECG监查:为检测和诊断心律失常推荐动态心电图检查。为评价QT间期变化或ST段变化推荐十二导联动态心电图检查(ⅠA)。当症状不定时发作,为确诊是否由短暂性心律失常导致,推荐心脏事件记录仪(ⅠB)。当症状不定时发生,如晕厥,同时疑似与心律失常有关及当症状-心律的相关性通过传统的诊断技术不能明确时,推荐植入式循环记录仪(ⅠB)。VA患者或处于发生致命性VA风险的患者,推荐信号平均心电图改善致心律失常性右室心肌病(arrhythrnogenic right ventricular cardiomyopathy,ARVC)的诊断(ⅠB)。③运动负荷试验:VA成人患者,通过年龄、诱发心肌缺血或VA的症状,考虑患CAD可能中度或更大,推荐运动负荷试验(ⅠB)。已知或疑似运动诱发VA患者包括儿茶酚胺敏感性多形性室性心动过速,为明确诊断和判断预后,推荐运动负荷试验(ⅠB)。已知运动诱发VA患者,为评价药物或消融治疗的反应,应考虑运动负荷试验(ⅡaC)。④影像检查:疑似或已知VA的所有患者,推荐超声心动图评价左室功能以及检测结构性心脏病(ⅠB)。发生严重VA或SCD高危的患者,推荐超声心动图评价左室和右室功能以及检测结构性心脏病,如扩张型心肌病、肥厚型心肌病或右室心肌病、急性心肌梗死幸存者或SCD相关遗传性疾病患者的亲属(ⅠB)。VA患者,通过年龄或症状考虑患CAD可能中度,但ECG不可靠(使用地高辛、左室肥厚、静息时>1 mm ST段下移、预激综合征、左束支传导阻滞),推荐运动影像试验(运动负荷超声心动图试验或核素心肌灌注扫描[SPECT])以检查无症状心肌缺血(ⅠB)。VA患者,通过年龄或症状考虑患CAD可能中度,但不能进行症状限制性运动试验,推荐药物负荷影像试验,以检查无症状心肌缺血(ⅠB)。VA患者,当超声心动图不能提供左室或右室功能的准确评价和(或)结构变化的评价,应考虑心脏核磁共振或CT(ⅡaB)。
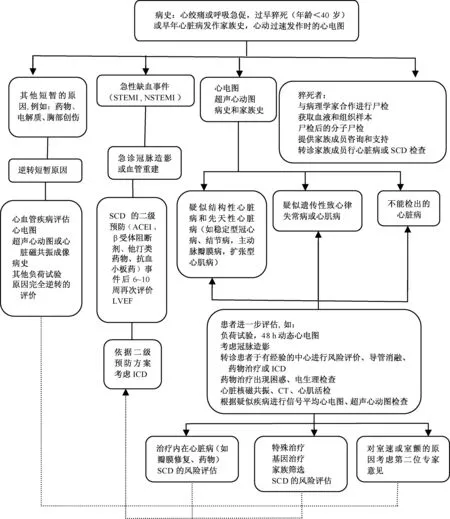
图1 持续性VT或室颤患者的诊断检查流程注:STEMI:ST段抬高心肌梗死;NSTEMI:非ST段抬高心肌梗死;ACEI:血管紧张素转换酶抑制剂
(3)疑似或已知VA患者的有创性评价:①冠状动脉造影:发生威胁生命VA的患者或SCD幸存者,通过年龄和症状考虑患CAD可能中度或更大,应该考虑冠状动脉造影确诊或排除显著阻塞性CAD(Ⅱ a C)。②电生理检查:推荐CAD患者行电生理学检查,诊断性评价陈旧心肌梗死患者出现提示VA的症状,包括心悸、先兆晕厥或晕厥(ⅠB)[10]。当依据症状(如心悸)或无创检查评价疑似缓慢或快速心律失常,尤其具有结构性心脏病,此时出现晕厥患者推荐进行电生理检查(Ⅰ C)。为鉴别诊断ARVC和良性右室流出道(right ventricular outflow tract,RVOT)心动过速或结节病,可以考虑电生理检查(Ⅱ b B)。
2VA的治疗
2.1内在心脏病的治疗
VA成功治疗和SCD预防的关键之一是有效治疗基础疾病和伴发病,必须预防这些疾病的急性恶化和慢性进展。伴发病也必须控制,其可能促发或有助于维持VA的基质产生。自从抗心律失常药和ICD开创性试验进行以来,心脏病的治疗发生了巨大的变化。由于重复过去这些试验的可能性不大,原始试验的治疗意义必须推广到现代背景。但是,基础心脏病的现代治疗必须进行优化。
2.2VA的药物治疗和SCD的预防
2.2.1综合治疗:VA合适治疗选择和SCD预防主要聚焦于心律失常本身、可能促发和(或)加剧心律失常的相关治疗、心律失常导致的风险以及潜在治疗风险-获益的各个方面。有症状心律失常的治疗可能包括致心律失常药物的停用、合适抗心律失常药治疗、植入装置、消融或手术。
2.2.2抗心律失常药:除β受体阻断剂外,目前使用抗心律失常药进行的随机对照试验(randomized controlled trial,RCT)结果未显示在威胁生命VA的治疗或SCD的预防方面有效。胺碘酮研究偶然为阳性结果,但目前仍无一致的结果。总的原则是,特定情况下,抗心律失常药作为心律失常易发患者的辅助治疗可能有效。但由于抗心律失常药潜在的不良反应,必须谨慎使用。本节回顾VA的药物治疗,以预防VT反复发作。
每种药物均具有致不良事件的潜在作用,包括致心律失常。许多市售的心脏和非心脏药物诱发窦性心动过缓和房室阻滞,某些损害希氏束-浦肯野纤维传导并产生房室或束支阻滞,而其他药物延长心室复极化和QT间期。因此,抗心律失常药可能潜在具有促致命性室性心动过速作用,与某些非心血管药物相似,可能也延长QT间期或减慢心室间传导。
与心血管专家关联药物中,IA抗心律失常药(如奎尼丁、双异丙吡胺)阻滞钠电流,也阻滞延迟整流钾电流的快速激活成份,可能延长QT间期。因此,对服用QT间期延长药物或遗传性LQTS患者发布使用钠通道阻滞剂的警示。但是最近的研究结果显示,某些钠电流阻滞剂(主要IB类美西律和IC类氟卡尼)快速抑制峰钠电流和晚钠电流。因此这些药物可能引起3型LQTS患者QT间期的缩短,由于该型LQTS是由晚钠电流增强突变导致。所以这些药物可以考虑用于3型LQTS患者,以缩短QT间期。药物诱导的QT间期延长和其他遗传变异型LQTS对QT缩短的晚钠电流阻滞剂是否也有作用,现在仍不清楚。
最近一项德国的研究使用积极的监查方法,报道药物诱导LQTS导致的尖端扭转性室速发生率约3.2/(100万人·年)。一旦认为VA可能由于抗心律失常药治疗导致,可能相关的药物就应停药,并进行适当的ECG随访监查。
CAST试验结果显示,与安慰剂治疗患者(3.0%)相比,心肌梗死后英卡胺或氟卡胺治疗患者死亡和非致命性心脏骤停的发生率增高(7.7%)。因此,发布了心肌梗死后禁忌使用IC类钠通道阻滞剂。禁忌证延伸至其他I类抗心律失常药,由于即使不增加死亡率,当用于降低心肌梗死后患者心律失常负担时,也不能降低死亡率。对遗传性原发性心律失常综合征(LQTS、短QT综合征、Brugada综合征)和心肌病的抗心律失常药使用,为标签外适应证。
β受体阻断剂:其抗心律失常疗效的机制包括交感神经介导触发机制的竞争性β肾上腺素能受体阻断,减慢窦性心率和可能抑制雷诺丁受体通道过量钙释放。β受体阻断剂有效抑制室性异位搏动和心律失常以及降低心脏衰竭和非心脏衰竭患者多种心脏疾病的猝死。β受体阻断剂通常是安全有效的抗心律失常药,可以认为是抗心律失常药的基石。然而最近34 661例STEMI和NSTEMI患者的注册研究结果发现,具有2项或以上休克风险[如年龄>70岁、心率>110次/min、收缩压<120 mmHg(1 mmHg=0.133 kPa)]的患者,使用β受体阻断剂治疗休克或死亡的风险明显增加。但总体来说,β受体阻断剂是治疗VA和预防SCD的一线治疗。
胺碘酮:其具有多种作用,包括阻滞去极化钠电流和复极钾通道,这些作用通过影响自律性和折返可能抑制或终止VA。SCD-HeFT试验结果显示,对LVEF≤35%的患者应用胺碘酮较安慰剂治疗缺乏生存益处。但不像钠通道阻滞剂,HF患者使用胺碘酮,不增加死亡率。一项荟萃分析包括了8 522例心肌梗死后或收缩性HF患者,随机给予胺碘酮或安慰剂治疗,结果显示,胺碘酮每治疗1 000例患者,可防止5例全因死亡、24例心血管死亡和26例猝死[11]。1.5%的全因死亡率绝对降低,但无统计学差异。胺碘酮的长期使用可导致复杂的药物相互作用以及多种心脏外(包括甲状腺、皮肤、偶然肺和肝脏)不良反应,因此需要定期监测肺、肝和甲状腺功能。通常,胺碘酮剂量越大、治疗时间越长,由于不良反应停药的可能性越大。与安慰剂相比,随机应用胺碘酮的10%患者停药。
索他洛尔/右旋索他洛尔:消旋索他洛尔是一种快速延迟整流钾电流抑制剂,兼具有β受体阻断剂特性,有效抑制VA。除合并HF外,索他洛尔可安全用于CAD患者。索他洛尔可显著降低持续性VA的复发率,但不改善寿命。一项研究使用右旋索他洛尔(d-sotalol)研究,其为纯粹快速延迟整流钾电流抑制剂,入组3 121例心肌梗死后左室功能障碍的患者,由于右旋索他洛尔组死亡率增加,试验提前终止[尽管尖端扭转性室速(TdP)例数极少]。所以索他洛尔不应用于这些患者,除非为植入ICD。索他洛尔抗心律失常使用的剂量需要ECG仔细监查,尤其低体质量指数或肾功能受损的患者。
联合治疗:目前缺乏资料指导抗心律失常药的联合治疗,对尝试其他抗心律失常治疗(包括不同制剂单种抗心律失常药、胺碘酮治疗和导管消融)不能满意抑制心律失常事件的患者,联合治疗应该保留。如频繁VT的患者,联合使用钠通道阻滞剂和钾通道阻滞剂(如美西律和索他洛尔或胺碘酮和氟卡胺/普罗帕酮),通常用于植入除颤器但VT频繁复发的患者。β受体阻断剂与胺碘酮联合治疗降低ICD放电次数,但是其不良反应可能导致更多患者停药。对于其他药物难治性患者,雷诺嗪联合其他抗心律失常药可抑制VT。这些患者需要严密监查ECG和心功能,以发现左室功能的恶化和(或)致心律失常的迹象。
2.2.3植入心脏转复除颤器患者的药物治疗:植入心脏转复除颤器的多数患者使用β受体阻断剂治疗,以使ICD的适当和不适当放电降到最少。反复心脏转复除颤器放电的患者,可能通过更换索他洛尔抑制房性心律失常和VA而获益。但是严重左室功能障碍的患者应避免使用索他洛尔,由于这些患者多数也合并肾功能障碍,胺碘酮和β受体阻断剂的更有效联合可能优于索他洛尔。
曾经发生致命性VA的患者,抗心律失常药从未明确显示可降低心律失常性猝死。但是心肌梗死和HF患者,胺碘酮可降低这些心律失常的复发;推测已经历过这些心律失常事件的患者,药物对严重VA确实提供一定保护作用。但是,心律失常性死亡的降低似乎并不导致总死亡率的降低,胺碘酮的不良事件进一步降低了治疗的益处。然而,植入ICD的患者,胺碘酮尤其与β受体阻断剂的联合使用可显著降低ICD放电。
植入ICD患者出现阵发性或慢性房颤合并快速心室率和不适当的心脏除颤放电,需要控制房颤的快速心室率,可以谨慎联合使用β受体阻断剂和(或)非二氢吡啶类钙通道阻滞剂。如果无效,胺碘酮可能有用。部分患者药物治疗和房颤消融无效,可能需要AV结消融。
2.2.4电解质:补钾恢复正常血钾,对参与VA的基质可能产生有益影响。补镁可能特别有助于抑制TdP。HF患者电解质紊乱常见,尤其使用大剂量保钾利尿剂的患者。最近一项数据库研究包括38 689例急性心肌梗死患者,显示钾浓度3.5~4.5 mmol/L时,VF、心脏骤停或死亡的风险最低。
2.2.5其他药物治疗:心肌梗死后或非缺血性心肌病发生的心室不良重构以及相关的离子通道改变可能加剧VA的发生率。多种药物如ACEI、血管紧张素II受体拮抗剂和盐皮质激素受体拮抗剂,改善逆转重构以及降低SCD发生率。同样,抗凝和(或)抗血小板治疗可能有助于降低高危患者冠脉血栓堵塞的发生率;他汀类药物可能降低高危患者致命性VA的发生。
2.3器械治疗
2.3.1植入型心脏转复除颤器:最初接受除颤器植入者是幸免于VF或心脏骤停复苏的患者,以后试验显示处于猝死风险的患者应用除颤器可获益。只要未患其他疾病而使患者预期寿命短于1~2年[12],心律失常性猝死高危的患者ICD治疗可预防猝死并延长寿命。ICD和心室再同步兼心脏转复除颤器(cardiac resynchronization therapy defibrillators,CRT-D)研究分别进行8年和7年的随访,结果显示,患者可长期获益。另一方面,除颤器可导致并发症,包括不适当放电,尤其儿童发生频繁。最近3 000例以上植入ICD或CRT-D患者的研究结果发现,12年不良事件发生率分别为:不适当放电为20%,器械相关感染为6%,电极失败率为17%。虽然循证资料强烈支持心肌梗死后射血分数减低患者是ICD治疗的适应证,但是多数国家指南和临床实践存在着明显差异。而ICD二级预防治疗指南已被普遍接受多年,最近无试验证据建议以往的推荐应大幅改变。
SCD和室性心律失常ICD的二级预防:明确的VF或血流动力学不能耐受的VT患者,无可逆原因或心肌梗死后48 h内并接受慢性优化药物治疗,身体机能状态良好、预期合理寿命1年以上,建议植入ICD(ⅠA)。复发性持续性VT(非心肌梗死后48 h内)患者并接受慢性优化药物治疗,LVEF正常以及良好身体功能状态预期的合理寿命1年以上,应考虑植入ICD(ⅡaC)。VF/VT患者并具有ICD植入的适应证,但当ICD不可用、因伴发疾病禁忌或患者拒绝,可考虑胺碘酮治疗(ⅡbC)。
2.3.2皮下植入型心律转复除颤器:具有ICD适应证患者,当不需要起搏、心脏再同步或抗心动过速起搏治疗时,应考虑皮下植入型心律转复除颤器,以替代经静脉途径除颤器(ⅡaC)。当静脉通路困难,因感染而拔出经静脉通路ICD或年轻患者需要长期ICD治疗时,可以考虑皮下植入型ICD,为经静脉通路ICD的良好替代(ⅡbC)。
2.3.3可穿戴式心脏复律除颤器:左室收缩功能不良的成年患者,有限的时间内处于心律失常性猝死风险,但并不适合植入型除颤器,可以考虑可穿戴式心脏复律除颤器(如心脏移植的桥接治疗,静脉途径植入的桥接治疗,围产期心肌病,活动性心肌炎和心肌梗死后早期心律失常)(ⅡbC)。
2.3.4公众使用的除颤:在心脏骤停相对常见和适合存放充电的地点(如学校、体育场馆、大型车站、赌场等),或无其他途径可行除颤的地方(如火车、游船、飞机等),推荐设立公众可使用的除颤器(ⅠB)。对SCD高危患者的家属可以考虑提供基础生命支持教育(ⅡbC)。
2.4持续性室性心律失常的急性治疗
心脏复律或除颤和持续性室速的急性治疗:持续性室性心动过速出现血流动力学不稳定的患者推荐直流电心脏复律(ⅠC)。血流动力学可耐受的持续性室性心动过速患者,无结构性心脏病(如特发性右室流出道室速),可以考虑静脉使用氟卡胺或传统的β受体阻断剂、维拉帕米或胺碘酮(ⅡbC)。
心脏骤停最常见的电生理机制是VF或VT、缓慢性心律失常、心脏停搏和电机械分离(无脉性电活动)。总体室性快速性心律失常患者较心脏停搏患者生存率好。2010年国际复苏联盟更新了国际共识会议的结论和推荐。心脏骤停时应按心肺复苏流程进行[13]。
除颤前是否应进行心肺复苏仍有待探讨。院外心脏骤停时,应立即胸外按压复苏直至可能除颤;院内心脏骤停应立即进行除颤,由于此时持续性室性快速性心律失常导致心脏骤停的可能性最大,建议最大功率开始除颤。半自动除颤器为最佳的技术覆盖全部院内除颤。植入ICD的患者,电极板最好置于胸壁距ICD至少8 cm。紧急情况时静脉给予胺碘酮有利于除颤和(或)预防VT或VF再发。
持续性室性心动过速患者应依据症状和心律失常的耐受性给予治疗。单形性室速出现血流动力学不稳定(伴晕厥VT)应进行直流电除颤。低血压但意识还清楚的患者,进行复律前应立即给予镇静剂。宽QRS心动过速而血流动力学稳定的患者,电复律应该是一线治疗方法。无严重HF或急性心肌梗死患者,可以考虑静脉使用普鲁卡因胺或氟卡胺。心力衰竭或疑似缺血的患者可以考虑静脉使用胺碘酮。单形性室性心动过速的患者静脉使用利多卡因仅仅具有中等效果。通常持续性室性心动过速而血流动力学稳定的所有患者应记录12导联ECG。
左室分支型室性心动过速患者应静脉给予维拉帕米或β受体阻断剂[右束支阻滞图形(RBBB)和电轴左偏]。
2.5介入治疗
2.5.1导管消融:(1)导管消融治疗持续性单形性室性心动过速,瘢痕相关性心脏病患者出现持续不断的VT或电风暴推荐进行紧急导管消融(ⅠB)。缺血性心脏病患者由于持续性室性心动过速出现ICD反复放电建议导管消融(ⅠB)。缺血性心脏病并植入ICD的患者持续性室性心动过速首次发作后应该考虑导管消融(ⅡaB)。
(2)瘢痕相关性心脏病患者:瘢痕相关心脏病患者出现VT或VF,导管消融已发展为重要的治疗选择。2项前瞻性随机大规模试验,对缺血性心脏病患者显示VT的导管消融,降低随后ICD的放电以及防止VT反复发作。而且导管消融常用于控制无休止的VT或电风暴(即反复VT或VF出现频繁ICD放电),降低或防止持续性室性心动过速的反复发作。
多项研究结果显示,ICD放电导致更高的死亡率并使生活质量下降。β受体阻断剂联合胺碘酮降低ICD的放电次数,但药品不良反应可能导致患者停药。通常瘢痕组织是VT患者的内在基质。导管消融靶点为VT折返环内缓慢传导的连接峡部(关键性峡部)。折返环可能跨越几厘米,以及可能涉及复杂三维结构的心内膜、中膜或外膜。瘢痕相关室速为典型的单形性和多种形状VT,同一患者均可能诱发。QRS波形态由折返出口部位确定,该部位为折返波的前沿,从瘢痕传出使心室肌除极。因此,VT 12导联体表ECG记录可能有助于标测定位和消融过程。非缺血性心肌病患者,QRS波形态可确定患者是否需要心外膜消融的可能性。而术前心脏核磁共振显像,可能有利于无创性确定既往心肌梗死或心外膜VT患者致心律失常的基质。
多形性室性心动过速定义为QRS波形态持续变化,通常涉及急性心肌梗死、获得性或遗传性离子通道病或心室肥厚。其中部分患者对药物治疗无反应,但浦肯野纤维触发的多形性室性心动过速可以通过导管消融控制。
心脏结构的无创性显像可用于规划和指导室速的消融过程,最好通过核磁共振显像检查。VT发作期间进行标测和消融(激动顺序标测)。三维电解剖标测系统可能有助于异常心室组织的定位,由于VT诱发时血流动力学不稳定,因此应在窦性心率而非室速诱发状态下进行消融(基质消融)。非接触式球囊标测系统可以用于血流动力学不稳定的VT。可使用多种技术,包括折返环出口部位逐点消融(去疤痕通道),线性消融或对瘢痕基质异常心室电活动局部消融。扩张型心肌病或致心律失常右室心肌病患者进行室速消融时,常需要心外膜标测和消融。心外膜穿刺和消融的潜在并发症是对冠脉血管的损伤或周围器官的意外损伤,左膈神经麻痹或出血导致心包填塞。
心肌梗死后瘢痕相关VT患者导管消融后,趋向于较非缺血心肌病室速患者具有更好的预后。五项前瞻性多中心研究评价导管消融治疗持续性室性心动过速的作用,约50%患者具有良好预后(即随访期间无临床VT再发),导管消融治疗较抗心律失常药治疗效果更好[14]。
心脏病患者VT导管消融的可能并发症包括:卒中、瓣膜损伤、心脏压塞或房室传导阻滞。介入相关的死亡率为0~3%,最常见死因是消融失败而室速无法控制。虽然导管消融对广范围VT基质是可接受的治疗选择,但缺乏前瞻性随机试验证据证实导管消融降低死亡率。
(3)无明显结构性心脏病患者:无明显结构心脏病患者的VT最常起源于右室或左室流出道。触发活动是最常见的内在病理生理机制,以及消融过程中消融激动最早部位成功率高,而该患者人群SCD的发生率通常低。少数情况患者可能表现为特发性左室心动过速,牵涉浦肯野纤维远端网。多数患者导管消融有效而并发症罕见。
2.5.2抗心律失常手术:经验丰富的电生理专家进行导管消融失败后又对抗心律失常药治疗耐药的VT患者,推荐在经验丰富的中心进行术前和术中电生理标测指导的手术消融治疗(ⅠB)[15]。导管消融失败后临床明确的VT或VF患者,可以考虑心脏手术(旁路移植术或瓣膜手术)的同时进行手术消融治疗(ⅡbC)。在导管消融治疗VA的年代,手术消融的需要变得非常少。对抗心律失常药无效和(或)在经验丰富中心导管消融失败后,可以考虑心律失常手术治疗,尤其适用于继发于心肌梗死左室室壁瘤和需要血管重建者。
2.6埋藏式复律除颤器置入后社会心理治疗
反复不适当放电患者推荐心理状况评价和治疗悲伤(ⅠC)。所有患者ICD植入前和疾病进展过程中,推荐探讨生活质量问题(ⅠC)。
3证据空白
(1)识别处于猝死风险的患者仍然是猝死预防的“点金之石”。SCD一级预防的有创和无创性检查风险分层仍不能令人满意。亟需研究识别处于猝死风险无症状人群的最佳方法。需要适合大众筛选的简单价廉方法。(2)确保一种有效和快速的治疗链是非常重要的,可改善猝死者的生存情况。需要更多研究评价此种生存链的最佳设计,包括院前治疗和院内治疗方案。(3)心肌梗死后CAD和HF的预防可大幅降低猝死,需要进一步研究猝死的其他原因。(4)部分患者应用可穿戴式除颤仪可能是一种可行的治疗选择,但需要大规模随机试验检验其适应证。(5)需要新的临床试验评价ICD对现代患者人群SCD一级预防的可能获益。(6)需要更多的研究检验循证干预对处于猝死风险的患者和家属可减少心理社会影响,优化治疗和提供心理社会支持。(7)VT可使各种结构性心脏病患者的预后恶化。急需新的抗心律失常药或其他治疗,使更广泛人群的首发或复发性致命性室性心律失常得以保护。特定的抗心律失常治疗是否可改善预后,仍然有待检验。虽然研究显示结构性心脏病患者复发性室性心动过速进行的导管消融能显著降低室速复发的次数,但室速导管消融对死亡率的影响仍不清楚,需要进一步研究。
参考文献
[1]Priori SG, Blomström-Lundqvist C, Mazzanti A, et al. 22015 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: The Task Force for the Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death of the European Society of Cardiology (ESC). Endorsed by: Association for Europ-ean Paediatric and Congenital Cardiology (AEPC)[J].Eur Heart J, 2015, 36(41):2793-2867.
[2]Zipes DP, Camm AJ, Borggrefe M, et al. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death-executive summary: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death) Developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society[J].Eur Heart J,2006,27(17):2099-2140.
[3]Pedersen CT,Kay GN,Kalman J,et al.EHRA/HRS/APHRS expert consensus on ventricular arrhythmias[J]. Europace,2014,16(9):1257-1283.
[4]Niemeijer MN,vandenBerg ME,Leening MJ,et al. Declining incidence of sudden cardiac death from 1990-2010 in a general middle-aged and elderly population: the Rotterdam Study[J].Heart Rhythm,2015,12(1):123-129.
[5]Mazzanti A,O’Rourke S,Ng K,et al. The usual suspects in sudden cardiac death of the young: a focus on inherited arrhythmogenic diseases[J].Expert Rev Cardiovasc Ther,2014,12(4):499-519.
[6]Basso C, Burke M, Fornes P, et al. Guidelines for autopsy investigation of sudden cardiac death[J].Virchows Arch,2008,452(1):11-18.
[7]Wellens HJ,Schwartz PJ,Lindemans FW,et al.Risk stratifi-cation for sudden cardiac death: current status and challenges for the future[J].Eur Heart J,2014,35(25):1642-1651.
[8]Levine YC,Rosenberg MA,Mittleman M,et al.B-type natriuretic peptide is a major predictor of ventricular tachyarrhythmias[J].Heart Rhythm,2014,11(7):1109-1116.
[9]Borjesson M,Serratosa L,Carre F,et al.Consensus document regarding cardiovascular safety at sports arenas: position stand from the European Association of Cardiov-ascular Prevention and Rehabilitation (EACPR), section of Sports Cardiology[J].Eur Heart J,2011,32(17):2119-2124.
[10]Zaman S,Narayan A,Thiagalingam A,et al.Significance of repeat programmed ventricular stimulation at electrophy-siology study for arrhythmia prediction after acute myo-cardial infarction.Pacing Clin Electrophysiol[J].2014,37(7):795-802.
[11]Piccini JP,Berger JS,O’Connor CM.Amiodarone for the prevention of sudden cardiac death:a meta-analysis of randomized controlled trials[J].Eur Heart J,2009,30(10):1245-1253.
[12]Smith T,Jordaens L,Theuns DA,et al.The cost-effectiv-eness of primary prophylactic implantable defibrillator therapy in patients with ischaemic or non-ischaemic heart disease: a European analysis[J].Eur Heart J,2013,34(3):211-219.
[13]Nolan JP,Hazinski MF,Billi JE,et al.Part 1:Executive summary:2010 International Consensus on Cardiopul-monary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations[J].Resus-citation,2010,81(Suppl 1):e1-e25.
[14]Della Bella P,Baratto F,Tsiachris D,et al.Management of ventricular tachycardia in the setting of a dedicated unit for the treatment of complex ventricular arrhythmias: long-term outcome after ablation[J].Circulation,2013,127(13):1359-1368.
[15]Mukaddirov M,Demaria RG,Perrault LP,et al.Reconstructive surgery of postinfarction left ventricular aneurysms: techniques and unsolved problems[J].Eur J Cardiothorac Surg,2008,34(2):256-261.
#通信作者:主任医师。研究方向:冠脉介入治疗。E-mail: iloveluner@sohu.com
中图分类号R972
文献标志码A
文章编号1672-2124(2016)06-0721-07
DOI10.14009/j.issn.1672-2124.2016.06.001
(收稿日期:2016-02-22)
*主任医师,教授。研究方向:冠心病的临床研究。E-mail:liangfeng666@aliyun.com
