高效液相色谱法测定盐酸二甲双胍缓释片中盐酸二甲双胍的含量和释放度
2016-07-21宋新康曾玉梅
宋新康,曾玉梅
(梅州市食品药品监督检验所化学室,广东 梅州 514071)
高效液相色谱法测定盐酸二甲双胍缓释片中盐酸二甲双胍的含量和释放度
宋新康*,曾玉梅
(梅州市食品药品监督检验所化学室,广东 梅州514071)
摘要目的:建立测定盐酸二甲双胍缓释片中盐酸二甲双胍含量和释放度的方法。方法:采用C18色谱柱(150 mm×4.6 mm,5 μm);流动相:0.05%庚烷磺酸钠溶液(用10%磷酸溶液调节pH至4.0)-乙腈(V ∶V=84 ∶16),流速:0.8 ml/min;检测波长:233 nm;柱温:35 ℃。结果:盐酸二甲双胍在2.45~98.00 μg/ml(r=1,n=6)呈良好的线性关系,回收率99.2%,RSD为0.84%。结论:该方法适用于盐酸二甲双胍缓释片的质量控制。
关键词HPLC; 盐酸二甲双胍缓释片; 含量; 释放度
盐酸二甲双胍缓释片是降糖药物,通过抑制肝糖原的输出,增加胰岛素敏感性从而达到降糖目的。临床上常用于单纯饮食控制不满意的Ⅱ型糖尿病患者,尤其是肥胖和伴高胰岛素血症者,用该药不但有降血糖作用,还可能有减轻体质量和高胰岛素血症的效果[1]。盐酸二甲双胍有片剂、胶囊剂、肠溶胶囊和缓释片等多个剂型,其他品种除肠溶胶囊剂外在《中国药典》[2]均用紫外分光光度法测定其含量及溶出度或释放度,唯缓释制剂收载于《国家药品标准》[3],且自2004年以来有43个批件号和散页标准[4],均使用紫外-可见分光光度法测定。为了更准确灵敏的考察该产品的内在质量,便以临床用药的选择需要,本研究参考多方文献[5-11]采用高效液相色谱法对释放度、含量进行测定,取得了较好效果。
1材料
1.1仪器
LC-20A高效液相色谱仪,SPD-20A检测器,LC-20AT泵,Labsolution色谱工作站(日本岛津公司);AUW220D岛津电子分析天平(日本岛津公司);MODEL HN1006超声波清洁器(昆山市超声仪器有限公司);RC806-1型溶出试验仪(天津天大天发仪器公司);紫外-可见分光光度计1601(日本岛津公司)。
1.2药品与试剂
盐酸二甲双胍缓释片(A:山西宝芝林药业有限公司,批准文号为国药准字H20060815,批号为131225;B:成都恒瑞制药有限公司,批准文号为国药准字H20030952,批号为815078;C:山西华元医药生物技术公司,批准文号为国药准字H20060815,批号为150301);盐酸二甲双胍对照品(批号为100664-201203,含量为100%,由中国食品药品监督研究院提供);乙腈(河北四友卓越科技有限公司,色谱纯);水为超纯水;其他试剂均为分析纯。
2方法与结果
2.1色谱条件与系统适用性
色谱柱:ECOSIL C18色谱柱(150 mm×4.6 mm,5 μm);流动相:0.05%庚烷磺酸钠溶液(用10%磷酸溶液调节pH至4.0)-乙腈(V∶V=84 ∶16);流速:0.8 ml/min;检测波长:233 nm;柱温:35 ℃;进样量:20 μl。理论板数按盐酸二甲双胍峰计不小于2 000。色谱图见图1。

A.对照品溶液;B.供试品溶液;C.阴性对照溶液A.reference substance solution; B.test sample solution; C.negative control solution图1 盐酸二甲双胍缓释片HPLC色谱图Fig 1 HPLC chromatogram of Metformin hydrochloride sustained-release tablets
2.2溶液的制备
2.2.1对照品溶液的制备:精密称定盐酸二甲双胍对照品10 mg,置于100 ml容量瓶中,加流动相溶解并稀释至刻度,摇匀,制成对照品储备溶液;精密量取对照品储备溶液5 ml置于25 ml容量瓶中,加流动相溶解并稀释至刻度,摇匀,作为对照品溶液。
2.2.2样品溶液的制备:取盐酸二甲双胍缓释片(A)20片,精密称定,研细,精密称取盐酸二甲双胍50 mg,分别置于200 ml容量瓶中,加缓冲液(0.1 mol/L盐酸溶液750 ml,加0.2 mol/L磷酸钠溶液250 ml,混匀,必要时用2 mol/L盐酸溶液或2 mol/L氢氧化钠溶液调节pH至6.8)100 ml,振摇10 min使盐酸二甲双胍溶解,用上述缓冲液稀释至刻度,摇匀,滤过,弃去初滤液20 ml,精密量取2 ml,至25 ml量瓶中,用流动相稀释至刻度,摇匀,作为供试品溶液。
2.2.3阴性溶液的制备:制备不含盐酸二甲双胍的阴性对照溶液。
2.3线性关系
精密量取“2.2.1”项下的对照品储备溶液5 ml,分别置于200、100、50、25、10、5 ml容量瓶中,加流动相稀释至刻度,得到系列浓度的对照品溶液,精密量取上述溶液各20 μl注入色谱仪,记录色谱图,以浓度(μg/ml)为横坐标(X),峰面积A为纵坐标(Y),进行线性回归,得线性方程为:Y=114 228X+18 251;r=1(n=6)。表明盐酸二甲双胍在2.45~98.00 μg/ml的范围内与峰面积呈良好的线性关系。
2.4精密度试验
精密量取“2.2.1”项下的对照品溶液20 μl,连续进样5次,测定峰面积,计算峰面积相对标准偏差RSD为0.30%。结果表明精密度良好,所选定的色谱条件系统稳定。
2.5重复性试验
取批号为131225同一供试品6份,按“2.2.2”项下的供试品溶液制备方法制备,在相同色谱条件下测定。结果样品中盐酸二甲双胍平均含量为98.22%,RSD为0.11%。表明用本法测定含量,重复性较好。
2.6稳定性试验
取“2.2.2”项下同一供试品溶液,分别于配制后0、2、4、8、12 h进样20 μl,测定其峰面积,结果盐酸二甲双胍测得的峰面积的RSD为0.92%,表明供试品溶液在12 h内稳定。
2.7加样回收试验
取9份已知含量的盐酸二甲双胍缓释片(A:山西宝芝林药业有限公司,批号为131225)的供试品0.05 g,精密称定,按低、中、高3个水平分别加入一定量的盐酸二甲双胍对照品,按供试品溶液的制备方法制备加样供试品溶液,测定,计算加样回收率,见表1。平均回收率为99.82%,RSD为0.84%。表明此方法测定含量,准确度高。

表1 加样回收试验结果(n=9)
2.8检测限与定量限
取“2.4线性关系考察”项下的已知低浓度的标准溶液,精密量取10 μl注入高效液相色谱仪,测出各标准物质较低浓度下的信噪比S/N,计算出当S/N为3时的各标准物质的浓度,以信噪比(S/N=3)时测得盐酸二甲双胍的仪器检出限分别为0.1 ng,以信噪比(S/N=10)时测得仪器定量限分别为0.3 ng。
2.9供试品测定
取不同批号盐酸二甲双胍缓释片各20片,按“2.2.2”项下方法进行操作,精密量取20 μl,并按上述色谱条件测定并计算样品中盐酸二甲双胍含量。其他条件保持不变,采用紫外分光光度法测定样品中盐酸二甲双胍含量,与高效液相色谱法进行对比,见表2。

表2 样品含量测定结果(μg/ml)
2.10释放度测定
取按原标准[3]中的释放度测定法第一法溶出度第一法测定,以磷酸盐缓冲液(pH=6.8)1 000 ml为释放介质,转速为100 r/min,依法操作。分别以1、3、10 h取样,并用溶出介质稀释成5 μg/ml 的溶液按“2.1”项下方法测定含量。其他条件保持不变,采用紫外分光光度法测定含量,与高效液相色谱法进行对比,结果表明2种方法测定结果相近,见表3。
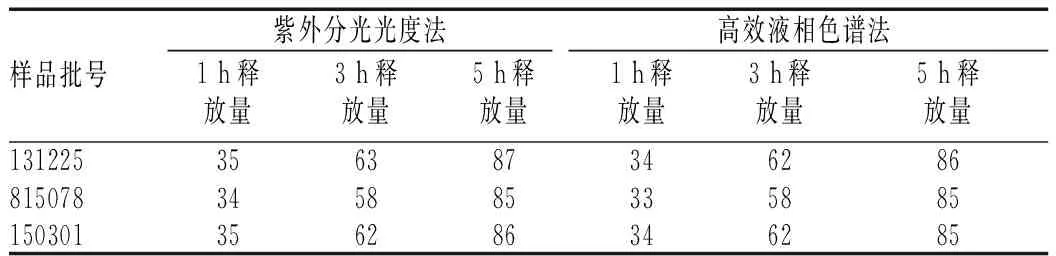
表3 释放度测定结果(%)
3讨论
本研究所用的色谱条件为《中华人民共和国药典:二部》(2015年版)[2]中盐酸二甲双胍肠溶胶囊含量和有关物质测定的色谱条件,该方法分离度好,灵敏度高,故未对其的方法耐用性进行考察。
目前,国家药品标准中收载了盐酸二甲双胍缓释片,其他剂型在《中华人民共和国药典》收载,但含量和释放度的测定方法不统一。本研究为了统一含量和释放度的测定方法,提高检验的效率和准确度,把原有的紫外分光光度法统一为高效液相色谱法,同时对2种方法进行了对比,测定结果相近,可以推广。
参考文献
[1]国家药典委员会.中华人民共和国药典·临床用药须知:化学药和生物制品卷[S].2015年版.北京:人民卫生出版社,2015:432.
[2]国家药典委员会.中华人民共和国药典:二部[S].北京:中国医药科技出版社,2015:859-861.
[3]国家药典委员会.国家食品药品监督管理局国家药品标准[EB/OL].http://www.nifdc.org.cn/jianybz/login.do?method=login.
[4]检验标准管理系统.中国药检标准库[DB/OL].[2016-01-14].http://www.nifdc.org.cn/jianybz/login.do?formAction=home.
[5]陈秀琳.HPLC法测定盐酸二甲双胍缓释片的含量[J].海峡药学,2013,25(12):108-109.
[6]曹玉华,杜熊心.盐酸二甲双胍片溶出度的测定分析[J].亚太传统医药,2009,5(3):33-34.
[7]王荭晖,姚玲,江中赞.盐酸二甲双胍缓释片的体外释放度测定方法的确定[J].安徽医药,2008,12(12):1170-1171.
[8]夏学军,汪仁芸,刘玉玲.盐酸二甲双胍缓释片的HPLC测定[J].中国医药工业杂志,2003,34(4):186-187.
[9]洪志慧,刘毓文.HPLC法测定盐酸二甲双胍缓释片的含量[J].中国现代药物应用,2008,2(18):32-33.
[10]李艺,王红,张良珂,等.HPLC法测定盐酸二甲双胍缓释片中盐酸二甲双胍的含量[J].中国药房,2011,22(24):2296-2297.
[11]孙凌云.HPLC法测定盐酸二甲双胍片的含量和有关物质[J].安徽医药,2010,14(4):408-410.
Content Determination and Release Rate in Metformin Hydrochloride Sustained-release Tablets by HPLC
SONG Xinkang, ZENG Yumei
(Dept.of Chemical, the Food and Drug Control Institute of Meizhou, Guangdong Meizhou 514071, China)
ABSTRACTOBJECTIVE:To establish a method of content determination and release rate in Metformin hydrochloride sustained-release tablets by HPLC. METHODS: C18chromatographic column (150 mm×4.6 mm,5 μm) was adopted, the mobile phase was 0.05% heptane sodium sulfonate solution (with 10% phosphoric acid solution to adjust pH value to 4.0) -acetonitrile(V ∶V=84 ∶16), with flow rate of 0.8 ml/min. The detection wavelength was 233 nm and the column temperature was 35 ℃. RESULTS: Metformin hydrochloride had good linear relationship in 2.45-98.00 μg/ml (r=1, n=6), The recovery rate was 99.2% and RSD was 0.84%. CONCLUSIONS: The method is suitable for Metformin hydrochloride sustained-release tablets quality control.
KEYWORDSHPLC; Metformin hydrochloride sustained-release tablets; Content; Release rate
中图分类号R927.2
文献标志码A
文章编号1672-2124(2016)06-0801-03
DOI10.14009/j.issn.1672-2124.2016.06.030
(收稿日期:2016-01-29)
*副主任药师。研究方向:药品标准的应用和研究。E-mail:may011499@163.com
*工程师。研究方向:制剂技术。E-mail:908552769@qq.com
