镍铁氧体催化过硫酸氢钾对奥卡西平的降解研究
2016-07-14施周衣启航卜令君
施周 衣启航 卜令君

摘要:研究了通过水热合成法制备的镍铁氧体 (NiFe2O4),催化过硫酸氢钾(PMS)产生自由基,在常温常压下降解奥卡西平(OXC).采用扫描电子显微镜 (SEM)、X射线粉末衍射 (XRD) 及磁滞回线对镍铁氧体催化剂进行了表征; 探究了PMS投加量、NiFe2O4投加量以及初始pH对OXC降解效率的影响,结果显示提高PMS和NiFe2O4的投量以及偏中性的初始pH均有利于OXC的降解.通过投加不同种类的猝灭剂(甲醇和叔丁醇),证实了OH·和SO4-·对OXC的降解起着重要作用, 且SO4-· 的作用更显著.此外,进一步的试验发现NiFe2O4具有较好的稳定性和重复利用性:经6次重复使用后,NiFe2O4对OXC的降解效率仍可以维持在88%左右; 并且,PMS/NiFe2O4对滤后水和原水中的OXC也能进行高效催化去除.这些试验结果表明PMS/NiFe2O4催化氧化体系对OXC等PPCPs的降解具有良好的应用前景.
关键词:催化氧化;镍铁氧体;过硫酸氢钾;自由基;奥卡西平
中图分类号:X522 文献标识码:A
随着工业技术的不断发展以及人们环境安全意识的不断提高,水体中新兴的微量有机污染物也开始进入到人们的视野中.药物和个人护理品(pharmaceutical and personal care products,PPCPs)作为一种常见的新兴污染物,因其大量生产、广泛使用以及难以被常规水处理工艺去除等特性[1],不断在地表水[2]、地下水[3] 以及处理水[4] 中被检出,危害着人类的健康.奥卡西平(oxcarbazepine,OXC)作为一种典型的PPCP,是一种新型抗癫痫药物[5].2009年,Ledercq等首次报道了OXC在污水处理厂的出水中被检出[6].近年来,奥卡西平及其同系物的用量日益增加,随之产生的环境问题也逐渐受到了关注.因此,研究OXC的降解及转化对于环境安全问题有着十分重要的意义.
高级氧化(advanced oxidation processes,AOP)是利用生成高活性的自由基(如SO4-·和OH·)来氧化分解有机物的一种工艺,具有强氧化性、选择性小、反应速率快以及反应条件温和等特点,其主要包括UV、电解、臭氧氧化和Fenton法等[7].由于SO4-·具有较高的氧化还原电位(2.5~3.1 V)[8],近年来,以SO4-·为基础的高级氧化已经成为难降解有机物的去除研究热点.SO4-·通常由过硫酸盐(persulfate, PS)或过硫酸氢盐(peroxymonosulfate,PMS)激发生成,相比于PS,PMS由于其分子结构的不对称性,更易于被过渡金属激发[9],但是通常情况下阳离子的获取需要引入大量的阴离子,抑制反应的进行.铁氧体(Fe3-XMXO4)作为一种新型磁性材料,具有特殊的表面结构[10],可以作为PMS的催化剂使用,且不会引入阴离子.另外,由于其具有一定磁性,具有易回收、可重复利用的特点.本文以OXC作为目标污染物、镍铁氧体(NiFe2O4)作为催化剂,探讨NiFe2O4投加量、PMS投加量、初始pH、自由基种类对OXC降解的影响,以及NiFe2O4的重复利用可行性等,为PMS/NiFe2O4在实际水处理方面的应用提供参考.
1材料与方法
1.1试验材料
如无特殊说明,试验所有试剂均为分析纯.OXC(C15H12N2O2,纯度≥99.9%)和PMS (KHSO5·0.5 KHSO4·0.5K2SO4,纯度≥47%)购于阿拉丁药剂公司,甲醇(MeOH,色谱纯,纯度≥99.9%)购于SigmaAldrich公司;氯化镍(NiCl2·6H2O,纯度≥98%)、硫酸亚铁(FeSO4·7H2O,纯度≥99%)、氨水(NH3·H2O,纯度≥99%)、乙二醇(纯度≥99%)、氢氧化钠(NaOH,片状,纯度≥96%)、浓硫酸(H2SO4)、无水乙醇(纯度≥99%)、叔丁醇(TBA,纯度≥99.9%)均购于上海国药集团化学试剂有限公司.试验中所有溶液如无特殊说明均由超纯水配制.试验中滤后水取自长沙市第二水厂,水源水取自湘江长沙段.
1.2NiFe2O4的制备
采用水热法[11] 制备NiFe2O4纳米颗粒.称取1.112 1 g FeSO4·7H2O和0.475 2 g NiCl2·6H2O于250 mL烧杯中,量取60 mL乙二醇和40 mL超纯水倒入烧杯中.待完全溶解后,加入4 mL氨水,用磁力搅拌器搅拌1 h.搅拌完成后将混合溶液倒入100 mL水热高压反应釜中(填充85%左右),置于180 ℃烘箱中反应24 h.反应完成后,将反应釜中黑色沉积物倒入烧杯中,用乙醇和超纯水清洗数遍.洗净后,置于60 ℃烘箱中烘干即得到NiFe2O4.
1.3NiFe2O4表征方法
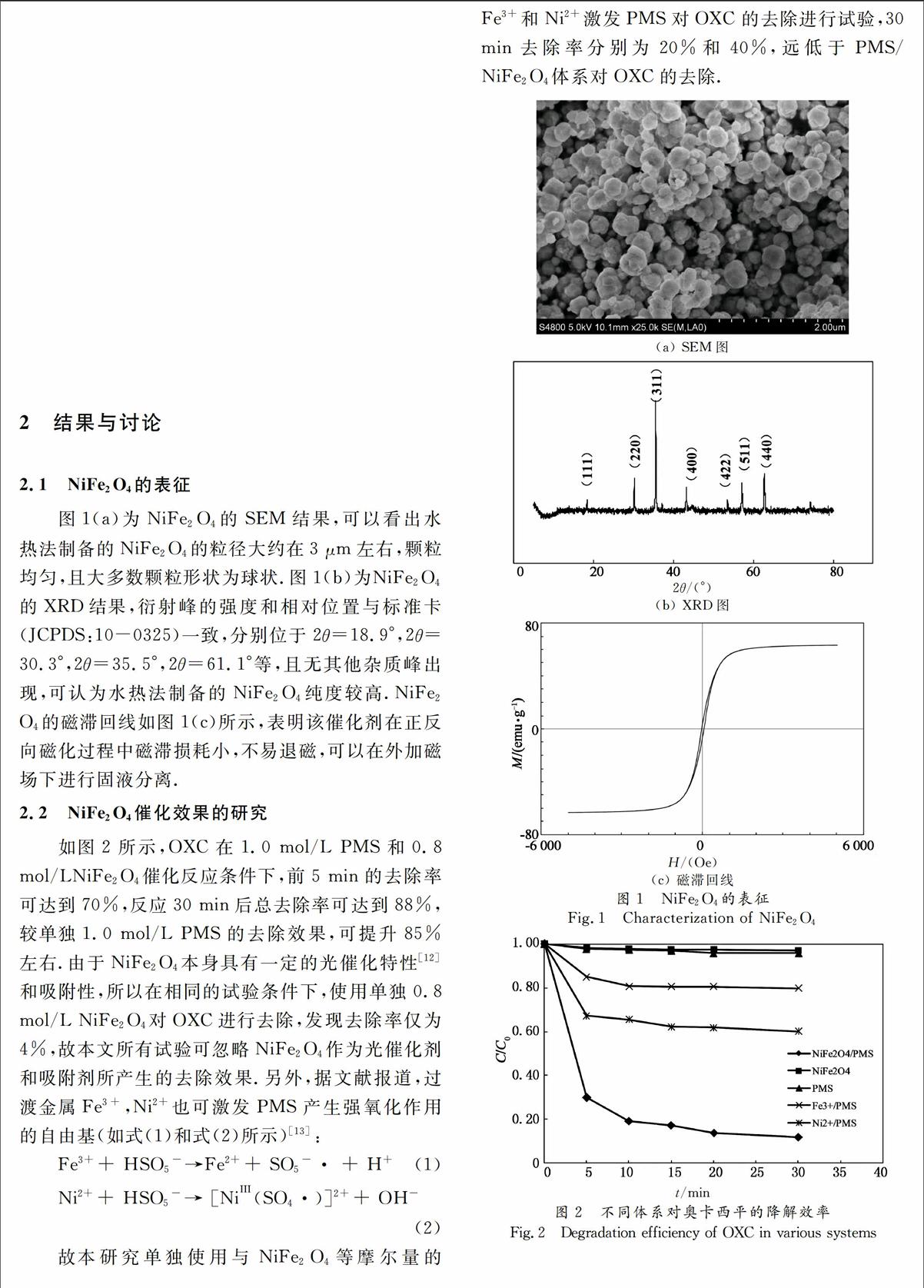
试验中采用了SEM,XRD以及磁滞回线对NiFe2O4进行了表征.其中SEM采用日本JEOL公司的JSM5600LV型扫描电镜进行分析,XRD采用德国布鲁克公司的D8 ADAVNCE型X射线衍射仪,磁性性能采用美国Quantum Design公司生产的MPMSXL7型超导量子干涉磁测量系统进行测试.
1.4试验方法
取25 mL预先配制的80 mol/L的OXC 溶液稀释至100 mL,并移入100 mL锥形瓶中,随后将20 mg NiFe2O4,1 mL 的PMS(0.1 mol/L)加入该锥形瓶中,置于恒温振荡箱恒温(25 ℃)振荡30 min,分别于0 min,5 min,10 min,15 min,20 min,30 min取样,经0.45 μm微孔滤膜滤过后,取样1 mL于液相小瓶中待测.液相小瓶中事先装入100 μL甲醇使反应在各取样时间点立刻停止.
1.5分析方法
试验中所有OXC样品浓度均采用高效液相色谱仪(HPLC,Agilent 1260,美国)测定.使用Symmetry C18柱(150 mm×4.6 mm×5 μm,Agilent,美国)和紫外波长检测器(VWD, Agilent,美国).检测方法:流动相中甲醇和超纯水的质量比为55∶45,流速1.0 mL/min,柱温35 °C.检测波长λ= 254 nm,计算方法:分别配制0 mol/L,1 mol/L,5 mol/L,10 mol/L,20 mol/L,30 mol/L,40 mol/L 标准样品做OXC 的标准曲线(R2=0.999 8),未知样品浓度根据标准曲线计算得到.OXC (20 mol/L)回收率为 (95.2±2.1)%.
3结论
1)单独使用NiFe2O4和PMS对奥卡西平均无明显去除效果,PMS/NiFe2O4体系能够有效降解水中奥卡西平;
2)对于PMS/NiFe2O4体系,较高的PMS和NiFe2O4投量以及偏中性的初始pH更有利于奥卡西平的降解;
3)在PMS/NiFe2O4体系对奥卡西平的降解过程中,SO4-·和OH·均发挥重要作用,且SO4-·作用更显著;
4)水热合成法制备的NiFe2O4催化剂具有较高的稳定性和重复利用性,其对于滤后水和水源水等实际水体中的奥卡西平的仍能高效降解.上述事实表明PMS/NiFe2O4体系可为PPCPs的降解去除提供一种可行的新途径.
参考文献
[1]MAGUREANU M, MANDACHE N B, PARVULESCU V I. Degradation of pharmaceutical compounds in water by nonthermal plasma treatment [J]. Water Research, 2015, 81: 124-136.
[2]KASPRZYKHORDERN B, DINSDALE R M, GUWY A J. The occurrence of pharmaceuticals, personal care products, endocrine disruptors and illicit drugs in surface water in South Wales, UK [J]. Water Research, 2008, 42(13): 3498-3518.
[3]HERBERER T, STAN H J. Determination of clofibric acid and N(phenylsulfonyl) sarcosine in sewage, river and drinking water [J]. International Journal of Environmental Analytical Chemistry, 1997, 67:113-124.
[4]BOYD G R, REEMTSMA H, GRIMM D A, et al. Pharmaceuticals and personal care products (PPCPs) in surface and treated waters of Louisiana, USA and Ontario, Canada [J]. Science of the Total Environment, 2003, 311(1/3): 135-149.
[5]EMRICH H M, DOSE M, VON Z D. The use of sodium valproate, carbamazepine and oxcarbazepine in patients with affective disorders [J]. Journal of Affective Disorders, 1985, 8(3): 243-250.
[6]LEDERCQ M, MATHIEU O, ELENA G, et al. Presence and fate of carbamazepine, oxcarbazepine, and seven of their metabolites at wastewater treatment plants [J]. Archives of Environmental Contamination and Toxicology, 2009, 56(1/3): 408-415.
[7]ANDREOZZI R, CAPRIO V, INSOLA A, et al. Advanced oxidation processes (AOP) for water purification and recovery [J]. Catalysis Today, 1999, 53(1):51-59.
[8]NETA P, HUIE R E, ROSS A B. Rate constants for reactions of inorganic radicals in aqueous solution [J]. Journal of Physical and Chemical Rerference, 1988, 17(3): 1027-1284.
[9]GUAN Yinghong, MA Jun, REN Yueming, et al. Efficient degradation of atrazine by magnetic porous copper ferrite catalyzed peroxymonosulfate oxidation via the formation of hydroxyl and sulfate radicals [J]. Water Research, 2013, 47(14):5431-5438.
[10]WEI Gaoling, LIANG Xiaoliang, HE Zisen, et al. Heterogeneous activation of Oxone by substituted magnetites Fe3-XMXO4 (Cr, Mn, Co, Ni) for degradation of Acid Orange II at neutral pH [J]. Journal of Molecular Catalysis A: Chemical, 2015, 398: 86-94.
[11]DENG Lin, SHI Zhou, PENG Xiaoxu. Adsorption of Cr(VI) onto a magnetic CoFe2O4/MgAlLDH composite and mechanism study [J]. RSC Advances, 2015, 61(5):49791-49801.
[12]PENG Tianyou, ZHANG Xiaohu, LV Hongjin, et al. Preparation of NiFe2O4 nanoparticles and its visiblelightdriven photoactivity for hydrogen production [J]. Catalysis Communications, 2012, 28:116-119.
[13]ANIPSITAKIS G P, DIONYSIOU D D. Radical generation by the interaction of transition metals with common oxidants [J]. Environmental Science & Technology, 2004, 38(13): 3702-3705.
[14]DENG Jing, SHAO Yisheng, GAO Naiyun, et al. CoFe2O4 magnetic nanoparticles as a highly active heterogeneous catalyst of oxone for the degradation of diclofenac in water [J]. Journal of Hazardous Materials, 2013, 262: 836-844.
[15]REN Yueming, DONG Qing, FENG Jing, et al. Magnetic porous ferrospinel NiFe2O4: A novel ozonation catalyst with strong catalytic property for degradation of dinbutyl phthalate and convenient separation from water [J]. Journal of Colloid and Interface Science, 2013, 382: 90-96.
[16]RASTOGI A, ALABED S R, DIONYSIOU D D, et al. Sulfate radicalbased ferrousperoxymonosulfate oxidative system for PCBs degradation in aqueous and sediment systems [J]. Applied Catalysis BEnvironmental, 2009, 85(3/4): 171- 179.
[17]XIE Pengchao, MA Jun, LIU Wei, et al. Removal of 2MIB and geosmin using UV/persulfate: Contributions of hydroxyl and sulfate radicals [J]. Water Research, 2015, 69: 223-233.
