卤氧化铋与半导体光催化剂偶合研究新进展
2016-06-15崔玉民李慧泉陶栋梁凡素华
崔玉民, 李慧泉, 苗 慧, 陶栋梁, 凡素华
阜阳师范学院化学与材料工程学院, 安徽环境污染物降解与监测省级实验室, 安徽 阜阳 236037
卤氧化铋与半导体光催化剂偶合研究新进展
崔玉民, 李慧泉, 苗 慧, 陶栋梁, 凡素华
阜阳师范学院化学与材料工程学院, 安徽环境污染物降解与监测省级实验室, 安徽 阜阳 236037
两种半导体耦合能够形成异质结而使系统的电荷分离效率得到提高,扩展对光谱吸收范围,以便提高其光催化性能。 半导体耦合在制备过程中容易受到制备方法、 反应温度等影响,引起耦合半导体晶体结构和表面性质发生变化,从而使得其光催化量子效率增大。 主要从以下三个方面进行了论述, (1) 卤氧化铋-氧化物偶合体系, 将半导体材料与BiOX进行复合,能够形成高效异质结型结构能提高光催化降解污染物光催化性能; (2)AgX-BiOX偶合体系, 与纯净的AgI或BiOI相比,复合光催化材料AgI/BiOI在可见光下具有更高的光催化反应活性。 (3)卤氧化铋与其它化合物偶合体系,Bi2S3与BiOX进行偶合后,光生电子在两种催化剂中进行迁移,提高了电子与空穴分离效率,因而偶合物的光催化性能得到提高。 另外,本文综述了近年来国内外半导体耦合制备方法、 影响其光催化性能的因素、 提高可见光利用效率的最新研究进展,并提出在半导体耦合研究中所要解决的主要问题及今后努力方向。
卤氧化铋; 异质结; 光催化; 耦合体系
引 言
半导体耦合是提高光催化效率的重要方法。 根据文献报道半导体耦合能够使系统的电荷分离效率得到有效提高, 扩展对光谱吸收范围[1]。 研究结果发现, 半导体耦合能够使一种半导体光催化量子效率得到提高[2]。 由于半导体复合能够在二者界面形成异质结, 这样能充分利用两种半导体能级结构的互补性, 也就是利用两种半导体之间的能级差使得电荷(电子与空穴)得到有效分离, 从而实现促使光生电子与空穴对分离、 转移及传递的目的, 即抑制了光生电子与空穴的复合[3-4]。 目前, 关于BiOX的许多耦合体系, 比如BiOI/Bi2WO6[5], BiOCl/BiOBr[2], BiOBr-g-C3N4[3], Ag/AgBr/BiOBr[6], (BiO)2CO3/BiOBr[7]和BiOI/ZnSn(OH)6[8]等已经报道, 比单独BiOX的催化剂具有更高光催化活性。 例如, Jiang等[9]研究发现ZnO/BiOI复合光催化剂的催化活性高于纯ZnO和纯BiOI, 研究结果表明提高光催化活性主要归因于这样一个事实: 在ZnO与BiOI的截面形成异质结, 使得光生电子与空穴对发生有效分离。 2012年, Cao等[10]发现在可见光照射下(>420 nm) Bi2S3/BiOI光催化降解甲基橙与纯BiOI相比具有优异的光催化活性, Bi2S3/BiOI光催化活性之所以增强, 是因为Bi2S3与BiOI形成异质结, 导致光生载流子的有效分离, 因而Bi2S3/BiOBr复合体系是增强光生载流子有效分离理想体系, 从而提高其光催化活性。
1 卤氧化铋-氧化物偶合体系
将半导体材料与BiOX进行复合, 能够形成高效异质结型结构, 并形成合适带隙能量、 相匹配的能带位置, 且由于其密切的接触都能提高光催化降解污染物光催化性能。 Cao等[11]通过氢碘酸与(BiO)2CO3反应制备p-n型BiOI/(BiO)2CO3异质结催化剂, 其相匹配的能带结构能够使电荷得到有效分离。 Chai等[12]研究了BiOCl/Bi2O3异质结光催化材料发现纯BiOCl或纯Bi2O3在可见光下降解污染物的能力较低, 然而, BiOCl/Bi2O3异质结光催化材料显示较高光催化活性。 因为三氧化二铋作为敏化剂在异质结中能吸收可见光, BiOCl在位于异质结材料的外层, 电子从BiOCl价带跃迁后留下的空穴(h+)将有机物污染物降解矿化成无机物。 Chakraborty等[13]研究发现在BiOCl/Bi2O3表面涂盖三氧化钨能够使BiOCl/Bi2O3的光催化和稳定性能提高, 然而, 当三氧化钨的用量过大时, 反而使得BiOCl/Bi2O3光催化活性急速降低。 Zhang等[14]合成了Fe3O4/BiOCl磁性复合光催化剂, 与一般催化剂Fe3O4/TiO2相比, 他们所制备的Fe3O4/BiOCl显示出更高光催化降解有机染料的催化活性。 这是因为BiOCl在复合催化剂中仍保留其特殊的层状结构, 且与Fe3O4形成异质结结构和特殊界面接触, 从而降低电子与空穴复合概率, 也就提高了光催化反应活性。
Li等[1]在室温条件下, 利用沉积法制备了BiOI敏化纳米锐钛矿型二氧化钛复合催化剂。 并研究了催化剂用量、 pH值、 甲基橙(MO)的起始浓度及KI用量对BiOI/TiO2光催化降解MO的影响, 其结果表明在优化条件下, BiOI/TiO2的可见光催化活性明显高于P25(TiO2), 而BiOI/TiO2的紫外光催化活性稍高于P25, 其反应最佳pH值为3.0, BiOI在BiOI/TiO2中最佳质量百分率为1.7%。 由于pH值对MO光催化效率影响受到多种因素制约, 例如在半导体光催化剂界面发生相关反应引起MO的降解, 因此对于pH值影响很难做出满意解释[15-16]。
Photocatalyst(光催化剂)+hν→e-+h+
h++H2O→·OH+H+
h++OH-→·OH
HOO·+HOO·→O2+H2O2
H2O2+e-→·OH+OH-
TiOH是表面基团, 预计甲基橙和1.7% BiOI/TiO2催化剂表面上的电荷将决定吸附程度是合理的。 当pH
2 AgX-BiOX偶合体系
由于AgX具有特殊的感光性能而被广泛应用在光催化剂及感光材料领域, 然而, 在AgX光照条件下不够稳定。 Cheng等[19]研究发现, 与纯净的AgI或BiOI相比, 复合光催化材料AgI/BiOI在可见光下具有更高的光催化活性, 并且, 最佳光催化活性的复合物是AgI在AgI/BiOI中质量百分率为20%。 他们利用荧光技术及实验分析发现, 由于电子跃迁留下的空穴(h+)成为主要的活性物种, 使AgI/BiOI光催化活性得到显著提高, 并且复合物AgI/BiOI显示了很好的稳定性。

3 卤氧化铋与其他化合物偶合体系
Liu[21]通过溶剂热法将CdS负载在BiOBr的片状结构上而形成异质结, 在内建电场和层状空间共同作用下, 光生电子与空穴对能够进行有效分离, 从而提高其光催化反应活性。 还有很多半导体光催化剂能够对BiOX进行改性提高其光催化活性, 例如, Bi2S3[22], BiWO6[23]等与BiOX进行偶合后, 二者之间由于能带差异, 光生电子在两种催化剂中迁移, 提高了电子与空穴分离效率, 因而偶合物的光催化性能得到提高。 Fu等[24]利用沉淀法把BiOBr沉积在C3N4表面上, 发现BiOBr/C3N4复合物的可见光响应与异质结结构的能带存在密切关系。 以罗丹明B作为模型污染物, 在优化条件下, BiOBr/C3N4复合物光催化活性分别是纯BiOBr、 纯C3N4的4.9倍、 17.2倍, 而且其光催化活性也明显高于C3N4/TiO2和BiOBr/TiO2异质结活性。
3.1 BiOI/Bi2WO6偶合体系
近年来, 典型的奥里维里斯氧化物Bi2WO6由于其优良的物理和化学特性在许多研究领域引起了广泛的关注, 并且, 其在染料和污染物降解方面是一种良好的可见光光催化剂, 然而, 由于其只能吸收小于450 nm光导致其光催化活性不够高, 因为吸收此波段的光增大了光生电子与空穴的复合概率[25-27]。 为了提高Bi2WO6光催化性能, 对其进行掺杂改性, 比如掺杂C60[28]、 贵金属Ag沉积[29]、 与AgBr偶合[30]以及与其他窄带隙能半导体复合在一起使用。 最近, 所制备的微纳米结构材料BiOI由于其在光催化降解环境物方面显示了高效性而引起了广泛关注[31-33]。 BiOI的带隙能为1.8 eV, 能够吸收大部分可见光, 而且对于宽带隙能半导体能够产生光敏化作用。 Chen等[34]采用一种简单的化学腐蚀方法, 以醋酸和KI为腐蚀剂与BiOBr反应合成了BiOI/BiOBr异质结催化剂, 所制备的BiOI/BiOBr样品与纯BiOI或纯BiOBr相比显示较高的可见光催化活性(λ>420 nm), 这归功于BiOI/BiOBr异质结形成导致光生电子与空穴得到有效分离。 Li等[5]采用室温沉积方法合成不同含量BiOI的BiOI/Bi2WO6复合催化剂。 通过对活性艳红X-3B光催化降解来考察BiOI/Bi2WO6复合催化剂催化活性。 实验结果表明随着BiOI在BiOI/Bi2WO6中质量百分比的增加, BiOI/Bi2WO6在380~600 nm范围对光的吸收强度逐渐增大, 且其吸收带边沿长波方向发生明显红移。 吸附研究表明, 与Bi2WO6催化剂相比, 13.2% BiOI/Bi2WO6催化剂对X-3B吸附能力更强。 对于甲苯和X-3B光催化降解活性, BiOI/Bi2WO6复合催化剂与单一的BiOI和Bi2WO6相比具有较高的紫外及可见光催化活性。 并用半导体催化剂能带位置和光致发光光谱讨论了BiOI/Bi2WO6增强反应机理。 不仅提供了一个在室温下简单合成BiOI敏化增强光催化纳米材料属性的方法, 而且还提供了一个设计高性能紫外和可见光驱动催化剂在环境和能源领域中应用有效途径。
3.2 BiOI/ZnSn(OH)6偶合体系
由于ZnSn(OH)6具有无毒性和安全性而被广泛应用于高效阻燃剂[35-36], 它是一种钙钛矿结构型氢氧化物, 其表面布满了OH基, 而OH基与光生电子结合形成羟基自由基(·OH), ·OH在光催化反应中是氧化性物种[37]。 2012年, Chen等[38]研究发现ZnSn(OH)6在光催化降解苯过程中显示了较高的紫外光催化活性。 另外, Fu等[37]报道ZnSn(OH)6在即使不担载贵金属情况下也表现了很高的光催化降解苯活性, 并且, 在紫外光照射50 h后, 其光催化反应活性也不降低。 然而ZnSn(OH)6具有宽的带隙能(Eg=4.0 eV)[38], 因此它只能利用占太阳能很少的部分紫外光。 为了使ZnSn(OH)6光向应范围从紫外光区域向可见光区域扩展, 以便提高光生电子与空穴分离效率, 所要采取常见措施之一是将ZnSn(OH)6与窄带隙半导体复合应用。 最近, BiOI作为一个有前景的光催化剂, 由于其在光催化降解有机污染物方面具有潜在的应用而引起了研究者的广泛兴趣[33-35]。 BiOI作为一个典型的p型半导体, 它可能是一个潜在的贵金属助催化剂的替代品。 BiOI/ZnSn(OH)6复合催化剂对于扩展其可见光响应范围及提高光生载流子的分离效率可能是一个理想体系。 Li等[8]于80 ℃采用温和沉积方法合成不同含量BiOI的BiOI/ZnSn(OH)6复合催化剂, 利用ZnSn(OH)6复合催化剂对光解乙醇产生H2及光催化降解苯酚进行研究。 结果表明当ω(BiOI)为19.7%和32.9%时, BiOI/ZnSn(OH)6展示正方晶系BiOI与立方钙钛矿晶系ZnSn(OH)6两者共存。 随着BiOI含量的增加, BiOI/ZnSn(OH)6在280~550 nm区域内光吸收强度逐渐增大, 值得注意的是BiOI/ZnSn(OH)6的吸收带边与纯净的ZnSn(OH)6相比向长波方向移动。 BiOI在BiOI/ZnSn(OH)6中的质量含量为19.7%时, BiOI/ZnSn(OH)6的相态和结构反应前后保持不变, 表明催化剂在光催化降解过程中保持稳定, 并且, ZnSn(OH)6复合催化剂与纯净的BiOI或ZnSn(OH)6相比具有较高的光催化活性, 这要归因于BiOI与ZnSn(OH)6紧密接触而使得其电荷更易转移及电子与空穴对有效分离, 从而提高复合催化剂BiOI/ZnSn(OH)6光催化活性。 这可从以下反应机理得到解释(如图1所示)。
两种具有不同的氧化还原能级的价带和导带半导体, 能够提高光生电子和空穴对的分离效率和光生电子的转移[9]。 从图1可以看到, ZnSn(OH)6价带和导带的值分别是4.20和0.49 eV, BiOI价带和导带的值分别是2.31和0.57eV。 显而易见, ZnSn(OH)6和BiOI能带之间的差距可以促使光生电子和空穴对在其能带之间进行转移。 当BiOI/ZnSn(OH)6样品被紫外光照射时, BiOI和ZnSn(OH)6都能够被激发, 进而在BiOI/ZnSn(OH)6系统中产生了大量的光生电子和空穴对。 光生电子从ZnSn(OH)6的导带转移到BiOI的导带上, 因为当ZnSn(OH)6与BiOI接触时, ZnSn(OH)6的导带电位与BiOI的导带电位相比更负, 因此电子从ZnSn(OH)6向BiOI转移, 导致了负电荷在靠近BiOI的连接处累积, 与此同时, 空穴对从BiOI的价带转移到ZnSn(OH)6的价带上, 当ZnSn(OH)6和BiOI的费米能级平衡时, 这种电荷扩散被阻止, 同时ZnSn(OH)6的能带向下移动靠近费米能级, 然而BiOI的能带向上移动[9, 36, 39][见图1(b)]。 在可见光照射下, BiOI被激发产生光生电子空-穴对。 BiOI的新导带边电位(约-0.65 eV)与ZnSn(OH)6的新导带边电位相比更负[36, 39], 从而导致光诱导电子从BiOI表面很容易地迁移到ZnSn(OH)6的CB能级上, 同时光激发的空穴保留在BiOI的价带(VB)上, 此外, 内在电场能够促进光生电子与空穴迁移, 因此, 光生电子与空穴对的复合受到有效地抑制, 相应的紫外和可见光的光催化活性将大大提高, 具体如式(1)—式(8)所示
(1)
(2)
(3)
(4)
(5)

(6)
phenol+H2O2→products
(7)

(8)
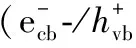

图1 在紫外(a)和可见光(b)照射下BiOI和ZnSn(OH)6的光生电子与空穴迁移及能级图
3.3 Bi2S3/BiOBr偶合体系
溴氧化铋(BiOBr)作为最好的催化剂之一, 由于其优良的光学特性已被广泛应用于环境污染物的降解[40-42]。 最近, 许多研究发现BiOBr复合催化剂具有优越性而引起广泛关注。 到目前为止, 报道了很多BiOBr偶合体系, 比如BiOCl/BiOBr[2], BiOBr-g-C3N4[3], Ag/AgBr/BiOBr[6], (BiO)2CO3/BiOBr[7], 这些偶合催化剂比单一的半导体催化剂具有更高的光催化性能。 另外, 通常用溶剂热法[2]、 化学浴法[3, 6]和酸腐蚀等方法[7]合成BiOBr复合材料。 然而, 这些制备方法通常涉及使用添加剂或表面活性剂以及用有机溶剂进行处理。 Bi2S3具有窄的带隙能(~1.30 eV)[43], BiOBr具有宽的带隙能(2.74~2.95 eV)[2-3, 6-7]。 Cao等[10]研究发现具有异质结构的Bi2S3/BiOI在光催化降解甲基橙过程中与纯BiOI相比显示良好的可见光(>420 nm)催化活性, Bi2S3/BiOI样品光催化活性增强的原因主要是Bi2S3和BiOI的表面形成的异质结能够促使光生电子与空穴对得到有效分离, 从而抑制了光生载流子的复合概率。 Bi2S3/BiOBr复合可能是一个理想的系统, 这个体系可以提高光生电子与空穴对的分离效率, 从而提高其光催化性能。 Cui等[44]于433 K采用温和水热方法合成不同质量百分含量Bi2S3的Bi2S3/BiOBr复合催化剂, 通过光催化降解甲基橙溶液来探究复合催化剂Bi2S3/BiOBr光催化活性。 研究结果发现复合催化剂Bi2S3/BiOBr光催化活性高于纯净的Bi2S3或BiOBr光催化活性。 其光催化活性增强的主要原因是: (1) Bi2S3与BiOBr间能形成异质结, 异质结可使BiOBr中的光生电子-空穴对得到更有效的分离, 从而提高光催化活性[9-10]; (2) Bi2S3使BiOBr的吸收带边向长波方向移动, 拓展了光的吸收范围, 从而提高光催化活性[44]。
4 卤氧化铋偶合光催化剂研究存在的问题及发展趋势
卤氧化铋与半导体偶合光催化剂作为一种新型的复合光催化剂, 虽然其在紫外光和可见光激发作用下具有较好的光催化活性, 但是, 卤氧化铋与半导体偶合光催化材料依然存在较多关键的科学技术问题, 这将抑制其工业化推广应用, 需要从三个方面进一步深入研究: (1)已开发的新型偶合光催化剂的光催化反应机理的研究还处于初步设想及推测阶段, 仍然需要实验进行验证, 即必须经过不断深入的研究和实践, 才能使得其光催化反应机理更加清晰、 更加成熟; (2)对于偶合光催化剂, 尽管研究发现了多种可见光响应光催化剂, 但是大多数光催化反应效率较低。 其中, 一部分光催化剂在可见光范围内催化能力并不高。 因而对现有体系需要进一步修饰改性; (3)通过以上研究发现, 卤氧化铋偶合光催化剂主要为粉末和薄膜, 进一步研究各种催化剂固定化技术、 催化剂表面改性技术及设计新颖、 长效的光催化装置仍是有待研究新课题。
[1] Li H Q, Cui Y M, Hong W S, et al. Rare Metals, 2012, 31(6): 604.
[2] Zhang J, Xia J X, Yin S, et al. Colloids Surf. A, 2013, 420: 89.
[3] Ye L Q, Liu J Y, Jiang Z, et al. Appl. Catal B, 2013, 142-143: 1.
[4] Li H Q, Cui Y M, Wu X C, et al. Acta Phys.-Chim. Sin., 2012, 28(8): 1985.
[5] Li H Q, Cui Y M, Hong W S. Applied Surface Science, 2013, 264: 581.
[6] Ye L Q, Liu J Y, Gong C Q, et al. ACS Catal, 2012, 2: 1677.
[7] Cao J, Li X, Lin H L, et al. Appl. Surf. Sci., 2013, 266: 294.
[8] Li H Q, Cui Y M, Hong W S, et al. Chemical Engineering Journal, 2013, 228: 1110.
[9] Jiang J, Zhang X, Sun P B, et al. J. Phys. Chem. C, 2011, 115: 20555.
[10] Cao J, Xu B Y, Lin H L, et al. Dalton Trans., 2012, 41: 11482.
[11] Cao J, Li X, Lin H L, et al. J. Hazar Mater, 2012, 239/240: 316.
[12] Chai S Y, Kim Y J, Jung M H, et al. J. Catal, 2009, 262: 144.
[13] Chakraborty A K, Rawal S B, Han S Y, et al. Appl. Catal A-Gen., 2011, 407: 217.
[14] Zhang L, Wang W Z, Zhou L, et al. Appl. Catal B-Environ., 2009, 90: 458.
[15] Muruganandham M, Swaminathan M. Dyes Pigm., 2006, 68(2-3): 133.
[16] Bauer C, Jacques P, Kalt A. J. Photochem. Photobiol. A, 2001, 140(1): 87.
[17] Tang W Z, Huang C P. Water Res., 1995, 29(2): 745.
[18] Galindo C, Jacques P, Kalt A. J. Photochem Photo.-biol. A, 2000, 130(1): 35.
[19] Cheng H F, Huang B B, Ying D, et al. Langmuir., 2010, 1(56): 1.
[20] Kong L, Jiang Z, Lai H H, et al. J. Catal, 2012, 293: 116.
[21] Liu Z S, Wu B T, Zhu Y B, et al. J. Colloid Interf. Sci., 2013, 392: 337.
[22] Cao J, Xu B Y, Lin H L, et al. Catal Comm., 2012, 26: 204.
[23] Li Y L, Liu Y M, Wang J S, et al. J. Phys. Chem. A, 2013, 1: 7949.
[24] Fu J, Tian Y L, Chang B B, et al. J. Mater. Chem., 2012, 22: 21159.
[25] Zhang Z J, Wang W Z, Shang M, et al. J. Hazard Mater, 2010, 177: 1013.
[26] Wu L, Bi J L, Li Z H, et al. Catal Today, 2008, 131: 15.
[27] Zhao X, Xu T G, Yao W Q, et al. Appl. Catal B: Environ., 2007, 72: 92.
[28] Zhu S B, Xu T G, Fu H B, et al. Environ. Sci. Technol., 2007, 41: 6234.
[29] Ren J, Wang W Z, Sun S M. Appl, Catal B: Environ., 2009, 92: 50.
[30] Zhang L S, Wong K H, Chen Z G. Appl. Catal A: Gen., 2009, 221: 363.
[31] Xia J X, Yin S, Li H M, et al. Colloids Surf. A: Physicochem. Eng. Aspects, 2011, 387: 23.
[32] Li Y Y, Wang J S, Yao H C, et al. J. Mol. Catal A: Chem., 2011, 334: 116.
[33] Wang Y N, Deng K J, Zhang L Z. J. Phys. Chem. C, 2011, 115: 14300.
[34] Cao J, Xu B Y, Lin H L, et al. Chem. Eng. J., 2012, 185-186: 91.
[35] Xu J Z, Zhang C Y, Qu H Q, et al. J. Appl. Polym. Sci., 2005, 98: 1469.
[36] Andre F, Cusack P A, Monk A W, et al. Polym. Degrad Stab., 1993, 40: 267.
[37] Fu X L, Wang X X, Ding Z X, et al. Appl. Catal B: Environ., 2009, 91: 67.
[38] Chen Y B, Li D Z, He M, et al. Appl. Catal B: Environ., 2012, 113-114: 134.
[39] Li Y Y, Wang J S, Yao H C, et al. Catal Commun., 2011, 12: 660.
[40] Xu J, Li L, Guo C S, Zhang Y, et al. Chem. Eng. J., 2013, 221: 230.
[41] Fang Y F, Huang Y P, Yang J, et al. Environ. Sci. Technol., 2011, 45: 1593.
[42] Wang Y, Shi Z Q, Fan C M, et al. Solid State Chem., 2013, 199: 224.
[43] Bessekhouad Y, Robert D, Weber J V, et al. J. Photochem. Photobiol. A, 2004, 163: 569.
[44] Cui Y M, Jia Q F, Li H Q, et al. Applied Surface Science, 2014, 290: 233.
The Latest Research Progress of Coupling between BiOX and Semiconductor Photocatalyst
CUI Yu-min, LI Hui-quan, MIAO Hui, TAO Dong-liang, FAN Su-hua
College of Chemistry and Materials Engineering, Fuyang Teacher’s College, Anhui Provincial Key Laboratory for Degradation and Monitoring of Pollution of the Environment, Fuyang 236037, China
The heterojunction was formed between two kinds of coupling semiconductors , which improved the charge separation efficiency of system, widened the spectral response range of catalysts and improved photocatalytic propertirs of catalysts. The process of preparation of semiconductors coupling was easily affected by preparation methods and reaction temperature and so on, which would cause the changes in crystal structure and surface properties of coupling semiconductors, thus photocatalytic quantum efficiency of coupling semiconductors was increased. In this article, the following three aspects were mainly discussed. (1) About the coupled system of halogen bismuth oxide and oxide, because generaling BiOX with the semiconductor material compound, the efficient heterojunction structure could be formed, photocatalytic performances of the photocatalytic degradation of pollutants were improved. (2) About the coupled system of AgX and BiOX, compared with the pure AgI or BiOI, composite photocatalytic materials of AgI/BiOI had higher photocatalytic reactivity in visible light. (3) About the coupled system of halogen bismuth oxide and other compounds, after Bi2S3coupled with BiOX, photoproduction electronic migrated in the two kinds of catalysts, the separation efficiency of electrons and holes was improved, and photocatalytic performances of coupling compound were improved. In addition, in recent years, the latest research progress of the preparation method, the influencing factors of the photocatalytic performance and improving the utilization efficiency of visible light of semiconductors coupling at home and abroad was reviewed in this paper. Finally, the main problems and the future striving direction in semiconductors coupling were presented.
BiOX; Heterojunction; Photocatalysis; Coupling system
Feb. 9, 2015; accepted Jun. 19, 2015)
2015-02-09,
2015-06-19
国家自然科学基金项目(21201037), 安徽省自然科学基金项目(1408085MB35), 安徽省高等学校省级自然科学研究重大项目(KJ2016SD46), 安徽省科技计划项目(1606C08227), 阜阳师范学院科技成果孵化基金项目(2013KJFH01), 阜阳师范学院校企合作实践教育基地项目(2013SJJD05)资助
崔玉民, 1963年生, 阜阳师范学院化学与材料工程学院教授 e-mail: cymlh@126.com
O643
A
10.3964/j.issn.1000-0593(2016)08-2579-06
