NaClO2水溶液脱硝的工艺条件及机理
2016-06-02叶春波涂先红李朝恒裴旭东陈卫红
叶春波,涂先红,李朝恒,裴旭东,陈卫红
中石化炼化工程(集团)股份有限公司洛阳技术研发中心,河南 洛阳 471003
NaClO2水溶液脱硝的工艺条件及机理
叶春波,涂先红,李朝恒,裴旭东,陈卫红
中石化炼化工程(集团)股份有限公司洛阳技术研发中心,河南 洛阳 471003
摘要:在小型填料塔中考察了NaClO2初始浓度、NO初始浓度、反应温度、初始pH值和液气比等因素对NaClO2水溶液吸收NOx过程的影响,分析了NaClO2水溶液脱硝的过程特性,并解析了NaClO2与NOx之间的反应机理。结果表明,NaClO2水溶液具有优良的脱硝性能,在合适的操作条件下,NO转化率可达到100%。
关键词:亚氯酸钠 氮氧化物 氧化脱硝 反应机理
近年来,重质原油的供应及加工量不断增加,重质油加工逐渐受到重视,这导致炼厂NOx排放量逐年增加。石化企业的NOx排放量占我国NOx总排放量的5%左右,其中近一半NOx来自催化裂化(FCC)装置,严重影响了炼厂所在地的空气质量。随着我国环境形势的日益严峻,必须控制FCC烟气中NOx的排放。目前,FCC烟气中NOx的达标减排主要采用选择性催化还原脱硝(SCR)技术,该技术在330~450 ℃,利用NH3或尿素等还原剂将烟气中的NOx催化还原为N2[1,2],从而减量排放NOx。但将SCR技术应用于FCC烟气脱硝时,需要对现有余热锅炉系统进行改造,投资成本较高。湿法烟气脱硝技术具有投资成本低、工艺简单和易于控制等特点,得到研究者的关注。但在通常情况下,烟气中NO2含量小于5%,NO2和NO体积比(即氧化度)过低导致采用硝酸[3]、氢氧化钠[4]和尿素[5,6]等溶液作为吸收剂脱除NOx所需的停留时间过长,不适合工业应用。为缩短湿法脱硝过程的停留时间,本工作选用亚氯酸钠(NaClO2)水溶液为脱硝吸收剂。NaClO2水溶液具有强氧化性,可将NOx氧化并最终转化为NO3-吸收,吸收过程所需的停留时间短,能达到工业应用的实际要求。因此,本工作以小型填料塔为吸收设备,考察了NaClO2初始浓度、NO初始浓度、反应温度、初始pH值和液气比等因素对NaClO2吸收NOx过程的影响,并分析了NaClO2水溶液与NOx的反应过程,以期为NaClO2水溶液脱硝过程的工业化应用提供一定的指导。
1 实验部分
1.1 实验流程
本实验流程包含配气、吸收反 应和在线检测三个系统,实验流程见图1。
配气系统包括转子流量计、质量流量控制器、缓冲罐、气体混合器和蒸汽发生器等,NO,N2与空气先混合,再经蒸汽发生器加湿升温后形成模拟烟气,NO,N2与空气的流量通过各自的质量流量计调节,而总气体流量则由转子流量计控制。
吸收反应系统由金属网环填料塔、储罐、计量泵和电加热带组成。模拟烟气由塔底部进入填料塔(30×500 mm,自制)与吸收液逆流接触后从塔顶排出。净化气经碱液吸收后排空,吸收富液由塔釜排出进入储罐。进料管线包有电加热带,在吸收液进料过程中,可将吸收液加热至设定温度,填料塔由电加热带加热保温。本吸收系统压降很低,最大压降不超过2 kPa。
在线检测系统由烟气分析仪和冷阱(自制)组成。在吸收塔进出口分别设置气体采样口,分析吸收前后烟气中NO含量。为防止烟气中夹带的水蒸汽损坏烟气分析仪的传感器,采样气体需先经冷阱脱除水蒸汽后,再与烟气分析仪连接。

图1 FCC烟气湿法脱硝实验流程Fig.1 Schematic diagram of the pilot experiment of wet denitrification process of FCC flue gas 1,2,3-buffer tank; 4,5,6-mass flow controller; 7-flue gas analyzer; 8-cold trap; 9,10- ball valve; 11-rotary flowmeter; 12-gas mixer;13-packer tower; 14-steamer; 15-absorption enrichment; 16,20-storage tank; 17-purified gas; 18-alkali absorption tank;19-measuring pump
1.2 分析方法
1.2.1 NOx浓度的测定
本实验使用烟气分析仪和气体检测管(日本光明理化学株式会社175SA型)分别检测装置进出口中NO和NO2浓度。当烟气分析仪与气体检测管的示数均达到稳定状态且在3 min内不发生改变,记录所测的数据,即为NO和NO2浓度。
1.2.2吸收液分析
2 结果与讨论
2.1 工艺条件的影响
2.1.1 NaClO2初始浓度的影响
当气时空速(GHSV)为0.3 s-1,NO进口含量(CNO)为400 mg/m3,O2含量(CO2,体积分数)为3%,反应温度(T)为60 ℃,液气比(L/G)为2.0 L/m3,常压下考察NaClO2浓度(CNaClO2)对脱硝过程的影响,结果见图2。由图可知,伴随着NaClO2浓度的增大,NO的转化率呈线性增加,当NaClO2浓度达到4 mmol/L后,NO转化率可达到100%。采用反应扩散方程计算可得NaClO2与NO的反应速率常数为6.55×108L2/(s·mol2),属于快速反应[8],因而即使在较低的浓度下,NaClO2溶液也可以展现出良好的氧化和脱硝性能。由图还可以看出,随着NaClO2浓度的增加,脱硝率快速提高,NaClO2浓度增加至5 mmol/L后,NOx去除率趋于稳定。这是由于在吸收液中NaClO2含量较低的情况下,提高NaClO2浓度有助于提高反应速率,使反应向NOx被吸收的方向移动;而当NaClO2浓度增加至一定程度后,反应速率远大于气液间的传质速率,气液传质速率已经成为影响NOx脱除的控制步骤,此时继续增大NaClO2浓度,NOx脱除率的升高趋势减缓。因此,当液气比为2 L/m3时,NaClO2的浓度为5 mmol/L较适宜。

图2 NaClO2浓度对NO转化率与NOx脱除率的影响Fig.2 Effect of initial concentration of NaClO2on NO conversion and NOxremoval efficiency
2.1.2 NO初始浓度的影响
气时空速为0.3 s-1,O2体积分数为3%,NaClO2初始浓度为5 mmol/L,反应温度为60 ℃时,考察NO初始浓度对脱硝过程的影响,结果见图3。由图可知,液气比为2.0 L/m3时,NO初始浓度在200~500 mg/m3,NO可被NaClO2溶液全部氧化,当NO浓度为600 mg/m3时,虽然此时溶液中NaClO2与NO的物质的量之比(3:4)刚好符合两者间化学反应的计量比,但在NaClO2脱硝的过程中,还伴有NaClO2分解等副反应的发生,因此NO不能被全部转化。当液气比为0.9 L/m3,增大NO的浓度,NO转化率和NOx脱除率下降的趋势更加明显。
提高NO的初始浓度对脱除NOx的影响主要有两方面:一是气相传质推动力增大,二是NaClO2与NOx间的摩尔比降低。根据气液传质理论,填料塔入口NOx含量的提高,增加了NOx在气相主体中的摩尔分数,这有助于提高气相传质推动力,从而促进NOx的吸收。但当NaClO2溶液的喷淋量不发生变化时,吸收液对NOx的吸收能力是一定的,增加填料塔入口NOx浓度使NaClO2在反应过程中消耗过快,造成填料塔下半段液膜内的传质阻力增大。从NO可迅速被NaClO2氧化可以得知,NO可以由气相主体迅速传递到气液相界面,即NOx的吸收主要受液膜控制,因此在上述两个因素中后者为影响NOx脱除的主要因素,故随NO初始含量的提升,脱硝率逐渐降低。

图3 NO初始浓度对NO转化率和NOx脱除率的影响Fig.3 Effect of initial concentration of NO on NO conversion and NOxremoval efficiency
2.1.3 反应温度的影响
气时空速为0.3 s-1,O2含量为3%,NO初始浓度为400 mg/m3,NaClO2浓度为5 mmol/L,液气比为2.0 L/m3的条件下,考察反应温度对脱硝过程的影响,结果见图4。由图可知,随着反应温度的提高,NOx的脱除率先迅速增大,当反应温度达到40 ℃后趋于稳定,保持在99%以上,而NO转化率随着反应温度的升高先增大后减小。反应温度的提高对NaClO2溶液脱硝过程有双重影响。根据阿伦尼乌斯方程,升高反应温度,可以加快吸收过程中的反应速率,从而有利于NaClO2溶液对NO的氧化和脱除;同时提高反应温度可以增大反应物分子的能量,使活化分子所占比例提高,反应速率也随之增大,促进脱硝过程的进行。但NaClO2溶液吸收NO是涉及到化学反应和吸收等多个环节的复杂过程,提高温度虽然有利于NO的氧化,但是NaClO2溶液与NOx间的反应为放热过程,吸收温度过高会对脱硝过程产生不利影响;此外,吸收温度的提高也会减小NO在吸收液中的溶解度,使NO的亨利系数增大,造成传质阻力的增大。因此,操作温度不宜过高。
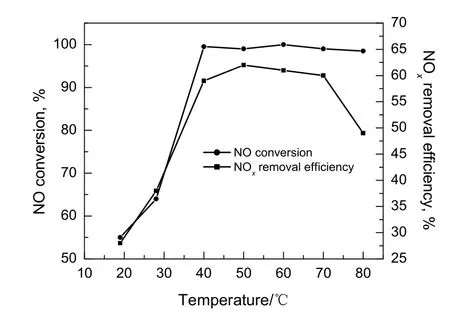
图4 反应温度对NO转化率和NOx脱除率的影响,Fig.4 Effect of reaction temperature on NO conversion and NOxremoval efficiency
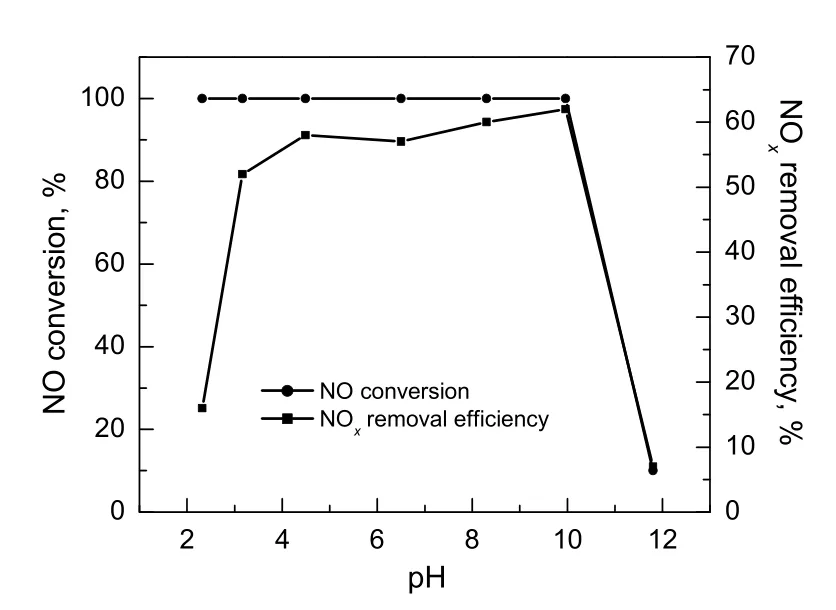
图5 NaClO2溶液初始pH值对NO转化率与NOx脱除率的影响Fig.5 Effect of initial pH value on NO conversion and NOxremoval efficiency
2.1.4 NaClO2溶液初始pH值的影响

图6 液气比对NO转化率和NOx脱除率的影响Fig.6 Effect of liquid-gas ratio on NO conversion and NOxremoval efficiency
NaClO2溶液初始pH值分别采用HNO3和NaOH来调节。在液时空速为0.3 s-1,O2含量为3%,液气比为2.0 L/m3,NO初始浓度为400 mg/m3,NaClO2浓度为5 mmol/L,温度为60 ℃的条件下,考察NaClO2溶液初始pH值对脱硝过程的影响,结果见图5。由图可知,NaClO2溶液初始pH值在2.32~9.96,提高溶液的pH值,NO的转化率基本上不发生变化,NO转化率基本维持在100%,当进一步提高pH值后,NO的转化率迅速降低至10%;当溶液的pH值由2.32增加至3.17时,NOx脱硝率由15%增大至51%,NaClO2溶液初始pH值在4.49~9.96,NOx脱除率基本维持在60%左右,当吸收液的初始pH值升高至11.8时,其脱硝率均迅速降至7%。
这是由于在酸性条件下,NaClO2会发生歧化反应,见式(7),产生氧化性能更强的ClO2[9],而ClO2的存在有利于将NO氧化为NO2和N2O5,可以促进NOx的吸收。但是过高的H+浓度会使NaClO2在储槽或管线内就已发生分解,ClO2在填料塔顶随烟气逃逸,从而影响NaClO2溶液对NOx的脱除。同时,在酸性环境中,Cl-会对管线和填料等产生严重的腐蚀。但当吸收液中OH-含量过高时,虽有助于NO2的吸收,但会抑制ClO2的产生,使NaClO2的氧化性能明显减弱,导致NOx的去除效果急剧下降[10]。本实验是在小型填料塔中气液以逆流形式接触的,因此,吸收液从填料塔上半部分进料时,适当高的pH值可以促进NO2的吸收,而NO2的吸收又使溶液的pH值降低,有利于在填料塔下半部分发挥NaClO2的氧化作用,将NO转化成NO2。综合考虑,本实验NaClO2溶液的pH值为9.50~9.96较合适。2.1.5 液气比的影响
气时空速为0.3 s-1,O2浓度为3%,NO初始浓度为400 mg/m3,反应温度为60 ℃的条件下,考察液气比对脱硝过程的影响,结果见图6。由图可知,NO的转化率随着液气比的增加顺序升高后趋于稳定,基本维持在100%,而NOx脱除率随液气比的增大而升高,升高幅度趋于平缓。这是由于液体的喷淋量增加,使得填料表面润湿更加充分,有效气液接触面积增大,同时加速了填料表面液膜的更新,有助于促进气液接触反应。根据相际传质理论,随着液相流量的增加,液相湍动加剧,填料塔中液膜阻力逐渐减小,而液膜阻力的降低也有利于促进NOx的脱除。在气体总流量一定的情况下,加大液气比有利于降低液相传质阻力,从而有效提高气液传质速率,加快NOx的吸收,使脱硝率也随之增大。由于继续提高吸收液喷淋量不仅会增加运行成本,还会使填料塔内的压降增大,导致严重的气体液沫夹带和出现NaClO2溶液返混等现象,甚至引起液泛,严重影响NOx的脱除效果。因此,为了降低运行成本和避免吸收液流量过大带来不利影响,液气比为2 L/m3较适宜。
2.2 反应机理分析
2.2.1 脱硝反应产物分析
在气相空速为0.3 s-1,氧含量为3%,NO含量400 mg/m3,NaClO2浓度为5 mmol/L,液气比为2.0 L/m3,NaClO2溶液初始pH值为9.96,反应温度为60 ℃的条件下进行脱硝反应,NaClO2溶液在脱硝反应前后发生了一系列变化。反应前吸收液呈无色无味;伴随着脱硝过程的进行,NaClO2溶液的颜色变为黄绿色并伴有类似于Cl2的刺鼻气味;待NaClO2溶液无效后,吸收液又呈现为无色,但刺激性气味并未消失。根据实验现象并查阅相关文献可知[8,11,12],在NaClO2溶液脱硝过程中,由于NOx的不断脱除,溶液的pH值逐渐降低,使发生歧化反应生成了ClO2和Cl2,这两种气体的存在使溶液呈现出黄绿色。而ClO2和Cl2在脱硝过程中又与烟气中的NOx反应,最终被消耗殆尽,溶液也再次变为无色透明。
分别采用离子色谱和连续碘量法分析了脱硝前后溶液中的离子浓度,结果见表1。由表可知,在脱硝反应过程中,吸收液的pH值由9.96降至2.76,说明随着NOx的吸收,OH-被逐渐耗尽,在后续吸收过程中又不断有H+产生,吸收液的pH值也随之不断降低。通过分析塔底脱硝产物可知,NOx与NaClO2溶液在填料塔内反应的最终产物是NO3-,而在塔底未检测到NO2-的存在,这说明NOx中的N元素能被ClO2-氧化为其最高价态即正五价。对比反应前和反应后吸收液中的阴离子种类和浓度可知,在脱硝过程中,大部分ClO2-最终转化成Cl-,而反应结束后的NaClO2溶液中ClO3-的含量略有增加。

表1 脱硝前后NaClO2溶液中离子组成分析Table 1 Analysis of ionic composition in the denitrification solution before and after absorption
通过检测吸收塔顶冷凝水的pH值和离子浓度可知,塔顶冷凝水也呈现酸性,其中含有少量的Cl-,NO-2和NO3-。塔顶冷凝水呈现酸性的原因是烟气中夹带的OH-继续与NOx反应,待OH-被耗尽后,NO2继续与水蒸汽反应,最终使冷凝水呈现出酸性。塔顶冷凝水中部分阴离子是被模拟烟气从填料塔中夹带出来的,也有一部分是NOx继续与模拟烟气中的H2O,O2或夹带出的ClO-2等反应过程中生成的。而其中NO2-的存在可能是由于NO2与烟气中夹带出的OH-反应生成NO3-和ClO-2。烟气中夹带的少量ClO-2继续同NOx或NO2-发生反应,将其氧化为NO3-,ClO-2则被完全消耗最终转化为Cl-,因此在吸收塔顶未检测出ClO-2存在。
2.2.2 NaClO2脱硝反应过程
根据模拟烟气脱硝实验和液相产物分析结果,在NaClO2溶液脱硝过程中,一部分NO被NaClO2溶液直接氧化吸收,一部分NO被迅速转化成NO2。生成的NO2又继续被NaClO2溶液氧化为NO3-,也有少量的NO2在碱性环境下先生成NO2-,ClO2-再将NO2-氧化为NO3-[12]。在脱除NOx的过程中,绝大部分ClO2-被还原为Cl-。填料塔中发生的脱硝反应为:

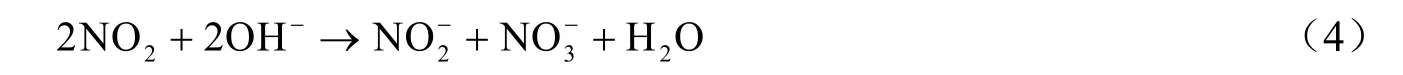

综上所述,在碱性环境中,NaClO2溶液脱除NOx的总反应为:

随着脱硝过程的进行,NaClO2溶液的pH值随着OH-不断被消耗而逐渐下降,在这个过程中,吸收液由碱性迅速变成酸性。NaClO2在酸性条件下会发生歧化反应,变为黄绿色的液体,生成氧化作用更强的ClO2,具体反应为:

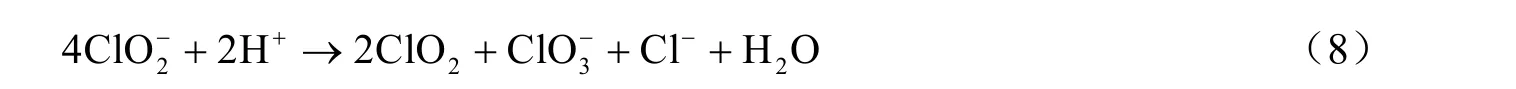

其中,反应(9)和(10)的发生解释了反应后吸收液中ClO3-升高的原因。ClO2与NOx间发生下述反应:

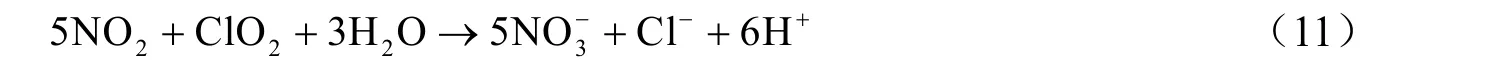

3 结 论
在小型填料塔中考察了操作条件对NaClO2水溶液脱硝过程的影响,发现NaClO2的浓度或液气比的提高均有助于提高NO转化率和NOx脱除率,但当NaClO2浓度和液气比增大至一定程度后,其对NaClO2水溶液脱硝过程的影响不明显;而随着填料塔入口NO初始浓度的增大,脱硝率略有减小。当反应温度在40~70 ℃、溶液初始pH值在4.49~9.96时,液气比为2.0 L/m3条件下的脱硝率均达到60%以上;在较优的操作条件下,NO基本能实现完全的脱除。基于NaClO2与NOx之间的实验现象及液相脱硝产物的检测结果,对NaClO2水溶液脱硝过程的反应机理进行了较详细的分析,这对继续研究NaClO2水溶液脱硝过程具有一定的指导意义。
参考文献:
[1] 孙克勤, 钟 秦. 火电厂烟气脱硝技术及工程应用[M]. 北京: 化学工业出版社, 2006: 18-25.
[2] 胡松伟. 炼油厂催化裂化装置烟气污染物的治理与建议[J]. 石油化工安全环保技术, 2011, 27(2): 47-51. Hu Songwei. Governance and suggestions of pollutants in flue gas from FCC unit of refining plant[J]. Petrochemical Safety and Environmental Protection Technology, 2011, 27(2): 47-51.
[3] 曾祥根. 硝酸尾气治理机理探讨与处理方法[J]. 化学工业与工程技术, 2004, 25(6): 45-47. Zeng Xianggen. Mechanism and treatment methods for nitric acid tail gas[J]. Chemical industry and Engineering Technology, 2004,25(6): 45-47.
[4] Pradhan M P, Joshi J B. Absorption of NOxgases in aqueous NaOH solutions: selectivity and optimization[J]. AIChE Journal, 1999,45(1): 38-50.
[5] 陈 理. 国外烟气脱硫脱硝技术开发近况[J]. 化工环保, 1997, 17(3): 145-150. Chen Li. Recent development of desulfurization and denitration technologies in foreign countries[J]. Environment Protection of Chemical Industry, 1997, 17(3): 145-150.
[6] 徐 姣, 张卫江. 尿素/双氧水湿法工业废气脱氮的试验研究[J]. 化工进展, 2007, 26(增刊): 89-91. Xu Jiao, Zhang Weijiang. Experimental study on waste gas denitration by wet method using urea/hydrogen peroxide[J]. Chemical Industry and Engineering Progress, 2007, 26(Supplementary Issue): 89-91.
[7] 刘志龙. 臭氧氧化法烟气脱硝初步研究[J]. 炼油技术与工程, 2012, 42(9): 23-25. Liu Zhilong. Preliminary study on nitrate removal by ozone oxidation from flue gas[J]. Petroleum Refinery Engineering, 2012, 42(9): 23-25. [8] Hsu H W, Lee C J, Chou K S. Absorption of NO by NaClO2solution: performance characteristics[J]. Chemical Engineering Communications, 1998, 170(1): 67-81.
[9] Deshwal B R, Lee S H, Jung J H, et al. Study on the removal of NOxfrom simulated flue gas using acidic NaClO2solution[J]. Journal of Environmental Sciences, 2008, 20(1): 33-38.
[10] Sada E, Kumazawa H. Absorption of lean NOxin aqueous solutions of NaClO2and NaOH[J]. Industrial and Engineering Chemistry Process Design and Development, 1979, 18(2): 275-278.
[11] 任晓莉, 张雪梅, 张卫江. 碱液吸收法治理含NOx工艺尾气实验研究[J]. 化学工程, 2006, 34(9): 63-66. Ren Xiaoli, Zhang Xuemei, Zhang Weijiang. Experimental study on tail gas treatment containing NOxby alkali absorption method[J]. Chemical Engineering, 2006, 34(9): 63-66.
[12] Sada E, Kumazawa H, Kudo I. Absorption of NO in aqueous mixed solutions of NaClO2and NaOH[J]. Chemical Engineering Science,1978, 33(3): 315-318.
Conditions and Mechanism of Denitrification of NaClO2Aqueous Solution
Ye Chunbo, Tu Xianhong, Li Chaoheng, Pei Xudong, Chen Weihong
Luoyang R&D Center of Technology, Sinopec Engineering (Group) CO LTD, Luoyang 471003, China
Abstract:In order to study the process characteristics of NOx absorption by aqueous solutions of NaClO2,effects of initial NaClO2and NO concentrations, reaction temperature, ratio of liquid to gas and initial pH value on the denitrification process were investigated in a compact packed tower. The experimental results revealed that the performance of NaClO2aqueous solutions was excellent and NO conversion could reach as high as 100% under appropriate operating conditions. In addition, reaction mechanism between NaClO2and NOxwas analyzed reasonably.
Key words:sodium chlorite; nitrogen oxide; oxidative denitrification; reaction mechanism
作者简介:叶春波(1986—),男,工程师。E-mail: yechunbo@sinopec.com。
收稿日期:2016-01-25;
修订日期:2016-03-02。
文章编号:1001—7631 ( 2016 ) 02—0176—07
中图分类号:X511
文献标识码:A
