1,6-己二醇二丙烯酸酯合成动力学
2016-06-02梁世伟孙晓红胡微月崔文岗李稳宏
梁世伟,孙晓红,胡微月,崔文岗,李稳宏
1.西北大学化工学院,陕西 西安 710069;2.陕西省产品质量检测检验研究院, 陕西 西安 710048
1,6-己二醇二丙烯酸酯合成动力学
梁世伟1,孙晓红1,胡微月2,崔文岗1,李稳宏1
1.西北大学化工学院,陕西 西安 710069;
2.陕西省产品质量检测检验研究院, 陕西 西安 710048
摘要:以固体酸SO42-/TiO2-SnO2-ZnO为催化剂,丙烯酸和1,6-己二醇为原料,考察了催化剂加量、转速以及催化剂粒径对酯化反应速率的影响。在消除内外扩散影响的前提下,建立了固体酸催化合成1,6-己二醇二丙烯酸酯拟均相反应动力学模型,得到了相应的动力学方程参数,动力学模型预测的结果与实验结果吻合良好。
关键词:固体酸催化剂 酯化反应 动力学
1,6-己二醇二丙烯酸酯(HDDA)是一种丙烯酸酯系列具有双官能团的丙烯酸酯功能单体,具有低收缩率、高活性和对皮肤刺激小等特点,主要应用于辐射固化、纺织业、涂料、粘合剂、造纸业以及其他行业领域[1,2]。目前,通过直接酯化法、酯交换法和酰氯法合成特种丙烯酸酯的研究主要集中于工艺优化和催化剂选择上。娄阳[3]以强酸性阳离子树脂D072为催化剂,工艺优化得到了合成HDDA的最佳工艺条件,强酸性阳离子树脂催化剂具有反应器效率高、产物后处理简单等优点,但对温度要求较为苛刻,不宜超过120 ℃,且单程转化率低,催化剂使用寿命短、再生困难,机械强度不高,使用受到限制。孟锐等[4]以对甲苯磺酸与亚磷酸液体酸为催化剂,通过直接酯化法合成HDDA,并确定了最佳工艺。该工艺简单,生产效率高,但在产品精制阶段需要大量水对粗产品进行洗涤中和以去除产品中残留的催化剂及阻聚剂,产生的大量工业废水和催化剂回收处理费时费力。近年来,固体酸催化剂引起了研究者的重视,在丙烯酸酯合成工艺中,这种催化剂能够有效简化产品分离纯化过程,降低原材料消耗和提高产物纯度等,粗产品洗涤过程省去大量洗涤操作。与液体酸催化剂相比,固体酸在反应完成后通过过滤的方式与反应体系分开,可回收并重复使用。目前已有不少固体酸类催化剂研究文献报道。邹艳红等[5]利用NaY分子筛为原料,制备出了HY分子筛固体酸催化合成己二酸二辛酯。赵倩[6]利用固体超强酸SO42-/TiO2和稀土固体超强酸SO42-/TiO2/La3+对甲基丙烯酸新戊二醇酯的催化合成进行研究,并取得较好的效果。何祖慧等[7]采用SO42-/SnO2-TiO2-Al2O3固体酸对壬二酸二辛酯的催化合成进行研究。但针对固体酸催化合成丙烯酸特种酯的反应动力学研究文献报道极少。
本工作以自制固体酸SO42-/TiO2-SnO2-ZnO为催化剂,在消除内外扩散的影响下研究该酯化反应的动力学,得到反应动力学模型、速率常数和活化能等相关参数,以期对后续的研究和工业生产提供理论和实质性的指导作用。
1 实验部分
1.1 催化剂制备
采用TiCl4为钛源,制备以钛基为载体,元素Sn和Zn为参杂组分的固体酸催化剂。将一定量的TiCl4水溶液、SnCl4乙醇溶液和ZnCl2水溶液按一定质量比例混合后加入适量的缓冲剂,并调节pH值至7左右,在80 ℃下恒温搅拌10 h,静置、陈化和干燥。将制得的前驱体在1.00 mol/L的硫酸铵溶液中浸泡4 h,在远红外干燥箱中于100 ℃干燥1.5 h,然后在马弗炉于460 ℃下焙烧4 h,制得固体酸催化剂。
1.2 催化剂表征
用Micromeritics公司的ASAP2000型自动物理吸附仪测定催化剂物化性质,测量前将催化剂在压力为1.3×10-2Pa下,350 ℃处理2 h,然后在液氮温度下吸附高纯氮,获得样品的N2吸附/脱附等温线,计算样品的比表面,催化剂物性参数见表1。
采用日本Rigaku公司D/max-2400型X射线衍射仪测定催化剂的元素含量,检测条件为N2气氛,扫描速度8 (°)/min,扫描范围为10~80°。用MDI Jade 6.0软件对催化剂的X射线衍射图进行数据处理,包括平滑、扣除背景和寻峰等,并将所得数据与标准卡片信息比配。

表1 催化剂物性参数Table 1 Physical properties of the catalysts
1.3 1,6-己二醇和丙烯酸酯化反应
称取一定量1,6-己二醇和丙烯酸原料(酸醇物质的量之比为3.5:1.0),加入装有分水器(连接冷凝管)、温度计、搅拌器和取样口的四口烧瓶中,使两者充分混合溶解后,取样分析样品中1,6-己二醇的含量,作为其起始含量。后加入固体酸催化剂(占原料总质量)2.6%、对苯二酚(占丙烯酸质量)0.6%和甲苯(占原料总质量)60%,反应温度维持在110~120 ℃,当反应有回流形成时,开始计时。
采用GC-2060气相色谱仪(上海瑞敏仪器有限公司),参考行标HBFG03-2009《辐射固化用多官能度丙烯酸酯单体纯度(酯含量)的测定》,间隔一定时间取样检测,气相色谱条件为:色谱柱OV-17,规格30 m×0.53 mm×1.0 μm;气化室温度300 ℃;检测室温度350 ℃;柱温70 ℃,保留时间2 min,程序升温,以10 ℃/min升至260 ℃,保持10 min;载气(N2)0.06 MPa;H20.04 MPa;空气0.05 MPa;进样量1 μL。采用外标法对反应体系中的1,6-己二醇的含量进行检测分析。在相同进样量的条件下,用反应前后1,6-己二醇峰面积的含量计算1,6-己二醇的转化率(X)。
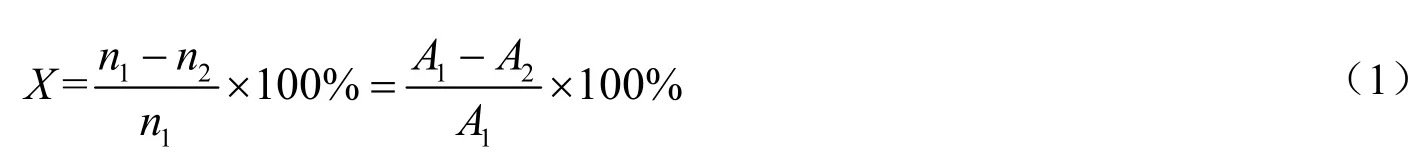
式中:n1和n2分别为开始和结束时刻1,6-己二醇的物质的量,mol;A1和A2分别为开始和结束时刻1,6-己二醇的气相色谱峰面积。
将粗产品进行减压蒸馏,反应温度逐渐升温达到90 ℃,蒸出甲苯及丙烯酸的混合物,用于回收后再利用,剩余的产物用质量分数为5%的NaOH溶液洗涤,去除残余的酸和阻聚剂,然后用饱和NaCl溶液洗涤至中性,无水Na2SO4干燥后将得到目的产物。
2 结果与讨论
2.1 影响因素分析
固体酸催化合成1,6-己二醇二丙烯酸酯的酯化反应是一个固-液相非均相体系,其与均相催化反应的差异之处是反应发生在固体酸催化剂的表面[8],因此需考察内外扩散和催化剂用量对反应转化率的影响。2.1.1 外扩散对反应转化率的影响
外扩散阻力主要来自流体与催化剂表面之间的静止层[9]。搅拌速率的大小直接影响着外扩散的传质速率,通过调整搅拌器转速来降低外扩散影响。在酸醇物质的量之比为3.5:1.0,催化剂用量为2.6%,催化剂粒径为0.113~0.136 mm(120~150目),对苯二酚用量为0.6%,反应温度120 ℃,反应时间4 h的条件下,考察不同的搅拌速率对反应转化率的影响,结果如图1所示。由图可看出:在相同的反应时间内,当搅拌速率小于500 r/min时,随着搅拌速率的增加,转化率随之增大,说明此时反应存在外扩散阻力的影响;当搅拌速率大于500 r/min时,相同时间内转化率变化不太明显,此时该酯化反应外扩散阻力影响可以忽略。故后续实验采用搅拌速率为500 r/min。

图1 搅拌速率对反应转化率的影响Fig.1 Effect of stirring speed on the conversion of 1,6-hexanediol

图2 催化剂粒径对反应转化率的影响Fig.2 Effect of size of the catalyst on the conversion of 1,6-hexanediol
2.1.2 内扩散对反应转化率的影响

图3 催化剂用量对转化率的影响Fig.3 Effect of dosage of the catalyst on the conversion of 1,6-hexanediol
固体酸催化剂的粒径与空隙大小直接影响着内扩散过程[5],通过改变催化剂粒径研究酯化反应过程中内扩散的影响。在酸醇物质的量之比为3.5:1.0,催化剂用量为2.6%,对苯二酚用量为0.6%,反应温度120 ℃,反应时间4 h,搅拌速率为500 r/min的条件下,考察不同催化剂粒径对反应转化率的影响,结果如图2所示。由图可看出,随着催化剂颗粒直径的不断减小,反应转化率随之增大,当催化剂粒径达到0.113~0.136 mm时,继续减小催化剂粒径,相同的反应时间下转化率变化不明显,此时可认为已消除内扩散阻力影响。故采用催化剂粒径为0.113~0.136 mm。
在酸醇物质的量之比为3.5:1.0,催化剂粒径0.113~0.136 mm,对苯二酚用量为0.6%,反应温度120 ℃,反应时间4 h,搅拌速率500 r/min的反应条件下,考察改变催化剂用量对反应转化率的影响,结果见图3。由图可知,催化剂用量对反应转化率影响较大。在催化剂用量较小时,随着催化剂用量的增加反应物转化率在不断地增大;当达到一定值后,随催化剂用量的增加反应物转化率不再增加,反而有轻微的下降趋势,这可能是由于随着催化剂量的增加,体系搅拌不均匀,传热效果降低,导致部分产品结焦,覆盖在催化剂的表面,降低了催化剂表面的有效活性中心,从而导致其转化率呈现小幅度的下降。因此适宜催化剂用量为原料总质量的2.6%。
2.2 HDDA酯化动力学研究
2.2.1动力学模型建立
合成HDDA的总反应方程式为:
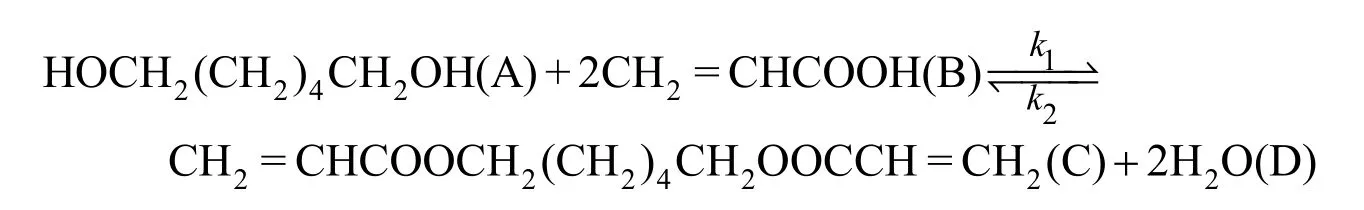
该酯化反应是一个可逆的反应,采用经典的幂函数型反应动力学模型描述。HDDA的生成反应速率方程可表示为:

式中:cA,cB,cC和cD分别为1,6-己二醇,丙烯酸,HDDA和生成水的浓度,mol/L;k1和k2分别为正逆反应速率常数;α和β为1,6-己二醇和丙烯酸正反应级数;φ和γ为HDDA逆向水解反应级数。其中,k1和k2满足Arrhenius方程:
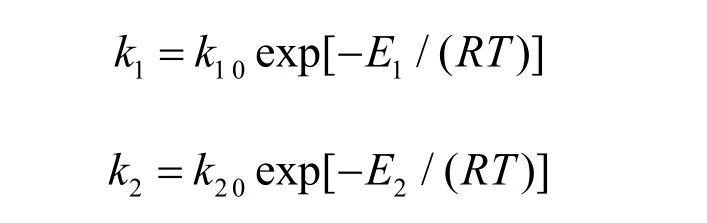
反应速率大小关键在于反应速率常数,由阿伦尼乌斯方程可知,反应常数是指前因子、反应活化能和反应温度共同作用的结果。因为温度的变化对活化能E1=E1 0+1/2RT,E2=E2 0+1/2RT,指前因子k1 0和k2 0两者之间引起的变化很小,完全可以忽略,所以在一定温度范围内,认为指前因子与活化能是恒定不变的,所以得到反应速率常数的关键是建立速率系数k = f (T )的函数关系[11]。
酯化反应均为可逆反应,为了促进反应平衡向正反应方向进行,将反应生成的水与携水剂甲苯形成共沸物连续分离出体系。忽略少量丙烯酸被反应生成水夹带分离出体系及分析取样对体系浓度的影响,携水剂能充分将反应体系中的水分分离,使得液相中不存在水分[12]。同时通过气质联用技术检测大量实验数据可知,产品中单酯含量较少,可以忽略不计。因此该酯化反应以不可逆反应的动力学方程描述,将式(2)简化为:


式中:nA和nB分别为1,6-己二醇和丙烯酸物质的量;V0和Vt分别为体系初始时刻和t时刻体积;nA= nA 0(1-X);nB= nB 0-2nA 0X; nA 0和nB 0分别为1,6-己二醇和丙烯酸初始物质的量。

由于水的排出,体系中各物质的浓度持续发生变化,但是在常压下,以甲苯为携水剂,甲苯与水形成共沸物具有恒定的组成含量,则式(5)可化简为:

如果将水的密度近似为1.0 g/mL,则:

由式(1),(4)和(6)可以推导出:

将式(8)代入式(3)可得酯化反应速率微分方程为:

反应级数是通过实验经验而得出的数值,然而根据经验可知,反应总级数的数值大多数都是小于3,大于或等于3的反应很少,因此假设该酯化反应级数为2级反应。其中,α和β均为1 ,则式(9)可简化为:

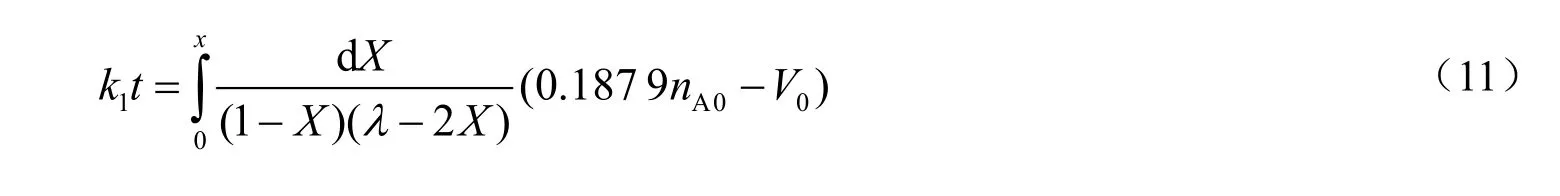
式中,λ为酸醇物质的量之比。
2.2.2动力学模型参数确定
在不同反应温度下,1,6-己二醇转化率与反应时间的关系见图4。由图可见,在不同的反应温度下,随着反应时间的延长,其转化率呈现连续性增加。在反应初始阶段由于反应物浓度较高,反应速率较快,随之反应速率逐渐减慢。
根据式(11)以Y为纵坐标对时间t的关系作线性回归,得到图5。由图可以得出,在不同的温度下积分值Y与反应时间t所对应的直线线性关系良好,直线斜率即为各个反应温度下的正向反应速率常数k1。各个直线斜率与其相关系数见表2。
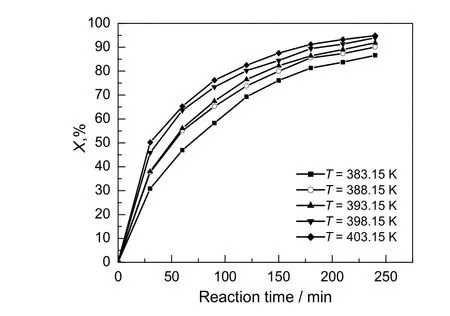
图4 不同反应温度下转化率随时间的变化Fig.4 The changes of X with time at different temperatures
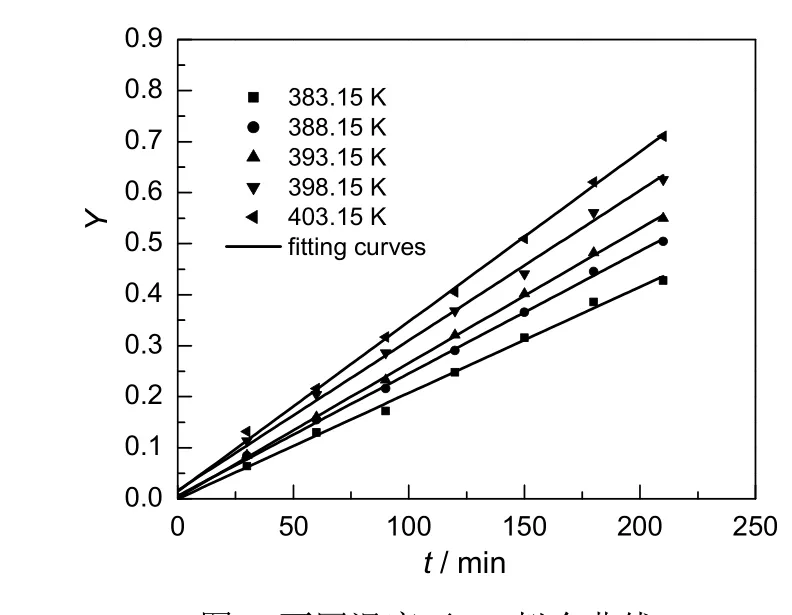
图5 不同温度下Y-t拟合曲线Fig.5 Y-t fitting curve at different temperatures
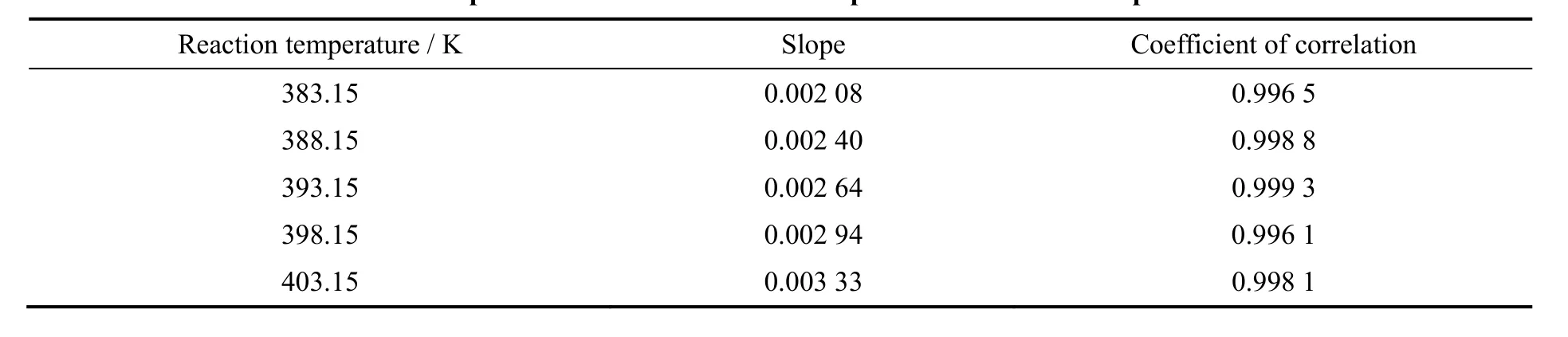
表2 不同反应温度下Y-t线性关系参数Table 2 The parameters of linear relationship of Y-t at different temperatures
根据Arrhenius公式:

对其进行数学整理线性回归得:


图6 lnk与T-1的关系Fig.6 The relationship between lnk and T-1
式中:Ea为反应活化能,J/mol;R为气体常数,8.314 5 J/(mol·K);k0为指前因子。Lnk对T-1作图,如图6所示。由图的拟合曲线可看出,lnk与T-1基本呈线性关系,相关系数R2为0.989 9,线性相关性良好。求得酯化反应的表观活化能为31.394 kJ/mol,频率因子为39.575 L/(mol·min)。则lnk与T的方程式为:

综上所述,固体酸催化剂催化合成1,6-己二醇二丙烯酸酯的酯化反应的反应动力学方程为:

2.2.3 动力学模型验证
为验证求得动力学模型的可靠性,以酸醇物质的量之比为2.2:1,1,6-己二醇的初始浓度为2.213 4 mol/L,催化剂用量2.6%,催化剂粒径为0.116~0.136 mm,搅拌速率为500 r/min,在反应温度为120 ℃的条件下进行实验,每隔一段时间取样求转化率(Xexp),并将与该酯化反应的动力学方程计算得到的转化率(Xcal)进行比较,所得结果见表3。由表可得出,由动力学模型计算所得转化率与实际测得的转化率之间的正负相对误差均小于2.5%,说明预测值与实际值相差不大,可见求得的动力学模型预测的结果与实验真实结果能够很好的吻合。
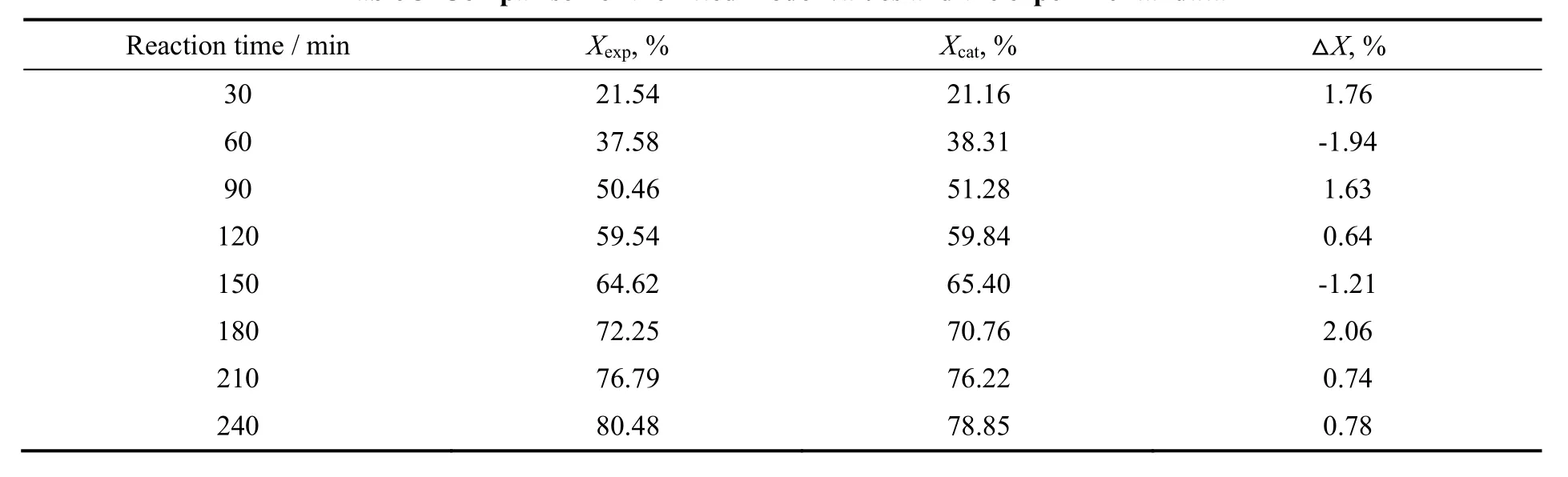
表3 模型值与实验数据比较Table 3 Comparison of the fitted model values and the experimental data
3 结 论
以固体酸为催化剂,在催化剂粒径为0.113~0.136 mm,转速为500 r/min的条件下,可消除内外扩散对酯化反应影响,并建立了固体酸拟均相催化反应动力学模型,求得该酯化反应为准2级反应,活化能为31.394 kJ/mol,频率因子为39.575 L/(mol·min)。该动力学模型预测值与实验值相吻合,说明其精确良好,为后续的反应器设计和工艺优化提供一定的理论基础和依据。
参考文献:
[1] 邹献武, 崔 波. 固体超强酸催化非均相酯化反应的动力学[J]. 青岛科技大学学报(自然科学版), 2003, (5): 405-408. Zou Xianwu, Cui Bo. Reaction kinetics of heterogeneous esterification reactions with super solid acid catalytic[J]. Journal of Qingdao University of Science and Technology, 2003, (5): 405-408.
[2] 高 虹, 聂 俊. 温度对1,6-己二醇二丙烯酸酯紫外光聚合的影响[J]. 辐射研究与辐射工艺学报, 2006, 24(5): 289-292. Gao Hong, Nie Jun. The effect of 1,6-hexanediol diacrylate of UV polymerization with temperature[J]. Journal of Radiation Research and Radiation Processing, 2006, 24(5): 289-292.
[3] 娄 阳. 催化合成1,6-己二醇二丙烯酸酯[J]. 精细石油化工, 2010, (6): 23-26. Lou Yang. Catalytic synthesis of 1,6-hexanediol diacrylate[J]. Speciaity Petrochemical, 2010, (6): 23-26.
[4] 孟 锐, 李晓刚. 1,6-己二醇二丙烯酸酯的合成[J]. 湖南文理学院学报(自然科学版), 2014, (3): 28-32. Meng Rui, Li Xiaogang. Synthesis of 1,6-hexanediol diacrylate[J]. Journal of Hunan University of Arts and Science, 2014, (3): 28-32.
[5] 邹艳红. 固体酸催化合成己二酸二辛酯的研究[D]. 湖南: 湖南师范大学, 2012.
[6] 赵 倩. 固体酸催化合成甲基丙烯酸新戊二醇酯的研究[D]. 天津大学, 2007.
[7] 何祖慧, 刘 勇, 成 昕. SO42-/SnO2-TiO2-Al2O3固体酸催化合成壬二酸二辛酯[J]. 应用化工, 2013, (4): 650-653. He Zuhui, Liu Yong, Cheng Xin. Synthesis of dioctyl azelate catalyzed by SO42-/SnO2-TiO2-Al2O3solid acid[J]. Applied Chemical Industry, 2013, (4): 650-653.
[8] Jayadeokar S, Sharma M M. Ion exchange resin catalyzed etherification of ethylene and propylene glycols with isobutylene[J]. Reactive Polymers, 1993, 20(1/2): 57-67.
[9] Altiokka M R, Odes E. Reaction kinetics of the catalytic esterification of acrylic acid with propylene glycol[J]. Appl Catal A, 2009,362(1/2): 115-120.
[10] 邱 挺, 黄智贤, 吴燕翔, 等. 阳离子交换树脂催化合成乙酸正丁酯的动力学[J]. 化学反应工程与工艺, 2009, 25(4): 355-359. Qiu Ting, Huang zhixian, Wu Yanxiang, et al. Kinetics of synthesis of n-butyl acetate over cation-exchange resin catalyst[J]. Chemical Reaction Engineering and Technology, 2009, 25(4): 355-359.
[11] 蒋广平, 罗 峰. 用阳离子交换树脂催化酯化合成乙酸异丙酯动力学研究[J]. 化学世界, 2012, (8): 471-474. Jiang Guangping, Luo feng. Kinetics of isopropyl acetate synthesis over cation-exchange resin catalyst[J]. Chemical World, 2012, (8): 471-474.
[12] Samantaray S K, Parida K. Modified TiO2-SiO2mixed oxides: effect of manganese concentration and activation temperature towards catalytic combustion of volatile organic compounds[J]. Applied Catalysis B: Environmental, 2005, 57(2): 83-91.
Kinetics of Synthesis of 1,6-Hexanediol Diacrylate over
SO42-/TiO2-SnO2-ZnO Solid Acid
Liang Shiwei1, Sun Xiaohong1, Hu Weiyue2, Cui Wengang1, Li Wenhong1
1. School of Chemical Engineering, Northwest University, Xi’an 710069, China;
2. Shaanxi Product Quality Supervision and Inspection Institute, Xi’an 710048, China
Abstract:The esterification of acrylic acid and 1,6-hexanediol catalyzed by the solid acid SO42-/TiO2-SnO2-ZnO was studied and the effects of the catalyst dosage, stirring speed, particle size were investigated. The corresponding intrinsic kinetic parameters were obtained and a kinetic model of the above pseudohomogeneous esterification was established under the conditions of eliminating internal and external diffusion effects. It was found that the kinetic model predictions were in good agreement with the experimental results.
Key words:solid acid catalyst; esterification reaction; kinetics
作者简介:梁世伟(1991—),男,硕士研究生;孙晓红(1959—),教授,博士生导师,通信联系人。E-mail: xhsun888@sohu.com。
收稿日期:2015-03-17;
修订日期:2016-01-25。
文章编号:1001—7631 ( 2016 ) 02—0137—07
中图分类号:O643.32+2
文献标识码:A
