双试剂阳性样本复检结果分析及检测策略调整研究
2016-05-26李红珠杨文玲
王 霞,潘 彤,李红珠,杨文玲
(天津市血液中心检验科,天津 300110)
双试剂阳性样本复检结果分析及检测策略调整研究
王霞,潘彤,李红珠,杨文玲△
(天津市血液中心检验科,天津 300110)
摘要:目的通过对双试剂阳性样本的复检结果进行分析,探讨现有检测策略调整的可行性。方法对2012年1月至2014年12月对HBsAg、抗-HIV、抗-HCV和抗-TP为ELISA双试剂检测阳性标本的复检结果进行统计分析。结果双试剂阳性标本复检阳性率分别为,HBsAg:99.69%~100%、抗-HIV:100%、抗-HCV:98.96%~99.94%和抗-TP:99.86%~100%。结论双试剂阳性样本复检结果可以作为对检测策略调整的依据。
关键词:酶联免疫吸附测定;乙型肝炎病毒;丙型肝炎病毒;梅毒螺旋体
ELISA试验可用于各种疾病的筛查和诊断,特别适用于血站输血相关感染的筛查。目前血站实验室采用ELISA主要检测HBsAg、抗-HIV、抗-HCV和抗-TP。按照《血站实验室质量管理规范》[1]、GBT22576-2008/ISO15189-2007《医学实验室质量和能力的专用要求》[2]、ISO/IEC15189-2008《医学实验室质量和能力的认可准则》及血站技术操作规程(2012)要求[3-4],血站血液筛查实验室在采用一项新的检测方法,或更换现有检测方法时需要考虑的因素包括完成检测必需的仪器、试剂、校准品、实验程序及其组合、检测策略等。笔者回顾性分析近3年的双试剂阳性样本复检结果,旨在探讨酶免检测策略调整的可行性及问题,现报道如下。
1材料与方法
1.1标本来源采自天津市血液中心2012年1月至2014年12月无偿献血者,年龄18~55岁,体检合格,献血前经过HBsAg初筛(金标法)及血液比重检测(硫酸铜比重法)合格。献血后按照卫生部要求对血样进行5个项目的初、复检。
1.2试剂与仪器HBsAg初筛金标试纸条(厦门新创公司),初、复检试剂(深圳丽珠、荷兰梅里埃公司);抗-HCV初、复检试剂(北京万泰、美国强生公司);抗-HIV初、复检试剂(北京万泰、荷兰梅里埃、法国伯乐及英国索灵公司);抗-TP初、复检试剂(北京华大吉比爱、北京万泰及北京高达公司);ALT初、复检试剂(上海荣盛、上海科华公司)。酶免初复检质控品为北京康彻斯坦,ALT高、低值质控品为朗道公司产品。所有试剂均通过中国药品生物制品检定所批检合格,且在有效期内使用。主要检测仪器包括STAR全自动加样系统和FAME24/20全自动酶免分析系统和东芝TBA-120FR全自动生化分析仪。
1.3方法ALT检测采用速率法,≥40 IU/L为不合格,HBsAg、抗-HCV、抗-HIV和抗-TP初、复检均采用ELISA法。目前本血站采用初、复检初次反应性均进行双孔复检,双孔阳性为阳性,复检结果一阴一阳也判定为阳性即作不合格报废处理,抗-HIV阳性送天津市疾病预防与控制中心进行确认。所有试验均严格按照试剂盒说明书要求进行操作。
1.4统计学处理使用统计软件SPSS16.0进行统计分析,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2结果
2.1HBsAg双试剂阳性标本的复检2012年1月至2014年12月献血者HBsAg双试剂阳性标本的复检结果见表1。各年份的复检不合格率间比较,差异无统计学意义(P>0.05)。
2.2抗-HIV双试剂阳性标本的复检2012年1月至2014年12月献血者抗-HIV双试剂阳性标本的复检结果见表2。各年份的复检不合格率间比较,差异无统计学意义(P>0.05)。
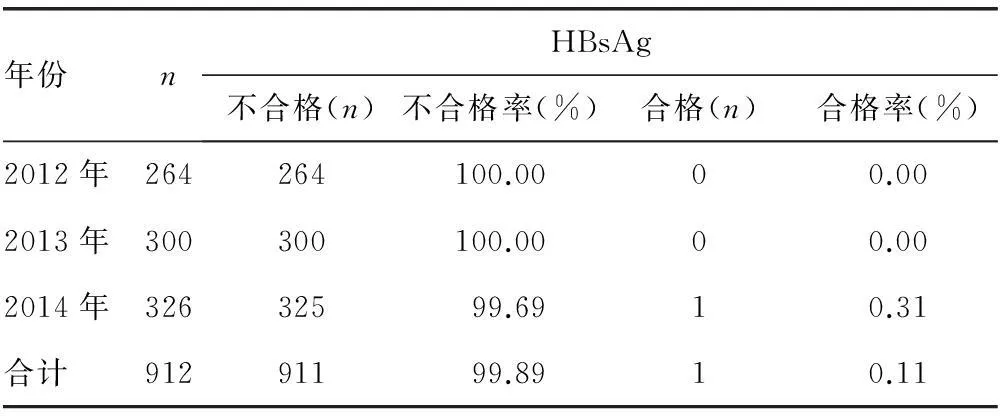
表1 HBsAg双试剂阳性结果的复检情况

表2 抗-HIV双试剂阳性的复检情况
2.3抗-HCV双试剂阳性标本的复检2012年1月至2014年12月献血者抗-HCV双试剂阳性标本复检结果见表3。各年份的复检不合格率间比较,差异无统计学意义(P>0.05)。

表3 抗-HCV双试剂阳性标本复检情况
2.4抗-TP双试剂阳性标本的复检2012年1月至2014年12月献血者血液检测抗-TP双试剂阳性复检结果见表4。各年份的复检不合格率间比较,差异无统计学意义(P>0.05)。
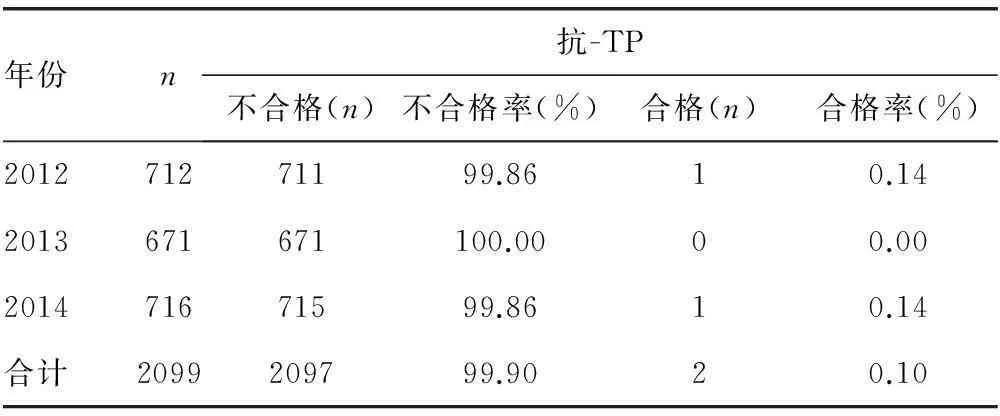
表4 抗-TP双试剂阳性标本复检情况
3讨论
血站技术操作规程对初次试验有反应性的检测标本的后续处理有2种方案[4]。方案1:以同一试验对原血样(或从血袋导管重新取样)做双孔复试,如果双孔复试结果均为无反应性,其初试有反应性可能由于假反应性或技术误差导致,检测结论为无反应性,血液可放行供临床使用;如果双孔复试结果中任何1孔为有反应性,则检测结论为有反应性,对应的血液及由其制备的所有成分应隔离并报废,将血液标本转送相关实验室做进一步确证或补充试验。方案2:不做重复试验,初次试验结论即为检测最终结论。
本血站检验科的既往检测策略是对ELISA初检有反应性标本均采用以同样的试验方法对原血样做双孔复试,如果双孔复试结果均为阴性,检测结论为阴性,血液可放行供临床使用;如果双孔复试结果中任何1孔为阳性,检测结论也为阳性,对应的所有产品均为不合格并作报废处理。回顾分析近3年的初次反应为双试剂阳性的样本,经二次复检后阳性率约为99.39%~100%,而且统计结果也表明3年4项血液筛查检测结果的不合格率也保持稳定状态。据此对检测策略进行更改:ELISA初次试验双试剂阳性标本,其检测结论为阳性,不再进行双孔复试;而对单试剂初次试验为阳性样本采用以同一试验对原血样做双孔复试,如果双孔复试结果均为阴性,检测结论为阴性,血液可放行供临床使用;如果双孔复试结果中任何1孔为为阳性,检测结论为阳性,对应的所有产品均为不合格。
通过此次检测策略的调整确认使有以下几点体会:(1)若检测策略调整为双试剂阳性直接报废不再进行复试对于提高血液安全是有利的但同时也可能会造成血液资源的浪费;(2)检测策略调整会大大减少不必要的复试从而减轻人力,节约物力与财力;(3)血液检测方法的确认不是一性次试验,而是一项需要持续开展的质量活动,实验室应在一定时间周期内对已经过确认的检查方法的性能包括策略等进行验证、确认与调整,才能获得准确、稳定检测结果的证据。
总之,血站血液筛查实验室应该在检测过程发生的变化进行必要的方法确认[5-7]。这些变化包括实验室首次引入的检测方法、已确认的方法条件发生变化、试剂的更换、仪器设备的大修及大保养等。凡是涉及实验室检测方法的任何改变,均需在投入使用前参照相关标准实施确认[8-12]。
参考文献
[1]中华人民共和国卫生部.卫医发[2006]183号 血站实验室质量管理规范2007[S].北京:中华人民共和国卫生部,2006.
[2]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GBT/T22576-2008医学实验室质量和能力的专用要求[S].北京:中国标准出版社,2010.
[3]中国合格评定国家认可委员会.EC15189-2008医学实验室质量和能力的认可准则[S].北京:中国合格评定国家认可委员会,2008.
[4]中华人民共和国国家卫生和计划生育委员会.国卫医发[2015]95号 血站技术操作规程[S].北京:中华人民共和国国家卫生和计划生育委员会,2015.
[5]葛红卫,王鸿捷.血站核酸检测实验室过程确认与变更控制[J].中国输血杂志,2012,25(6):519-523.
[6]葛红卫,王鸿捷.血站实验室血液检测方法确认的技术实践[J].中国输血杂志,2014,27(4):345-348.
[7]王鸿捷,葛红卫.医药领域的确认指南对血站实施确认活动的启示[J].中国输血杂志,2011,24(10):915-920.
[8]Clinical and Laboratory Standards Institute.EP5-A2 Evaluation of precision performance of quantitative measurement methods;approved guideline[S].Wayne,PA,USA:CLSI,2010.
[9]Clinical and Laboratory Standards Institute.EP6-A Evaluation of the linearity of quantitative measurement procedures:a statistical approach[S].Wayne,PA,USA:CLSI,2010.
[10]Clinical and Laboratory Standards Institute.EP10-A3 Preliminary evaluation of quantitative clinical laboratory methods:approved guideline[S].Wayne,PA,USA:CLSI,2010.
[11]Clinical and Laboratory Standards Institute.EP12-A2 User protocol for evaluation of qualitative test performance;approved guideline[S].Wayne,PA,USA:CLSI,2010.
[12]Clinical and Laboratory Standards Institute.EP15-A2 User verification of performance for precision and trueness:approved guideline[S].Wayne,PA,USA:CLSI,2010.
(收稿日期:2016-02-11)
DOI:10.3969/j.issn.1673-4130.2016.08.047
文献标识码:A
文章编号:1673-4130(2016)08-1123-03
△通讯作者,E-mail:yangwenling@tjbc.org.cn。
·临床研究·
