氧化铈空心微球的制备及表征*
2016-05-17邓维钧张问问陈东辉
邓维钧,张问问,陈 亮,胡 静,陈东辉,3
(1. 东华大学 环境科学与工程学院,上海 201620;
2. 上海应用技术学院 香料香精技术与工程学院,上海 201418;
3. 上海应用技术学院 化学与环境工程学院,上海 201418)
氧化铈空心微球的制备及表征*
邓维钧1,张问问2,陈亮1,胡静2,陈东辉1,3
(1. 东华大学 环境科学与工程学院,上海 201620;
2. 上海应用技术学院 香料香精技术与工程学院,上海 201418;
3. 上海应用技术学院 化学与环境工程学院,上海 201418)
摘要:通过聚合物模板法和高温煅烧法制备了氧化铈空心微球,并考察了其光催化性能。采用透射电镜(TEM)和扫描电镜(SEM)研究氧化铈空心微球的尺寸和微观形貌,通过傅立叶转换红外线光谱(FT-IR),X射线衍射(XRD)和比表面积(BET)表征空心微球、晶型结构、比表面积。结果表明,以粒径为220 nm的聚苯乙烯微球可以制得球径约为220 nm的CeO2空心微球。壳层厚度约为20 nm。在模拟可见光的条件下,氧化铈空心微球对罗丹名B的降解率在3 h内可达到95%以上,表现出优异的光催化降解性能。
关键词:模板法;氧化铈;空球;可见光;光催化
0引言
光催化氧化技术是近年发展起来的一种节能、环保的绿色环保技术。TiO2是应用最为广泛的光催化剂,具有廉价、无毒、稳定性好等特点,但是TiO2本身存在的问题比如能带较高、量子效率低的缺点阻碍了其进一步应用,因此,开发新型光催化剂成为拓展光催化应用的有效途径之一[1]。
稀土元素的氧化物的光催化剂也引起了广泛关注,尤其是铈具有独特的4f电子构型,可提供良好的导电性和热稳定性。同时可以同有机分子的功能基团如路易斯碱(胺、醛、醇等)相互作用[2]。铈在我国的储藏量大。氧化铈禁带宽度为2.95 eV,理论上,波长小于420 nm的光可以被吸收,所以氧化铈在可见光下具有一定的光催化性能。氧在CeO2晶格中的扩散速率很快,可以提高光催化反应速率。并且CeO2具有高密度表面晶格缺陷,光催化过程中可以有效地抑制光生电子和空洞的复合,进一步提高光催化活性[3-5]。Zhai等[6]采用沉淀法以碳酸氢铵为沉淀剂,制备了碳酸铈沉淀,并高温煅烧,得到粒径为8~34 nm的CeO2纳米晶体,对可见光存在强吸收。在可见光下对酸性黑10B进行光催化处理可使97%的染料褪色。Wu等[7]通过模板法制备CeO2掺杂介孔材料FSM-16。复合材料在可见光下光催化降解多种染料,降解性能可与P25相媲美。
为了提高光催化性,还可将CeO2与半导体TiO2,SnO2催化剂掺杂。Tian等[8]采用水热法复合TiO2和CeO2,使响应光区移至可见光区。该复合光催化剂可见光条件下对甲基橙的降解性明显优于P25。Jiang等[9]通过凝胶浸渍提拉法制备了CeO2/TiO2复合膜,发现复合膜内表面上的电荷可由TiO2转移到CeO2,实现电荷分离。复合膜的光催化性显著提高。Hiroshi等[10]将金沉积在CeO2粉体上,发现金颗粒可形成局域化的表面等离子体振荡,在550 nm处的可见光区具有最大吸收。该光催化剂在可见光条件下可降解不同有机酸。Xia等[11]通过锰掺杂CeO2纳米棒,使吸收光从紫外光区迁移到红外光区。
无机空心微球具有形态可控、尺寸均匀、比表面积大等特点[12]。与其它形貌材料相比,反应物分子更容易地转移到多孔壳壁的活性位置而提高催化效率。并且,这种空心结构光在内部孔洞中多次反射而提高光源的利用率。在当前环境污染严重的形势之下,无机空心球的光催化特性已成为解决环境问题的途径之一[13-15]。CeO2空心微球可以通过模板法制备。如Guo等[16]以SiO2溶胶颗粒为模板制备了粒径为200 nm的CeO2空心微球。Wang等[17]以碳球为模板,利用碳球表面的羟基与Ce3+作用,制备粒径为150 nm的CeO2空球。Chen等[18]以油菜花粉为模板,制备了粒径为10 μm的CeO2空心球,在可见光照射下对品红溶液降解。目前,使用模板法制备CeO2空心微球的方法要么表面改性较为复杂[16-17],要么受制于天然原料难于规模化[18]。CeO2空心微球简便的制备方法鲜有报道。
本文通过聚合物模板和高温煅烧的方法制备氧化铈空心微球,并考察了其在可见光光照条件下的光催化性能。首先以苯乙烯为原料,制备了聚苯乙烯微球模板,然后硝酸铈为铈源,氨水为pH值调节剂,使用溶胶-凝胶法,制备了Ce(OH)3@PS 复合微球,最后高温煅烧,制备了粒径均匀、形貌规整的氧化铈空心微球。在模拟可见光的条件下,研究了其对罗丹名B的降解性能。
1实验
1.1实验材料
苯乙烯单体(St,99%),无水乙醇(99.7%),氨水(25%~28%)购于国药集团化学试剂有限公司;过硫酸钾(KPS,99.8%)购于上海化学试剂公司;六水合硝酸铈(Ce(NO3)3·6H2O)购于Aldrich公司(美国)。实验室全程使用去离子水。
1.2实验方法
1.2.1PS模板的制备
称取10 g苯乙烯单体,100 g水,加入250 mL三口烧瓶中,室温通入氮气30 min,搅拌,升温到70 ℃,加入0.1 g过硫酸钾(提前溶解于10 mL水),保持温度,共计10 h,之后缓慢冷却。制备胶体溶液离心分离,超声分散于水中,制得5%的PS微球模板。
1.2.2氧化铈空心微球的制备
称取40 g PS微球模板溶液,25 mL水,加入三口烧瓶中,超声10 min,然后搅拌,升温到60 ℃,加入0.434 g Ce(NO3)3·6H2O,反应2 h,加入0.25 g NH3·OH(提前溶解于20 mL水中),反应2 h后,自然冷却。产物离心,分别用水和乙醇洗涤2次。产物放置在恒温干燥箱中干燥6 h,最后将样品在马弗炉中500 ℃下煅烧2 h,制得氧化铈空心微球。
1.3样品的表征
用扫描电子电镜(SEM,Hitachi S-3400N)和透射电子显微镜(TEM,Tecnai G2 F30)研究样品的形貌和尺寸;采用Rigaku D/Max 2500v/pc型X射线衍射仪采集XRD图谱,测试条件为Cu Kα辐射(λ=15 418 nm),管压40 kV,管流20 mA,以4°/min的速度连续扫描,扫描范围2θ=20~80°。用Micromeritics ASAP2020 HD88比表面分析仪,测定液氮(77 K)等温吸附-脱附等温线,得到比表面积(BET);用傅里叶变换红外光谱仪和NETZSCH STA 449 F3同步得到热重分析(TGA)和差示扫描量热(DSC)。
1.4光催化实验
使用比郎光化学反应仪考察样品在可见光条件下对RhB光催化降解性能。具体为称取30 mg样品加入50 mL、10 mg/L的RhB溶液中。暗处理60 min后,打开氙灯,间隔取样,离心,取出上层清液,在λ=553 nm处,测量其吸光度。根据吸光度判定RhB的降解情况。
2结果与讨论
2.1氧化铈空心微球的制备
图1简要描述了制备氧化铈空心球的过程。第一步,制备了粒径均一的PS胶体微球。第二步,以溶胶-凝胶法,将氢氧化铈颗粒吸附沉积到PS胶体微球的表面,形成Ce(OH)3@PS复合微球的核壳结构产物。第三步,通过煅烧移除PS微球模板,得到氧化铈空心微球。在制备的3个步骤中,对不同因素的控制,可以调控氧化铈空心微球的最终形貌。

图1 氧化铈空心微球的制备示意图
Fig 1 Schematic illustration of CeO2hollow spheres fabrication
2.1.1PS模板的制备
如图1(a)所示,使用无皂乳液聚合,苯乙烯单体为原料,KPS为引发剂,制备了粒径均一的PS胶体微球。图2(a)为制备的PS微球的SEM照片。可以看出,所得PS微球粒径约为220 nm,且单分散性好,表面光滑圆润。苯乙烯的无皂乳液聚合属于自由基聚合,生成PS微球。制备的PS微球的表面带有正电荷[19]。通过调节单体量和引发剂量,可以控制聚合反应的速度和进程,得到不同粒径的PS微球。其可控性得到广泛的研究[20]。PS微球粒径影响氧化铈空球的内径。
2.1.2Ce(OH)3@PS复合微球的制备
如图1(b)所示,使用硝酸铈为铈前驱体,氨水为pH值调节剂,以溶胶-凝胶法,将氢氧化铈颗粒通过电荷吸附作用,吸附到PS胶体微球的表面,形成Ce(OH)3@PS的核壳结构产物。图2(b)为所制备的Ce(OH)3@PS微球的SEM照片。可以看出,复合微球单分散性好,粒径约为250 nm。粒径增加约为40 nm,即壳层厚度为20 nm。壳层的厚度影响氧化铈空心球的壳层厚度。表面较为粗燥,这可能是Ce(OH)3颗粒沉积在PS 微球上的结果。溶胶-凝胶时,胶体溶液中pH值使用氨水调节到9左右,铈离子与氢氧根配位,电负性增加,乃至形成氢氧化铈沉淀颗粒。胶体颗粒形成的过程可以简单表述为式(1)。带有负电荷的胶体颗粒通过电荷吸引,吸附在带有正电荷PS微球的表面,形成核壳结构复合微球。
(1)
2.1.3氧化铈空心微球的制备
如图1(c)所示,通过煅烧Ce(OH)3@PS微球,移除PS微球模板得到空心微球,同时在高温热解作用下,非晶结构Ce(OH)3转换为CeO2晶体结构。因而制备空心微球为CeO2空心微球。图2(c)为制备的CeO2空心微球的SEM照片。从照片可以看出,CeO2空心微球粒径约为220 nm,单分散性好。大部分为球形,部分空心球带有孔洞和破裂。图2(d)为制备的CeO2空心微球的TEM照片。可以看出,CeO2空心微球粒径约为220 nm,壳层厚度约为20 nm。空心微球单分散性好。大部分为球形,部分空心球破裂。在煅烧过程中,Ce(OH)3@PS复合微球存在一定的收缩,这可能是因为在高温煅烧时,受到高温的作用,壳层减少表面能。

图2PS微球、Ce(OH)3@PS复合微球和CeO2空心微球的SEM和TEM照片
Fig 2 SEM images of PS spheres, Ce(OH)3@PS composite spheres and CeO2hollow spheres and TEM images of CeO2hollow spheres
图3为Ce(OH)3@PS 复合微球的TGA和DSC曲线。可以看到,当温度升高到220 ℃时,质量损失逐渐加快,这是因为结合水加速离开微球和PS微球逐渐开始热解。当温度在350 ℃时,质量损失剧烈,同时DSC显示大量能量放出,这是由于壳层包覆的PS,因热解作用,集中放出的热量。因为热解的能量突破壳层的约束,短时间放出,壳层形成孔洞或者直接爆破,形成半球面或者碎片,同时质量锐减。这是氧化铈空心微球具有破损、不完整的直接原因。在这个温度范围,减缓温度上升的速度,利于空心球形貌的完整。温度>400 ℃时,失重变得不明显。

图3 Ce(OH)3@PS的TGA 和DSC曲线
Fig 3 TGA and DSC curves of Ce(OH)3@PS composite spheres
如前所述,Guo等[16]以SiO2溶胶颗粒为模板水热法制备了SiO2/CeO2复合微球,然后使用浓的苛性钠刻蚀掉SiO2模板制得CeO2空心微球。SiO2微球作为刚性模板能够较好复制模板的形貌。当硅球的形貌和单分散性良好时,制得空心微球形貌和单分散性应当较好。但是从该报道中的SEM电镜照片可以清楚地看出微球的表面过于粗糙,这可能是水热条件下晶体颗粒过度地生长造成;此外SiO2模板的移除必须依赖于浓的苛性钠或HF。Wang等[17]以碳球为模板,采用制备了CeO2空心微球。从电镜图片可以看出,所得空心球不够圆,粒径大小不一。这可能是碳球模板不够圆润和大小不一的原因。但是基于碳球模板,制备的CeO2空心微球具有较大的孔径和比表面积。本文使用聚苯乙烯微球为模板,采用溶胶-凝胶法制备了CeO2空心微球,方法简单,耗时短,避免使用有机溶剂,而且聚苯乙烯适合工业化,聚合反应可以调控制得不同粒径微球,制备的CeO2空心微球形貌均一,单分散性好,因而更加具有优势,制备的CeO2空心微球具有更好的应用前景。
2.2氧化铈空心微球的表征
图4(a)为PS微球、Ce(OH)3@PS复合微球和CeO2空心微球的FT-IR图谱。1 492.6和1 600.6 cm-1处为苯环的特征峰,3 000.7和3 058.5 cm-1处为C—H特征峰。它们都是PS的特征峰,在PS和Ce(OH)3@PS微球中出现,而在CeO2空心微球中消失。这表明高温煅烧完全地移除PS模板,形成不带PS残余的CeO2空心微球。
图4(b)为CeO2空心微球XRD曲线。对比CeO2晶体的标准卡(JCPDF#34-0394)发现制备的氧化铈空心微球的特征衍射峰(111,200,220,311)的位置,相对强度与标准卡一致。无其它杂质的衍射峰,说明所制备的样品的纯度高,晶型为CeO2立方萤石结构。此外图中各衍射峰比较尖锐,样品结晶性比较好[23]。
通过以上的分析,可以推测,在高温煅烧和冷却的过程中,Ce(OH)3@PS壳层中的Ce(OH)3发生的化学变化可以表达为式(2)、(3)。
(2)
(3)
立方萤石型CeO2从热力学的角度,比Ce2O3具有更低的焓,更稳定[24]。在氧分压极低的情况下,晶格中的氧的丢失,形成氧缺陷。氧缺陷在氧化铈的催化性能中发挥重要的作用。在氧气充分的条件下,氧缺陷部分可以得到氧,形成相对稳定的CeO2。从氧的丢失和获得的角度,反应式(3)又可以写成反应式(4)

(4)


图4 FT-IR和XRD曲线
Fig 4 FT-IR of PS spheres, Ce(OH)3@PS composite spheres and CeO2hollow spheres and XRD curve of CeO2hollow spheres
2.3氧化铈空心微球的光催化性能
图5为所制备的CeO2空心微球对RhB的可见光光催化降解曲线。可以发现, RhB的降解3 h达到95%以上,远远大于商业氧化铈纳米颗粒。证明CeO2空心微球具有优异的光催化性能。
CeO2空心微球的相貌结构是其具有优异光催化性能的原因。对比商业氧化铈纳米颗粒的XRD发现,其晶型与CeO2空心微球相同。BET的测试结构表明,CeO2空心微球的表面积为47 m2/g,而商业氧化铈纳米颗粒仅为15 m2/g。更重要的原因在于空心微球的结构提升了光催化性能。氧化铈空心微球其独特的空心结构使得微球外层和内层都可以吸附RhB,增加反应的活性点,从而提高CeO2空心微球光催化性能。文献[16]报道的CeO2空心球,主要用途为紫外线的屏蔽剂,这可能的原因是空心球的壳层太厚,无法内外层增加反应活性点,同时壳层的表面没有较多的氧缺陷,活性较低。
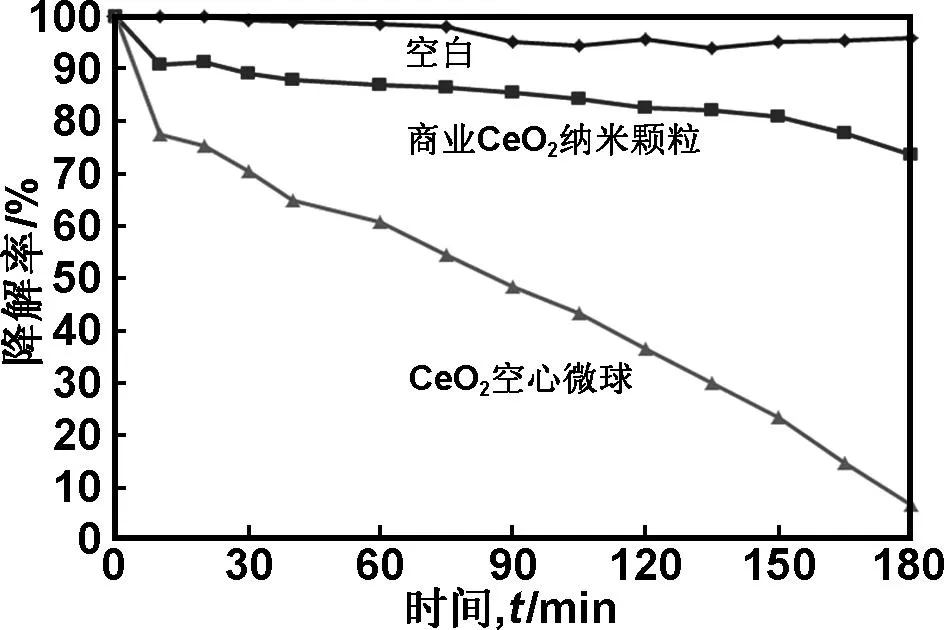
图5 CeO2空心微球的可见光光降解RhB
Fig 5 Photodegradation of Rhodamine B with as-obtained CeO2hollow spheres and commercial CeO2nanoparticles
3结论
通过聚合物模板法和高温煅烧法制备了氧化铈空心微球,并考察了其可见光降解RhB的性能。实验结果表明,制备的CeO2空心微球的球径约为220 nm,壳层厚度约为20 nm。氧化铈空心微球粒径均匀,单分散。可见光条件下,光催化降解RhB的实验表明氧化铈空心微球具有优异的光催化性能。
参考文献:
[1]Linsebigler A L, Lu G, Yates J T. Photocatalysis on TiO2surfaces: principles, mechanisms, and selected results[J]. Chem Rev,1995,95:735-758.
[2]Wang C, Ao Y, Wang P, et al. Preparation, characterization, photocatalytic properties of titania hollow sphere doped with cerium[J]. J Hazard Mater, 2010, 178: 517-521.
[3]Chaudhary Y S, Panigrahi S, Nayak S, et al. Facile synthesis of ultra-small monodisperse ceria nanocrystals at room temperature and their catalytic activity under visible light[J]. J Mater Chem, 2010, 20: 2381-2385.
[4]Bamwenda G R, Uesigi T, Abe Y, et al. The photocatalytic oxidation of water to O2over pure CeO2, WO3, and TiO2using Fe3+and Ce4+as electron acceptors[J]. Appl Catal A: Gen, 2001, 205: 117-128.
[5]Zhong L, Hu J, Cao A, et al. 3D flowerlike ceria micro/nanocomposite structure and its application for water treatment and CO remove[J]. Chem Mater, 2007, 19:1648-1655.
[6]Zhai Y, Zhang S, Pang H. Preparation, characterization and photocatalytic activity of CeO2nanocrystalline using ammonium bicarbonate as precipitant[J]. Mater Letters, 2007, 61: 1863-1866.
[7]Wu Y, Liu S, Zuo Y, et al. Photodegradation of some dyes over Ce/FSM-16 catalyst under solar light[J]. Catal Lett, 2007, 119: 245-251.
[8]Tian J, Sang Y, Zhao Z, et al. Enhanced photocatalytic performances of CeO2/TiO2nanobelt heterostructures[J]. Small, 2013, 22(9):3864-3872.
[9]Jiang B, Zhang S, Guo X, et al. Preparation and photocatalytic activity of CeO2/TiO2interface composite film[J]. Appl Surf Sci, 2009, 255: 5975-5978.
[10]Hiroshi K, Atsuhiro T, Keiji H. Gold nanoparticles supported on cerium(Ⅳ) oxide powder for mineralization of organic acids in aqueous suspensions under irradiation of visible light of 530 nm[J]. Chem Commun,2010, 46: 1287-1289.
[11]Xia C, Hu C, Chen P, et al. Magnetic properties and photoabsorption of the Mn-doped CeO2nanorods[J]. Mater Res Bull, 2010, 45: 794-798.
[12]Hu J, Chen M, Fang X, et al. Fabrication and application of inorganic hollow spheres[J]. Chem Soc Rev, 2011, 40: 5472-5491.
[13]Li G, Liu F, Zhang Z H. Enhanced photocatalytic activity of silica-embedded TiO2hollow microspheres prepared by one-pot approach[J]. J Alloys Compounds, 2010, 493: 1-7.
[14]Zhao W, Feng L L, Yang R. Synthesis, characterization, and photocatalytic properties of Ag modified hollow SiO2/TiO2hybrid microspheres[J]. Appl Catal B: Environ, 2011,103: 181-189.
[15]Zhang L, Li X, Chang Z X. Preparation, characterization and photoactivity of hollow N,Co codoped TiO2/SiO2microspheres[J]. Mater Sci Semicond Proces, 2011, 14: 52- 57.
[16]Guo Z, Jian F, Du F. A simple method to controlled synthesis of CeO2hollow microspheres[J]. Scripta Materialia, 2009, 61: 48-51.
[17]Wang S, Zhang J, Jiang J. Porous ceria hollow microspheres: synthesis and characterization[J]. Micropor Mesopor Mater, 2009, 123:349-353.
[18]Chen F, Wang W, Chen Z, et al. Biogenic synthesis and catalysis of porous CeO2hollow microspheres[J]. J Rare Earths, 2012, 30: 350-354.
[19]Deng Z, Chen M, Zhou S, et al. A novel method for the fabrication of monodisperse hollow silica spheres[J].Langmuir, 2006, 22, 6403-6407.
[20]Gu Z, Chen H, Zhang S, et al. Rapid synthesis of monodisperse polymer spheres for self-assembled photonic crystals[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2007, 302(1-3):312-319.
[21]Sun C, Li H, Chen L. Nanostructured ceria-based materials: synthesis, properties, and applications[J]. Energy Environ Sci, 2012,5:8475-8505.
[22]Tuller H. Ionic conduction in nanocrystalline materials[J]. Solid State Ionics, 2000,131:143-157.
Synthesis and characterization of ceria micro hollow spheres
DENG Weijun1, ZHANG Wenwen2, CHEN Liang1, HU Jiang2, CHEN Donghui1,3
(1. College of Environmental Science and Engineering,Donghua University, Shanghai, 201620, China;2. School of Perfume and Aroma Technology, Shanghai Institute of Technology, Shanghai 200235, China;3. School of Chemical and Enviromental Engineering, Shanghai Institute of Technology,Shanghai 200235, China)
Abstract:Cerium (Ⅲ) hydroxide @ polystyrene micro spheres was synthesized via a co-precipitation process with additive of ammonia in a water bath. Cerium (Ⅳ) oxide micro hollow spheres were obtained upon calcination at temperature of 500 ℃ over two hours. The morphology, size, structure, crystallinity and FT-IR spectrum of Cerium (Ⅳ) oxide micro hollow spheres were characterized by scanning electron microscopy, transmission electron microscopy, X-ray diffraction and FT-IR spectrograph. The formation mechanism was discussed. The results show that the diameters of the as-prepeared Cerium (Ⅳ) oxide micro hollow spheres are about 220 nm in diameter and 20 nm in shell thickness. The as-prepared samples are uniform, well dispersed and of high purity. TGA, DSC and FT-IR verify that polystyrene was completely decomposed. XRD shows that shell was highly pure and in crystal structure. Photodegradation experiments demonstrate that as-prepared sample has better photocatalytic activity.
Key words:cerium (Ⅳ) oxide; micro hollow spheres; ammonia; co-precipitation process; synthesis
DOI:10.3969/j.issn.1001-9731.2016.02.040
文献标识码:A
中图分类号:TQ133.3
作者简介:邓维钧(1976-),男,安徽宿州人,博士,师承陈亮教授和陈东辉教授,从事环境材料和环境科学研究。
基金项目:国家自然科学基金资助项目(21106084);上海科研创新基金资助项目(14zz164);上海启明星计划资助项目(14QA143300)
文章编号:1001-9731(2016)02-02201-05
收到初稿日期:2015-04-10 收到修改稿日期:2015-11-10 通讯作者:陈亮,E-mail: chliang@dhu.edu.cn,胡静
