Ag-Zn3(VO4)2催化剂的水热合成及其可见光催化活性
2016-04-25陈建林王孟晴朱雪娇
方 琴,陈建林,王孟晴,朱雪娇
(南京大学环境学院 污染控制与资源化研究国家重点实验室,江苏 南京 210023)
Ag-Zn3(VO4)2催化剂的水热合成及其可见光催化活性
方琴,陈建林*,王孟晴,朱雪娇
(南京大学环境学院 污染控制与资源化研究国家重点实验室,江苏 南京 210023)
摘要:以Zn(NO3)2·6 H2O、AgNO3和NaVO3为原料,采用水热法合成Ag-Zn3(VO4)2催化剂,并通过SEM、TEM和UV-Vis DRS等对催化剂进行表征分析。以甲基橙染料废水为探针污染物,考察Ag+与Zn(2+)物质的量比、水热温度和水热时间对Ag-Zn3(VO4)2光催化剂催化活性和表面形貌的影响。结果表明,在Ag+与Zn(2+)物质的量比为0.15、水热温度160 ℃和水热时间16 h条件下,合成的Ag-Zn3(VO4)2光催化剂光催化活性最好,光照5 h后,对甲基橙染料的脱色率达99.18%,较Zn3(VO4)2催化剂(合成条件为pH=10和160 ℃水热反应16 h)提高43.99%。采用水热合成法制备的催化剂Ag-Zn3(VO4)2具有较好的可见光活性。
关键词:催化剂工程;Ag-Zn3(VO4)2光催化剂;可见光催化;水热合成;甲基橙降解
CLC number:O643.36;TQ034Document code: AArticle ID: 1008-1143(2016)01-0052-05
针对环境污染和能源短缺两大经济发展瓶颈,同时为达到日益严格的环境标准要求,光催化已经在不同领域广泛应用,包括用于室内空气净化器、降解空气和水中的各类污染物、光分解水制取氢气以及制作染料敏化太阳能电池等,光催化技术在环境净化和新能源的开发方面表现出广阔的发展和应用前景[1-3]。
某些钒酸盐在光催化领域存在巨大的应用潜力[4-5],是一类新型的高活性光催化剂。有学者提出能带工程[6-7]概念研究可见光催化剂,发现通过引入 d10电子构型的Zn、 Ag或ns2构型的 p 区元素能够提升价带位置,进而很好地缩短带隙宽度。通过引入过渡金属 V 或 p 区元素 In[8-9],可以设计导带位置较低的新型可见光催化材料。Zn3(VO4)2由于具有较好的荧光性能及光催化性能,逐渐引起关注。Ni S B等[10]以Zn(NO3)2、V2O5和C6H12N4为原料,制得的Zn3(VO4)2颗粒在可见光下具有很好的发光性能,特别在568 nm处发射峰强度很强。Chanchal Mondal等[11]第一次使用湿化学法不添加任何模板剂和结构导向剂合成出Zn3(VO4)2,可在紫外光下降解有机染料,且循环使用几次后依然保持原来的光催化活性。由于具有较窄的禁带宽度,Ag3VO4也是应用非常广阔的的可见光响应催化剂[12]。Konta R等[13]研究发现,只有Ag3VO4的可见光催化活性较好。Huang Chaoming等[14]采用低温水热法合成出具有可见光响应的钒酸银催化剂,光催化效果好,其较高的光催化活性主要归因于Ag4V2O7和α-Ag3VO4混晶相的组成,α-Ag3VO4是主要成分。Hu Xuexiang等[15]采用沉淀法制备了单斜结构的Ag3VO4,并通过降解偶氮染料酸性红B评价在可见光下的催化活性,发现V过量或是Ag过量比按照化学计量比制得的Ag3VO4表现出更好的可见光催化活性。张绍岩等[16]制备的α-AgVO3微米棒在紫外和可见光区均具有较强的吸收性能。Wang G等[17]采用软化学法合成了高可见光催化活性的Ag-Ag3VO4,研究发现,Ag-Ag3VO4在降解有机污染物方面是一种高效、稳定的可见光催化剂。
本研究采用水热合成法制备Ag-Zn3(VO4)2可见光催化剂,考察Ag+与Zn2+物质的量比、水热温度和水热时间对Ag-Zn3(VO4)2光催化剂的催化活性和表面形貌的影响。
1实验部分
1.1试剂与仪器
Zn(NO3)2·6H2O,分析纯,成都市科龙化工试剂厂;NaVO3,分析纯,上海阿拉丁生化科技股份有限公司 ;AgNO3,分析纯,南京化学试剂有限公司;NaOH,分析纯,南京化学试剂有限公司;HNO3,分析纯,南京化学试剂有限公司;甲基橙,工业级,上海三爱思试剂有限公司;蒸馏水,分析纯,东南大学。
自制光催化反应器;T-6M紫外/可见分光光度计,南京菲勒仪器有限公司;DGG-9070B电热恒温鼓风干燥箱,上海森信实验仪器有限公司;KQ2200DE超声波清洗器,昆山市超声仪器有限公司;UV3600紫外-可见扫描仪,日本岛津公司;JA1003N电子天平;85-1磁力搅拌器,南京科尔仪器设备有限公司;6171型pH计,上海任氏电子仪器有限公司;聚四氟乙烯水热反应罐,京君龙实验仪器(北京)有限公司。
实验采用的光源均为南京灯泡厂日光色镝灯,功率400 W,主波长560 nm,光通量为32 000 lm。
1.2催化剂制备
按不同Ag+与Zn2+物质的量比称取AgNO3和Zn(NO3)2·6H2O粉末,溶于适量的蒸馏水中磁力搅拌至完全溶解。再按照化学计量比称取一定量的NaVO3并溶于0.4 mol·L-1的NaOH溶液中,磁力搅拌至NaVO3完全溶解。
将硝酸银和硝酸锌的混合液缓慢滴入NaVO3溶液中,磁力搅拌30 min,调节前驱液pH=10,继续磁力搅拌30 min,超声均化30 min得到浅黄色的悬浊液。将此悬浊液移入聚四氟乙烯反应罐,将反应罐密封于反应釜中。将反应釜放入烘箱,在一定温度进行反应,待反应釜静置冷却至室温后,取出聚四氟乙烯反应罐,用蒸馏水对得到的沉淀物进行抽滤,抽滤洗涤多次后,烘箱60 ℃烘干,研钵研细后置于马弗炉600 ℃焙烧4 h,样品随炉体自然冷却后取出,研磨制得Ag-Zn3(VO4)2催化剂,置于干燥器中避光保存。
1.3光催化活性实验
取20 mg·L-1甲基橙溶液和2.0 g·L-1的光催化剂,避光磁力搅拌30 min,光源距反应溶液液面约15 cm。实验中以针筒取样器取样,经0.22 μm水系滤头过滤后,于462 nm处测定滤液的吸光度,并根据甲基橙浓度-吸光度标准曲线计算甲基橙浓度。催化剂的光催化活性用甲基橙脱色率表示。
2结果与讨论
2.1Ag+与Zn2+物质的量比
在160 ℃水热反应16 h再焙烧条件下,考察Ag+与Zn2+物质的量比对合成的Ag-Zn3(VO4)2光催化剂甲基橙脱色率的影响,如图1所示。

图 1 Ag+与Zn2+物质的量比对合成的Ag-Zn3(VO4)2光催化剂甲基橙脱色率的影响Figure 1 Removal rate of methyl orange over Ag-Zn3(VO4)2 photocatalysts prepared with different Ag+/Zn2+ molar ratios
由图1 可以看出,Ag-Zn3(VO4)2的光催化活性均优于未掺杂的Zn3(VO4)2,而且光催化活性随掺杂量的提高先增后降,当Ag+与Zn2+物质的量比为0.15时,Ag-Zn3(VO4)2的光催化活性最好,光照5 h后,脱色率99.18%,较纯Zn3(VO4)2的光催化活性提高43.99%;继续增加Ag掺杂量,甲基橙脱色率反而降低,表明Ag掺杂量存在一个最佳值。
2.2水热温度
在Ag+与Zn2+物质的量比为0.15、一定温度水热反应16 h再焙烧条件下,考察水热温度对合成的Ag-Zn3(VO4)2光催化剂甲基橙脱色率的影响,结果如图2所示。
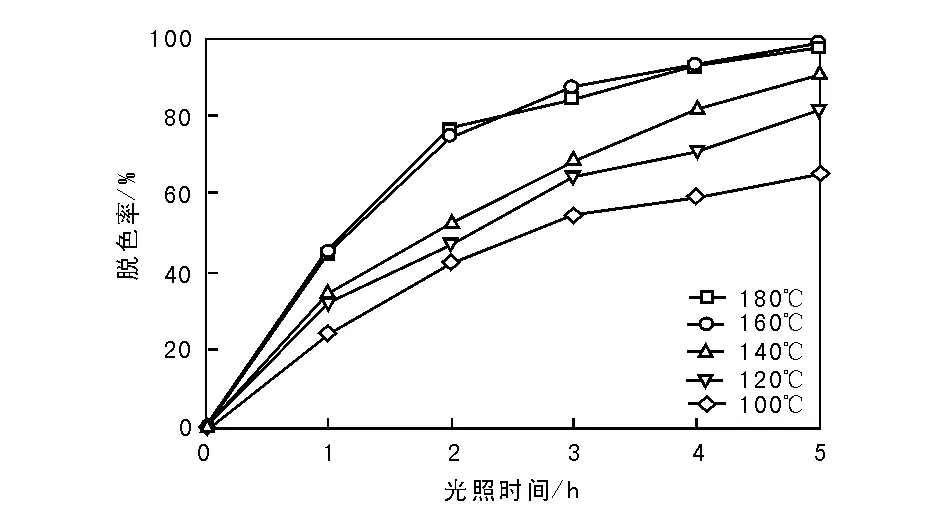
图 2 水热温度对合成的Ag-Zn3(VO4)2光催化剂甲基橙脱色率的影响Figure 2 Removal rate of methyl orange over Ag-Zn3(VO4)2 photocatalysts prepared at different hydrothermal temperatures
由图2可以看出,甲基橙溶液的降解效果随水热温度的升高而增强,160 ℃和180 ℃合成的催化剂的光催化活性最好。水热温度对光催化活性的影响可能与催化剂的结晶度及粒径有关,水热温度较低时,合成的催化剂结晶度较差,而随着水热温度的升高,催化剂的结晶度虽然趋于成熟,但其粒径逐渐变大,比表面积逐渐变小。综合考虑,确定制备催化剂的最佳水热温度为160 ℃。
2.3水热时间
在 Ag+与Zn2+物质的量比为0.15、一定时间水热温度160 ℃再焙烧条件下,考察水热时间对合成的Ag-Zn3(VO4)2光催化剂甲基橙脱色率的影响,结果如图3所示。
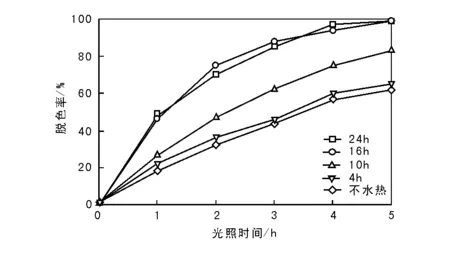
图 3 水热时间对合成的Ag-Zn3(VO4)2光催化剂甲基橙脱色率的影响Figure 3 Removal rate of methyl orange over Ag-Zn3(VO4)2 photocatalysts prepared for different hydrothermal time
由图3可以看出,水热时间16 h和24 h的光催化活性最好,光照5 h后,对甲基橙溶液的脱色率分别达99.18%和99.35%。综合考虑催化剂的性能和制备成本,确定16 h为最佳水热合成时间。
2.4Ag-Zn3(VO4)2光催化剂性能
在最佳条件Ag+与Zn2+物质的量比为0.15、160 ℃水热反应16 h再焙烧制备的Ag-Zn3(VO4)2催化剂和相同条件下的纯Zn3(VO4)2以及不进行焙烧的Zn3V2O7(OH)2·2H2O的光催化活性进行对比,结果见图4。

图 4 Ag-Zn3(VO4)2光催化剂、纯Zn3(VO4)2和Zn3V2O7(OH)2·2H2O对甲基橙脱色率的影响Figure 4 Removal rate of methyl orange over Ag-Zn3(VO4)2 photocatalyst,pure Zn3(VO4)2and Zn3V2O7(OH)2·2H2O
由图4可以看出,在最佳条件下制备的Ag-Zn3(VO4)2催化剂光催化活性最好,甲基橙脱色率较同条件下的纯Zn3(VO4)2提高了43.99%,不进行焙烧的Zn3V2O7(OH)2·2H2O在可见光下不具催化活性。
2.5SEM和TEM
图5分别为Ag+与Zn2+物质的量比为0.15、160 ℃水热反应16 h再焙烧制备的Ag-Zn3(VO4)2催化剂的SEM及其TEM照片。由图5可以看出,Ag-Zn3(VO4)2光催化剂外貌为不规则的大颗粒物上分布着很多小颗粒,大颗粒粒径小于10 μm,小颗粒粒径大于0.5 μm,颗粒间有较强的团聚现象。更大的放大倍数下可见颗粒有一定烧结,可能与催化剂的高温焙烧处理有关。由图5还可以看出,颗粒具有清晰的边界,说明催化剂结晶状态良好,和XRD结果一致。TEM照片显示的颗粒粒径大于100 nm,颗粒间有明显的团聚现象,SEM观察到相对较大的颗粒粒径可能与颗粒的团聚有关。

图 5 Ag-Zn3(VO4)2光催化剂的SEM与TEM照片Figure 5 SEM and TEM images of Ag-Zn3(VO4)2 photocatalyst
2.6Ag-Zn3(VO4)2光催化剂的响应范围
分别对Ag+与Zn2+物质的量比为0和0.15、160 ℃水热反应16 h再焙烧制备的的Zn3(VO4)2和Ag-Zn3(VO4)2进行UV-Vis DRS分析,结果如图6所示。由图6可以看出,纯Zn3(VO4)2和Ag+与Zn2+物质的量比为0.15的Ag-Zn3(VO4)2光催化剂在紫外和可见光区均有吸收峰,且Ag掺杂后吸收带边发生明显红移,表明Ag掺杂后禁带宽度变窄;光吸收强度在紫外和可见光区也明显增加,在一定程度上提高了Ag-Zn3(VO4)2光催化剂对可见光的利用率。
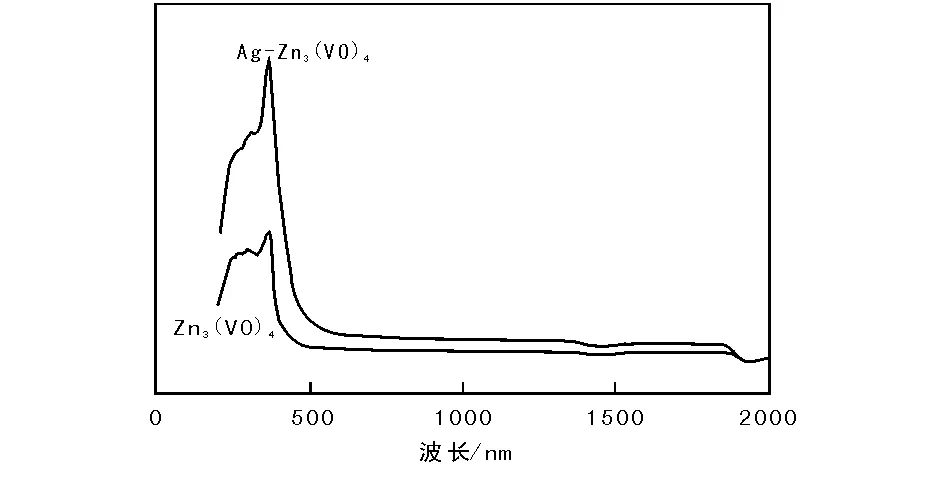
图 6 Zn3(VO4)2和Ag-Zn3(VO4)2光催化剂的UV-Vis DRS谱图Figure 6 UV-Vis DRS spectra of Zn3(VO4)2 and Ag-Zn3(VO4)2 photocatalyst
3结论
(1) 以Zn(NO3)2·6H2O、AgNO3和NaVO3为原料,采用水热法合成的Ag-Zn3(VO4)2具有较好的可见光催化活性。
(2) 在Ag+与Zn2+物质的量比为0.15、160 ℃水热反应16 h焙烧制备的Ag-Zn3(VO4)2光催化剂催化活性最好,光照5 h时,甲基橙脱色率99.18%,较相同条件下的纯Zn3(VO4)2提高了43.99%,而不进行焙烧制得的Zn3V2O7(OH)2·2H2O在可见光下不具催化活性。
(3) 通过XRD、UV-Vis DRS等对催化剂进行表征分析发现,Ag掺杂量影响催化剂的晶相组成和结晶度;最佳条件下的Ag-Zn3(VO4)2在紫外和可见光区均有吸收,较掺杂前吸收带边发生明显红移,光吸收强度在紫外和可见光区也明显增加,在一定程度上提高了对可见光的利用率。
参考文献:
[1]Hoffmann M R,Martin S T,Choi W Y.Environmental application of semiconductor photocatalyst[J].Chemical Reviews,2005,95(1):69-96.
[2]Yan H J.Soft-templating synthesis of mesoporous graphitic carbon nitride with enhanced photocatalytic H2evolution under visible light[J].Chemical Communications,2012,48:3430- 3432.
[3]Mo J,Zhang Y,Xu Q,et al.Photocatalytic purification of volatile organic compounds in indoor air:a literature review[J].Atmospheric Environment,2009,43(14):2229-2246.
[4]Harada H,Hosoki C,Kudo A.Overall water splitting by sonophotocatalytic reaction:the role of powdered photocatalyst and an attempt to decompose water using a visible-light sensitive photocatalyst[J].Journal of Photochemistry and Photobiology A:Chemistry,2001,141(2):219-224.
[5]Ye J,Zou Z,Arakawa H,et al.Correlation of crystal and electronic structures with photophysical properties of water splitting photocatalysts InMO4(M=V5+,Nb5+,Ta5+)[J].Journal of Photochemistry and Photobiology A:Chemistry,2002,148(1):79-83.
[6]Ye J H,Zou Z G.Visible light sensitive photocatalysts In1-xMxTaO4(M=3d transition-metal) and their activity controlling factors[J].Journal of Physics and Chemistry of Solids,2005,66(2):266-273.
[7]Hitoki G,Takata T,Kondo J N,et al.An oxynitride,TaON,as an efficient water oxidation photocatalyst under visible light irradiation(λ≤500 nm)[J].Chemical Communications,2002,16:1698-1699.
[8]Zhou L,Wang W Z,Liu S W,et al.A sonochemical route to visible-light-driven high-activity BiVO4photocatalyst[J].Journal of Molecular Catalysis A:Chemical,2006,252(1):120-124.
[9]Tang J W,Zou Z G,Katagiri M,et al.Photocatalytic degradation of MB on MIn2O4(M=alkali earth metal) under visible light:effects of crystal and electronic structure on the photocatalytic activity[J].Catalysis Today,2004,93:855-889.
[10]Ni S B,Wang X H,Zhou G,et al.Crystallized Zn3(VO4)2:synthesis,characterization and optical property[J].Journal of Alloys and Compounds,2010,491:378-381.
[11]Chanchal Mondal,Mainak Ganguly,Arun Kumar Sinha,et al.Robust cubooctahedron Zn3V2O8in gram quantity:a material for photocatalytic dye degradation in water[J].CrystEngComm,2013,15,6745.
[12]Huang C M,Pan G T,Li Y C,et al.Crystalline phase and photocatalytic activities of hydrothermal synthesis Ag3VO4and Ag4V2O7under visible light irradiation[J].Applied Catalysis A:General,2009,358(2):164-172.
[13]Konta R,Kato H,Kobaoshi H,et al.Photophysical properties and photocatal-ytic activities under visible light irradiation of silver vanadates[J].Physical Chemistry Chemical Physics,2003,5(14):3062-3065.
[14]Huang Chaoming,Pan Guanting,Yuchu M Li,et al.Cryatalline phases and photocatalytic activities of hydrothermal synthesis Ag3VO4and Ag4V2O7under visible light irradiation[J].Applied Catalysis A:General,2009,358:164-172.
[15]Hu Xuexiang,Hu Chun.Preparation and visible-light photocatalytic actiyity of Ag3VO4powders[J].Journal of Solid State Chemistry,2007,180:725-732.
[16]张绍岩,肖霄,任蕾,等.ɑ-AgVO3微米棒的制备及光吸收性能[J].人工晶体学报,2011,40(4):1039-1042.
Zhang Shaoyan,Xiao Xiao,Ren Lei,et al.Synthesis and optical properties of α-AgVO3Microrods[J].Journal of Synthtic Crystals,2011,40(4):1039-1042.
[17]Wang G,Ren Y,Zhou G J,et al.Synthesis of highly efficient visible light Ag@Ag3VO4plasmonic photocatalysts[J].Surface & Coatings Technology,2013,228:283-286.
Hydrothermal synthesis of Ag-Zn3(VO4)2photocatalysts and their catalytic activity under visible light
FangQin,ChenJianlin*,WangMengqing,ZhuXuejiao
(State Key Laboratory of Pollution Control & Resource Reuse, School of the Environment,Nanjing University, Nanjing 210023, Jiangsu, China)
Abstract:Using Zn(NO3)2·6H2O,AgNO3 and NaVO3 as the raw materials,the visible-light photocatalyst Ag-Zn3(VO4)2 was synthesized by hydrothermal process.The as-prepared photocatalysts were characterized by SEM,TEM and UV-Vis DRS.The influence of Ag+/Zn(2+) molar ratios,hydrothermal synthetic temperatures and time on catalytic activity and surface morphology of Ag-Zn3(VO4)2 photocatalysts was investigated by using methyl orange dye wastewater as probe pollutant.The results showed that Ag-Zn3(VO4)2 photocatalyst possessed the best photocatalytic activity under the preparation condition of Ag+/Zn(2+) molar ratio 0.15,hydrothermal synthetic temperature 160 ℃ and hydrothermal synthetic time 16 h.After visible light illumination for 5 h,methyl orange degradation rate over Ag-Zn3(VO4)2 photocatalyst was 99.18%,which was 43.99% higher than that over Zn3(VO4)2 catalyst prepared under the condition of pH=10 and 160 ℃ hydrothermal reaction for 16 h.Ag-Zn3(VO4)2 prepared by hydrothermal method exhibited excellent catalytic activity under visible light irradiation.
Key words:catalyst engineering; Ag-Zn3(VO4)2 photocatalyst; visible light catalysis; hydrothermal synthesis; methyl orange degradation
中图分类号:O643.36;TQ034
文献标识码:A
文章编号:1008-1143(2016)01-0052-05
doi:10.3969/j.issn.1008-1143.2016.01.009 10.3969/j.issn.1008-1143.2016.01.009
作者简介:方琴,1989年生,女,安徽省铜陵市人,在读硕士研究生,研究方向为水处理。
收稿日期:2015-09-28修回日期:2015-12-30
催化剂制备与研究
通讯联系人:陈建林,男,副教授,研究方向为水处理和固废资源化。
