四川栽培和野生型大黄五种蒽醌类成分的含量对比研究
2016-04-23李奇娟胡慧玲王战国王友
李奇娟,胡慧玲,王战国,王友
四川栽培和野生型大黄五种蒽醌类成分的含量对比研究
李奇娟1,胡慧玲1,王战国2,王友3
[摘要]目的:比较分析四川栽培和野生型大黄五种蒽醌类成分的含量差异。方法:采用Chromasil C(18)色谱柱(5μm,250 × 4.6 mm),流动相为甲醇-0.1%磷酸溶液(85:15),体积流量1.0 mL/min,柱温30 ℃,检测波长254 nm。结果:芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚分别在4.1~65.1、3.9~63.1、4.0~63.4、4.1~66.0、2.0~31.6 μg/mL 浓度范围内与峰面积积分值线性关系良好(R2≥0.9996),平均加样回收率为96.47~102.38 %,RSD均小于2.56 %。采用建立的HPLC方法测定茂县、北川两地栽培的唐古特三年生大黄及野生型唐古特大黄、药用大黄等6批样品中五种蒽醌类成分的总含量分别为2.33 ± 0.02,2.42 ± 0.03,2.88 ± 0.02,1.63 ± 0.04,3.51 ± 0.07,2.76 ± 0.06 %,结果表明,栽培唐古特大黄均已达到2010版中国药典规定的药用标准,但是较野生型唐古特大黄的总蒽醌含量要低,其与野生型药用大黄相当。结论:栽培唐古特大黄符合药典药用标准,但总蒽醌含量较野生型含量低。其结果可为临床应用栽培大黄提供参考。
[关键词]芦荟大黄素;大黄酸;大黄素;大黄酚;大黄素甲醚;栽培大黄
[作者单位]1.成都中医药大学药学院,四川 成都 611137;2.成都大学医学院(护理学院),四川 成都610106;3.阿坝州犇鸿天然中药材有限责任公司,四川 茂县 623200
大黄为多民族常用药[1],蒙古药音译为给喜古讷,维吾尔药音译为热万,藏药音译为君札,羌药音译为刷格或崇隔等。中国药典收载大黄为蓼科植物掌叶大黄(Rheum palmatum L.)、唐古特大黄(R.tanguticum Maxim.ex Balf.)、药用大黄(R.officinale Bailll.)的干燥根和根茎[2]。唐古特大黄主要分布在青海、西藏、四川、甘肃等地,药用大黄在四川分布较广;栽培大黄多为唐古特大黄。大黄主要含蒽醌类成分,包括大黄素、大黄酚、大黄酸、芦荟大黄素和大黄素甲醚及其苷类成分,其测定方法多采用HPLC测定酸水解后的这五种成分的含量来控制大黄的质量[2~6]。本实验以《中华人民共和国药典》(2010版第一部) 所载HPLC方法为参考,通过调整色谱条件建立HPLC分析方法[2~6],测定和比较了茂县、北川两地栽培唐古特三年生大黄及野生型药用大黄、唐古特大黄中五种蒽醌类成分的含量,其结果对人工栽培大黄质量控制具有较大意义,同时可为人工栽培大黄的临床合理应用提供参考数据。
1 仪器与试药
Agilent 1100 高效液相色谱仪(HPLC),包括4元泵系统、全自动脱气单元、VWD 检测器单元和Agilent 1100 色谱工作站等(Agilent Techologies,USA);CP225D 和BS 210S 电子天平(Sartorius,德国);KH-300DB 型数控超声仪(昆山禾创超声仪器有限公司);Chromasil C18色谱柱(5μm,250 × 4.6 mm)(成都为科学仪器有限公司,中国)。TGL-16C 台式高速离心机(上海市安亭科技仪器厂);WSD-II型超纯水系统(成都威思达智能科技有限公司)。
栽培大黄采集于茂县雅都乡(ZP1)和土门乡(ZP2),北川羌族自治县构枝乡(ZP3)和梓潼乡(ZP4),经鉴定均为唐古特大黄;野生型唐古特大黄(YS1)、药用大黄(YS2)均采集于茂县雅都乡。芦荟大黄素(批号L-014-140730,≥98%)、大黄酸(批号D-010-140728-2,≥98%)、大黄酚(批号D-017-150115,≥98%)、大黄素(批号D-029-140728-2,≥98%)、大黄素甲醚(批号D-004-140728-1,≥98%)均购自成都瑞芬思生物科技有限公司。乙腈、甲酸为色谱纯,水为超纯水,其余试剂均为分析纯。
2 方法与结果
2.1色谱条件
色谱柱,Chromasil C18色谱柱(5μm,250 × 4.6 mm);流动相,甲醇-0.1%磷酸溶液(每1000mL含1mL磷酸)为85:15(V/V);检测波长,254 nm;流速,1.0 mL/min,柱温:30℃;进样量10 μl。
2.2对照品储备溶液的制备
精密称取芦荟大黄素对照品(16.28 mg)、大黄酸对照品(15.79 mg)、大黄素对照品(15.84 mg)、大黄酚对照品(16.50 mg)和大黄素甲醚对照品(7.89 mg)适量,分别置于50 mL的棕色容量瓶中,分别加甲醇制成每1mL含芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚分别为325.7、315.7、316.8、330.1、157.8 μg的对照品储备液。分别精密量取上述对照品溶液各2 mL,置于10 mL棕色容量瓶中,混匀定容至刻度,即得每1mL中含芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚分别为65.1、63.1、63.4、66.0、31.6 μg的混合对照品储备溶液。
2.3供试品溶液的制备
分别精密称取6批不同批号(ZP1-4,YS1-2)的粉碎过四号筛大黄粉末样品(n=3)约 0.15 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,加热回流1小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过。精密量取续滤液5 mL,置烧瓶中,挥去溶剂,加8%盐酸溶液10 mL,超声处理2分钟,再加三氯甲烷10 mL,加热回流1小时,放冷,置分液漏斗中,用少量三氯甲烷洗涤容器,并入分液漏斗中,分取三氯甲烷层,酸液再用三氯甲烷提取3次,每次10 mL,合并三氯甲烷液,减压回收溶剂至干,残渣加甲醇使溶解,转移至10 mL量瓶中,加甲醇至刻度,摇匀,过0.45 μm滤头过滤,即得。
2.4线性关系考察
将混合对照品储备溶液作为线性关系考察1号对照品溶液(S1);另采用倍数稀释法,精密量取S1对照品溶液5 mL,置 10 mL 棕色量瓶中,加入甲醇约 4 mL,超声处理 5 min,混匀,冷却后,用甲醇定容至刻度,得2号对照品溶液(S2);精密量取S2对照品溶液5 mL,置 10 mL 棕色量瓶中,加入甲醇约4 mL,超声处理 5 min,混匀,冷却后,用甲醇定容至刻度,得3号对照品溶液(S3);按上法,依次获得 S4~S5。S1~S5对照品溶液分别过 0.45 μm 微孔滤膜后,按上述色谱条件进样测定,记录色谱峰。以色谱峰面积为纵坐标,质量浓度为横坐标进行线性回归,结果表明芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚分别在4.1~65.1、3.9~63.1、4.0~63.4、4.1~66.0、2.0~31.6 μg/mL 浓度范围内与峰面积积分值线性关系良好(R2≥0.999 6)。
2.5系统适应性考察
选择3号对照品溶液(S3),大黄供试品溶液(样品ZP1),按上述色谱条件进样分析,记录其色谱图(图1)。芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚峰形尖锐对称,保留时间分别约为5.8、6.1、11.3、15.2、21.8 min,与其他色谱峰的分离度大于1.5,理论塔板数均大于5000,拖尾因子符合分析要求,供试品溶液中其它物质不干扰此五种成分的测定。
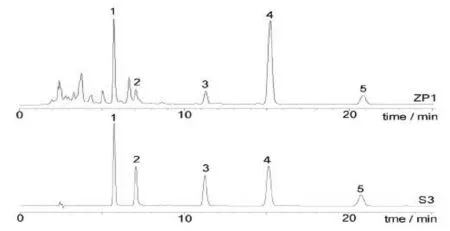
图1 大黄供试品溶液(ZP1)和对照品溶液(S3)的HPLC色谱图
2.6精密度试验
选择对照品溶液(S3),按上述色谱条件进样测定,分别连续进样 5 次,记录色谱图,记录芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚峰面积数据,其峰面积的RSD均小于2.36 %,表明精密度良好。
2.7稳定性试验
取样品(ZP1)溶液,在室温(21 ℃)条件下分别于 0,4,8,16,24 h 按上述色谱条件进样测定,记录芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚峰面积数据,其峰面积的RSD均小于3.24%,表明供试品溶液在24 h内的稳定性较好。
2.8重现性试验
取样品(ZP1),按供试品溶液制备方法,平行制备供试品溶液5份,按上述色谱条件进样测定,记录色谱图,记录芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的峰面积,计算得芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚含量分别为0.54 ± 0.01、0.37 ± 0.00、0.24 ± 0.00、、0.93 ± 0.01、0.25 ± 0.00%,其五种成分含量的RSD均小于2.56%,表明方法的重现性良好。
2.9加样回收率试验
取重现性用试验样品(ZP1)共5份,每份精密称取0.10 g,按照“2.3 供试品溶液的制备”项下制备样品,于“残渣加甲醇使溶解”后,分别精密加入混合对照品贮备液S1(1 mL),转移至10 mL量瓶中,加甲醇至刻度,摇匀,过0.45 μm滤头过滤,即得供加样回收率试验测定样品,按照按上述色谱条件进样测定,计算芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚含量。加样回收率按如下公式计算,即(测得含量-已知样品中的含量)/加入对照品量×100%,结果显示,此五种成分的平均加样回收率为96.47~102.38 %,RSD均<2.56 %。表明方法加样回收率符合要求。
2.10样品含量测定
采用所建立的HPLC方法分别测定6批大黄样品中芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量,结果见表1。

表1 大黄样品中芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量测定结果(n=3)
结果表明,茂县、北川两地的栽培三年的唐古特大黄均已达到中国药典2010版规定的药用标准,但是较野生型唐古特大黄的总蒽醌含量要低,但与野生型药用大黄相当。值得注意的是ZP4样品中五种蒽醌类成分的总含量相对较低,仅仅略高于药典标准的1.50%,分析可能是由于采集的新鲜样品有明显腐败发生导致的。
3 讨论
试验参照药典和相关文献方法[1~6],以大黄样品水解后的总蒽醌苷元即芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚为指标,探讨分析了四川茂县、北川两地栽培型唐古特大黄与野生型大黄的含量差异。本文所建立的HPLC同时测定大黄中的芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚含量的分析方法,可用于开展栽培大黄不同生长年限、不同产地间的品质评价分析研究,有利于大黄人工栽培技术的发展及栽培大黄的临床应用。其结果可为进一步开展多产地、多样品中此五种成分的比例关系研究,开展大黄的药效学、临床疗效评价等研究提供依据。
备注:感谢北川羌族自治县中羌医医院提供大黄样品。
[参考文献]
[1]贾敏如,李星炜.中国民族药志要[M].北京:中国医药科技出版社,2005,513-514.
[2]国家药典委员会.中华人民共和国药典2010版一部[S].北京:中国医药科技出版社,2010,(1):22-23.
[3]李元辉.HPLC法测定不同产地大黄中四种蒽醌类化合物含量[J].中药研究与信息,2005,06:17-18.
[4]林瑞民,李磊,陈华山,等.不同品种不同产地大黄中五种蒽醌类化合物的HPLC测定[J].中药材,2005,03:197-198.
[5]毛春芳,施忠,罗琳,等.HPLC法同时测定大黄中芦荟大黄素等11种成分的量[J].中草药,2014,16:2400-2403.
[6]邹亮,周浓,谢静,等.栽培药用大黄不同部位中5种蒽醌类衍生物的含量分析[J].广东农业科学,2012,18:118-122.
(责任编辑:何瑶)
Comparative research of the contents of five anthraquinones from Dahuang of cultivated and wild varieties in Sichuan
LI Qi-juan1, HU Hui-ling1, WANG Zhan-guo2,WANG You3
(1.School of Pharmacy, Chengdu University of Traditional Chinese Medicine, Chengdu 611137, Sichuan; 2.Chengdu University School of Medicine , Chengdu 610106, Sichuan;3.Aba Prefecture Benhong Nature herbal medicine Co.Ltd., Maoxian 623200, Sichuan)
[Abstract]Objective: To compare the differences of contents of five anthraquinones from cultivated and wild Dahuang in Sichuan.Method: C(18)Chromasil chromatography column (5μm, 250*4.6mm) was used in the determination.Mobile phase was methanol-0.1%phosphoric acid solution (85: 15) with flow rate of was 1.0mL.min(-1).Column temperature was 30℃, and detection wavelength was set at 254nm.Result: Aloe-emodin, rhein, eomdin, chrysophanol and physcion contents had a good linear relationship with peak area in the range of constituents of 4.1~65.1 μg.mL(-1), 3.9~63.1 μg.mL(-1), 4.0~63.4 μg.mL(-1), 4.1~66.0 μg.mL(-1), 2.0~31.6 μg.mL(-1)(R2≥0.9996).The average recovery was 96.47~102.38%, RSD<2.56 %.The total contents of five anthraquinones in six samples including triennial cultivated and wild varieties in Maoxian and Beichuan were 2.33 ± 0.02, 2.42 ± 0.03, 2.88 ± 0.02, 1.63 ± 0.04, 3.51 ± 0.07, 2.76 ± 0.06 % by the HPLC method.It turned out that cultivated R.tanguticum Maxim.ex Balf.had reached the standard in Pharmacopoeia of China (2010).The content of total anthraquinone was equal to wild R.Officinale Baill., but it was lower than wild R.tanguticum Maxim.ex Balf.Conclusion: R.tanguticum Maxim.ex Balf.of cultivated variety conforms to the standard in Pharmacopoeia of China, but the contents of total anthraquinone are lower than the wild variety.The result can provide reference for clinical application of Rhei Radix of cultivated variety.
[Key words]Aloe-emodin; rhein; eomdin; chrysophanol; physcion; cultivated Dahuang
[收稿日期]2015-11-20
[通讯作者]胡慧玲,女,副教授,主要从事中药制剂学研究Email:hhlmedicine@126.com
[作者简介]李奇娟,女,2012级中药基地班Email:18380445398@163.com
[基金项目]国家自然科学基金青年基金项目(81403178),四川省科技厅项目(2014SZ0131)
[中图分类号]R 282
[文献标识码]A
[文章编号]1674-926X(2016)01-002-04
