有机大分子对聚酰胺复合纳滤膜偏硅酸钠污染的影响
2016-04-16张晓婷杨若松王佳璇西安建筑科技大学环境与市政工程学院陕西西安710055
张晓婷,王 磊,杨若松,王佳璇 (西安建筑科技大学环境与市政工程学院,陕西 西安 710055)
有机大分子对聚酰胺复合纳滤膜偏硅酸钠污染的影响
张晓婷,王 磊*,杨若松,王佳璇 (西安建筑科技大学环境与市政工程学院,陕西 西安 710055)
摘要:选用腐殖酸(HA),海藻酸钠(SA),牛血清蛋白(BSA)和偏硅酸钠分别模拟水体中有机大分子和无机污染物对聚酰胺复合纳滤膜进行了膜污染试验.结合原子力显微镜(AFM)及自制的胶体探针定量测定了不同条件下,膜-偏硅酸钠以及偏硅酸钠-偏硅酸钠之间的作用力.分析了污染膜的表面结构特征及其通量恢复率,系统考察了膜表面吸附不同有机大分子后,对随后硅酸盐污染行为的影响.结果表明:膜表面吸附HA和SA后,膜面负电位增加,与偏硅酸钠之间静电斥力变大,导致其结合能力减弱,减缓了结垢污染.然而,吸附BSA后的膜与无有机条件膜相比,负电位基本一致,故对纳滤膜结垢过程几乎无影响.
关键词:聚酰胺复合纳滤膜;有机物大分子;偏硅酸钠;膜污染;黏附力
* 责任作者, 教授, wl0178@126.com
纳滤(nanofiltration, NF)是一种以压力为驱动力的新型膜分离过程,介于反渗透膜(RO)和超滤膜(UF)之间[1].其以操作压力低,多荷电性以及对多价离子和相对分子量在200以上的有机物有较高的去除率等优点被广泛应用于水处理领域中[2].然而,实际水体中含有大量无机盐、有机物、胶体等物质,它们会在膜面或膜孔不断累积造成膜污染,导致膜通量下降,膜分离过程运行成本及能量消耗增加[3-4].这一现象严重制约了纳滤在水处理技术中的广泛应用[5-7].
既往的膜污染研究表明,相对单一污染,共存污染表现出更显著的污染行为,有机污染物会影响无机污染物的形成过程,在压力驱动的膜分离过程中,有机物与无机物形成密实的网状结构会影响膜面污染程度[8-11].此外,诸多研究者发现,水体中同时存在有机与无机污染物时,有机物会优先吸附到膜面,改变膜表面原有特性,使得膜污染过程更加复杂[12-14].Liu等[15]用海藻酸钠和硫酸钙分别模拟水体中的有机及无机污染物对正渗透(FO)膜污染进行了研究,结果表明当海藻酸钠与硫酸钙共存时,膜通量下降速率比单一污染物污染更快,进一步研究发现当海藻酸钠污染层预先在膜面形成后,膜面硫酸钙污染程度更加严重.他们认为可能是有机物在膜表面的不断积累,改变了膜表面的化学性质而影响随后的污染行为.因此,研究有机污染后膜的污染行为对阐明膜污染机理及控制膜污染至关重要.然而,关于纳滤膜污染的此类研究甚少.
本研究采用聚酰胺复合纳滤膜,选用典型有机物牛血清蛋白(BSA),海藻酸钠(SA),腐殖酸(HA)模拟水体中有机污染物,使用偏硅酸钠模拟水体中广泛存在的硅酸盐无机污染物[16-18],进行了膜污染试验,结合扫描电镜(SEM)对膜面污染层进行分析,并使用原子力显微镜(AFM)结合胶体探针定量测定了Virgin(无有机污染参比)/ BSA/ SA/ HA膜-偏硅酸钠、偏硅酸钠-偏硅酸钠之间相互作用力,进一步研究说明不同有机污染物对纳滤膜硅酸盐污染行为的影响,此研究旨在为纳滤膜污染的防治提供更多的理论支持.
1 实验部分
1.1 实验材料
膜材料:聚砜(PSF,E6010,德国BASF);聚乙烯吡咯烷酮(PVP k30,分析纯,上海蓝季科技发展有限公司);N,N-二甲基乙酰胺(DMAc,分析纯,天津市福晨化学试剂厂);聚乙二醇(PEG600,分析纯,天津市科密欧化学试剂有限公司);聚乙二醇辛基苯(TritonX-100,分析纯,国药化学试剂有限公司);丙烯酸(AA,分析纯,天津市福晨化学试剂厂);无水哌嗪(PIP,分析纯,国药化学试剂有限公司);均苯三甲酰氯(TMC,98%, Sigma-Aldrich); 三乙胺(TEA,分析纯,国药化学试剂有限公司).
污染物材料:腐殖酸(HA, Sigma-Aldrich, St. Louis, Mo);海藻酸钠(SA, Sigma-Aldrich, St. Louis, Mo);牛血清蛋白(BSA, Sigma-Aldrich, St. Louis, Mo);偏硅酸钠五水合物(Na2O3Si·5H2O,国药化学试剂有限公司).SA和BSA标准储备液(2g/L)是将固体溶解在去离子水中并在室温下连续搅拌24h. HA标准储备液是将2g HA固体溶于200ml NaOH (0.1mol/L)溶液中,充分溶解后稀释至1L. SA和HA储备液用0.45 μm微滤膜(密理博,比勒利卡,MA)过滤去除悬浮颗粒及未溶解的有机物.最后将BSA、SA、HA储备液转移至无菌玻璃瓶中并在4 ℃的冰箱中储存.制备定量的Na2O3Si·5H2O (0.032mol/L), NaCl (0.7mol/L) 和MgCl2(0.1mol/L)标准储备液用于污染试验.储备液放置于室温以备使用.在每一个污染试验之前,将储备液稀释至所需浓度,分别作为基线、有机条件、无机结垢污染试验的原液,使用前将储备液摇匀并超声15min以获得均质溶液.使用1mol/L的盐酸以及NaOH溶液将所有污染物溶液的pH值调节至7.5±0.1.原液的化学组成列于表1.

表1 原液的化学组分Table 1 Chemical composition of the feed solutions
1.2 聚酰胺复合纳滤膜制备
通过溶液相转化法制备聚砜超滤膜.首先将PSF、PVP k30、PEG600、Triton X-100、AA按一定比例同时加入溶剂DMAc中,并在70 ℃条件下机械搅拌16h得到匀质铸膜液,铸膜液于70℃恒温静置脱泡后将其均匀涂覆在装有无纺布的玻璃板上刮制成一定厚度的溶液膜,随后立即浸入恒温水浴中分相,得到聚砜超滤膜.
通过界面聚合法制备聚酰胺复合纳滤膜.在室温下,将PIP及TEA按一定比例配制成水溶液,将一定量的TMC溶解于正己烷配制成有机溶液.首先将已制备好的聚砜超滤膜在PIP水溶液中浸泡一定时间,取出晾干,随后在TMC有机溶液中浸泡一定时间,取出晾干后经过80℃热处理即得到聚酰胺复合纳滤膜,反复漂洗后存放于水中备用.在20±1℃、0.6MPa、错流速度为4.5cm/s的条件下,其纯水渗透通量为(40±5)L/(m2·h);接触角为(55±2)°,平均粗糙度Ra为10.6nm,截留分子量为(400±50) Da.
1.3 膜污染试验
采用小型错流平板纳滤试验装置进行纳滤膜污染试验[19],如图1所示.过滤试验条件均为:温度20±1℃,压力0.6MPa,错流速度4.5cm/s.

图1 小型错流平板纳滤测试装置示意Fig.1 Schematic diagram of cross flow flat nanofiltration test device
膜的渗透通量J计算公式如下:

式中:J为渗透通量,L/(m2·h);V为溶液渗透量,L;S为膜的有效面积,m2;t为过滤时间,h.试验分两类,第一类是无机结垢试验结束后直接将膜取出晾干,取小块样品用于原子力显微镜(AFM)测定污染膜表面形貌,其余用扫描电镜(SEM)观测污染膜表面的污染层结构.第二类是无机结垢试验结束后,用去离子水立即清洗膜面后测定膜通量,目的是研究膜通量的恢复状况.
试验具体步骤如下:(1)将一张干净的自制纳滤膜安装于试验装置中,首先使用去离子水预压纳滤膜直至膜通量达到一稳定值.(2)随后换用基线溶液作为原液过滤1h,待通量稳定后记录初始膜通量J0,J0取值范围为(30±5)L/(m2·h).(3)换用新制备的有机污染液作为原液进行有机污染试验24h,为了保持原水中化学组成恒定,滤液回流至原液槽,并用电子天平实时监测污染过程膜通量J1.(4)换用偏硅酸钠结垢溶液作为原液进行无机结垢污染试验48h,滤液不回流,并用电子天平实时监测污染过程膜通量.(5)结垢污染试验后进行膜通量恢复率测试试验,即用去离子水在错流速度10cm/s条件下清洗膜40min;再用基线溶液过滤1h,待通量稳定后记录膜通量J.
1.4 胶体探针制备及黏附力的测定
1.4.1 SiO2胶体探针的制备 试验中使用SiO2模拟偏硅酸钠制备无机污染物探针.通过物理黏附法,在光学显微镜(奥林巴斯,TH4-200,日本)视野中实时监测制备过程.具体制备方法如下:首先按一定比例配置双组分环氧树脂胶(Epo Tek公司),其次将AFM SiN无针尖探针(NP-010,德国布鲁克)及特定比例的双组分环氧树脂分别放置于微操作器和显微镜视野中,通过微操作器控制无针尖探针微悬臂的三维移动,在微悬臂自由端黏附适量环氧树脂,随后将云母片表面的SiO2胶体颗粒(Polysciences)引入到显微镜视野中,再次通过微操作器调节无针尖探针微悬臂的三维移动,依靠微悬臂自由端环氧树脂的毛细管力黏附一直径为5µm的SiO2胶体颗粒,最后将黏附有SiO2颗粒的胶体探针从微操作器中取下,在紫外灯照射下修复20min,静置固化一周以上待用[20]. 图2为SiO2胶体探针的扫描电镜(SEM)图.

图2 SiO2胶体探针扫描电镜图Fig.2 SEM image of SiO2colloidal probe
1.4.2 黏附力的测定 使用Multimode 8.0原子力显微镜(AFM)结合SiO2胶体探针测定膜-偏硅酸钠,偏硅酸钠-偏硅酸钠之间黏附力.制备与各个阶段膜污染试验相对应的污染膜样品,置于相应的污染液中以保持膜面污染层的稳定性和完整性,待用.测定步骤:将污染膜置于液体池底部,然后将液体池及SiO2胶体探针安装于AFM上,设定参数后在液态“接触”模式下进行黏附力测定.为了减少试验误差,在每个样品上选取至少6个不同的局域点进行力测定,每个点进行10次重复测定.为了保证测量的准确性,每次测试前后皆在显微镜下进行胶体探针的完整性检测[21].
1.5 分析方法
采用小型错流平板纳滤试验装置进行膜污染试验.用接触角仪(SL200B,科诺,美国)测定膜表面的接触角.用Zeta电位仪(ZS90Zeta,马尔文,英国)测定不同污染物的Zeta电位,使用纳米粒度和Zeta电位仪(DelsaNano C, Beckman,美国)分析Virgin膜表面Zeta电位.用原子力显微镜(AFM, Multimode 8.0,德国布鲁克)扫描污染膜的微观形貌,并测量其表面粗糙度.用扫描电镜(SEM, JSM-6510LV,日本JEOL)观测污染膜表面的污染层结构.
2 结果与讨论
2.1 不同有机条件对膜通量的影响
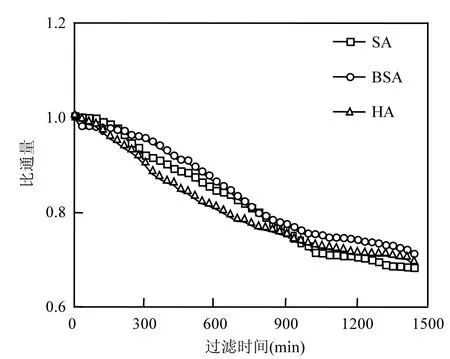
图3 不同有机条件下膜通量衰减曲线Fig.3 Membrane flux decline curves under different organic conditions
图3为3种有机条件下膜通量衰减曲线.将3种有机条件污染过程中膜通量按有机条件污染试验初始膜通量标准化(即J1/J0).由图3可以看出,3种有机条件下膜通量衰减趋势一致.这是由于有机污染物污染纳滤膜的主要影响因素有污染物浓度、离子强度、Ca2+浓度、溶液pH值及试验操作条件等[22].然而,本研究中有机污染物浓度、离子强度、试验操作条件均相同,溶液pH值均为7.5,且溶液中无Ca2+存在,故有机污染物在膜表面的污染行为相似,因此对膜通量的影响程度基本一致.
2.2 不同有机条件对膜硅酸盐结垢形成过程的影响
图4为不同条件下膜偏硅酸钠结垢污染过程膜通量衰减曲线.这一阶段对比了Virgin膜偏硅酸钠结垢污染试验的结果,并将4种条件膜结垢污染过程中膜通量按各自偏硅酸钠结垢污染试验初始膜通量标准化.

图4 不同条件下膜偏硅酸钠结垢过程膜通量衰减曲线Fig.4 Membrane flux decline curves in metasilicate scaling process under different conditions
由图4可见,在结垢污染试验的前12h里, BSA膜、SA膜、HA膜以及Virgin膜通量衰减率分别为23%、11%、14%及26%.而在12~48h的运行阶段,上述4种条件膜通量衰减率分别为17%、15%、12%及16%.显然,在任一条件膜的偏硅酸钠结垢污染试验过程中,膜通量皆是在污染初期衰减相对较快,随着污染试验的进行,膜通量衰减速率逐渐减缓.这是由于在膜结垢污染初期,膜面大量聚集硅酸盐,快速形成结垢层,使得膜通量下降较快,而随着污染试验的进行,膜面结垢层逐渐趋于稳定,形成结构稳定的结垢层,故膜通量衰减逐渐趋缓[23-25].
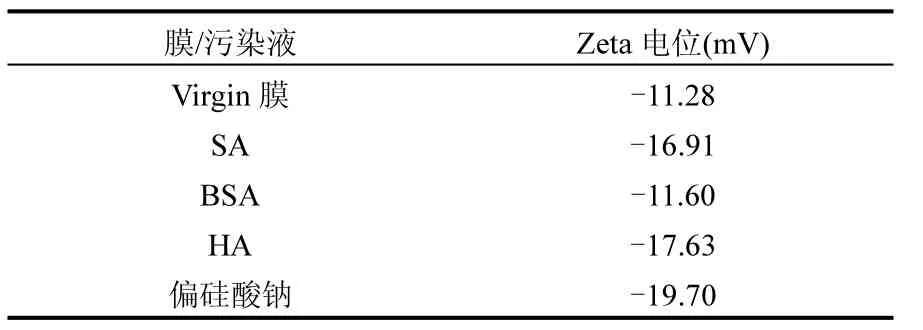
表2 膜和不同污染物Zeta电位Table 2 Zeta potentials of membrane and different foulants
(2) 不同条件膜偏硅酸钠结垢污染过程的膜通量衰减规律有明显差异.BSA膜与Virgin膜的偏硅酸钠结垢污染程度接近且衰减趋势基本一致.而SA膜和HA膜结垢过程中的膜通量衰减曲线基本重合,通量衰减约为26%,较Virgin膜以及BSA膜,SA和HA条件膜结垢污染程度较缓.这可能与不同条件膜表面所带负电荷量有关,有机条件后膜表面形成一层有机污染层,其所带电荷量会影响膜面偏硅酸钠结垢程度.为了进一步分析此过程的污染机理,我们分别测定了Virgin膜以及各类污染物的Zeta电位值,结果如表2所示.
由表2可以看出,污染物均带负电.SA与HA所带电荷量较大,分别为-16.91,-17.63mV.而BSA 与Virgin膜所带电荷量较小,分别为-11.60, -11.28mV. SA与HA所带负电荷量较大,为SA和HA条件膜结垢污染程度较缓提供了有力依据.
2.3 污染膜表面结构的研究

图5 不同条件下膜偏硅酸钠污染后的扫描电镜图: Virgin膜(a), BSA膜(b), SA膜(c), HA膜(d)Fig.5 SEM images of membrane after metasilicate scaling under different conditions: Virgin(a), BSA(b), SA(c), and HA(d)
无机结垢污染试验结束后取出试验膜,分别用扫描电镜和原子力显微镜测定污染膜表面结垢层形态及表面形貌,结果分别如图5和图6.图5是用扫描电镜观察的污染膜表面的污染层结构,Virgin膜及BSA膜表面结垢物块大而密实,而SA膜和HA膜表面污染层形态相近,结垢物小且较为松散. 图6是原子力显微镜下2µm×2µm范围内不同条件膜的微观表面形貌.各条件膜的表面粗糙度分别为:Virgin膜2.86nm; BSA膜3.16nm; SA膜5.34nm; HA膜5.92nm. Virgin膜和BSA膜表面粗糙度小,SA膜和HA膜表面粗糙度较大.由此可见,污染膜的表面粗糙度与污染层的疏散程度有着密切的关系:污染层越疏松,其表面粗糙度越大;反之,污染层越致密,其表面粗糙度越小.

图6 不同条件下膜偏硅酸钠污染后的表面形貌图: Virgin膜(a1), BSA膜(b1), SA膜(c1), HA膜(d1)Fig.6 Images of membrane surface morphology after metasilicate scaling under different conditions: Virgin(a1), BSA(b1), SA(c1), and HA(d1)
2.4 黏附力分析
为了进一步分析结垢污染试验结果,本研究定量测定了膜-偏硅酸钠、偏硅酸钠-偏硅酸钠之间黏附力. Costa等[26]的研究表明,在测试过程中,探针先与样品表面接触,随后在二者分离过程中测定黏附力,故所测黏附力为负值.探针与样品表面之间的黏附力计算公式如下:

式中:F是分子间的黏附力,N;R是微颗粒半径, m;W(∞)是将一无限接近于平面的微颗粒移走时每单位面积需要的能量,J/m2.在这里,黏附力可以理解为阻止污染物到达膜表面所需要的能量.显然,AFM胶体探针所测定的黏附力与胶体颗粒的半径成正比关系,所以为了避免不同胶体探针的尺寸差异所致的黏附力大小差异,本研究将所测定的黏附力除以胶体颗粒探针的半径(F/R).相应的典型黏附力曲线及概率分布见图7.
由图7(a)可以看出:Virgin膜及BSA膜与偏硅酸钠之间的平均黏附力大小相接近,分别为0.899,0.831mN/m.而SA膜及HA膜与偏硅酸钠之间的平均黏附力大小相接近,分别为0.328, 0.287mN/m.且Virgin膜及BSA膜与偏硅酸钠之间的平均黏附力明显大于SA膜及HA膜与偏硅酸钠之间的平均黏附力.这主要是因为污染物以及Virgin膜皆带负电,故膜-偏硅酸钠之间的静电斥力与膜表面所带静电荷量呈正相关关系.而经过有机污染物污染过的膜表面会形成一层有机层,此时膜表面的带电特性将由这层有机层决定,故BSA膜、SA膜以及HA膜的表面电性分别由BSA、SA以及HA所控制.结合表2可得,BSA所带静电荷量与Virgin膜差异不大,SA所带静电荷量接近HA,且BSA及Virgin膜所带静电荷量明显小于SA和HA.所以SA膜及HA膜与偏硅酸钠之间的静电斥力明显大于BSA及Virgin膜与偏硅酸钠之间的静电斥力,而静电斥力会削弱膜与偏硅酸钠之间的黏附力.结合图4中的偏硅酸钠结垢污染试验膜通量衰减曲线可以发现不同条件膜与偏硅酸钠之间的黏附力与其在此阶段运行初期的膜通量衰减速率成正相关关系,即膜与偏硅酸钠之间的黏附力越大,膜运行初期的通量衰减速率越快;反之,膜通量衰减速率较缓慢.这是由于膜与偏硅酸钠之间黏附力越大,膜面与偏硅酸钠结合越快,膜污染程度越严重.反之,膜污染程度越轻.所以降低膜与污染物之间的黏附力对控制膜污染至关重要[27].
结合图7(b)和图4能够发现,4种不同条件膜偏硅酸钠污染物之间的黏附力变化趋势与对应的污染膜运行后期的稳定通量趋势一致.偏硅酸钠污染物分子之间的黏附力越大,污染物分子结合越紧密,污染层越密实,膜污染越严重,污染膜的稳定通量越小.相反,污染物分子之间的黏附力越小,污染层越松散,膜污染程度越轻,运行后期的稳定通量越大.

图7 不同条件下膜与偏硅酸钠(a)及偏硅酸钠与偏硅酸钠(b)之间黏附力曲线及相应作用力概率分布Fig.7 Representative normalized adhesive force distance curves of the membrane–metasilicate type (a), the metasilicatemetasilicate type (b) and the frequency distribution of the corresponding forces under different conditions
2.5 膜清洗结果分析
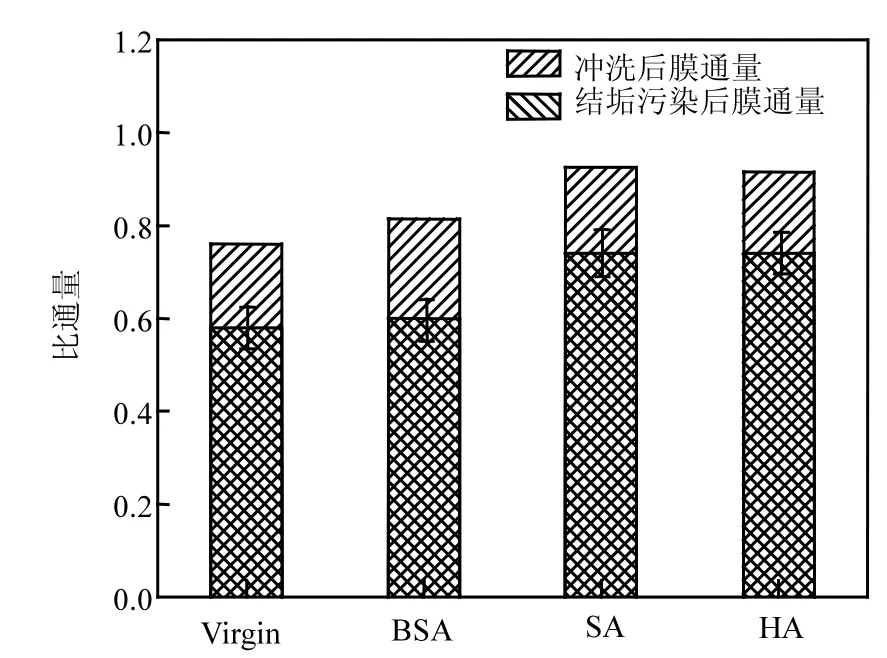
图8 不同条件下膜污染及其清洗后膜通量对比Fig.8 Comparison chart of membrane fluxes after scaling and cleaning under different conditions
偏硅酸钠结垢污染试验结束后,立即用去离子水在错流速度10cm/s条件下清洗污染膜40min.污染及清洗后膜通量均按结垢污染试验开始前膜通量进行标准化处理.由图8可以看出:Virgin膜通量恢复率为76%, BSA膜的通量恢复率为81%.而HA膜和SA膜通量恢复率均高达90%.结合图7(b)分析结果,发现,污染物之间黏附力越小,膜通量越容易恢复.这是由于不同条件膜面的偏硅酸钠污染物分子之间的黏附力越小,污染物分子间的结合能力越弱,结垢层越疏松,在清洗过程中,清洗水更易进入垢层内部破坏其结构,从而使得清洗更加彻底,膜通量恢复效果好.反之,其黏附力越大,分子结合能力越强,结垢层越密实,导致清洗困难,膜通量恢复率低.
3 结论
3.1 纳滤膜表面吸附不同有机污染物能够影响其偏硅酸钠结垢的形成.尤其是当膜表面吸附HA和SA后,有机污染后的膜面较无有机条件膜电负性增强,与偏硅酸钠之间静电斥力增大,减缓了膜面偏硅酸钠结垢层的形成,从而减缓膜结垢污染程度,且清洗后膜通量恢复率高.然而,BSA吸附至膜表面后,对膜表面性质影响不大,膜结垢污染程度和无有机条件膜基本无差异.因此,可以通过膜面吸附负电荷性较强的有机物,改变纳滤膜表面性质,从而改变膜的无机污染程度.
3.2 膜与偏硅酸钠之间的黏附力越大,膜污染运行初期的通量衰减速率越快;偏硅酸钠污染物分子之间的黏附力越大,污染物分子结合越紧密,结垢层越密实,导致膜稳定通量越低且清洗越困难,膜通量恢复率较低.
参考文献:
[1] 纪树兰,朱安娜,龙 峰,等.平板型纳滤膜处理洁霉素废水的膜性能比较 [J]. 中国环境科学, 2002,22(1):36-39.
[2] Jin L, Shi W, Yu S, et al. Composite nanofiltration membranes synthesized from PAMAM and TMC by interfacial polymerization [J]. Journal of Harbin Institute of Technology, 2012,19(1):116-120.
[3] 彭 茜,冉德钦,王 平,等.不同pH值下腐殖酸反渗透膜污染中的界面相互作用解析 [J]. 中国环境科学, 2011,31(4):616-621.
[4] 黄 健,舒增年,张四海.亲水荷电超滤膜的制备及对腐殖酸的分离性能 [J]. 中国环境科学, 2014,11(11):2831-2837.
[5] Mattaraj S, Jiraratananon R, Jarusutthirak C. Influence of inorganic scalants and natural organic matter on nanofiltration membrane fouling [J]. J. Membrane Science, 2007,287(1):138-145.
[6] Mo Y, Xiao K, Liang P, et al. Effect of nanofiltration membrane surface fouling on organic micro-pollutants rejection: The roles of aqueous transport and solid transport [J]. Desalination, 2015, 367:103–111.
[7] Verliefde A R D, Cornelissen E R, Heijman S G J, et al. Influence of membrane fouling by (pretreated) surface water on rejection of pharmaceutically active compounds (PhACs) by nanofiltration membranes [J]. Journal of Membrane Science, 2009,330:90–103.
[8] Lee S, Elimelech M. Relating organic fouling of reverse osmosis membranes to intermolecular adhesion forces [J]. Environmental Science & Technology, 2006,40(3):980-987.
[9] Li Q, Elimelech M. Organic fouling and chemical cleaning of nanofiltration membranes: measurements and mechanisms [J]. Environmental Science & Technology, 2004,38(17):4683-4693.
[10] Lee S, Elimelech M. Salt cleaning of organic-fouled reverse osmosis membranes [J]. Water Research, 2007,41(5):1134-1142.
[11] Hatziantoniou D, Howell J A. Influence of the properties and characteristics of sugar-beet pulp extract on its fouling and rejection behaviour during membrane filtration [J]. Desalination, 2002,148(1):67-72.
[12] Mansouri J, Harrisson S, Chen V. Strategies for controlling biofouling in membrane filtration systems: challenges and opportunities [J]. J. Materials Chemistry, 2010,20(22):4567-4586.
[13] Crozes G, Anselme C, Mallevialle J. Effect of adsorption of organic matter on fouling of ultrafiltration membranes [J]. Journal of Membrane Science, 1993,84(1):61-77.
[14] Jermann D, Pronk W, Boller M. Mutual influences between natural organic matter and inorganic particles and their combined effect on ultrafiltration membrane fouling [J]. Environmental Science & Technology, 2008,42(24):9129-9136.
[15] Liu Y, Mi B. Combined fouling of forward osmosis membranes: synergistic foulant interaction and direct observation of fouling layer formation [J]. J. Membrane Science, 2012,407:136-144.
[16] Den W, Wang C J. Removal of silica from brackish water by electrocoagulation pretreatment to prevent fouling of reverse osmosis membranes [J]. Separation and Purification Technology, 2008,59(3):318-325.
[17] Koo T, Lee Y J, Sheikholeslami R. Silica fouling and cleaning of reverse osmosis membranes [J]. Desalination, 2001,139(1):43-56.
[18] Ning R Y. Discussion of silica speciation, fouling, control and maximum reduction [J]. Desalination, 2003,151(1):67-73.
[19] 王 磊,刘婷婷,米 娜,等.PDA/PIP二胺混合聚酰胺复合纳滤膜制备及性能表征 [J]. 西安建筑科技大学学报:自然科学版, 2015,47(1):108-114.
[20] Mi B, Elimelech M. Silica scaling and scaling reversibility in forward osmosis [J]. Desalination, 2013,312:75-81.
[21] 苗 瑞,王 磊,田 丽,等.海藻酸及腐殖酸共存对PVDF超滤膜的污染行为 [J]. 中国环境科学, 2014,34(10):2568-2574.
[22] Ang W S, Elimelech M. Protein (BSA) fouling of reverse osmosis membranes: Implications for wastewater reclamation [J]. Journal of Membrane Science, 2007,296(1/2):83–92.
[23] Hashino M, Hirami K, Katagiri T, et al. Effects of three natural organic matter types on cellulose acetate butyrate microfiltration membrane fouling [J]. J. Membrane Science, 2011,379(1):233-238.
[24] Wang L, Miao R, Wang X, et al. Fouling behavior of typical organic foulants in polyvinylidene fluoride ultrafiltration membranes: characterization from microforces [J]. Environmental Science & Technology, 2013,47(8):3708-3714.
[25] Huisman I H, Prádanos P, Hernández A. The effect of protein–protein and protein–membrane interactions on membrane fouling in ultrafiltration [J]. J. Membrane Science, 2000, 179(1):79-90.
[26] Costa A R, de Pinho M N, Elimelech M. Mechanisms of colloidal natural organic matter fouling in ultrafiltration [J]. J. Membrane Science, 2006,281(1):716-725.
[27] Kang S, Asatekin A, Mayes A M, et al. Protein antifouling mechanisms of PAN UF membranes incorporating PAN-g-PEO additive [J]. J. Membrane Science, 2007,296(1):42-50.
Effects of organic macromolecular on sodium metasilicate fouling behavior of polyamide composite nanofiltration membrane.
ZHANG Xiao-ting, WANG Lei*, YANG Ruo-song, WANG Jia-xuan (College of Environmental and Municipal Engineering, Xi’an University of Architecture and Technology, Xi’an 710055, China). China Environmental Science, 2016,36(2):460~467
Abstract:The polyamide composite nanofiltration membrane fouling experiments were carried out by using humic acid (HA), sodium alginate (SA), bovine serum albumin (BSA) as model organic macromoleculars, sodium metasilicate as model inorganic foulant in natural water. The adhesion forces of membrane-sodium metasilicate and sodium metasilicate-sodium metasilicate under different conditions were tested by atomic force microscopy (AFM) in conjunction with self-made colloidal probe. The surface structural characteristics of the fouled membranes and flux recovery rates of the corresponding fouled membranes were analyzed. Besides, the effects of different membrane surface conditions on silicate scaling behavior were investigated. The results showed that the negative potential of the membrane surface increased after adsorption of HA or SA on membrane surface. Hence, the electrostatic repulsion between the membrane and sodium metasilicate increased. Therefore, the binding capacity between fouled membrane and sodium metasilicate was weakened and the scaling behavior was mitigated. However, compared with the membrane without organic conditioning, adsorption of BSA on the membrane surface had little influence on silicate scaling of nanofiltration membrane owing to the similar negative potentials of the two kinds of membranes.
Key words:polyamide composite nanofiltration membrane;organic macromolecular;sodium metasilicate;membrane fouling;adhesion force
作者简介:张晓婷(1990-),女,陕西西安人,西安建筑科大学硕士研究生,主要从事从微观角度解析纳滤膜的污染机制的研究.
基金项目:国家自然科学基金(51178378,51278408);陕西省科技创新项目(2012KTCL03-06,2013KTCL03-16)
收稿日期:2015-07-10
中图分类号:X703.1
文献标识码:A
文章编号:1000-6923(2016)02-0460-08
