黄芪总黄酮对小鼠的急性毒性和致突变性研究
2016-04-07延边大学农学院动物医学系吉林延吉133002
(延边大学农学院动物医学系,吉林延吉 133002)
黄芪总黄酮对小鼠的急性毒性和致突变性研究
(延边大学农学院动物医学系,吉林延吉 133002)
摘要:用小鼠最大耐受量法、小鼠骨髓嗜多染红细胞微核试验和小鼠精子畸形试验等方法,研究黄芪总黄酮对小鼠的急性毒性和致突变性作用。结果显示,黄芪总黄酮的小鼠急性经口最大耐受剂量(MTD)大于15 g/kg,小鼠骨髓嗜多染红细胞微核试验和小鼠精子畸形试验结果均为阴性。结果表明,黄芪总黄酮属无毒物,对小鼠体细胞、雄性生殖细胞均无致突变性。
关键词:黄芪总黄酮;小鼠;急性毒性;致突变性
黄芪Astragalus为豆科多年生草本植物,药用历史悠久,古有“补药之长”之称[1]。黄芪性温、味甘,归脾、肺经,临床应用多为蒙古黄芪干燥根,有补中益气、温养脾胃之功效[2]。黄芪具有分布广泛、易人工种植、炮制方法简单、药用价值高等优点[3]。黄芪的主要成分包括黄芪总黄酮、黄芪多糖、黄芪皂苷、生物碱及多种微量元素等[4]。黄芪总黄酮(total flavonoids ofAstragalus, TFA)作为黄芪的主要活性成分之一,能显著增强小鼠的免疫功能[5],具有体外抗炎[6]、体内抗炎[7]等活性。国内外对黄芪总黄酮药理作用的报道很多,但是对其急性毒性、致突变性均无报道。本研究采用小鼠急性经口毒性试验、小鼠骨髓嗜多染红细胞微核试验和小鼠精子畸形试验等方法,研究黄芪总黄酮对小鼠的急性毒性和致突变性,以期为黄芪总黄酮的毒性相关机制提供理论依据。
1材料与方法
1.1材料
1.1.1试验药品黄芪总黄酮,购自南京泽朗医药科技有限公司;环磷酰胺(CP),购自江苏恒瑞医药股份有限公司;羧甲基纤维素钠(CMC),购自天津科密欧化学试剂有限公司;瑞特-姬姆萨染色液(Wright-Giemsa stain),购自珠海贝索生物技术有限公司。
1.1.2实验动物昆明种雌雄小鼠,购自延边大学实验动物中心。饲养于独立通风笼盒,自由采食,维持12 h光照/黑暗的节律,正式试验前均适应喂养3 d。
1.2方法
1.2.1小鼠急性经口毒性试验采用最大耐受量法进行试验[8]。昆明种小鼠18 g~22 g,20只,雌雄各半。TFA配制成浓度为0.25 g/mL混悬液。小鼠禁食不禁水16 h,称重,间隔4 h分别以0.3 mL/10 g进行灌胃,总剂量为15 g/kg。立即观察并连续定时观察14 d,记录小鼠中毒症状、死亡情况及出现时间。
1.2.2小鼠骨髓嗜多染红细胞微核试验采用30 h试验法[8]。昆明种小鼠25 g~30 g,25只,随机分成5组,分别为CMC阴性对照组,环磷酰胺40 mg/kg阳性对照组,TFA分10、5、2.5 g/kg 3个剂量组。小鼠称重,间隔24 h以0.225 mL/10 g灌胃2次,2次给药后6 h处死小鼠。取小鼠股骨骨髓制片,自然干燥,甲醇固定,Wright-Giemsa染色。油镜观察,每只小鼠200个嗜多染红细胞(polychromatic erythrocytes,PCE),计数相同区域内的成熟红细胞(mature erythrocytes,NCE),计算PCE/(PCE+NCE)比值;每只小鼠1 000个PCE,记录出现微核的PCE数,计算PCE微核率=含微核PCE数/检查PCE数×100%。
1.2.3小鼠精子畸形试验参照文献[8],昆明种雄性小鼠18 g~22 g,25只,随机分成5组,分别为CMC阴性对照组,环磷酰胺40 mg/kg阳性对照组,TFA分10、5、2.5 g/kg 3个剂量组。小鼠称重,以0.15 mL/10 g每天定时灌胃3次,连续5 d,首次给药后35 d处死小鼠。取小鼠双侧附睾,置于生理盐水中,剪碎、过滤,吸取滤液涂片,干燥,甲醇固定。镜下观察,每只小鼠1 000个结构完整的精子,计数畸形精子类型及数目,计算精子畸形率=畸形精子数/检查精子数×1 000‰。

2结果
2.1小鼠急性经口毒性试验
小鼠在14 d观察期内,未见任何中毒反应并无死亡状况,表明TFA对小鼠经口最大耐受量大于15 g/kg。据急性毒性分级标准,TFA被判定为无毒。
2.2小鼠骨髓嗜多染红细胞微核试验
本研究PCE/(PCE+NCE)比值均处于正常范围,表明试验结果可靠。结果显示CP阳性对照组微核率与CMC阴性对照组比较有极显著性差异(P<0.01);TFA各剂量组微核率与CP阳性对照组比较,差异有统计学意义(P<0.05),与CMC阴性对照组比较,差异无统计学意义(P>0.05,表1)。
2.3小鼠精子畸形试验
CP阳性对照组精子畸形率与CMC阴性对照组比较,有极显著差异(P<0.01);TFA各剂量组微核率与CP阳性对照组比较,均有极显著差异(P<0.01),与CMC阴性对照组比较,差异无统计学意义(P>0.05)。结果表明TFA各剂量不能引起小鼠精子畸形率增高(表2)。
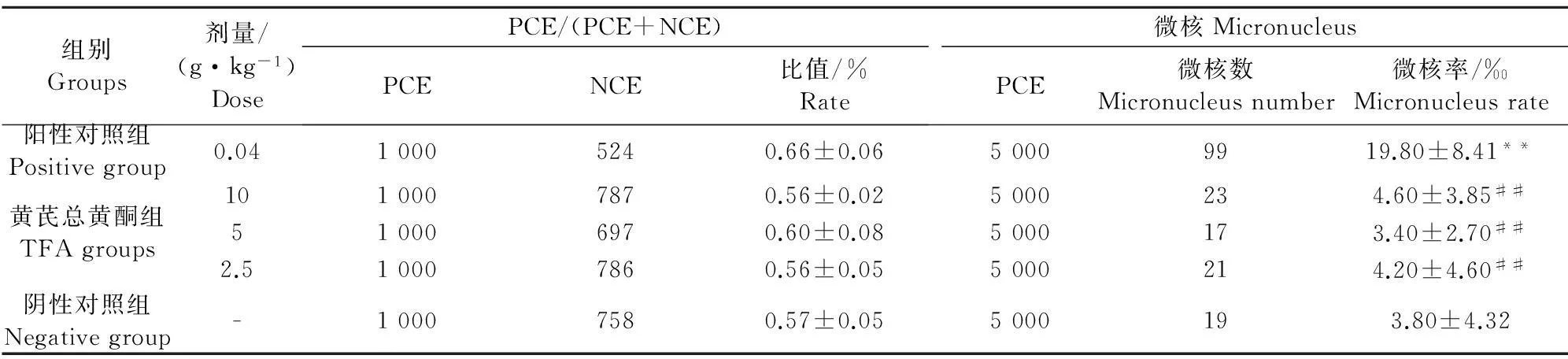
表1 TFA对小鼠骨髓嗜多染红细胞微核率的影响
注:与阴性对照组比较,*P<0.05,**P<0.01;与阳性对照组比较,#P<0.05,##P<0.01。
Note: Compared with the negative group,*P<0.05,**P<0.01;Compared with the positive group,#P<0.05,##P<0.01.
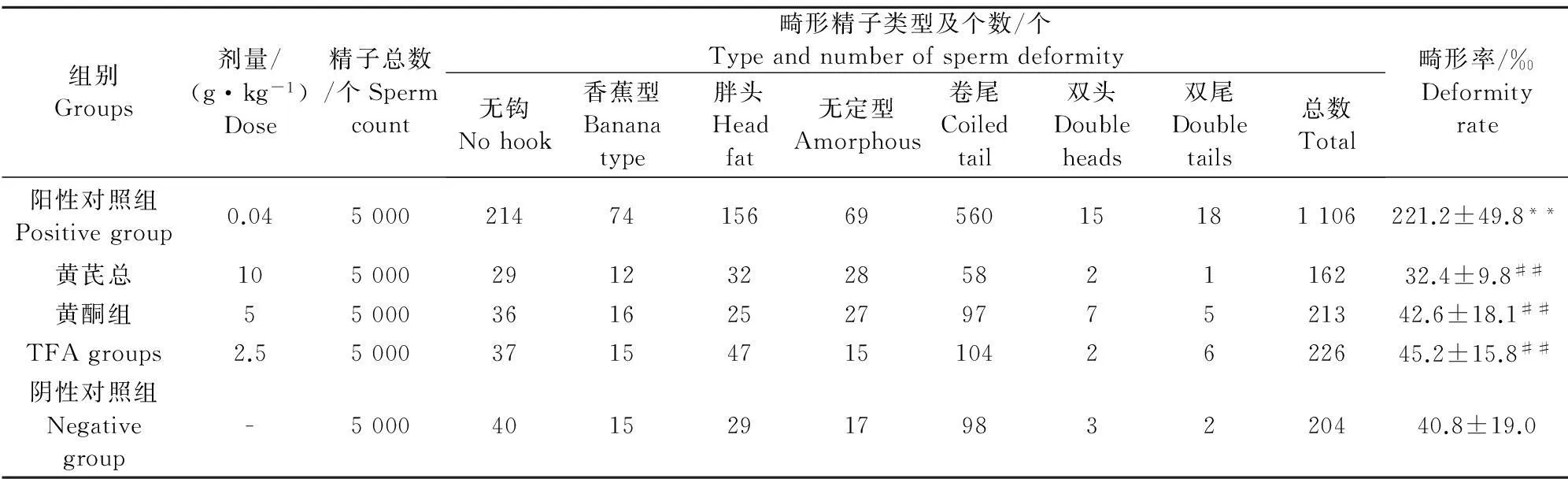
表2 TFA对小鼠精子畸形的影响
注:与阴性对照组比较,*P<0.05,**P<0.01;与阳性对照组比较,#P<0.05,##P<0.01。
Note:Compared with the negative group,*P<0.05,**P<0.01;Compared with the positive group,#P<0.05,##P<0.01。
3讨论
本研究采用小鼠急性经口毒性试验是毒理学安全性评价第一阶段最基础性的试验[9],结果表明,TFA对小鼠经口最大耐受量大于15 g/kg,判定为无毒级。
致突变性研究采用小鼠骨髓嗜多染红细胞微核试验和小鼠精子畸形试验两种方法,以CP为阳性对照物,CP属氮芥类烷化剂,为常用临床抗癌药,但有抑制骨髓、抑制免疫功能和遗传毒性等毒副作用[10]。有研究显示TFA对化学物诱导的DNA损伤具有一定的保护作用,即TFA有抗突变作用[11],但未对TFA的毒性做出评价。本研究两项致突变性试验结果均呈阴性,分别从染色体水平、基因水平表明TFA无致突变性。
参考文献:
[1]吴大真,余传隆,袁钟,等.中医辞海:中册[M].中国医药科技出版社,1999:1226.
[2]李娜,李峰.黄芪抗病毒作用研究进展[J].山东中医杂志,2015,34(7):566-568.
[3]中华人民共和国国家药典委员会.中华人民共和国药典:一部[M].北京:化学工业出版社,2010:212.
[4]刘德丽,包华音,刘杨.近5年黄芪化学成分及药理作用研究进展[J].食品与药品,2014,16(1):68-70.
[5]徐璐,李艳明,刘靖陶,等.黄芪总黄酮对小鼠免疫功能的影响[J].动物医学进展,2013,34(11):36-39.
[6]张贤,郭泽,张冲,等.黄芪总黄酮对脂多糖体外诱导的RAW264.7细胞的细胞因子和NO分泌水平的影响[J].中国兽医科学,2015,45(3):321-324.
[7]郭泽,邹娟,张贤,等.黄芪总黄酮小鼠体内抗炎作用研究[J].动物医学进展,2015,36(9):64-66.
[8]中华人民共和国卫生部.保健食品检验与评价技术规范[S].2003年版.北京:卫生部,2003:22-34.
[9]肖经纬,李斌,张星.急性经口毒性评价试验方法的研究进展[J].国外医学:卫生学分册,2007(2):84-88.
[10]Masuda R,Abe S,Yoshida M C,et al.Cytochrome P-450 andchromosome damage by cyclophosphamide in LEC strain rats predisposed to hereditary hepatitis and liver cancer [J].Mutat Res,1990,244(4):309-316.
[11]汪德清,田亚平,宋淑珍,等.黄芪总黄酮抗突变作用实验研究[J].中国中药杂志,2003,28(12):1164-1167.
Acute Toxicity and Mutagenicity of Total Flavonoids ofAstragalusin Mice
WANG Sha-sha,WANG Ying,GUO Ze,WANG Ping,ZHANG Chong,LI Hai-feng,ZHANG Xue-mei
(DepartmentofAnimalMedicine,AgriculturalCollegeofYanbianUniversity,Yanji,Jilin,133002,China)
Abstract:The acute toxicity and mutagenicity of total flavonoids of Astragalus in mice were investigated.Acute toxicity test with the maximum tolerance dose,bone marrow polychromatic erythrocyte micronucleus test and sperm deformity test in mice were adopted.The results showed that the acute oral maximum tolerated dose (MTD)of total flavonoids of Astragalusmice was higher than 15 g/kg.bw,bone marrow polychromatic erythrocyte micronucleus test and sperm deformity test in mice were negative.The results proved that the total flavonoids of Astragalusare non-toxic,and non-mutagenicon to somatic cells and male germ cells in mice.
Key words:total flavonoids of Astragalus; mice; acute toxicity; mutagenicity
文章编号:1007-5038(2016)03-0071-03
中图分类号:S853.7
文献标识码:A
作者简介:王沙沙(1992-),女,吉林榆树人,硕士研究生,主要从事兽医药理学与毒理学研究。 *通讯作者
基金项目:国家自然科学基金项目(31260622)
收稿日期:2015-08-06
王沙沙,王莹,郭泽,王平,张冲,李海峰*,张雪梅*
