胶束增敏荧光法测定大鼠血清中荜茇宁
2016-03-24敖登高娃
领 小,苗 澍,敖登高娃
(内蒙古大学 化学化工学院,内蒙古 呼和浩特 010021)
胶束增敏荧光法测定大鼠血清中荜茇宁
领小*,苗澍,敖登高娃
(内蒙古大学化学化工学院,内蒙古呼和浩特010021)
摘要:蒙药荜茇有效成分荜茇宁具有荧光,且荧光可被表面活性剂吐温-20增敏,同时,其同步荧光光谱能消除血清样品的背景荧光对荜茇宁荧光光谱的干扰,据此建立了直接测定大鼠血清中荜茇宁浓度的新方法。荜茇宁的线性范围为5.47×10-3~3.28 μg·mL-1,检出限为1.20×10-3μg·mL-1,样品回收率为100.6%,相对标准偏差为2.7%。方法可用于大鼠血清样品中荜茇宁浓度的直接测定。
关键词:荜茇宁;胶束体系;荧光分析法;血清
荜茇(Piper longum L.)为胡椒科植物荜茇的未成熟果穗,是常用蒙药。荜茇宁(Piperlonguminine,GBN)是荜茇的活性成分之一,具有降血脂活性[1-2]。作为药物,荜茇宁只有被血液吸收才能产生降血脂作用。血液中荜茇宁的浓度决定了其药效和毒理,因此建立生物样品中荜茇宁含量的有效测定方法十分必要。目前,荜茇宁的分析测定方法有分光光度法[3]、荧光光谱法[4]和高效液相色谱法[5]等。近年来,荧光法广泛应用于药物分析工作中[6-7]。但由于生物样品中内源性荧光物质的干扰,直接测定生物样品中荜茇宁浓度的荧光光谱方法尚未见文献报道。本文对荜茇宁的荧光特性进行了研究,建立了检测生物样品血清中荜茇宁的荧光分析方法。该方法操作简便,灵敏度高,选择性好,为荜茇宁的临床药物浓度测定和药代动力学研究提供了方法学基础。
1实验部分
1.1仪器与试剂
F-3010型荧光分光光度计(日本日立公司);pHS-3C 型酸度计(上海第二分析仪器厂);TGL-16G冷冻离心机(上海安亭科学仪器厂)。
荜茇宁标准品(99.9%)乙醇溶液;Mcllvaine(Na2HPO4-C6H8O7)缓冲溶液,pH 6.5;0.01 mol·L-1吐温-20溶液;血清样品为10 000 r/min下离心5 min所得。实验所用的其它试剂均为分析纯,实验用水为超纯水。
1.2实验方法
在10 mL比色管中,依次加入一定量的荜茇宁溶液、0.5 mL吐温-20溶液与2.0 mL Mcllvaine缓冲溶液,用水稀释至刻度,摇匀,放置10 min。用1 cm的石英荧光池,在λex/λem=344/464 nm处测定荧光强度,激发及发射狭缝宽度均为5 nm。

图1 荜茇宁的荧光发射光谱Fig.1 Emission spectrum of GBN1.0.5 mmol·L-1 Tween-20;2.1.37 μg·mL-1 GBN;3.GBN- Tween-20
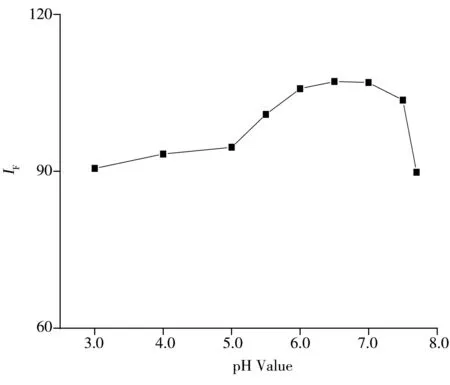
图2 pH值对体系荧光强度的影响Fig.2 Effect of pH value on fluorescence intensity
2结果与讨论
2.1发射光谱
荜茇宁乙醇溶液在激发波长为 340 nm、发射波长为472 nm 处具有荧光,但荧光较弱且不稳定。表面活性剂形成的胶束微环境对物质荧光有增敏作用[8],加入表面活性剂吐温-20后,体系在λex/λem=344/464 nm处的荧光强度增加、稳定性升高,在最大发射波长处几乎无干扰(图1)。且随着体系中荜茇宁浓度的增加,荧光强度在一定浓度范围内呈线性增强。因此,该体系可用于荧光分析法测定荜茇宁。
2.2缓冲溶液及pH值的影响
溶液的pH值将会影响体系的光谱性质[9]。考察了在Mcllvaine、Britton-Robinson等缓冲溶液体系中不同pH值对体系荧光强度的影响(见图2)。结果表明,pH 6.0~7.5的 Mcllvaine缓冲体系中,缓冲溶液的用量为1.5~2.5 mL时,荧光强度最大且稳定,因此实验选取Mcllvaine缓冲溶液,其pH 值为6.5,用量为2.0 mL。
2.3表面活性剂及用量的选择
考察了表面活性剂溴化十六烷基三甲基铵(CTMAB)、十二烷基硫酸钠(SDS)、十二烷基苯磺酸钠(DSS)、OP -10、曲拉通X-100及吐温-20等的荧光增敏作用。结果发现,吐温-20的增敏、增稳作用最显著,其用量为0.3~0.7 mL时效果最佳。用量小于0.3 mL时,增敏效果不明显;用量大于0.7 mL时,体系荧光光谱出现杂峰,基线上升,干扰测定。故选用0.5 mL吐温-20溶液进行后续实验。
2.4试剂加入顺序的影响
在选定实验条件下,考察了试剂加入顺序对荜茇宁体系荧光强度的影响。实验发现,试剂加入顺序为荜茇宁、吐温-20溶液、Mcllvaine缓冲溶液时,体系的荧光强度最大且恒定。故选择此顺序加入试剂。
2.5离子强度的影响
选用NaCl溶液考察了离子强度对体系荧光强度的影响。结果表明,当体系中 NaCl 的浓度小于0.585 mg·mL-1时,体系的荧光强度基本不变;NaCl 浓度大于0.585 mg·mL-1时,体系的荧光强度显著下降。这可能是由于大量存在的Na+和Cl-对胶束体系的稳定性产生影响,因此实验过程中未加入NaCl溶液,以保持较低的离子强度。
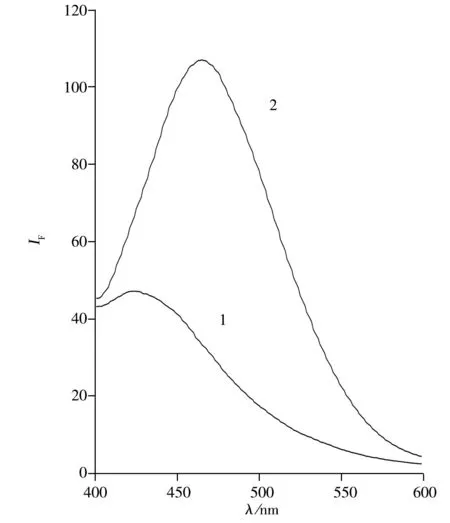
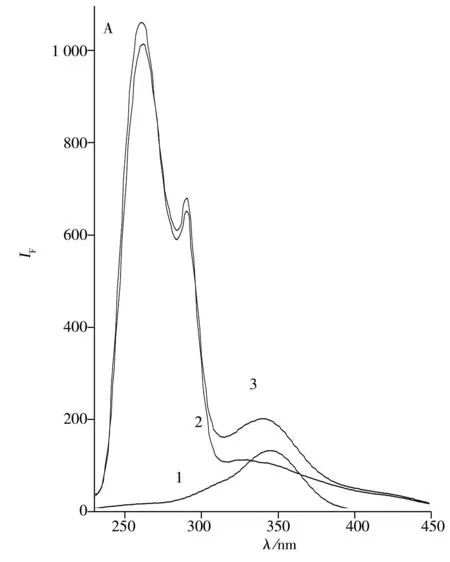
图3 空白血清与标样的荧光发射光谱Fig.3 Emission spectra of blank serum and standard solution1.blank serum-Tween-20;2.GBN- Tween-20
2.6干扰离子的影响
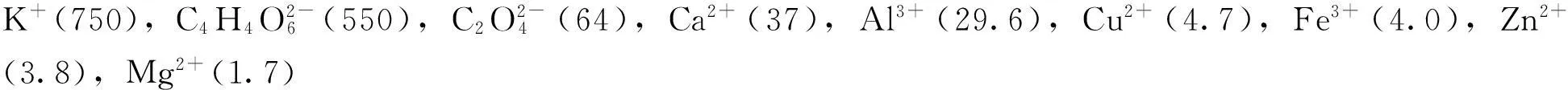
3样品分析
3.1常规荧光光谱
在 10 mL 比色管中,分别加入1.0 mL空白血清和荜茇宁乙醇溶液,再加入0.5 mL吐温-20溶液,扫描激发波长为 344 nm,按实验方法在400~600 nm 范围内扫描荧光发射光谱(图3)。结果发现,荜茇宁与血清样品的荧光光谱出现重叠,采用常规荧光光谱难以准确测定血清样品中的痕量荜茇宁。
3.2同步荧光光谱
同步荧光法在不分离情况下能解决生物样品与目标物的荧光重叠问题[10-11]。本实验中,分别扫描波长差Δλ=120 nm时血清样品及荜茇宁的同步荧光光谱(图4A),发现基本消除了血清样品的背景干扰。在pH 6.5的吐温-20胶束体系中,随着荜茇宁浓度的增加,体系同步荧光强度在一定范围内呈线性增强(图4B)。故同步荧光光谱法可用于血清中荜茇宁浓度的测定。
3.3Δλ的选择
同步荧光技术最大的影响因素是Δλ,它直接影响着方法的灵敏度与选择性[12]。本文分别考察了Δλ为0,50,60,70,80,90,100,110,120,130,140,150,160 nm时血清样品和荜茇宁混合体系的同步荧光光谱,发现Δλ=120 nm时荜茇宁与血清中荧光物质的分辨率最高,荧光信号最强。因此本实验选择Δλ=120 nm。
3.4标准曲线与精密度
于10 mL比色管中加入1.0 mL血清样品及一定量荜茇宁、0.5 mL吐温-20和2.0 mL缓冲溶液,稀释至刻度。设置Δλ=120 nm,在220~450 nm波长范围内进行同步荧光光谱扫描。结果表明,荜茇宁的质量浓度(ρ,μg·mL-1)在5.47×10-3~3.28 μg·mL-1范围内与体系荧光强度(IF)呈良好的线性关系,线性方程为IF=33.008ρ+114.44,相关系数(r)为0.999 6。对空白对照液进行11次平行测定,根据公式cL=3s/k(s为空白溶液的标准偏差,k为标准曲线斜率),计算得检出限为1.20×10-3μg·mL-1。对浓度为1.37 μg·mL-1的荜茇宁溶液平行测定11次,相对标准偏差(RSD)为1.3%,表明该方法的精密度良好。
3.5血清样品中荜茇宁的回收率
3.5.1新生牛血清中荜茇宁的回收率测定取新生牛血清样品(北京元亨圣马生物技术研究所)适量,10 000 r/min离心5 min,使其杂质沉淀完全。取适量上清液,按照标准曲线绘制方法进行荜茇宁浓度及加标回收率的测定,结果见表1。新生牛血清中未测出荜茇宁,方法的加标回收率为98.9%~100%,表明该方法精确可行。

表1 新生牛血清样品中荜茇宁的测定结果(n=5)
*:no detected
3.5.2大鼠血清中荜茇宁的回收率测定Wistar雄性大鼠(北京维通利华实验动物技术有限公司,合格证号为SCXK(京)2012-0001),体重为(200±20) g。用0.5%的CMC-Na将荜茇宁制成混悬液,按100 mg·kg-1剂量灌胃给大鼠,大鼠每200 g体重灌胃1 mL荜茇宁混悬液,连续灌胃3 d。末次给药后2 h股动脉取血,放置30 min。3 000 r/min离心15 min,取上清液,进行荜茇宁浓度及加标回收率的测定,结果显示大鼠给药2 h的血清中荜茇宁的浓度达1.04 μg·mL-1,加标回收率为100.6%,RSD为2.7%。表明该方法灵敏度高,能够测定血清中的荜茇宁。
4结论
基于pH 6.5的缓冲溶液中,荜茇宁的荧光强度可被表面活性剂吐温-20增敏的特性,建立了一种快速灵敏的蒙药中有效成分荜茇宁的荧光测定方法。血清样品的本底荧光与荜茇宁的荧光光谱重叠,而选择Δλ=120 nm进行同步荧光光谱分析可实现二者的分离,从而基本消除血清样品的背景干扰。据此提出直接测定大鼠血清中荜茇宁浓度的同步荧光光谱法,加标回收率为100.6%,RSD为2.7%。该法简便、快速、灵敏度高、选择性好,为荜茇宁的生物体内直接检测提供了可能,对荜茇宁血清药物的化学研究具有重要意义。
参考文献:
[1]Ma C J,Bo G R L T,Hu R L B G,Te G X,Su R N.ChinaJ.Chin.Mater.Med.(麻春杰,博·格日勒图,呼日乐巴根,特格希,苏日娜.中国中药杂志),2008,33(4):436-440.
[2]Borijihan G R L T,Na S S,Jin Z,Zhao R G,Gao J,Song L.China Patent(博日吉汗格日勒图,那生桑,金桩,赵睿国,高杰,松林.中国专利)ZL,200410096611.7,[2006-12-06].
[3]Aodeng G W,An N,Ling X,Miao S.Chin.J.Lumin.(敖登高娃,安娜,领小,苗澍.发光学报),2012,33(5):558-561.
[4]Ling X,Bo G R L T,Na R S,Zhao R G T.Chin.J.Anal.Lab.(领小,博·格日勒图,那日苏,昭日格图.分析试验室),2009,28(6):21-23.
[5]Erdenebaatar S,Borjihan G,Baigude H R C,Ao N,Meng H,Na R S,Zhao R G T.Biomed.Chromatogr.,2013,27:821-824.
[6]Luo J J,Ma H Y,Ma Y,Xin J W,Wang H.J.Instrum.Anal.(罗娟娟,马红燕,马莹,辛建伟,王浩.分析测试学报),2011,30(5):553-557.
[7]Zhang Y,Ma R,Fan S H.Chin.J.Anal.Chem.(张悦,马睿,范世华.分析化学),2010,38(7):958-962.
[8]Zheng Y X,Li L D.Chin.J.Anal.Chem.(郑用熙,李隆弟.分析化学),1990,18(3):292-299.
[9]Wang S J,Zhang Q,Wang L P,Wei Y J.J.Instrum.Anal.(王淑静,张晴,王立屏,魏永巨.分析测试学报),2014,33(2):138-143.
[10]Ibrahim F A,EI-Enany N,EI-Shaheny R N ,Mikhail I E.Luminescence,2015,30:485-494.
[11]Yin X L,Wu H L,Zhang X H,Gu H W,Yu R Q.ActaChim.Sin.(尹小丽,吴海龙,张晓华,谷惠文,俞汝勤.化学学报),2013,71:560-566.
[12]Yang J,Yu D S,Liu S P,Tian Y F,Mo B B.Chin.J.Anal.Chem.(杨军,余德顺,刘绍璞,田弋夫,莫彬彬.分析化学),2009,37(1):107-110.
Determination of Piperlonguminine in Rat Serum Using Micelle Sensitized Fluorescence Spectrometry
LING Xiao*,MIAO Shu,AODENG Gao-wa
(College of Chemistry and Chemical Engineering,Inner Mongolia University,Hohhot010021,China)
Abstract:Piperlonguminine,the effective composition of the Mongolian medicine Piper longum L.,has fluorescence and its fluorescence signal could be greatly enhanced by the surfactant Tween -20.The synchronous fluorescence spectroscopic method could eliminate the interference of the background fluorescence from serum samples on fluorescence spectra of piperlonguminine.According to this technique,a method was established for the determination of piperlonguminine in rat serum.The linear range of this method was in the range of 5.47×10-3-3.28 μg·mL-1,the detection limit for piperlonguminine was 1.20×10-3μg·mL-1,and the relative standard deviation(RSD) was 2.7%.The method was successfully applied in the detection of piperlonguminine in rat serum amples,with recovery of 100.6%.
Key words:piperlonguminine;micellar system;fluorescence spectrometry;serum
中图分类号:O657.3;TQ460.72
文献标识码:A
文章编号:1004-4957(2016)02-0225-05
doi:10.3969/j.issn.1004-4957.2016.02.015
*通讯作者:领小,博士,副教授,研究方向:药物分析,Tel:0471-4992511,E-mail:lingxiaobao@126.com
基金项目:国家自然科学基金项目(81060366);内蒙古自然科学基金项目(2014MS8024)
收稿日期:2015-07-10;修回日期:2015-08-19
