前列腺素E1预处理对缺血再灌注肺组织TNF—α和PAF表达的影响
2016-03-17蔡晓菲焦桂萍
蔡晓菲 焦桂萍
【摘要】 目的 观察大鼠肺缺血再灌注(LIRI)损伤后肿瘤坏死因子-α(TNF-α)、血小板活化因子(PAF)含量及相关酶学变化, 探讨前列腺素E1预处理对大鼠肺LIRI的保护作用。方法 建立原位阻断肺门的大鼠肺缺血再灌注模型, 将54只雄性清洁级SD大鼠随机分成假手术组(SO组)、LIRI组(IR组)和前列腺素E1组(PGE1组), 每组18只。每组均分别在缺血45 min, 再灌注1、2 h三个时间点处死大鼠, 比较三组大鼠不同时间点肺组织病理学改变及肺组织干/湿重(D/W)比值, TNF-α、PAF水平, 丙二醛(MDA)浓度及超氧化物歧化酶(SOD)活性表达水平。结果 PGE1组肺组织D/W比值, TNF-α、PAF、MDA浓度及SOD活性水平均较IR组显著改善, 差异有统计学意义(P<0.05)。结论 前列腺素E1预处理可以减轻LIRI肺损伤, 其可能机制是通过减轻LIRI后的炎症反应而起到肺组织保护作用。
【关键词】 前列腺素E1;缺血再灌注;肺;肿瘤坏死因子-α;血小板活化因子
DOI:10.14163/j.cnki.11-5547/r.2016.07.214
前列腺素E1长期作为一种血管扩张剂及抑制血小板聚集剂用于急性肺损伤的临床治疗。国外有文献表明PGE1对LIRI后的炎性介质具有调节作用, 可阻断LIRI现象的发生。然而目前国内关于PGE1对LIRI影响的临床研究甚少, 且作为炎性介质PAF对于LIRI的影响更是少有报道。本研究通过建立大鼠肺LIRI损伤模型, 观察PGE1对肺内炎性介质TNF-α、PAF及相关酶学表达的影响, 探讨其对LIRI的保护作用机制, 为其临床研究提供理论依据。
1 材料与方法
1. 1 材料 选取健康成年雄性清洁级SD大鼠54只, 重量280~350 g, 由郑州大学医学院实验动物中心提供。随机分为三组:假手术组(SO组)、LIRI组(IR组)、前列腺素E1组(PGE1组), 每组18只。每组随机再分缺血45 min, LIRI后1、2 h 三个亚组, 每个亚组6只。
1. 2 动物模型制备 IR组:取大鼠称重, 予3%戊巴比妥钠30 mg/kg腹腔注射麻醉, 麻醉满意后气管切开插管接DH-140B型动物人工呼吸机(f=70次/分、I∶E=1.25∶1、V=10~15 ml/kg), 大鼠右侧卧位, 经左前侧第5肋间进入胸腔, 解剖左侧肺门。肝素50 U用生理盐水稀释至500 μl经阴茎背静脉注射, 5 min后于肺充盈状态下用无创微血管夹依次夹闭左肺动脉、支气管与肺静脉, 45 min后放开血管夹恢复灌注和通气, 造成LIRI模型。再灌注期间腹腔注射生理盐水0.5 ml/h, 各组均分别于缺血45 min和再灌注1、2 h后经颈动脉放血处死大鼠。SO组:完成除夹闭肺门的其他一切手术操作, 余同IR组。PGE1组:缺血前5 min阴茎背静脉注射PGE1(北京泰德制药有限公司)(10 μg/kg溶于0.5 ml生理盐水), 余同IR组。
1. 3 检测指标及方法
1. 3. 1 肺组织切片病理学观察 取部分左肺上叶组织10%中性甲醛固定, 常规脱水、包埋、切片、脱蜡、HE染色, 光镜下观察细胞形态学变化。
1. 3. 2 肺组织干/湿重比测定 取部分左肺下叶组织, 滤纸吸干表面液体, 称其湿重。然后置入恒温干燥箱(80℃), 烘烤48 h后取出称其干重, 计算D/W。
1. 3. 3 肺组织TNF-α、PAF含量测定 采用双抗体夹心ELISA法测定10%肺组织匀浆TNF-α、PAF含量, 严格按照试剂盒说明书进行。
1. 3. 4 肺组织SOD、MDA水平测定 取10%肺组织匀浆测定SOD、MDA水平, 操作步骤按照南京建成生物工程研究所提供的试剂盒说明书。
1. 4 统计学方法 采用SPSS18.0统计学软件进行统计分析。计量资料以均数±标准差( x-±s)表示, 组内比较采用重复测量的方差分析, 组间比较采用单因素方差分析。P<0.05表示差异具有统计学意义。
2 结果
2. 1 肺组织病理切片结果 SO组:肺泡结构完整, 毛细血管内无充血, 肺泡腔内无或少许白细胞、红细胞渗出。IR组:部分肺泡萎陷不张, 毛细血管明显扩张、充血, 肺泡腔及肺间质可见大量白细胞、红细胞渗出, 水肿液明显渗出。PGE1组:肺泡结构尚可, 毛细血管轻度充血, 各时间点肺间隔及肺泡腔出血、渗出较IR组明显减轻。
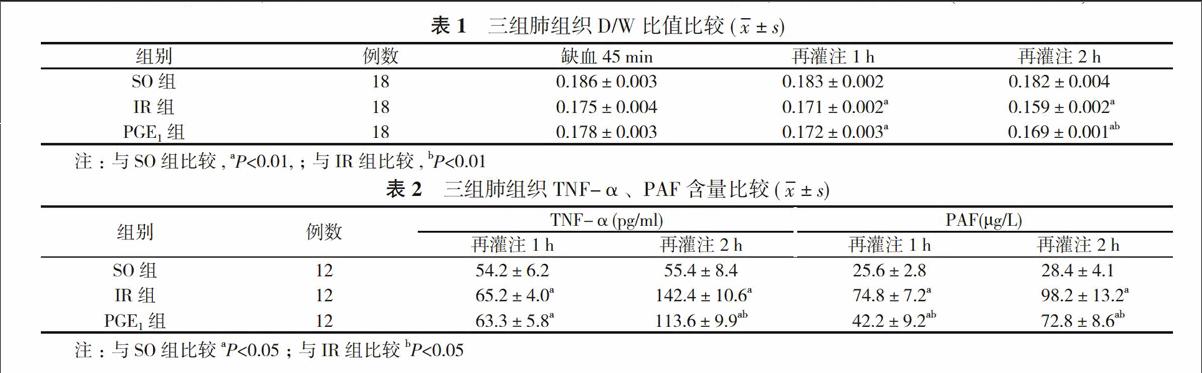
2. 2 肺组织D/W比值比较 缺血45 min三组大鼠肺组织D/W比值差异无统计学意义(P>0.05);IR组及PGE1组随再灌注时间延长D/W比值逐渐下降, 与SO组比较差异有统计学意义(P<0.05或P<0.01);PGE1组再灌注各时间点肺组织D/W比值下降无IR组显著, 再灌注2 h两组比较差异有统计学意义(P<0.01)。见表1。
2. 3 肺组织TNF-α、PAF含量比较 SO组各时间点TNF-α、PAF含量差异无统计学意义(P>0.05);IR组及PGE1组两指标再灌注各时间点与SO组比较比较差异有统计学意义(P<0.05);PGE1组两指标随时间延长亦有升高, 但低于IR组, 两组TNF-α(再灌注2 h)、PAF(再灌注1、2 h)比较差异有统计学意义(P<0.05)。见表2。
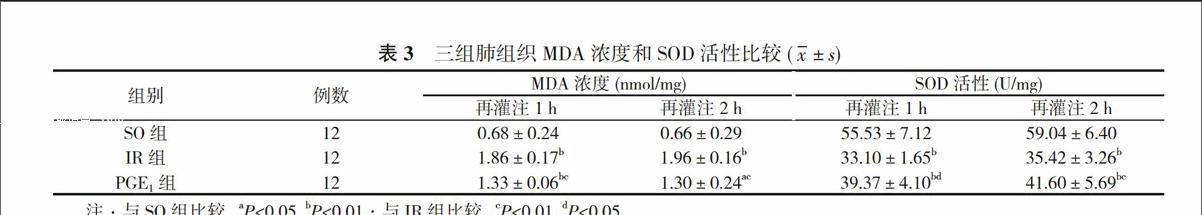
2. 4 肺组织MDA浓度和SOD活性水平比较 PGE1及IR组再灌注各时间点肺组织MDA、SOD均较SO组有改善, 差异有统计学意义(P<0.05或0.01);且 PGE1组两指标改善情况与IR组比较, 差异有统计学意义(P<0.05或0.01)。见表3。
3 讨论
LIRI是由多种炎性介质和效应细胞共同参与的一种呈级联放大的瀑布样炎症损伤, 检测炎性指标PAF、TNF-α的变化可以很好的表示LIRI后肺组织因炎症所致的损害程度[1]。PAF是具有广泛生物活性的脂类炎性介质, 是迄今为止发现的最强的血小板聚集诱导剂, 亦是内源性炎症过程启动与放大的重要调节递质, 其通过与相应受体结合而参与LIRI的发生发展。TNF-α是LIRI过程中最早释放的细胞因子, 对其他细胞因子起诱导和调节作用, 通过多种途径引起肺损伤。TNF-α拮抗剂可有效中和TNF-α并阻断其生物学活性, 抑制炎性细胞因子释放从而起到减轻LIRI的作用。由上可知, TNF-α、PAF是LIRI过程中具有关键作用的炎性因子, 抑制其生成有助于缺血肺功能的恢复。本实验中作者采用大鼠肺缺血再灌注模型, 发现IR组TNF-α、PAF含量在再灌注各时间点均较SO组明显升高(P<0.05), PGE1组各时间点两者含量均低于IR组而显著高于SO组(P<0.05), 说明PGE1能减少肺组织TNF-α、PAF含量达到肺组织的保护作用。
正常情况下, 肺内氧化与抗氧化系统处于平衡状态, 而机体缺血缺氧后可释放大量炎性细胞因子及氧自由基, 肺组织中MDA含量和SOD活性可判定LIRI后肺的氧化和抗氧化能力及氧自由基对肺组织攻击的严重程度。实验中观察到:IR组大鼠肺组织MDA含量显著升高, SOD活性下降;而PGE1组MDA含量低于IR组, SOD活性高于IR组(P<0.05)。表明PGE1缺血前干预LIRI能增强机体对氧自由基的清除, 具有抗脂质过氧化反应, 从而减轻LIRI造成的肺组织损伤。肺水肿是LIRI的一个重要的病理改变, 而D/W比值可反应肺组织充血水肿的程度, 间接评价LIRI后肺损伤情况。本实验中观察到IR组在再灌注各时间点D/W比值随时间逐渐减低, 而PGE1组D/W比值亦下降, 但下降没有IR组显著。同时, 光镜下亦观察到PGE1组肺泡腔及间质白细胞、红细胞浸润、渗出较IR组减轻。
脂质体前列腺素E1(Lipo-PGE1)以脂质体微球作为药物载体, 减少了药物毒副作用并增强临床疗效。Lipo-PGE1能选择性地活化中性粒细胞(PMN), 从而增强PGE1对PMN的靶向抗炎作用, 抑制肺内PMN聚集活化, 减轻大鼠急性肺损伤。文献表明Lipo-PGE1属于抗炎因子, 通过抑制TNF-α、PAF等炎性介质的产生及释放从而发挥肺组织保护作用[2]。
综上所述, Lipo-PGE1预处理可以减轻缺血再灌注肺损伤, 其保护作用机制可能与下调TNF-α、PAF的表达以及抑制PMN浸润和激活有关。
参考文献
[1] 倪程耀, 陈新, 吴胜军.免疫因素在大鼠肺缺血再灌注损伤中的作用.中国老年学杂志, 2014, 34(18):5192-5193.
[2] 陈立新, 刘德昭.前列地尔对围术期机械通气肺损伤的肺保护作用.实用医学杂志, 2011, 27(3):2432-2434.
[收稿日期:2015-11-11]
