兰花颗粒质量标准研究
2016-03-16康玉霞郭飞燕王晓娟陕西中医药大学药学院咸阳71046军事口腔医学国家重点实验室第四军医大学口腔医院药剂科西安71003
康玉霞,雷 丸,王 莹,郭飞燕,王晓娟*(1.陕西中医药大学药学院,咸阳 71046;.军事口腔医学国家重点实验室,第四军医大学口腔医院药剂科,西安 71003)
兰花颗粒质量标准研究
康玉霞1,2,雷丸2,王莹2,郭飞燕2,王晓娟2*(1.陕西中医药大学药学院,咸阳712046;2.军事口腔医学国家重点实验室,第四军医大学口腔医院药剂科,西安710032)
摘要:目的建立兰花颗粒的质量标准。方法采用薄层色谱法(TLC)鉴别本制剂中的板蓝根、大青叶和忍冬藤;采用高效液相色谱法(HPLC)测定制剂中(R,S)-告依春的含量,色谱柱为Spursil C18(250 mm×4.6 mm,5 μm);流动相为甲醇-水(7∶93);检测波长为245 nm。结果在选定的薄层色谱条件下,斑点显色清晰,分离效果良好。(R,S)-告依春质量浓度在0.30~2.12 μg·mL-1内呈良好的线性关系(r=0.999 7);平均回收率为87.5%,RSD为1.0%(n=9)。结论该方法专属性强、重复性好、简便可行,可用于兰花颗粒的质量控制。
关键词:兰花颗粒;(R,S)-告依春;薄层色谱;高效液相色谱;
疱疹性口炎病原体为Ⅰ型疱疹病毒引起的急性口腔黏膜炎症[1],婴幼儿感染多为原发性,无明显季节性,一年四季散发[2]。研究发现疱疹病毒集中于完整疱疹液内,溃破后引发感染症状,使得疼痛严重[3]。兰花颗粒是由第四军医大学口腔医院研制的中药复方制剂,主要由板蓝根、大青叶、忍冬藤等五味中药组成,具有清热解毒、解表通便之功效,主治疱疹性口炎、病毒性上呼吸道感染、四时感冒等症。板蓝根具有清热解毒、凉血利咽[4]、调节和保护机体免疫力的作用[5]。大青叶具有清热解毒、利咽止痛[6]、抑制病原微生物和提高机体免疫力的作用[7]。为有效控制药品质量、保证药品疗效,笔者对兰花颗粒的质量标准进行研究,采用薄层色谱法对板蓝根、大青叶和忍冬藤进行鉴别,并采用高效液相色谱法对板蓝根中的主要药效成分(R,S)-告依春进行含量测定,建立可控制该制剂质量的标准。
1仪器与试药
1.1仪器高效液相色谱仪(LC-20AT,日本岛津公司);KQ5200E型超声清洗仪(昆山市超声仪器有限公司);十万分之一电子天平(BT125D,德国赛多利斯公司);离心机(LD5-10,北京医用离心机厂)。
1.2试药靛玉红对照品(批号110717-200204,质量分数100%)、板蓝根对照药材(批号121117-200302)、大青叶对照药材(批号121367-200602)、忍冬藤对照药材(批号121069-201105)、(R,S)-告依春对照品(批号111753-201304,质量分数99.9%),均由中国食品药品检定研究院提供;兰花颗粒(规格:12 g×10包/盒,批号:140807,140909,141013,第四军医大学口腔医院药剂科);兰花颗粒(大青叶、板蓝根阴性,自制);兰花颗粒(忍冬藤阴性,自制);兰花颗粒(板蓝根阴性,自制);甲醇为色谱纯;其余试剂为分析纯;水为超纯水。
2方法与结果
2.1定性鉴别
2.1.1大青叶、板蓝根TLC鉴别取本品2包,研细,加氯仿30 mL,加热回流1 h,过滤,滤液蒸干,残渣加氯仿1 mL复溶,作为供试品溶液[8]。另取大青叶、板蓝根对照药材各1 g,同法制成大青叶、板蓝根对照药材溶液。再取靛玉红对照品,加三氯甲烷制成1 mL含0.1 mg的对照品溶液。再取大青叶、板蓝根阴性样品24 g,按照供试品的制备方法制成阴性对照溶液。依照薄层色谱法(《中国药典》2010年版一部附录ⅥB)实验,吸取供试品溶液、对照品溶液、大青叶对照药材溶液、板蓝根对照药材溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以环己烷-三氯甲烷-丙酮(5∶4∶2)为展开剂,展开,取出,晾干。供试品色谱中,在与对照品和对照药材色谱相应的位置上,显示相同颜色的斑点,阴性对照无干扰,见图1。
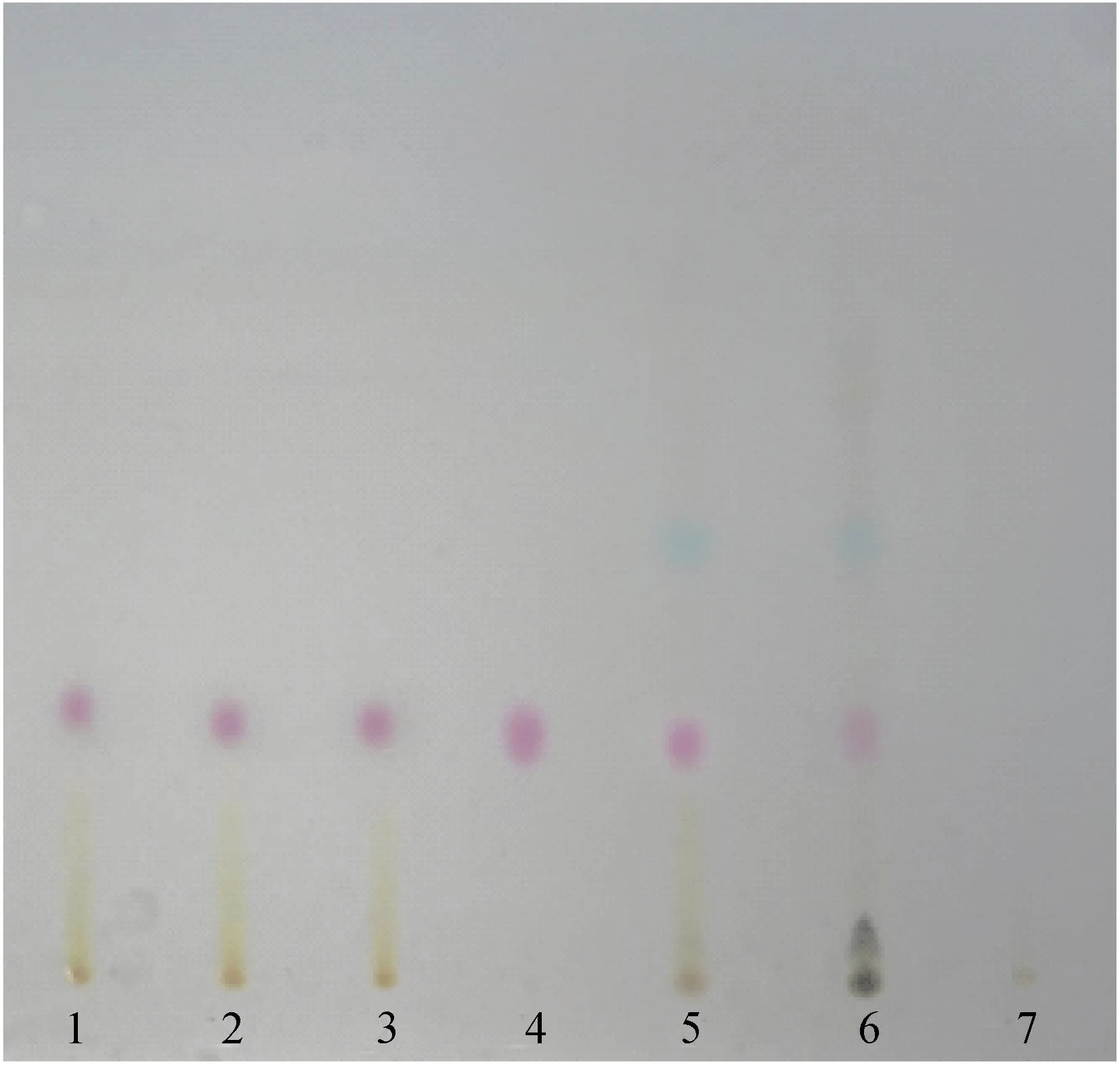
图1大青叶与板蓝根薄层色谱图
1~3.供试品;4.靛玉红对照品;5.大青叶对照药材;6.板蓝根对照药材;7.阴性对照
Fig.1 TLC ofRadixisatidisandFoliumisatidis
1-3.sample solution;4.indirubin control substance;5.Foliumisatidisreference substance;6.Radixisatidisreference substance;7.negative control
2.1.2忍冬藤TLC鉴别取本品2包,研细,加体积分数为50%的甲醇40 mL,超声处理30 min,离心,取上清液作为供试品溶液[9]。另取忍冬藤阴性样品24 g,同法制成阴性对照溶液。再取忍冬藤对照药材1 g,加入体积分数为50%的甲醇10 mL,超声处理30 min,离心,取上清液作为对照药材溶液。依照薄层色谱法(《中国药典》2010年版一部附录ⅥB)实验,吸取供试品溶液、对照药材溶液、阴性对照溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-水(13∶7∶2)10 ℃以下放置的下层溶液为展开剂,展开,取出,晾干,喷以体积分数为10%的硫酸乙醇溶液,105 ℃加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,显示相同颜色的斑点,阴性对照无干扰,见图2。
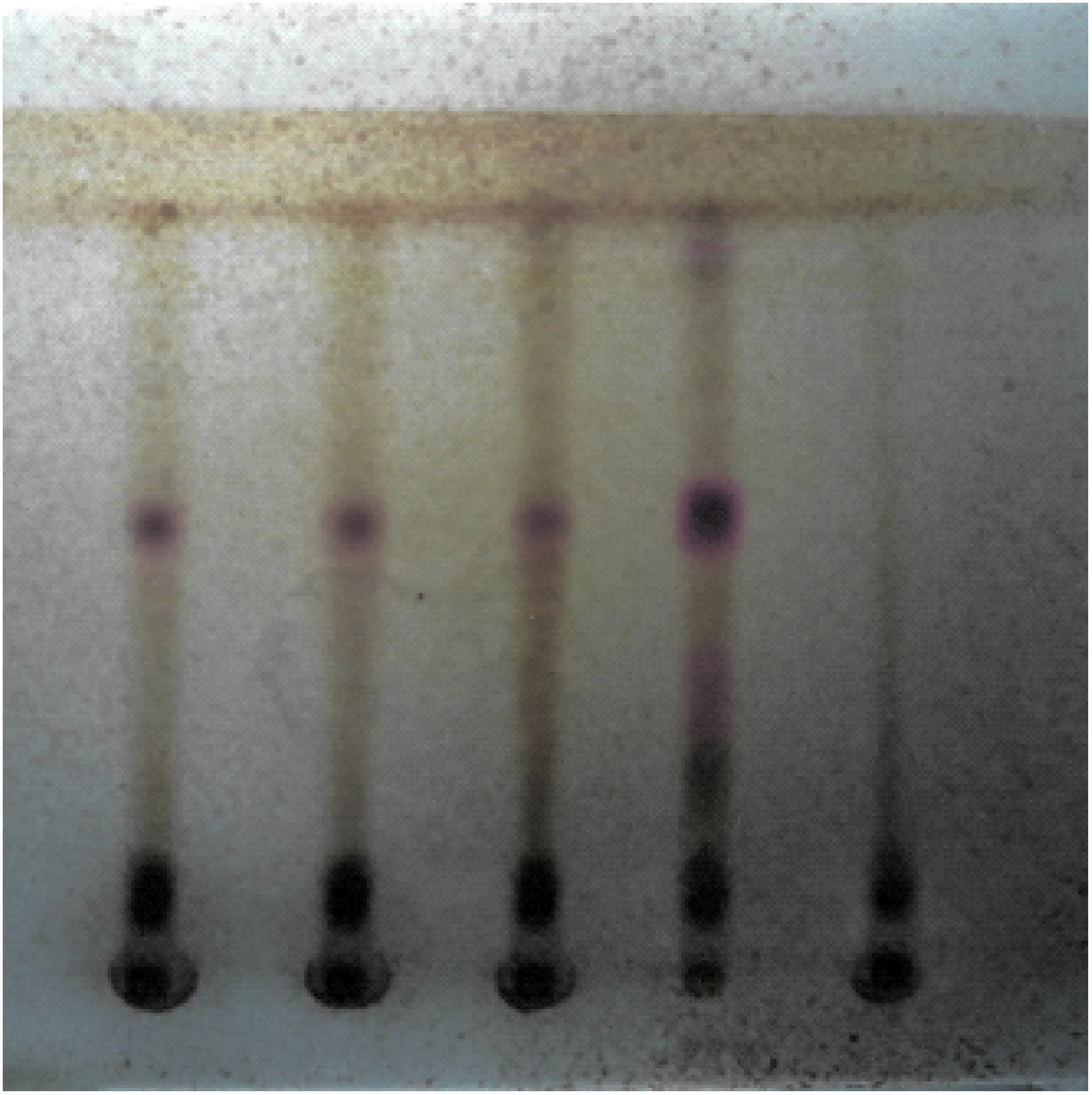
图2 忍冬藤薄层色谱图
1~3.供试品;4.忍冬藤对照药材;5.阴性对照
Fig.2 TLC ofCaulislonicerae
1-3.sample solution;4.Caulisloniceraereference substance;5.negative control
2.2含量测定
2.2.1色谱条件色谱柱:Spursil C18(250 mm×4.6 mm,5 μm);流动相:甲醇-水(7∶93);检测波长:245 nm;流速:1.0 mL·min-1;进样量:10 μL;理论板数按(R,S)-告依春峰计算应不低于5 000。
2.2.2对照品溶液的制备精密称取(R,S)-告依春对照品5.05 mg,置于5 mL量瓶中,加甲醇溶解,定容至刻度,摇匀,得质量浓度为1.01 mg·mL-1的对照品母液。精密吸取该对照品母液1 mL,置于10 mL量瓶中,加甲醇定容至刻度,摇匀,即得质量浓度为0.10 mg·mL-1的对照品储备溶液。再量取对照品储备溶液0.38 mL,置于25 mL量瓶中,加甲醇定容至刻度,摇匀,即得质量浓度为1.52 μg·mL-1的对照品溶液。
2.2.3供试品溶液的制备取兰花颗粒5包,研细,混合均匀,取10 g,精密称定。加水100 mL,回流2 h,取出,放冷,加水补足减失的质量,摇匀,用0.45 μm的微孔滤膜滤过,即得。
2.2.4阴性对照溶液的制备取板蓝根阴性样品适量,按照2.2.3项下的方法制备阴性对照溶液。
2.2.5专属性实验精密吸取对照品溶液、供试品溶液和阴性对照溶液各10 μL,按照2.2.1项下的色谱条件进样测定,结果显示,供试品溶液与对照品溶液的保留时间一致,阴性对照溶液在(R,S)-告依春相应的保留时间内未出现色谱峰,表明在该色谱条件下(R,S)-告依春的吸收良好,兰花颗粒中其他成分对(R,S)-告依春的测定无干扰。见图3。
图3HPLC图
a.对照品溶液;B.供试品溶液;C.阴性对照;1.(R,S)-告依春
Fig.3 HPLC chromatograms
a. (R,S)-goitrin control substance;B.sample solution;C.negative control;1.(R,S)-goitrin
2.2.6线性关系考察精密量取对照品储备溶液0.30,0.60,0.90,1.20,1.50,1.80和2.10 mL,分别置于100 mL量瓶中,加甲醇定容至刻度,摇匀,制成质量浓度分别为0.30,0.61,0.91,1.21,1.52,1.82和2.12 μg·mL-1的对照品系列溶液。精密吸取上述对照品系列溶液各10 μL,按照2.2.1项下的色谱条件进样测定,记录峰面积,以(R,S)-告依春对照品的峰面积(Y)对(R,S)-告依春的进样质量浓度(X)进行线性回归,得回归方程:Y=59 879X+3 681.4(r=0.999 7),表明(R,S)-告依春质量浓度在0.30~2.12 μg·mL-1范围内线性关系良好。
2.2.7精密度实验按照2.2.1项下的色谱条件,精密吸取(R,S)-告依春对照品溶液(1.52 μg·mL-1)10 μL,重复进样6次,每次10 μL,记录峰面积,计算其RSD为0.79%,表明仪器精密度良好。
2.2.8稳定性实验精密吸取同一供试品溶液10 μL,在0,2,4,6,8,10和12 h时,按照2.2.1项下的色谱条件,分别进样测定,记录其峰面积值,计算RSD为1.66%,表明供试品溶液在12 h内稳定性良好。
2.2.9重复性实验取同一批兰花颗粒(批号140807)内容物,按照2.2.3项下的方法,制备6份供试品溶液,并按照2.2.1项下的色谱条件进样测定,记录峰面积,结果显示,(R,S)-告依春的平均含量为14.31 μg·g-1,RSD为1.90%(n=6),表明该方法重复性良好。
2.2.10加样回收率实验分别称取5.0 g已知含量(每克含有(R,S)-告依春14.31 μg)的兰花颗粒9份,精密称定,分别按照高、中、低质量浓度加入一定量的(R,S)-告依春对照品储备溶液,加水100 mL,回流2 h,取出,放冷,加水补足减失的质量,摇匀。精密吸取10 μL,然后按照2.2.1项下的色谱条件进样测定,计算加样回收率,结果见表1。
表1加样回收率实验结果
Tab.1 Results of the recovery tests
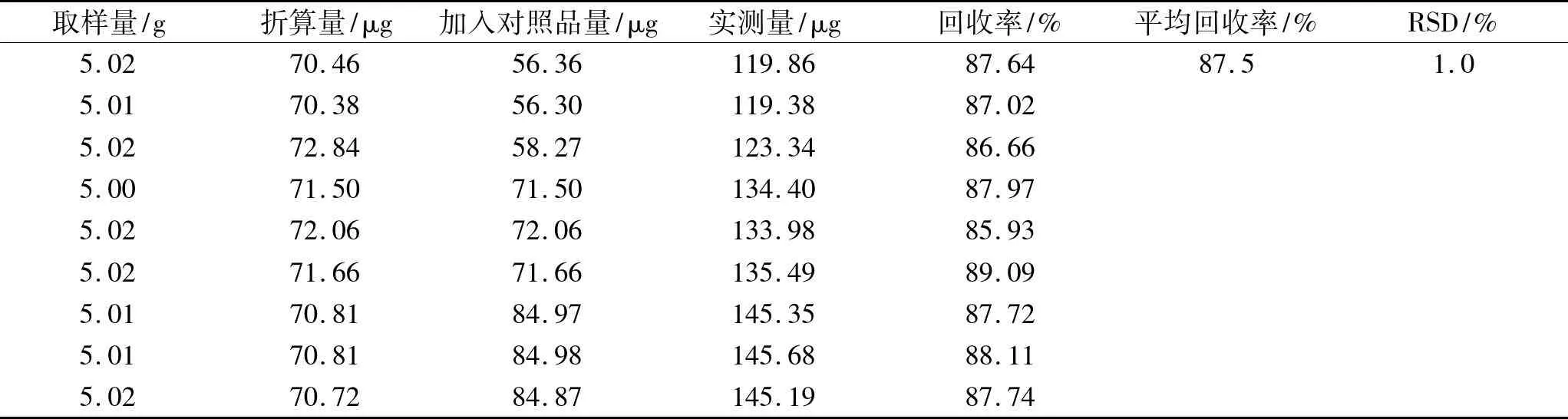
(n=9)
2.2.11样品含量测定精密称取3批兰花颗粒(批号140807,140909,141013),按照2.2.3项下的制备方法进行制备,按照2.2.1项下的色谱条件进样测定,并计算样品中(R,S)-告依春的含量,分别为168.36,175.32和171.60 μg·袋-1,平均含量为171.76 μg·袋-1。
3讨论
在板蓝根的薄层鉴别中,笔者考察了以下条件:3种提取溶剂:体积分数为70%的乙醇[10]、稀乙醇[11]和乙酸乙酯[12];3种展开系统:正丁醇-冰醋酸-水(19∶5∶5)[11],三氯甲烷-甲醇(4∶1)[13],三氯甲烷-丙酮-甲酸(5∶4∶1)[12];2种显色剂:茚三酮试液[11],磷钼酸试液[13]。对上述条件进行分析比较。用体积分数为70%的乙醇提取时,样品因含糖量过大,点样困难,干扰较大,薄层色谱图较难辨认,不予采用。尝试其余的方法,薄层色谱图均能呈现斑点,分离度良好,显色清晰的效果,但阴性均有干扰。由于处方中板蓝根和大青叶来源于同一植物,只是部位不同,两者含有共有成分,因此专属性不强。通过查阅相关文献[6],最终选择用靛玉红鉴别制剂中的板蓝根和大青叶。
在(R,S)-告依春的含量测定中,考查了几种不同的流动相系统:甲醇-0.5 mL·L-1的磷酸溶液(7∶93)[14]、甲醇-0.2 mL·L-1磷酸溶液(7∶93)[15]、甲醇-水(7∶93),结果发现效果无明显差异,故选择了甲醇-水(7∶93)为流动相系统。
板蓝根为本方的君药,其主要成分为(R,S)-告依春,故笔者在本质量标准研究中建立了(R,S)-告依春的含量测定方法。通过本实验建立的薄层鉴别方法和高效液相色谱含量测定方法对3批样品进行质量控制,发现本方法简便易行、灵敏度高、重复性好,可用于兰花颗粒的质量控制。
参考文献:
[1]王倩倩,吕霞.自拟中药方治疗急性疱疹性口炎33例临床观察[J].中医临床研究,2015,7(1):75-76.
[2]睢颖.口炎清颗粒为主治疗小儿疱疹性口炎50例疗效观察[J].浙江中医杂志,2014,49(9):669.
[3]叶森娣,舒香云,叶静梅,等. 输液式口腔冲洗法在疱疹性口炎患儿中的应用[J].护理实践与研究,2011,8(10):104-105.
[4]韩立,班付国,周红霞,等.高效液相色谱法测定板蓝根注射液中(R,S)-告依春的含量[J].中国兽药杂志,2014,48(4):32-34.
[5]王林林,史玉柱,王雪,等. 中药抗流感病毒研究进展[J].西北药学杂志,2012,27(6):600-604.
[6]刘文,郭世宁,武瑞.大青叶抗病毒的研究进展[J].中兽医医药杂志,2007,(3):73-74.
[7]周艳,罗阿利,韩丹,等.中药外治预防尖锐湿疣复发的临床观察[J].西北药学杂志,2014,29(4):408-410.
[8]曾聪彦,高玉桥,钟希文.悦康外感凉茶的薄层鉴别研究[J].中华中医药学刊,2008,26(10):2247-2248.
[9]国家药典委员会.中国药典2010年版[S].一部.北京:中国医药科技出版社,2010:179.
[10]叶文婷,卢绵,欧阳惠芳.板蓝根核苷类中薄层层析研究[J].临床医学工程,2010,17(2):46-47.
[11]黄际薇,麦海燕,江先合.岗梅感冒灵颗粒薄层色谱鉴别方法的研究[J].中国实用医药,2013,8(25):1-2.
[12]马琳,孟祥超,李兰芳.板蓝根药材及板蓝根颗粒中有机酸成分薄层色谱鉴别分析[J].国际医药卫生导报,2008,14(10):74-75.
[13]曾茂贵,李颖,高锦娟,等.双芩清解颗粒的质量标准研究[J].中国药师,2014,17(10):1649-1652.
[14]巩伟,赵庆华,张琨,等.HPLC法测定复方板柴口服液中表-告依春的含量[J].实用医药杂志,2014,31(2):155-156.
[15]吴静,陈丽芬.板蓝根颗粒浸膏中(R,S)-告依春的含量测定研究[J].大众科技,2014,16(8):107-108.
Study on the quality standard of Lanhua Granules
KANG Yuxia1,2,LEI Wan2,WANG Ying2,GUO Feiyan2,WANG Xiaojuan2*(1.College of Pharmacy,Shaanxi University of Chinese Medicine,Xianyang 712046,China;2.State Key Laboratory of Military Stomatology,Department of Pharmacy,School of Stomatology,the Fourth Military Medical University,Xi′an 710032,China)
Abstract:Objective To establish the quality standard of Lanhua Granules. Methods Radix isatidis,Foliumi isatidis and Caulis lonicerae stem in Lanhua Granules were identified qualitatively by TLC.The content of (R,S)-goitrin in the preparation was determined by HPLC.The chromatographic column was Spursil C18(250 mm×4.6 mm,5 μm), with methanol-water(7∶93) as the mobile phase, detection wavelength at 245 nm. Results Under the selected TLC conditions,the spots were clear,and the separation effect was good. (R,S)-goitrin showed a good linear relationship in the range of 0.30-2.12 μg·mL-1with r=0.999 7,and the average recovery was 87.5% with RSD 1.0% (n=9). Conclusion The method is specific,repeatable and simple, and can be used for the quality control of Lanhua Granules.
Key words:Lanhua Granules;(R,S)-goitrin; TLC;HPLC
(收稿日期:2015-06-11)
*通信作者:王晓娟,女,主任药师,硕士研究生导师
作者简介:康玉霞,女,在读硕士研究生
基金项目:口腔专科特色非标准制剂标准提高研究(编号:14ZJZ06)
中图分类号:R284
文献标志码:A
文章编号:1004-2407(2016)02-0138-05
doi:10.3969/j.issn.1004-2407.2016.02.009
