顶空毛细管气相色谱法测定奥硝唑原料的溶剂残留
2016-03-16王嫦鹤刘雪峰苗莉莉陕西省食品药品检验所西安710061
王 发,王嫦鹤,王 莉,刘雪峰,苗莉莉(陕西省食品药品检验所,西安 710061)
顶空毛细管气相色谱法测定奥硝唑原料的溶剂残留
王发,王嫦鹤,王莉,刘雪峰,苗莉莉(陕西省食品药品检验所,西安710061)
摘要:目的建立奥硝唑原料药中5种有机溶剂残留量的顶空毛细管气相色谱测定法。方法使用Agilent DB-624毛细管气相色谱柱(30 m×0.32 mm×0.18 μm),FID检测器,进样口温度150 ℃,检测器温度250 ℃。程序升温45 ℃,保持15 min,然后以40 ℃·min-1的速率升至220 ℃。顶空进样,平衡温度85 ℃,平衡时间30 min。结果在上述条件下,甲醇,乙醇,乙酸乙酯,二氯乙烷和环氧氯丙烷的分离度均在2.0以上,线性关系良好(r在0.997 8~0.999 9之间),平均回收率(n=6)在100.9%~103.4%之间,RSD在1.4%~3.3%之间。结论该法简单、准确,可用于奥硝唑原料中残留溶剂的测定。
关键词:奥硝唑;顶空进样法;毛细管气相色谱法;溶剂残留
奥硝唑是继甲硝唑、替硝唑后上市的抗厌氧菌和抗滴虫药物,其抗厌氧菌、抗原生质感染和抗毛滴虫的作用均高于前两者。临床上用于毛滴虫引起的男女泌尿生殖道感染,阿米巴原虫引起的肠、肝阿米巴虫病,贾第鞭毛虫病,厌氧菌感染、术后感染和口腔感染等。奥硝唑的耐受性良好,不良反应较少,主要是皮肤变态反应、消化系统反应、循环系统反应等[1-3]。根据标准的查询情况,现行的USP、EP、BP、JP均没有收载奥硝唑原料。《中国药典》(2010年版)第二增补本[4]和国家食品药品监督管理局进口药品标准JX20100049[5]收载有奥硝唑,但未对残留溶剂进行控制或只对甲醇、二氯乙烷和环氧氯丙烷3种残留溶剂进行检测。奥硝唑原料在合成、纯化及精制过程中可能使用的溶剂有甲醇、乙醇、乙酸乙酯、二氯乙烷和环氧氯丙烷等。本实验参考《中国药典》2010年版二部附录“残留溶剂测定法”项下残留溶剂及限度规定[6]和部分文献方法[7-10],建立了奥硝唑原料药中甲醇、乙醇、乙酸乙酯、二氯乙烷和环氧氯丙烷的毛细管气相色谱测定方法,从方法学验证结果来看,该方法简便准确、重复性好,可用于奥硝唑原料药中残留溶剂的质量控制。
1仪器与试药
1.1仪器安捷伦6890N气相色谱仪,氢火焰离子检测器(FID),安捷伦G1888型自动顶空进样器,梅特勒AE-240电子分析天平,中惠HA-300氢空一体机。
1.2试药甲醇、无水乙醇、二氯乙烷、乙酸乙酯和环氧氯丙烷均为分析纯,N-N二甲基乙酰胺为色谱纯;奥硝唑原料,共21批,分别由8个不同企业提供,记作S1~S21。
2方法与结果
2.1气相色谱条件检测器:氢火焰离子检测器(FID);进样口温度:150 ℃;检测器温度:250 ℃;色谱柱:DB-624毛细柱(30 m×0.32 mm×0.18 μm);程序升温,初始温度:45 ℃,保持15 min,然后以40 ℃·min-1的速率升至220 ℃;顶空瓶平衡温度:85 ℃;平衡时间:30 min;顶空进样,进样时间:0.5 min。
2.2对照品溶液制备精密称取环氧氯丙烷0.999 5 g,二氯乙烷0.053 80 g,置于100 mL量瓶中,用N,N-二甲基乙酰胺(以下简称溶解介质)稀释至刻度,摇匀,作为对照品储备液①。精密称取甲醇1.507 8 g、无水乙醇2.468 5 g和乙酸乙酯2.527 4 g,置于同一100 mL量瓶中,精密加入对照品储备液① 5 mL,用溶解介质稀释至刻度,摇匀,作为对照品储备液②。
精密量取对照品储备液② 10 mL,置于100 mL量瓶中,用溶解介质稀释至刻度,即得对照品溶液(甲醇、乙醇、乙酸乙酯、二氯乙烷和环氧氯丙烷的质量浓度分别为1.507 8,2.468 5 ,2.527 4,0.002 690 和0.049 98 g·L-1)。
2.3样品溶液制备取奥硝唑原料1.0 g,精密称重,置于顶空瓶中,加入溶解介质2.0 mL,密封,即得。
2.4系统适用性实验精密量取上述对照品溶液和溶解介质各2.0 mL,置于顶空瓶中,密封,按照上述色谱条件进行测定,结果表明,该色谱条件下各组分分离度均符合要求,溶解介质对样品的测定无干扰。见图1。
2.5标准曲线制备精密量取对照品储备液②适量,用溶解介质逐步稀释制成质量浓度(以甲醇计)为0.904 7,1.206 2,1.507 8,1.809 4和2.110 9 g·L-1的溶液,作为线性对照溶液,按照上述气相色谱条件测定,以对照品溶液峰面积为纵坐标(Y)、质量浓度为横坐标(X),建立线性方程,结果见表1。
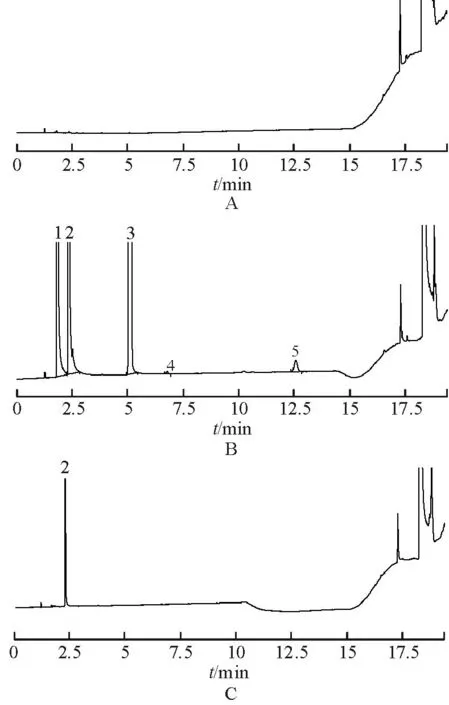
图1GC图
a.溶解介质;B.对照品;C.样品;1.甲醇;2.乙醇;3.乙酸乙酯;4.二氯乙烷;5.环氧氯丙烷
Fig.1 GC chromatograms
a. blank solvent;B. reference substances;C .sample;1.methanol;2.ethanol;3.ethyl acetate;4.dichloroethane;5.epichlorohydrin
表15种残留溶剂的线性方程和线性范围
Tab.1 Regression equations and linear ranges of calibration curves of 5 residual solvents
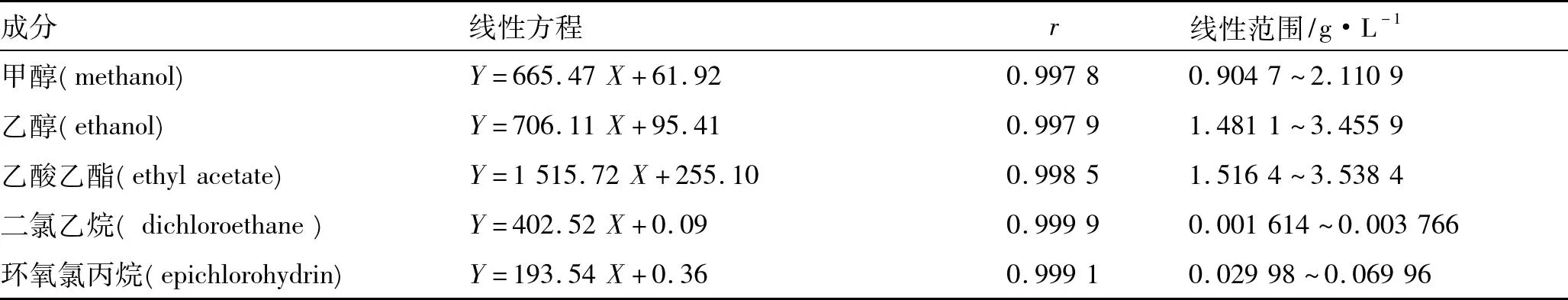
成分线性方程r线性范围/g·L-1甲醇(methanol)Y=665.47X+61.920.99780.9047~2.1109乙醇(ethanol)Y=706.11X+95.410.99791.4811~3.4559乙酸乙酯(ethylacetate)Y=1515.72X+255.100.99851.5164~3.5384二氯乙烷(dichloroethane)Y=402.52X+0.090.99990.001614~0.003766环氧氯丙烷(epichlorohydrin)Y=193.54X+0.360.99910.02998~0.06996
2.6精密度实验精密量取对照品溶液6份,每份2.0 mL,按照上述色谱条件分别进样测定,结果测得6次甲醇、乙醇、乙酸乙酯、二氯乙烷和环氧氯丙烷峰面积的RSD分别为2.0%,2.4%,2.2%,3.9%和3.4%。实验结果表明,本方法精密度良好。
2.7重复性实验制备同一样品溶液6份,按照上述色谱条件分别进样测定,结果本品中乙醇的含量为0.014%,RSD为2.3%,甲醇、乙酸乙酯、二氯乙烷和环氧氯丙烷均未检出。实验结果表明,本方法重复性良好。
2.8检测限实验精密量取不同体积的对照品溶液,用溶解介质逐步稀释,按照上述色谱方法进样,记录色谱图,当所测残留溶剂的信噪比为3∶1时,甲醇、乙醇、乙酸乙酯、二氯乙烷和环氧氯丙烷对应的质量浓度分别为0.000 60,0.000 99,0.001 0,0.001 1和0.004 0 g·L-1。
2.9回收率实验精密称取已知甲醇、乙醇、乙酸乙酯、二氯乙烷、环氧氯丙烷含量的同一奥硝唑原料6份,每份1.0 g,分别置于顶空瓶中,分别精密加入对照品溶液2.0 mL,密封,按照上述色谱条件分别进样测定,计算回收率。甲醇、乙醇、乙酸乙酯、二氯乙烷和环氧氯丙烷的回收率分别为100.9%,101.0%,101.4%,103.4%和102.1%,RSD分别为1.5%,1.7%,1.4%,2.4%和3.3%。实验结果表明,本方法回收率良好。
2.10奥硝唑样品的测定按照2.2和2.3项下方法,分别制备对照品溶液和样品溶液,按照上述色谱条件进行测定。结果显示,甲醇、乙酸乙酯、二氯乙烷和环氧氯丙烷在全部21批样品中均未检出。乙醇有10批样品检出,检出量远小于《中国药典》2010年版二部的限度规定,最高含量为0.02%,为药典对乙醇规定限度的4%。结果见表2。
表2奥硝唑溶剂残留测定结果
Tab.2 Results of residual solvents in ornidazole
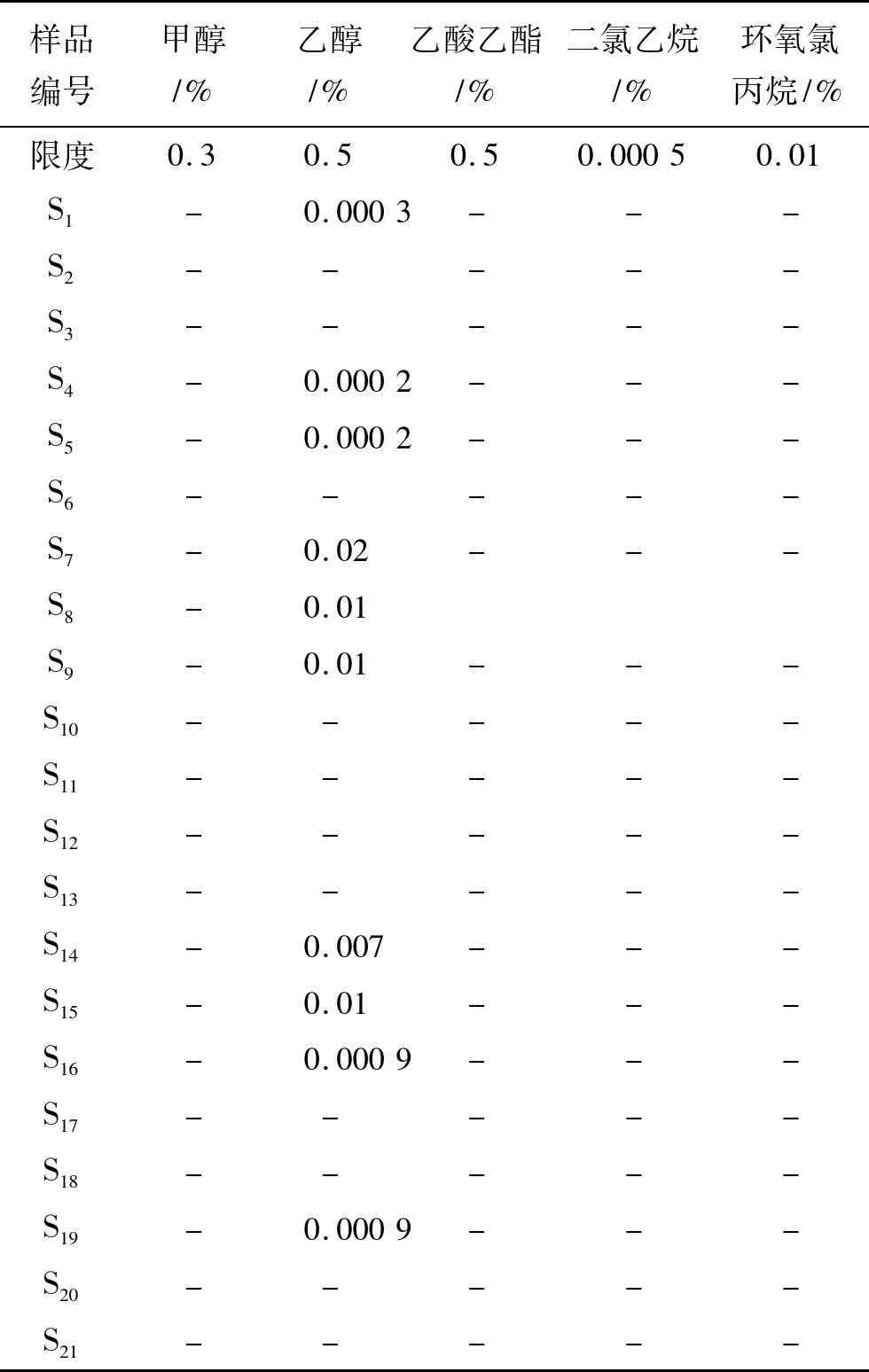
样品编号甲醇/%乙醇/%乙酸乙酯/%二氯乙烷/%环氧氯丙烷/%限度0.30.50.50.00050.01S1-0.0003---S2-----S3-----S4-0.0002---S5-0.0002---S6-----S7-0.02---S8-0.01S9-0.01---S10-----S11-----S12-----S13-----S14-0.007---S15-0.01---S16-0.0009---S17-----S18-----S19-0.0009---S20-----S21-----
注:-表示未检出。
3讨论
3.1溶解介质的选择顶空进样通常以水为溶解介质,对于非水溶性药物,多采用N,N-二甲基甲酰胺或其他适宜溶剂。溶解性实验表明,奥硝唑在水中微溶,在N,N-二甲基甲酰胺和N,N-二甲基乙酰胺中均极易溶解。根据奥硝唑和5种待测残留溶剂的溶解性,应选择N,N-二甲基甲酰胺或N,N-二甲基乙酰胺。因N,N-二甲基甲酰胺中常含有微量的甲醇,对测定有干扰,因此选择N,N-二甲基乙酰胺作为溶解介质。实验表明,奥硝唑原料和5种残留溶剂对照品均在N,N-二甲基乙酰胺中完全溶解,且N,N-二甲基乙酰胺作为溶解介质对实验无干扰。
3.2顶空温度的选择顶空平衡温度的选择主要根据样品中待测溶剂的沸点和溶解介质的沸点而定。残留溶剂的沸点越高,需要选择的顶空平衡温度也较高。但随着温度的升高,样品热分解产物对测定干扰的风险增大,因此,在保证检测方法灵敏度的基础上,应选择较低的顶空平衡温度,以避免样品热降解产物的干扰。实验结果表明,本方法在85 ℃时即可保证检测的灵敏度,因此选择85 ℃作为顶空温度,选择较低的顶空温度可以有效避免奥硝唑原料在较高温度时产生热降解产物对测定的干扰。
参考文献:
[1]方正明,吕红,姚蓝.奥硝唑不同剂型抗阴道毛滴虫作用的比较研究[J].热带医学杂志,2010,10(11):1274-1276.
[2]吕红,方正明,龚凡荣,等.奥硝唑凝胶剂体内外抗阴道毛滴虫作用[J].中国医院药学杂志,2010,30(14):1203-1206.
[3]刘柳芳,黄文荣,李雪飞.奥硝唑对牙周炎患者疗效以及炎症因子影响的临床价值分析[J].医学综述,2014,20(9):1703-1705.
[4]国家药典委员会.中国药典2010年版:第二增补本[S].北京:中国医药科技出版社,2010:334-335.
[5]JX20100049[S].国家食品药品监督管理局进口药品注册标准.
[6]国家药典委员会.中国药典2010年版[S].二部.北京:中国医药科技出版社,2010:61-65.
[7]王嫦鹤,雷琨,王荪璇.顶空毛细管气相色谱法测定乌拉地尔原料药的溶剂残留量[J].中国医院药学杂志,2013,33(3):218-220.
[8]高秀蕊,徐英,孙士民,等.顶空进样气相色谱法测定奥美拉唑原料药中的残留溶剂[J].齐鲁药事,2008,27(12):716-717.
[9]吕卓,张秉华,王莉,等.食用植物油中残留溶剂的气相色谱分离与测定[J].西北药学杂志,2014,29(1):24-27.
[10]张秉华,马雯霞,王发.气相色谱法测定硝酸咪康唑原料的溶剂残留[J].西北药学杂志,2014,29(4):368-370.
Determination of the residual solvents in ornidazole by headspace capillary GC
WANG Fa,WANG Changhe,WANG Li,LIU Xuefeng,MIAO Lili (Shaanxi Province Institute for Food and Drug Control,Xi′an 710061,China)
Abstract:Objective To establish a headspace capillary GC method for the determination of the residual solvents in ornidazole.Methods An Agilent DB-624 capillary column(30 m×0.32 mm×0.18 μm) was used. The inlet temperature was 150 ℃ and the FID detector temperature was 250 ℃.The oven temperature was initially held at 45 ℃ for 15 min and then programmed to 220 ℃ at 40 ℃·min-1. The headspace sampling was used at heated temperature 85 ℃ for 30 min. Results The linear correlation cofficients of this method for methanol,ethanol, ethyl acetate,dichloromethane,epichlorohydrin were between 0.997 8-0.999 9,respectively. All the average recoveries were between 100.9%-103.4%,RSDs were between 1.4%-3.3%.Conclusion The method was simple,accurate,so it is proposed for the determination of the residual solvents in ornidazole.
Key words:ornidazole;headspace injecting;capillary GC; residual solvents
(收稿日期:2015-06-23)
中图分类号:R927.2
文献标志码:A
文章编号:1004-2407(2016)02-0146-03
doi:10.3969/j.issn.1004-2407.2016.02.011
