手性氨基醇的合成进展
2016-02-07冯瑞
冯 瑞
(河南南阳医学高等专科学校,河南 南阳 473000)
手性氨基醇的合成进展
冯 瑞
(河南南阳医学高等专科学校,河南 南阳 473000)
本文综述了近几年以糖、酮、胺、氨基酸、醇等为原料合成新型手性氨基醇的方法。文中共涉及到40种新物质,并对有些物质作为手性催化剂或配体,在不对称合成中的效果进行评价。
手性氨基醇;合成;不对称合成
手性氨基醇是一类重要的具有光学活性的手性化合物。由于氨基醇分子中具有良好配位能力的N原子和O原子,可与多种元素形成络合物,是合成手性催化剂或配体及某些手性化合物的重要手性源,因此被广泛应用于精细化工、材料、医药、生物学等有机合成和药物中,如苏氨醇、丙胺醇、苯丙氨醇等已被应用于多肽类药物和喹诺酮类手性药物中[1]。手性氨基醇具有很高的立体选择性和催化效率,最成功的是广泛应用于醛的催化不对称烷基化、芳基化以及不对称迈克尔加成等一系列反应中[2]。因此,研究手性氨基醇的合成,具有很强的实际应用价值。
1 以糖为手性源
1.1 以单糖为原料
施梅等[3]以D-葡糖胺为原料设计合成一系列新型手性β-氨基醇。D-葡糖胺首先与氯甲酸甲酯缩合得到化合物1,再经过甲基化得到化合物2,苄叉保护得到化合物3,经过碱性水解反应,得到4,6-O-苄叉基-2-脱氧-2-氨基-α-D-吡喃葡萄糖甲苷4。进一步将化合物4的糖环2-位氨基通过N-烃化反应或N-磺酰化反应合成得到10种新型手性β-氨基醇5a~5j,ee值在58%~91%,这些化合物中有的将是性能很好的催化剂。合成路线见Scheme 1。

Scheme 1
1.2 以双糖为原料
侯学会等[4]以蔗糖6为起始原料,经缩水、水解和缩合反应制得一种新型C12糖——2-[1R-(1,4:3,6-二缩水果糖)]-异甘露醇7。以7为手性拆分剂,用甲醇作溶剂,拆分(R,S)-β-氨基醇(ArOCH2CH(OH) CH2NH2),得到(β)-氨基醇和(S)-β-氨基醇,收率分别为40.5%和40.1%,ee值均大于99%,效果很好。具体反应路线见Scheme 2。

Scheme 2
2 以酮为手性源
陈长福[5]以便宜、易得的天然樟脑为原料,分别经过六步合成了2个含有樟脑烷骨架的手性氨基醇配体8和9。
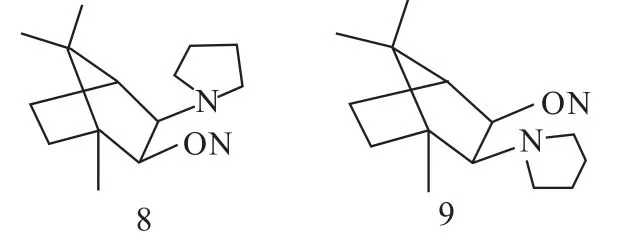
手性配体8和手性配体9催化前手性二乙基锌对苯甲醛不对称加成反应,结果配体8催化得到(S)-构型仲醇,配体9催化得到(R)-构型仲醇,最好的化学收率ee值分别高达100%和98%,反应路线如Scheme 3所示。

Scheme 3
3 以胺为手性源
韩美玲等[6]以便宜易得的(S)-α-苯乙胺10为原料,经过一步反应制得了一系列新型手性氨基醇配体11a~11d。将该类配体应用到Ru催化芳香酮的不对称转移氢化反应中,分别得到71%~100%的转化率和67%~95%的对应选择性。反应路线如Scheme 4所示。

Scheme 4
4 以氨基酸为手性源
由于氨基酸在自然界中广泛存在,因此以廉价、易得的氨基酸为手性源合成手性氨基醇是最常见的方法。
4.1 以苯甘氨酸为原料
刘丰良、肖清波、沈霞等[7]将叔丁基苯胺经二甲基化、甲酰化得到5-叔丁基-2-二甲氨基苯甲醛12,与 L-苯甘氨酸经LiAlH4直接还原,得到二齿手性氨基醇13,经缩合、还原,得到新型三齿手性氨基醇(2S)-2-[(5-叔丁基-2-二甲氨基)苯基]甲氨基-2-苯基乙醇14,ee值为98%。反应路线如Scheme 5所示。

Scheme 5
刘丰良、尹军、肖清波等[8]以L-苯甘氨酸为原料,经酯化、格氏反应得到产物 15,再与5-叔丁基-2-二甲氨基苯甲醛 16经缩合、还原反应,得到新型三齿手性氨基醇(2S)-2-(5-叔丁基-2-二甲氨基)苯甲氨基17,总收率 35%。反应路线如Scheme 6所示。
布洛芬为手性非甾体类抗炎药,具有较强的解热、镇痛、抗炎作用。研究表明,该药活性源于右旋布洛芬对映体,而左旋的为非活性成分,且具有潜在的包括胃肠道毒性、水钠潴留等毒副作用。初步运用 HNMR考察发现,化合物17对布洛芬对映体有手性识别能力。

Scheme 6
刘丰良、刘言萍、沈霞等[9]以L-苯甘氨酸为手性源,经甲酯化、格氏化两步反应得到化合物18,L-苯甘氨酸直接还原得到化合物19,N,N-二甲基苯胺通过对位溴化、Vilsmeier反应得到醛20。18和19分别与醛20经缩合、还原反应得到新型多齿手性氨基醇21和22,产率分别为73.8%和83.8%。该反应路线具有反应条件温和、收率高等优点(Scheme 7)。
潘圣强等[10]从易得原料D-苯甘氨酸出发,经酯化、N-烷基化及还原等三步反应合成了5个新颖手性β-氨基醇23a、23b、23c、24a、24b,反应路线如Scheme 8所示。
以上面5个手性β-氨基醇作为手性配体,分别对苯甲醛25进行不对称催化,得到化合物26a、26b、26c。产率为84%~92%,ee值为10.1%~61.8%,实验证明25是一种很好的手性催化剂。反应路线如Scheme 9所示。
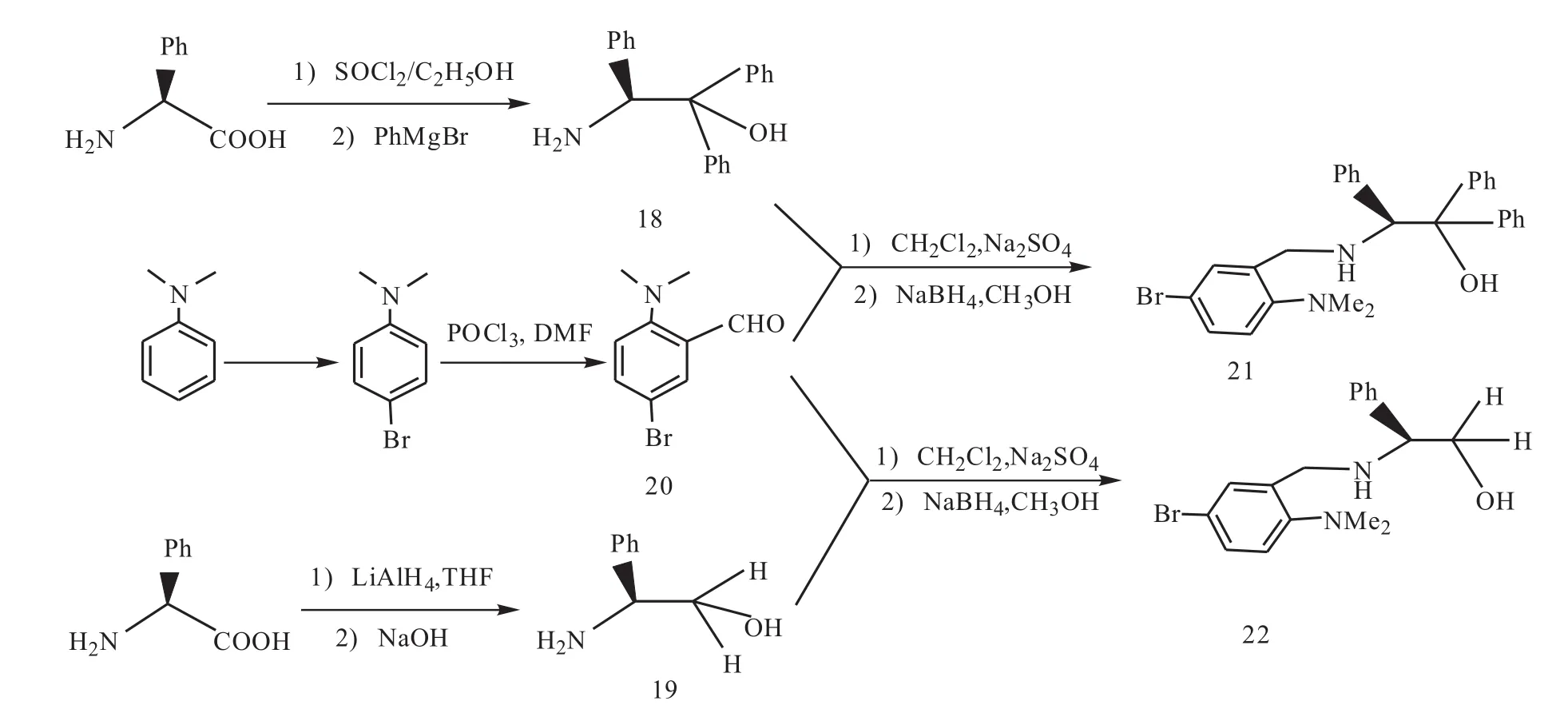
Scheme 7

Scheme 8

Scheme 9
4.2 以L-亮氨酸为原料
刘丰良、徐军、刘言萍等[11]以N,N-二甲基苯胺为原料,经对位溴化、邻位甲酰化得到5-溴-2-(二甲氨基)苯甲醛27。L-亮氨酸经酯化、格氏反应得到二齿手性氨基醇28。将27与28经缩合、还原,得到三齿手性氨基醇29,ee值为62%。反应路线如Scheme 10所示。其中28和29作为手性溶剂,实验表明都没有表现出对手性羧酸类药物布洛芬和扁桃酸对映体的手性识别能力,但化合物29对布洛芬及扁桃酸的一对对映体手性碳上的质子有良好的手性识别能力。
刘丰良、李媛媛、王文革等[12]将甲基苯胺经甲基化、甲酰化得到N,N,N-三甲基-2-氨基苯甲醛30。L-亮氨酸经酯化、格氏反应得到二齿手性氨基醇31。将30与31经缩合、还原,得到三齿手性氨基醇32,ee值为62%。反应路线如Scheme 11所示。其中考察了主体三齿手性氨基醇对客体布洛芬和扁桃酸对映体的手性识别能力,结果表明,当主客体物质的量之比为1∶1时,化合物32对布洛芬及扁桃酸消旋体的α位甲基质子分别产生11.2Hz和9.2Hz的化学位移差值。

Scheme 10

Scheme 11
4.3 以L-丝氨酸为原料
赵文献等[13]以L-丝氨酸为手性源,经过酯化、缩合、还原氨化、关环反应合成33,然后用无水THF作溶剂,催化量碘存在下与异丙基溴化镁发生格式反应,成功得到了一种具有光学活性的新的手性β-氨基醇34(手性胡椒醛基氮杂环丙醇),反应路线如Scheme 12所示。首次将其应用于催化二乙基锌对苯甲醛的不对称加成反应中,得到了较高的产率82.8%和较好的ee值76.1%。
赵瑞娟等[14]以L-丝氨酸为手性源,经酯化、缩合、还原氨化、关环等反应,得到含1个手性中心的茚满基氮杂环丙基羧酸酯35,之后与环丙基溴化镁发生格氏试剂反应,于酸性条件下水解得到一种新的茚满基氮杂环丙基二环丙基三级醇手性配体36,产率83.86%,反应路线如Scheme 13所示。这为合成这类具有光学活性化合物提供了一条高效便捷的方法。

Scheme 12

Scheme 13
4.4 以其它L-氨基酸为原料
此外,杨光云等[15]以天然的L-亮氨酸、L-缬氨酸、L-苯丙氨酸为原料,经还原、缩合,合成了3种(S)-2-咪唑基手性醇。李俊奇等[16]以天然L-苯丙氨酸为起始原料,经简单的两步反应生成手性β-氨基醇。
4.5 以含硫原子的L-甲硫氨酸为原料
赵文献等[17]以L-甲硫氨酸为手性源,经酯化、缩合、还原氨化及格氏试剂反应,合成了一种新型的含硫二茂铁基的β-氨基醇手性配体37[4-N-(二茂铁亚甲基)-6-甲硫基-3-乙基-3-己醇]。以L-甲硫氨酸为手性源,合成手性配体和应用的研究报道为数不多,该论文具有重要的参考价值。合成路线如Scheme 14所示。
5 以环状氨基醇为手性源
叶海伟等[18]以(R)-3-羟基吡咯烷38为原料,先经氨基选择性保护和脱保护反应,再与环氧环己烷开环反应制得混旋体39,最后经化学拆分制得光学纯的目标产物40 [1R,2R)-2-((R)-3-(苄氧基)吡咯烷基)环己醇(RRR-2)] ,它是合成一种新型抗心律失常药物维纳卡兰的关键中间体,总收率达38%(文献收率15%),是合成RRR-2的一种很好的方法,具体合成路线如Scheme 15所示。
手性氨基醇具有广泛用途,所以合成手性氨基醇仍是学者们未来的重要任务之一[19-20],寻找新型手性催化剂或配体及某些手性化合物,具有深远的意义。
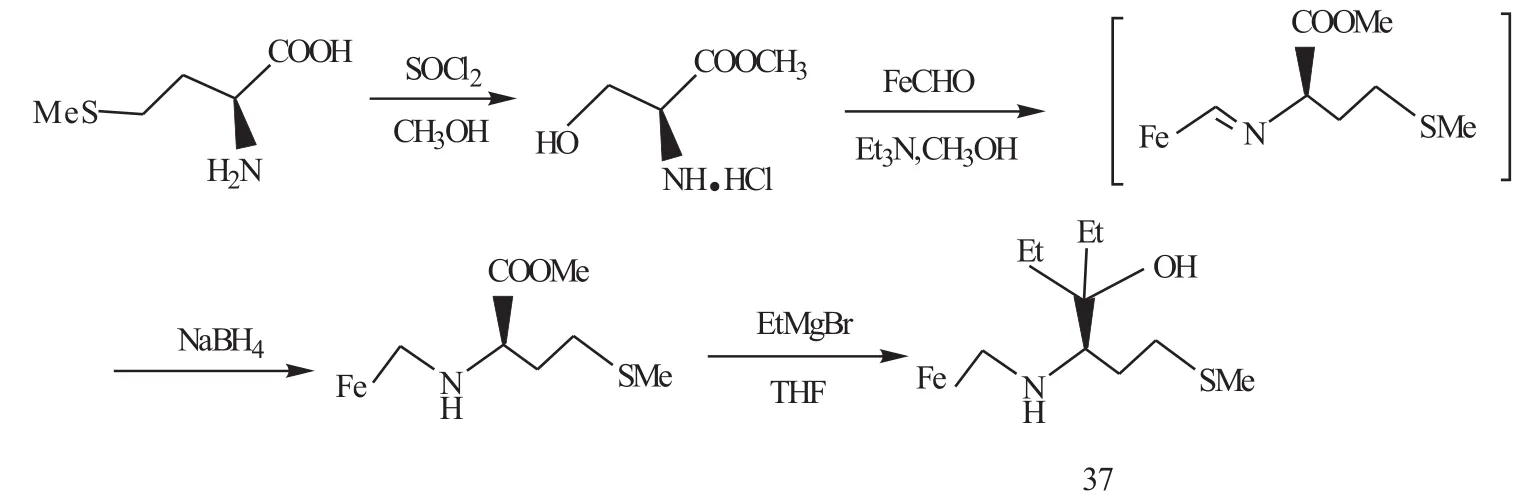
Scheme 14

Scheme 15
[1] 王乃兴.利用天然手性源合成复杂手性化合物的方法[J].中国科学:化学,2010,40:295-302.
[2] WANG M C, LIU Z K, LI S, et al. An experiment and theoretical study on free ligand conformational preferences and enantioselectivity relationship for the asymmetric addition of diethylzinc to benzaldehyde [J].Tetrahedron: Asymmetry, 2010, 21: 486-493.
[3] 施梅,周宏,薛蒙伟.基于D-葡糖胺的手性β-氨基醇的合成[J].化学研究与应用,2015,27(1):70-71.
[4] 侯学会,赵立魁,张京玉.新型C12糖的合成及其在β-氨基醇手性拆分中的应用[J].合成化学,2012,20(4):438-440.
[5] 陈长福.含樟脑烷骨架的手性氨基醇配体的合成与应用[D].郑州:郑州大学,2012.
[6] 韩美玲,陈立功.博士论坛化工分论坛论文集[C].天津:天津大学,2011.
[7] 刘丰良,肖清波,沈霞,等.L-苯甘氨酸衍生物新型三齿手性氨基醇的合成[J].广州化学,2011, 36(4):17-20.
[8] 刘丰良,尹军,肖清波,等.新型手性氨基醇的合成及其对布洛芬对映异构体的手性识别[J].广州化学,2012,37(1):19-21.
[9] 刘丰良,刘言萍,沈霞,等.新型多齿手性氨基醇的合成和结构表征[J].化学研究,2012,23(4):6-8.
[10] PAN S Q, ZHANG C H, LI Y, et al. Convenient synthesis of chiral β-amino alcohols and their asymmetric catalytic reactions[J].J.Org. Chem., 2011, 31(5): 1-4.
[11] 刘丰良,徐军,刘言萍,等. L-亮氨酸衍生物手性氨基醇的合成与应用[J].广州化学,2011,36(1):1-4.
[12] LIU F L, LI Y Y, WANG W G, et al. Synthesis of chiral amino alcohols from L-leucine and their chiral recognition of enantiomers of ibuprofen and mandelic acid[J].J.Org. Chem., 2011,31(5): 747-751.
[13] 赵文献,刘冠军,张朋飞,等.一种新的手性氨基醇配体的合成及在二乙基锌对苯甲醛的不对称加成反应中的应用[J].商丘师范学院学报,2012,28(9):42-43.
[14] 赵瑞娟,张安安,孔伟光,等.一种新的光学纯茚满基氮杂环丙基 二环丙基三级醇手性配体的合成与表征[J].商丘师范学院学报,2013,29(9):55-58.
[15] 杨光云,毛璞,杨亮茹,等.咪唑基手性醇的合成及条件优化[J].精细石油化工,2011,28(4):51-54.
[16] 李俊奇,乔治国,崔付娜,等.一种新型手性席夫碱和手性β-氨基醇配体的合成[J].浙江工业大学学报,2011,39(5):508-510.
[17] 赵文献,胡春华,刘念,等.新型4-N-(二茂铁亚甲基)-6-甲硫基-3-乙基-3-己醇手性配体的合成[J].合成化学,2011,19(4):508-510.
[18] 叶海伟,俞传明,钟为慧,等.(1R,2R)-2-((R)-3-(苄氧基)吡咯烷基)环己醇的合成研究[J].高校化学工程学报,2014,28(3):606-611.
[19] Schwab R S, Galetto F Z, Azeredo J B, et al. Organic catalytic asymmertric aldol reactions mediated by a cysteine- derivd prolinamide[J].Tetrahedron Lett., 2008, 49(34): 5049-5097.
[20] XU J X. Influence of the electronic effect of catalysts on the enantioselectivity:applicability and complexity[J].Curr.Org. Synth., 2010(6): 650-676.
Progress in Synthesis of Chiral Amino Alcohols
FENG Rui
(Nanyang Medical College, Nanyang 473000, China)
In this paper, the synthesis methods of novel chiral amino alcohols were reviewed with sugars, ketones, amines, amino acids, alcohols et al, as raw materials in recent years. The paper involved 40 kinds of new material, and evaluated for the effect of some substances as chiral catalysts and ligands in asymmetric synthesis.
chiral amino alcohols; synthesis; asymmetric aynthesis
TQ 226.34
A
1671-9905(2016)12-0019-06
冯瑞(1975-),女,副教授,硕士,主要从事有机合成的研究,电话:13525107689 , E-mail: fengrui20032006@163.com
2016-10-14
