溶解度曲线及其应用
2016-02-06罗明奎
□罗明奎
溶解度曲线及其应用
□罗明奎
溶解度曲线及其应用是中考常考的知识点,多通过给出两种或三种物质的溶解度曲线,考查与溶液的形成及溶解度相关知识的应用.下面我们通过一道基础题,并对该题进行变形和拓展,来帮助同学们更好地掌握该部分内容.
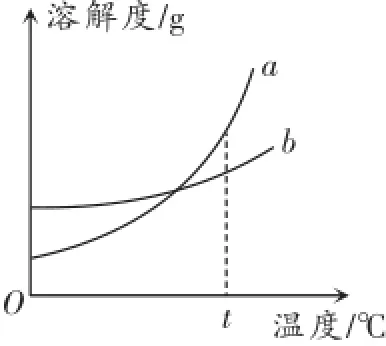
例题:如图是a、b两种固体物质的溶解度曲线.从图中你能得到哪些信息?

解析:本题通过给出溶解度曲线考查溶解度的含义及应用.溶解度曲线表示某种物质在不同温度时溶解度变化的规律,因此根据溶解度曲线可判断该物质受温度影响的情况,也可以查出某物质在某温度时的溶解度.此外,如果同时给出几种物质的溶解度曲线,可以比较它们在某一温度时溶解度的大小.如果溶解度曲线相交于一点,表示该温度时几种物质的溶解度相同.根据溶解度曲线还可以判断出该物质适合的结晶方法,如果某物质的溶解度受温度影响较大,一般采用降温结晶的方法;如果某物质的溶解度受温度影响变化不大,一般采用蒸发结晶的方法.本题具有很强的开放性,只要围绕溶解度知识回答即可.
答案:(1)a、b两种物质的溶解度均随温度的升高而增大;(2)t℃时,a、b的溶解度相等;(3)温度低于t℃时,同温下,b的溶解度大于a的溶解度;(4)温度高于t℃时,同温下,a的溶解度大于b的溶解度;(5)从溶液中分离出a应采用降温结晶的方法.(合理即可)
变式一:下图是a、b、c三种物质的溶解度曲线.由图示判断下列说法中不正确的是().
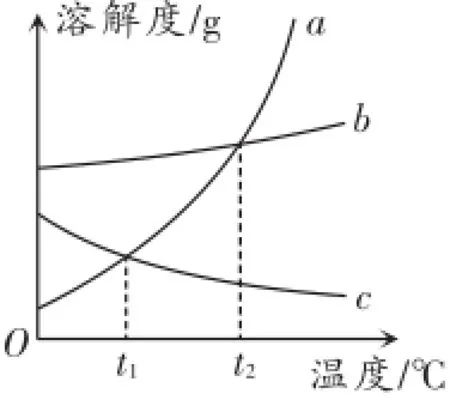
A.在t1℃时,a的溶解度等于c的溶解度
B.c的溶解度随温度的升高而减小
C.a的饱和溶液从t2℃降温至t1℃时变为不饱和溶液
D.当a中含有少量b时,可以用降温结晶的方法提纯a
解析:根据所给溶解度曲线可知,在t1℃时,a的溶解度等于c的溶解度,故A选项正确;c的溶解度随温度的升高而减小,故B选项正确;由于a的溶解度随温度升高而增大,因此a的饱和溶液从t2℃降温至t1℃时会有a晶体析出,剩余溶液仍为饱和溶液,故C选项错误;由于a的溶解度受温度影响变化较大,b的溶解度受温度影响变化不大,因此当a中含有少量b时,可以用降温结晶的方法提纯a,故D选项正确.
答案:C
变式二:根据如图所示信息判断,下列叙述不正确的是().
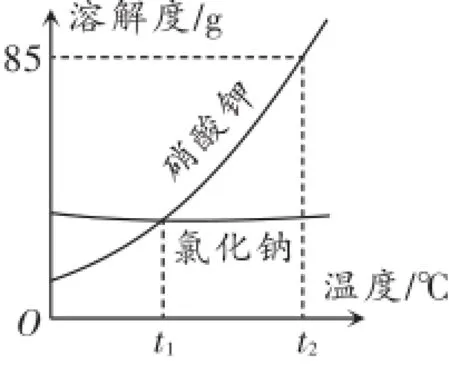
A.硝酸钾的溶解度随温度升高而增大
B.t1℃时,氯化钠和硝酸钾的溶解度相同
C.将t2℃时的硝酸钾饱和溶液降温到t1℃,有晶体析出
D.t2℃时,80g硝酸钾溶于100g水中可制得饱和溶液
解析:本题通过给出具体物质的溶解度曲线考查溶解度曲线的应用.根据二者的溶解度曲线可判断A、B、C正确.由于t2℃时硝酸钾的溶解度是85g,故t2℃时100g水中溶解85g硝酸钾刚好达到饱和状态,因此t2℃时溶解80g硝酸钾,制得的不是饱和溶液.
答案:D
变式三:下图是甲、乙两种固体物质的溶解度曲线.
(1)t2℃时,甲物质的溶解度为
.
(2)从图中你还能获得哪些信息?(任填一条).
(3)分析t1℃时,将10g乙物质放入100g水中,充分溶解后所得的溶液是.(选填“饱和”或“不饱和”)溶液.
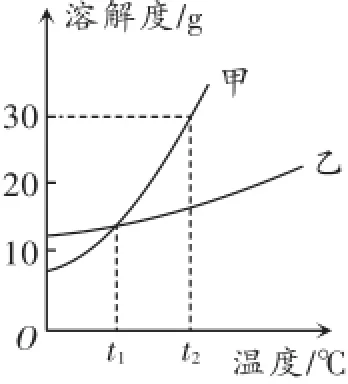
解析:本题考查溶解度曲线的应用.(1)根据甲的溶解度曲线可知t2℃时甲的溶解度为30g.(2)根据基础题答出一条即可.(3)根据t1℃时乙物质的溶解度大于10g,因此t1℃时将10g乙物质放入100g水中,充分溶解后所得的溶液是不饱和溶液.
答案:(1)30g;(2)甲、乙的溶解度均随温度的升高而增大;(3)不饱和
专项练习:氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示:

(1)30℃时,硝酸钾的溶解度为.
(2)等质量的两种物质的饱和溶液从40℃降温到10℃时析出晶体更多的是.
(3)若两种物质的溶解度相等,此时所对应的温度范围在之间.
(4)下图中能表示KCl溶解度曲线的是
(选填“a”或“b”).
参考答案:(1)45.8g(2)硝酸钾(3)20℃~30℃(4)b

