急性缺血性卒中静脉应用阿替普酶纳入及排除标准的科学声明(第一部分)
2016-01-18沈东超王子璇肖伏龙张玮艺张潇潇张宁王春雪
沈东超,王子璇,肖伏龙,张玮艺,张潇潇,张宁,王春雪
本声明中讨论的排除标准内容仅包括美国心脏协会(American Heart Association,AHA)/美国卒中协会(American Stroke Association,ASA)指南,美国食品和药品管理局(Food and Drug Administration,FDA)药品说明,尤其是唯一被批准用于急性缺血性卒中治疗的组织型纤溶酶原激活剂——阿替普酶说明中的禁忌证、风险、警告及排除标准内容。本声明未包括其他国际指南或其他国家对于阿替普酶的应用限制,因为这些不涵盖在本声明内容之内。但在确定每条排除标准时,我们回顾并参考了国际上的研究。文献搜索方法仅见于线上阅读内容中的“补充数据”部分。
本声明意于针对阿替普酶,而非其他或所有种类的溶栓药物,且仅适用于静脉应用阿替普酶,而不包括其他介入性或经动脉使用阿替普酶进行血管再通的治疗方法。不同于静脉应用阿替普酶已得到FDA批准,上述方法仍存在许多争议,目前尚未获得FDA认可。
推荐意见按照AHA标准确定(表1,表2)。所有撰写小组成员均有机会参与推荐意见编写及最终版声明的核准。本声明在经AHA科学顾问和协调委员会审批前,需经AHA内部广泛的同行评论,卒中委员会审查,以及科学声明监理会认可。
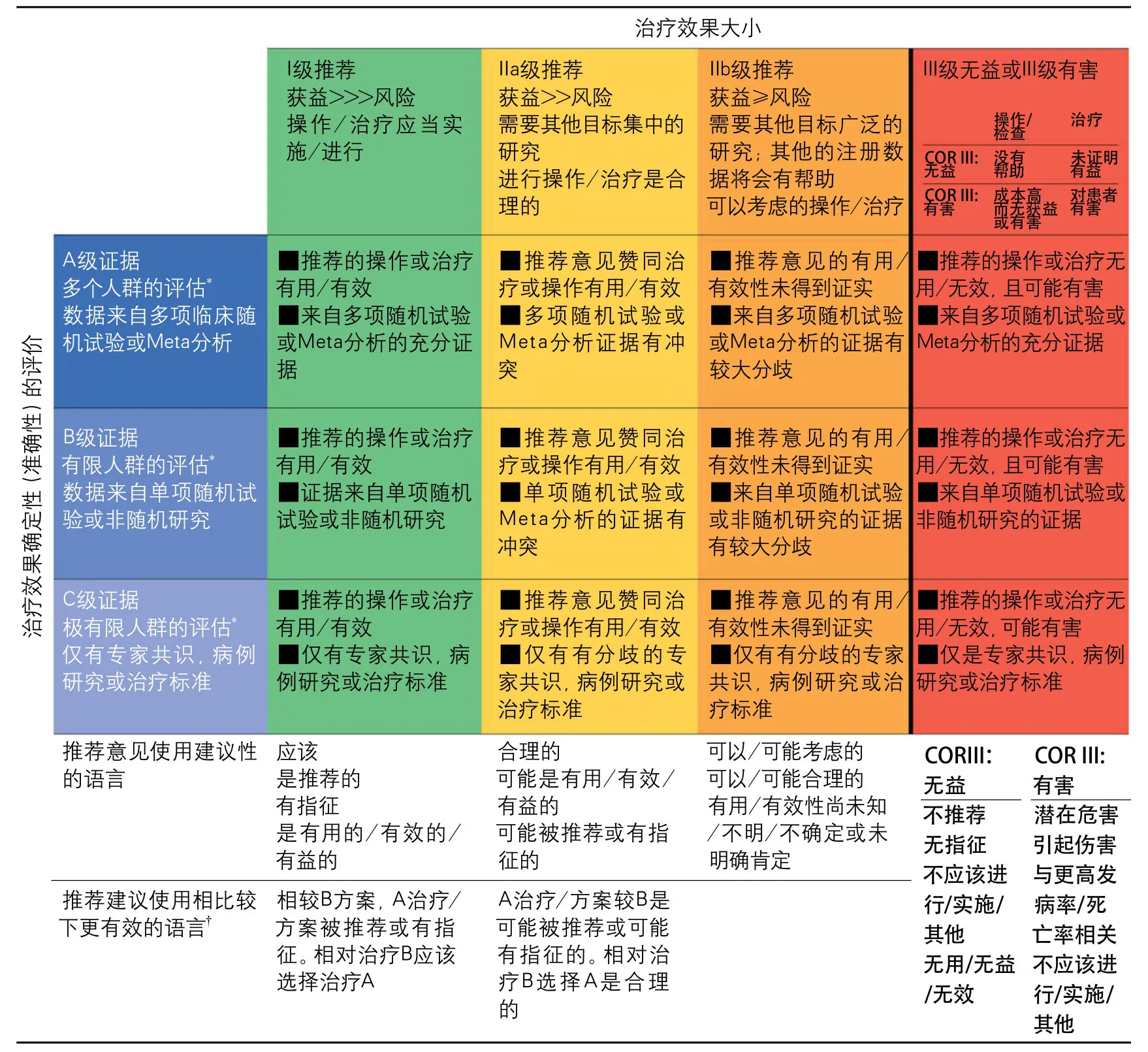
表1 采用的推荐意见的分类和证据等级

表2 AHA/ASA推荐意见中证据水平及分类等级的定义
1 前言
FDA于1996年首次批准组织型纤溶酶原激活剂(阿替普酶)用于缺血性卒中超急性期治疗,这也是目前唯一一个被批准的,在缺血性卒中急性期应用可改善预后的药物。自有重要意义的阿替普酶临床试验发表后,大量临床试验及国家卒中登记研究都证明了阿替普酶在降低缺血性卒中患者致残率方面的获益。
但不幸的是,尽管应用阿替普酶确能获益,但美国仅有极少部分急性缺血性卒中患者实际接受了此种治疗。尽管一些医院及质量注册部门评估的阿替普酶使用率可达20%~30%,但根据国家估计,自2004年起阿替普酶的使用率仅有3%~5%。尽管阿替普酶的使用率较低,但每年仍缓慢增长。阿替普酶的低使用率或可归结于以下几点原因,包括缺乏公众教育,使普通民众不能早期识别急性卒中的症状、征象,并及时做出反应,基层医疗机构采用阿替普酶比率较低,及不同层次医院间医疗系统的复杂性,而这对于阿替普酶安全及时的应用是必需的。尽管上述原因都非常重要,但目前仍认为最重要的原因是适于阿替普酶治疗的患者比率较低。
缺血性卒中患者适于阿替普酶治疗的比率占全部卒中患者的6%~8%,横断面研究中此比率更高。患者不能接受阿替普酶治疗最常见的原因是送医的延误。在全部缺血性卒中的患者中,仅有22%~31%的患者可在症状发生3 h内抵达急诊科治疗。除此之外,送诊的到达时间不呈线性分布。大部分患者到达医疗机构的时间在症状发生后2 h内或8 h以上。上述结果已由以多人群为基础的队列研究证明,结果展示在表3中。
考虑到阿替普酶治疗相关的出血风险,许多临床、影像学及实验室指标被纳入治疗的排除标准,并已列入AHA/ASA急性卒中管理指南(表4)。
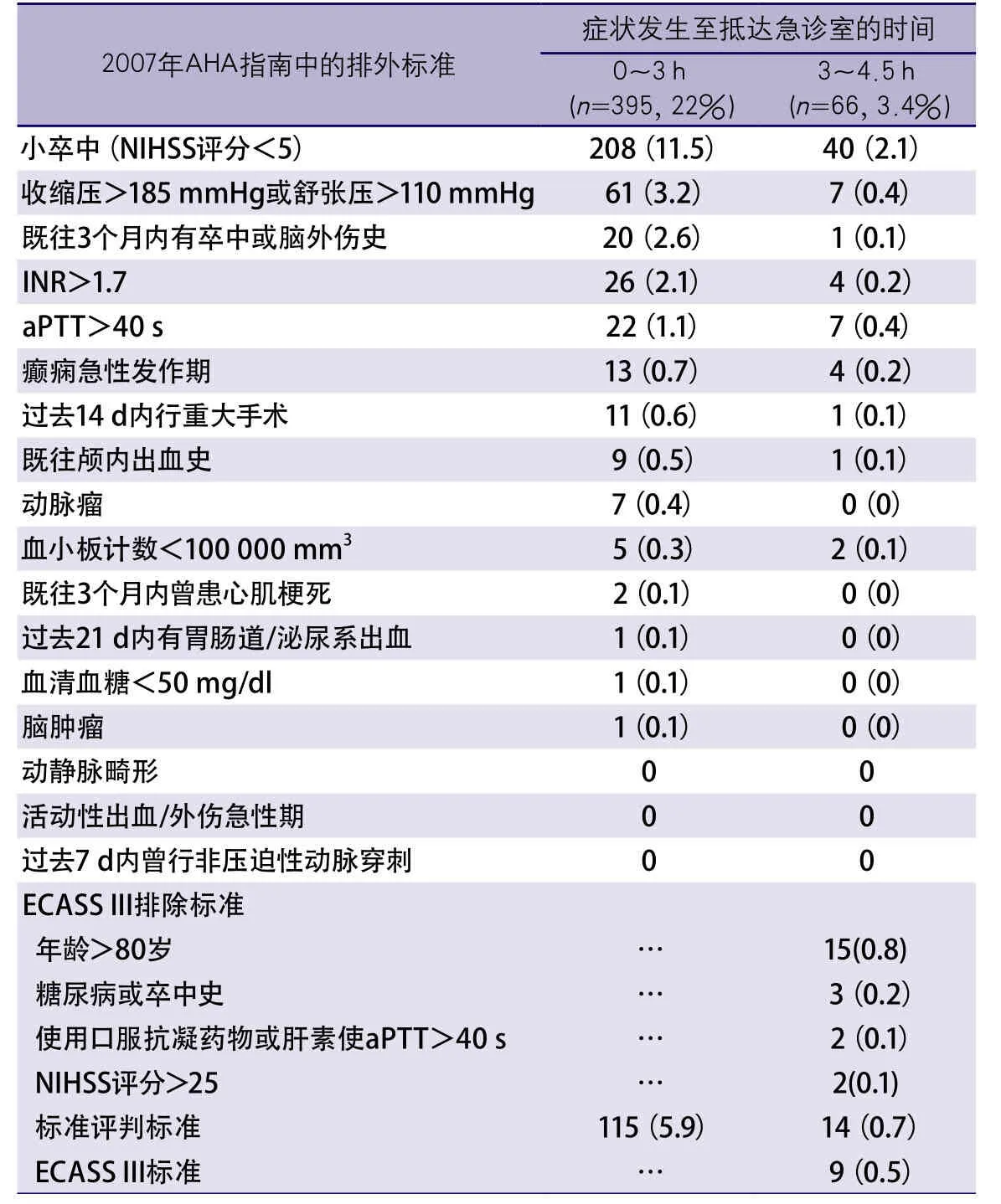
表3 急性缺血性卒中患者发病后0~3 h或3~4.5 h就医应用rtPA治疗的标准
其中部分排除标准较其他排除标准更为常见,部分可在使用阿替普酶前治疗、调整或逆转。阿替普酶治疗的排除标准在发病3 h内抵院患者中的发生率已列在表5中。在此项研究中,即使所有缺血性卒中患者均在治疗时间窗内抵达,仍仅有29%的患者可应用阿替普酶治疗。
目前AHA/ASA2013年急性卒中管理指南中列出的排除标准,大部分以国家神经疾病和卒中研究所(National Institute of Neurological Disorders and Stroke,NINDS)1996年发表的意义重大的阿替普酶临床试验中的标准为基础,并逐年进行少量调整。该研究中的排除标准最初是为阿替普酶的初步试验制订,许多标准来源于心脏相关文献、心脏溶栓临床研究及其他基础科学研究发表的文章。

表4 发病3 h内能接受静脉rtPA溶栓患者的纳入及排除标准
然而部分阿替普酶应用的排除标准存在争议。国内许多专家认为部分排除标准(或禁忌证)是“相对的”而非“绝对的”。近期一项在卒中专家中的调查显示,不同专家在临床过程中对某条排除标准的遵循程度存在较大差异(图1)。该调查在急性卒中转化研究特别项目(Specialized Program of Translational Research in Acute Stroke,SPOTRIAS)的47人中进行。该研究为美国国立卫生研究院资助的一项急性卒中治疗临床研究网络项目。
另一临床中阿替普酶治疗排除标准存在差异的例子是轻度卒中患者的治疗。SPOTRIAS网络中来自8个中心的注册数据显示轻型卒中患者使用阿替普酶治疗的比率为2.7%~18%。
随着溶栓技术的进步,有关阿替普酶治疗的适应证、获益及风险的相关文献日益增多,而文献中的许多情况在最初设计阿替普酶临床研究时是不存在的。本声明旨在批判地回顾文献,评估每一条阿替普酶使用标准的合理性(适应证及禁忌证),并探究关于此种治疗的一些疑问。本篇声明若成功发表,不仅将帮助临床医师决策患者是否适合阿替普酶治疗,也会为未来关于扩展阿替普酶治疗适应证的研究确定重点。本声明为AHA/ASA急性卒中管理指南的辅助建议声明,但不能替代急性卒中管理指南。
本声明逐条分析了阿替普酶治疗纳入及排除标准,这是非常必要的。2015年2月份FDA对阿替普酶处方信息(prescribing information,PI)的变动中也强调了其必要性(附录)。需要说明的是,此改动属于PI的常规内容更新,以保持其与2006年起设立的医师标签规则(Physician Labeling Rule)一致。该处方信息更新的内容不要求阿替普酶生产公司提供新数据,或经FDA批准。医师标签规则列
出了调整的内容、药品及生物制品说明书的格式。该规定旨在为处方信息提供标准格式,以保证其清楚、准确,便于医务工作者阅读、理解及使用。尤其需要注意的是,禁忌证、警示及预防措施的定义已做如下更改。
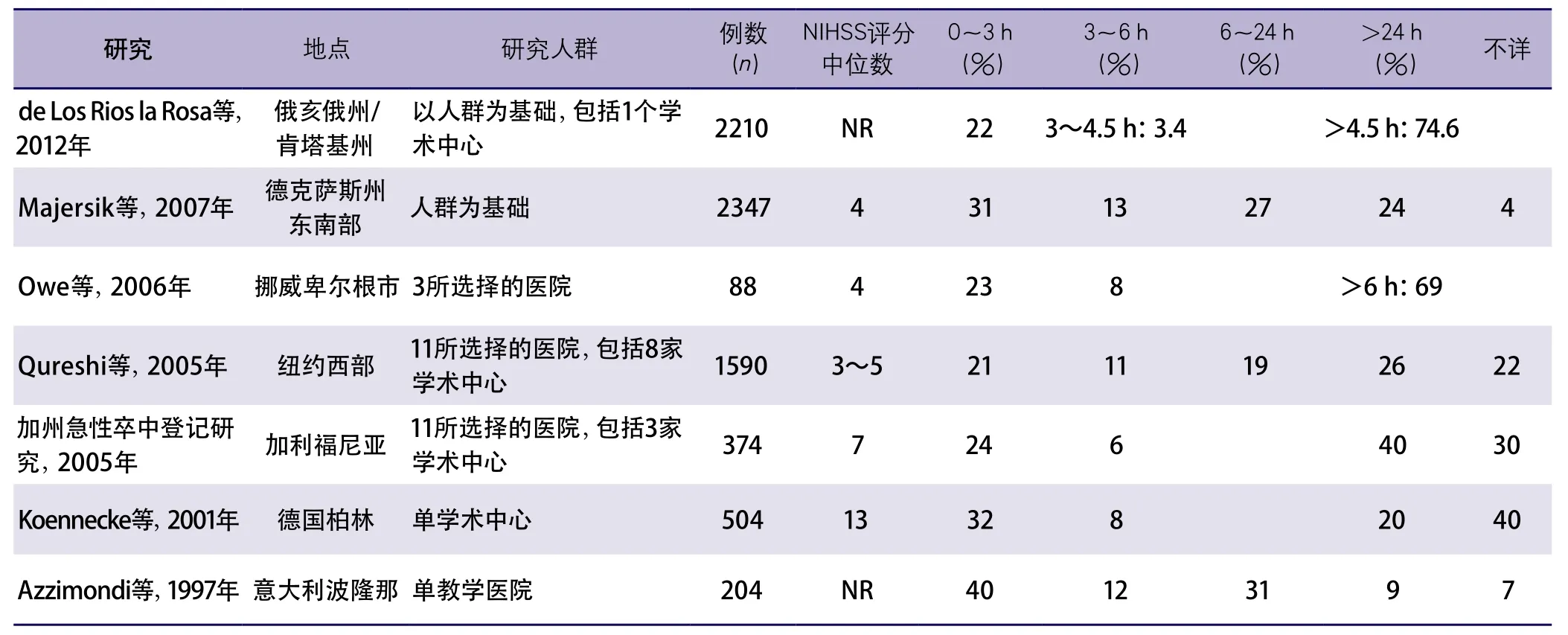
表5 急性缺血性卒中患者就诊时间
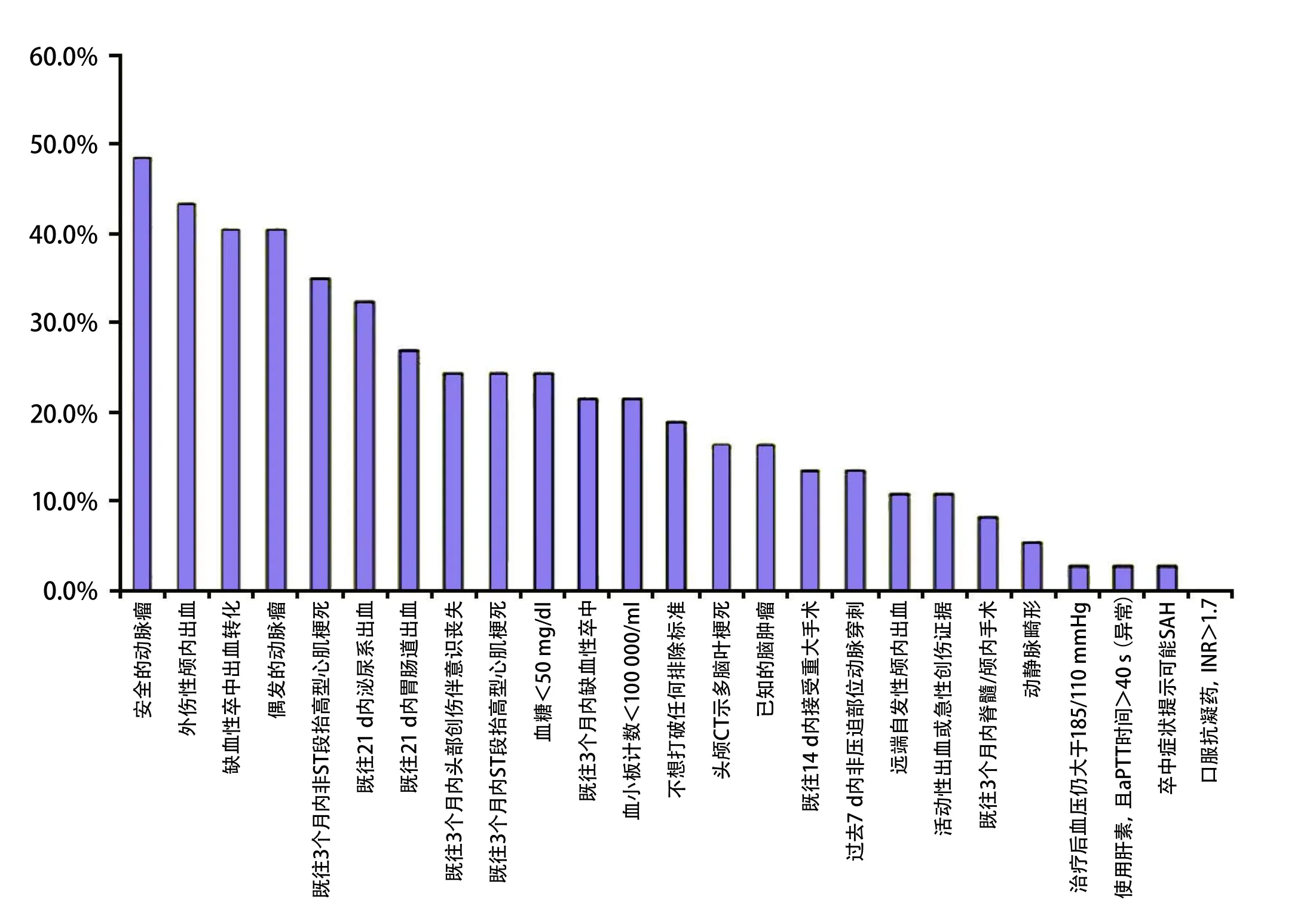
图1 对美国卒中临床医师的调查,询问是否愿意在以下排除标准存在的情况下使用rtPA进行溶栓治疗
·禁忌证:在以下临床情况下,药物应禁忌使用:药物使用的风险明显大于可能获得的治疗获益。上述风险指已知的危害,而非建立在理论上的可能性。
·警告及注意事项:警告及注意事项旨在描述药物的一系列不良反应,及其他潜在的安全风险。上述两者对于临床决策意义重大,因为其对药物开具及患者治疗有指导意义。本部分中出现的药物不良反应需具备证据,证明药物及不良事件间的因果关系,但此因果关系不需完全确定。
阿替普酶处方信息已重新分类及简化,以满足医师标签规则的要求。上述更改已在附录中总结列出。大部分更改内容在禁忌证、警告及注意事项部分。特别是对于没有已知风险的不良反应,已按照医师标签规则在处方信息中除去或简化。需要注意的是,本声明撰写专家小组认为,临床医师在治疗急性缺血性卒中患者或下达临床决策时应将AHA/ASA急性卒中管理指南与本声明结合理解并应用。这一点非常重要,因为此次FDA对处方信息的更改建立在没有新文献更新的基础上。
本声明旨在帮助临床医师依照阿替普酶治疗的绝对、相对风险及获益进行临床决策,减少治疗中的不确定性或存在的疑问,特别是关于治疗的排除标准部分,并且帮助临床医师量化评估存疑患者阿替普酶治疗的风险与获益。专家小组希望本科学声明能够帮助医师与患者及其家属,在了解当前文献研究结果的基础上,建立良好的临床决策制订模式。
2 年龄相关问题
根据FDA说明,发病3 h以内的成年急性缺血性卒中患者,若除外颅内出血,则有静脉应用阿替普酶治疗的指征,以促进神经功能恢复,减少残疾的发生率。说明还提出高龄患者应慎用阿替普酶,尤其对于年龄大于75岁的患者,阿替普酶治疗的风险可能增加,故应权衡风险与预期效果。更新的说明内容还强调,儿童使用阿替普酶的风险及有效性尚不明确。2013年AHA/ASA指南推荐,发病3 h内就诊,符合阿替普酶治疗标准的成年急性缺血性卒中患者,应尽早静脉应用阿替普酶治疗(Ⅰ级推荐,A级证据)。但对于发病3~4.5 h的年龄大于80岁的患者,静脉使用阿替普酶治疗的有效性尚未得到充分证实,需进行进一步研究(Ⅱb级推荐,C级证据)。
年龄是影响卒中发生风险及相关结局最重要的因素之一。55岁后,年龄每增长10岁,发生缺血性卒中的风险就会增加1倍。一项大型队列研究发现,年龄为80~90岁,及大于90岁的患者,其出院时死亡率较更年轻的患者分别增高2~3倍(7.7%及10.3%,更年轻患者为4.0%,P<0.0001),该项队列研究由AHA/ASA发起,名为“遵循指南临床研究”(Get With The Guidelines,GWTG),包括>500 000例患者。此外,年龄小于80岁及大于80岁的患者,其临床结局也有较大差异,特别是远期结局(如:1年时死亡),有更大差异。因此,溶栓药物有效性重大随机对照试验的研究人群不包括老年人也不足为奇了。本部分内容旨在探究不同年龄患者在发病3 h治疗时间窗内静脉应用阿替普酶溶栓的获益及安全性。而发病3 h~4.5 h静脉应用阿替普酶溶栓的适宜人群将在“治疗时间窗的扩大”部分详述。
2.1 年龄为80岁及以上的患者静脉应用阿替普酶治疗的有效性
目前有3项随机试验及12项观察性研究探讨年龄大于等于80岁的卒中患者应用阿替普酶治疗的获益问题。其中与老年患者使用阿替普酶获益相关性最高的是随机对照试验,因为其提供了各个年龄层使用阿替普酶患者及未使用患者临床结局的信息。相反,大多数真实世界旨在监测溶栓治疗安全性的观察性研究,仅能提供已接受静脉阿替普酶溶栓患者的信息,即年龄大于80岁及年龄小于80岁患者卒中结局的信息(通常缺少非阿替普酶治疗患者的信息)。
仅3项多中心、随机的卒中临床研究的人群包括了年龄大于等于80岁的患者(表6)。
总体来说,共1711例年龄大于等于80岁的卒中患者参与了这些临床研究。其中,2项NINDS阿替普酶临床研究仅包括了69例年龄大于等于80岁的患者。回波平面成像评价溶栓试验(Echoplanar Imaging Thrombolytic Evaluation Trial,EPITHET)研究中有25例老年患者。第三次国际卒中试验(Third International Stroke Trial,IST-3)是目前参与人数最大的随机试验(应用阿替普酶组1515例,对照组1520例),为老年急性缺血性卒中患者应用阿替普酶获益的研究提供了证据。IST-3研究发现,年龄大于等于80岁患者应用阿替普酶有主要终点事件的获益(发病后6个月时)存活并功能独立[比值比(odds ratio,OR)为1.35,95%可信区间(confidence interval,CI)为0.97~1.88],但在小于80岁的人群中未发现获益(OR=0.92,95%CI0.67~1.26,P<0.029)(表7)。
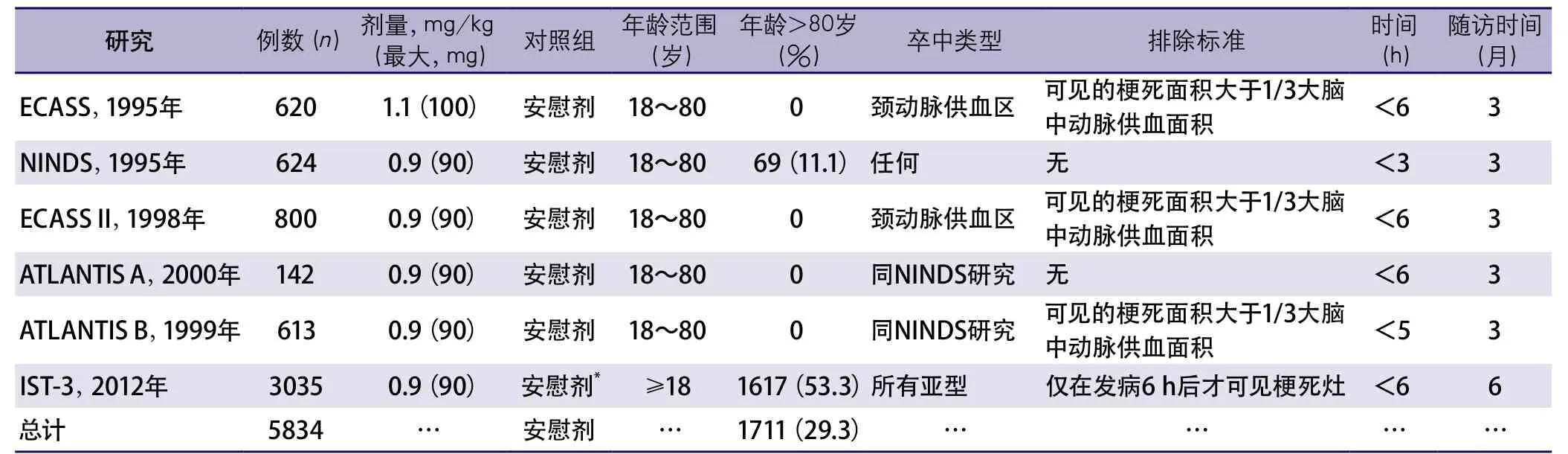
表6 发病3 h内静脉tPA溶栓治疗随机对照研究人群的年龄分布及年龄大于80岁患者的比例
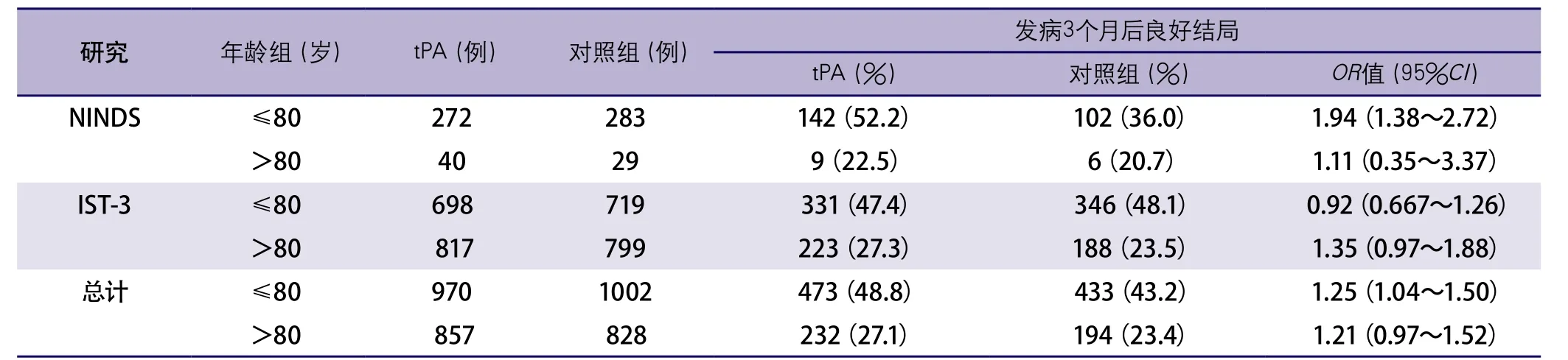
表7 NINDS及IST-3试验中年龄小于80岁人群及年龄大于80岁人群应用tPA溶栓治疗组及对照组在发病后90 d良好结局的比较
一篇近期的Meta分析发现,青年(OR=1.51,95%CI1.18~1.93)及老年(OR=1.68,95%CI1.20~2.34)患者发病3 h内接受静脉阿替普酶治疗均可获益,该项Meta分析包括了6项随机临床试验。在所有年龄>80岁,发病3 h内接受静脉阿替普酶溶栓治疗的患者中,每治疗1000例,即有大于96例患者在随访结束时存活并达到功能独立(接受组织型纤溶酶原激活剂治疗组28.9%,对照组19.3%,P<0.003)。同样的结果也存在于年龄<80岁的患者中(接受组织型纤溶酶原激活剂治疗组49.%,对照组40.1%,P<0.001),即每1000例年龄<80岁,并于发病3 h内接受治疗的患者中,就有大于95例患者存活并达到功能独立。
观察性研究的数据也得出相似结果。目前,最大的评估不同年龄患者阿替普酶治疗获益的观察性研究为卒中治疗安全保证研究——国际卒中溶栓登记研究(Safe Implementation of Treatments in Stroke-International Stroke Thrombolysis Registry,SITSISTR)。
一项研究囊括了SITS-ISTR及虚拟国际卒中试验档案——卒中治疗安全保证研究(Virtual International Stroke Trials Archive,VISTA)研究的数据,共包括29 500例患者。其中3472例(11.8%)为年龄≥80岁的患者。转移分析发现阿替普酶治疗3个月后,改良Rankin量表(modified Rankin Scale,mRS)评分分布与临床研究观察结果相似(年龄≤80岁的患者,OR=1.6,95%CI1.5~1.7,n=25 789;年龄>80岁的患者,OR=1.4,95%CI1.3~1.6,n=3439)。将mRS评分二分类后,敏感性分析同样得出了阿替普酶治疗优于对照组的结果(mRS评分为0~2分,OR=2.1,95%CI1.7~2.5;mRS评分为0~1时为良好结局,OR=1.9,95%CI1.5~2.3)。在将研究人群范围限制在参与VISTA研究的患者中时同样可得出阿替普酶治疗更好的结论(老年患者,OR=1.34,95%CI1.05~1.70;年龄≤80岁的患者,OR=1.42,95%CI1.26~1.59),在研究人群仅限于SI T S-IS T R研究,或研究人群存在阿替普酶治疗排除标准时,也可获得同样的结论。静脉阿替普酶溶栓治疗获益的大小随年龄(每10岁)变化较小(41~50岁,OR=1.5,95%CI1.2~1.8;51~60岁,OR=1.6,95%CI1.4~1.8;61~70岁,OR=1.5,95%CI1.4~1.7;71~80岁,OR=1.6,95%CI1.5~1.8;81~90岁,OR=1.5,95%CI1.3~1.7)。在另一包括13项观察性研究的Meta分析中,共有3178例患者接受阿替普酶治疗(2411例患者年龄<80岁,764例患者年龄≥80岁),结果显示,与对应的年龄更低的患者相比,年龄≥80岁的患者在治疗3个月后获得较好结局的可能性降低50%(OR=0.49,95%CI0.40~0.61)。同样,在一项包括2项随机对照研究及10项观察性研究的二次分析中得到了相似的结果,即阿替普酶治疗后3个月结局较好(图A,仅供在线浏览的补充数据)。无论是否进行阿替普酶溶栓治疗,都不难想到与年轻患者相比,老年患者更不易获得良好结局。但需要注意的是,大多数观察性研究仅评价了年龄不一致性,即仅比较了老年及更年轻的患者接受阿替普酶治疗的结局,而未比较老年患者接受阿替普酶治疗与未接受治疗的结局有无不同。
2.2 死亡率
在2项NINDS阿替普酶卒中研究中,同年龄层阿替普酶溶栓治疗组与对照组在发病3个月后的死亡率差异无显著性(年龄≤80岁的患者中:阿替普酶组死亡率为21.0%,对照组死亡率为26.9%,P=0.10;年龄>80岁的患者中:阿替普酶组死亡率为52.5%,对照组为48.3%,P=0.73)。同样,在EPITHET及IST-3研究中上述年龄组患者的死亡率差异也无显著性。
SITS-ISTR及VISTA研究数据汇总后结果(n=29 500)显示接受阿替普酶治疗的患者发病后3个月死亡率降低(OR=0.85,95%CI0.78~0.92)。年龄≥80岁的患者中(n=2628),接受阿替普酶治疗组患者(n=21 099)发病后3个月死亡率为13.6%,对照组(n=4929)死亡率为14.8%。年龄更高的患者中(n=3472),接受阿替普酶治疗的患者死亡率(32.6%)同样低于对照组(35.3%)。校正后的OR值分析结果也得出了相似的支持阿替普酶治疗的结果,即更年轻及老年患者,接受阿替普酶治疗后死亡率均下降(更年轻患者中:OR=0.87,95%CI0.79~0.95;老年患者中,OR=0.89,95%CI0.76~1.0)。
VISTA研究分析结果(n=5817:1585例患者接受阿替普酶治疗,4232例对照组患者)发现在年龄≤80岁患者中,阿替普酶治疗组患者有更高的生存率(OR=1.44,95%CI1.18~1.76)。但在年龄>80岁患者中,阿替普酶治疗组及对照组患者生存率差异无显著性(OR=1.20,95%CI0.90~1.65)。
在SPOTRIAS研究中,3378例患者接受静脉阿替普酶治疗。经过校正,与更年轻的接受阿替普酶治疗的卒中患者相比,年龄>80岁接受阿替普酶治疗的卒中患者的院内死亡风险是前者的2倍。[校正OR值(adjusted odds ratio,aOR)=2.13,95%CI1.60~2.84]。同样,在SITS-ISTR观察性研究中,老年卒中患者较年龄≤80岁的患者有更高的死亡率(30%与12%,aOR=1.53,95%CI1.43~1.65)(1831例患者年龄>80岁,19 411例患者年龄≤80岁)。
观察性研究的Meta分析(n=3178)指出,年龄≥8 0岁患者接受阿替普酶治疗,其死亡风险是年轻患者的3倍(OR=2.77,95%CI2.25~3.40)。但对照组老年患者与年轻患者死亡率比较的信息不详,因为观察性研究中未包括没有接受阿替普酶治疗的患者。
近期一篇Meta分析提出,接受阿替普酶治疗在7 d内有更高的死亡风险(接受阿替普酶治疗死亡率11%,对照组死亡率7%,OR=1.60,95%CI1.22~2.08),该篇Meta分析包括了3035例参与随机对照研究的患者。但不同年龄组死亡率的差异在该篇文章中并未阐明。纳入IST研究(阿替普酶治疗组发病后7 d死亡率与对照组发病后7 d死亡率相比,OR=1.58,95%CI1.23~2.03)或可解释该分析结果与此前Meta分析之间的差异。
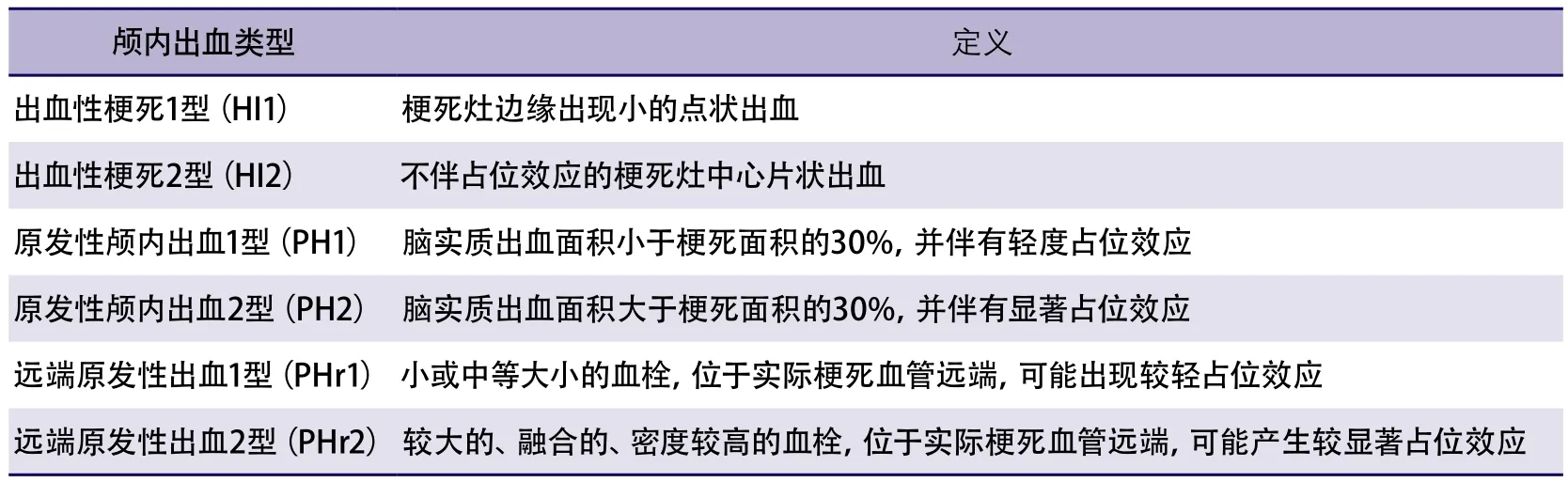
表8 阿替普酶静脉溶栓后颅内出血的分类
2.3 安全性:出血性并发症
症状性颅内出血(symptomatic intracerebral hemorrhage,sICH)是静脉阿替普酶治疗后最可怕的并发症。所有研究均表明阿替普酶治疗与不使用阿替普酶治疗相比,有更高的出血性转化风险。近期一篇包括6项随机对照研究及1779例患者的Meta分析表明,发病3 h内静脉阿替普酶静脉治疗有近5倍的症状性出血风险(OR=4.55,95%CI2.92~7.09;绝对风险为8.04%,风险差6.79%)。
同样,接受阿替普酶治疗后年龄≥80岁患者颅内出血(intracerebral hemorrhage,ICH)风险与更年轻患者阿替普酶治疗后ICH风险的比较也是需要关注的问题(仅供在线阅读的补充数据,图B)。2项随机对照试验及15项观察性研究的数据提供了相关信息。为更好地回答上述问题,需区分随机对照研究与观察性研究中对ICH的定义(表8)。表8描述了不同种类的出血及其定义。例如,在欧洲协作性急性卒中研究Ⅲ(European Cooperative Acute Stroke Study Ⅲ,ECASS Ⅲ)中出血性转化被归类入出血性梗死[hemorrhagic infarction(HI1,HI2)]、脑实质出血[parenchymal hemorrhage(PH1,PH2)]及远端脑实质出血[remote parenchymal hemorrhage(PHr1,PHr2)]。
sICH定义为与基线相比国立卫生研究院卒中量表(National Institute of Health Stroke Scale,NIHSS)评分增加≥4分或发病后36 h内死亡,或发生PH2或PH2出血。按照ECASSⅢ研究定义,年龄>80岁及年龄<80岁患者sICH的发生率总结在表9中。在2项NINDS研究中,sICH定义为发病后36 h内发生ICH,在CT或磁共振成像(magnetic resonance imaging,MRI)上可见,并由临床医师确定患者临床情况因出血而恶化。依据NINDS研究对sICH的定义,将各个研究中sICH发生频率总结在表10中。
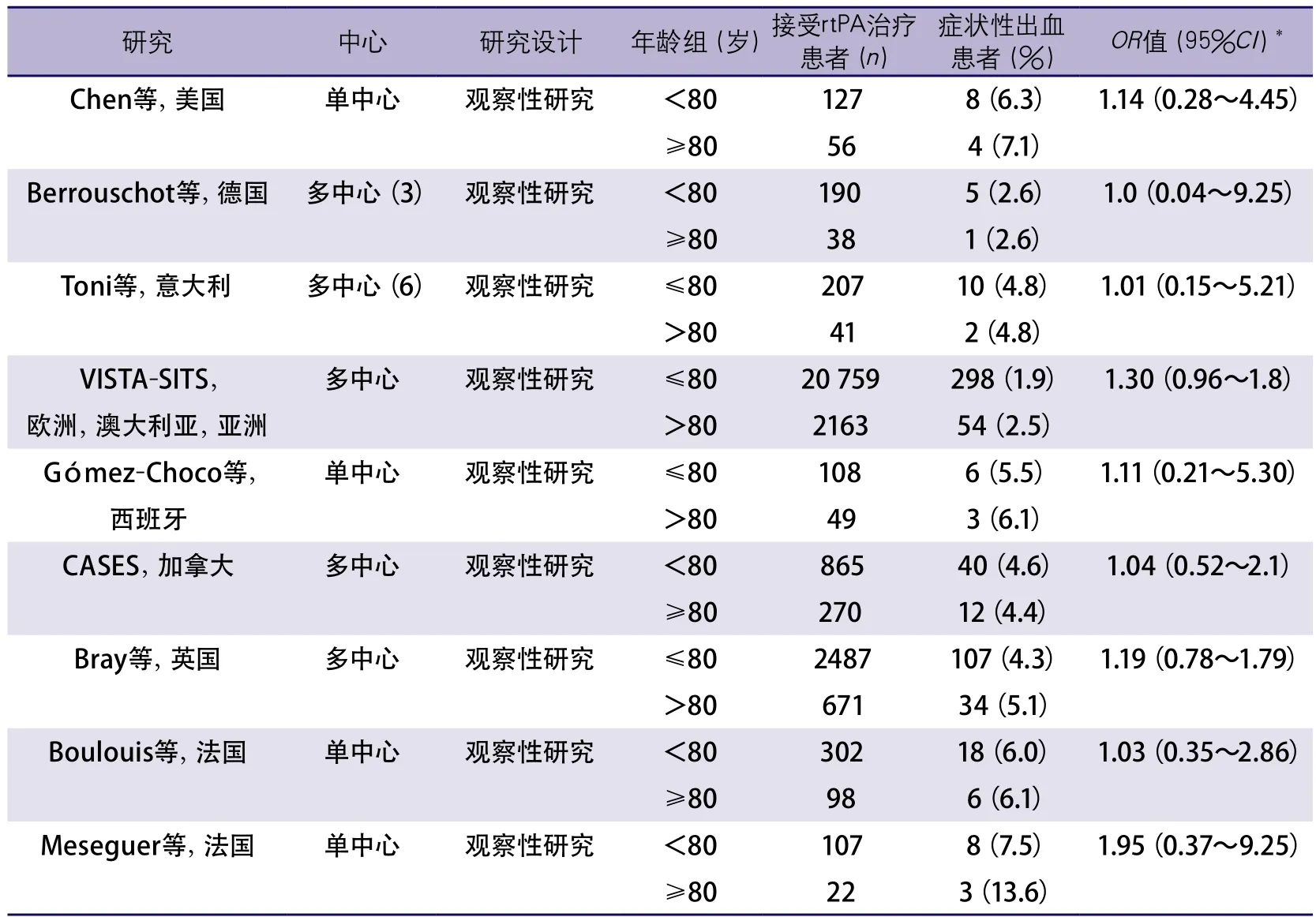
表9 按照ECASS III症状性出血定义不同年龄组患者接受rtPA溶栓治疗后发生sICH的风险
一篇Meta分析纳入了阿替普酶治疗患者症状性出血风险的相关研究,并表明,年龄>80岁及年龄<80岁患者的sICH差异无显著性(OR=1.31,95%CI0.93~1.84)。一项仅包括大于10 0例卒中患者的研究分析发现年龄≥80岁的患者有更高的出血风险。当出血定义与ECASS定义相同时,OR=1.38,95%CI0.93~1.84,n=28 560;当出血定义与NINDS定义相同时,OR=1.40,95%CI1.22~1.61,n=24 327(详见在线阅读补充数据,图C)。但即使有更高ICH的风险,阿替普酶治疗仍可使此组患者获益。
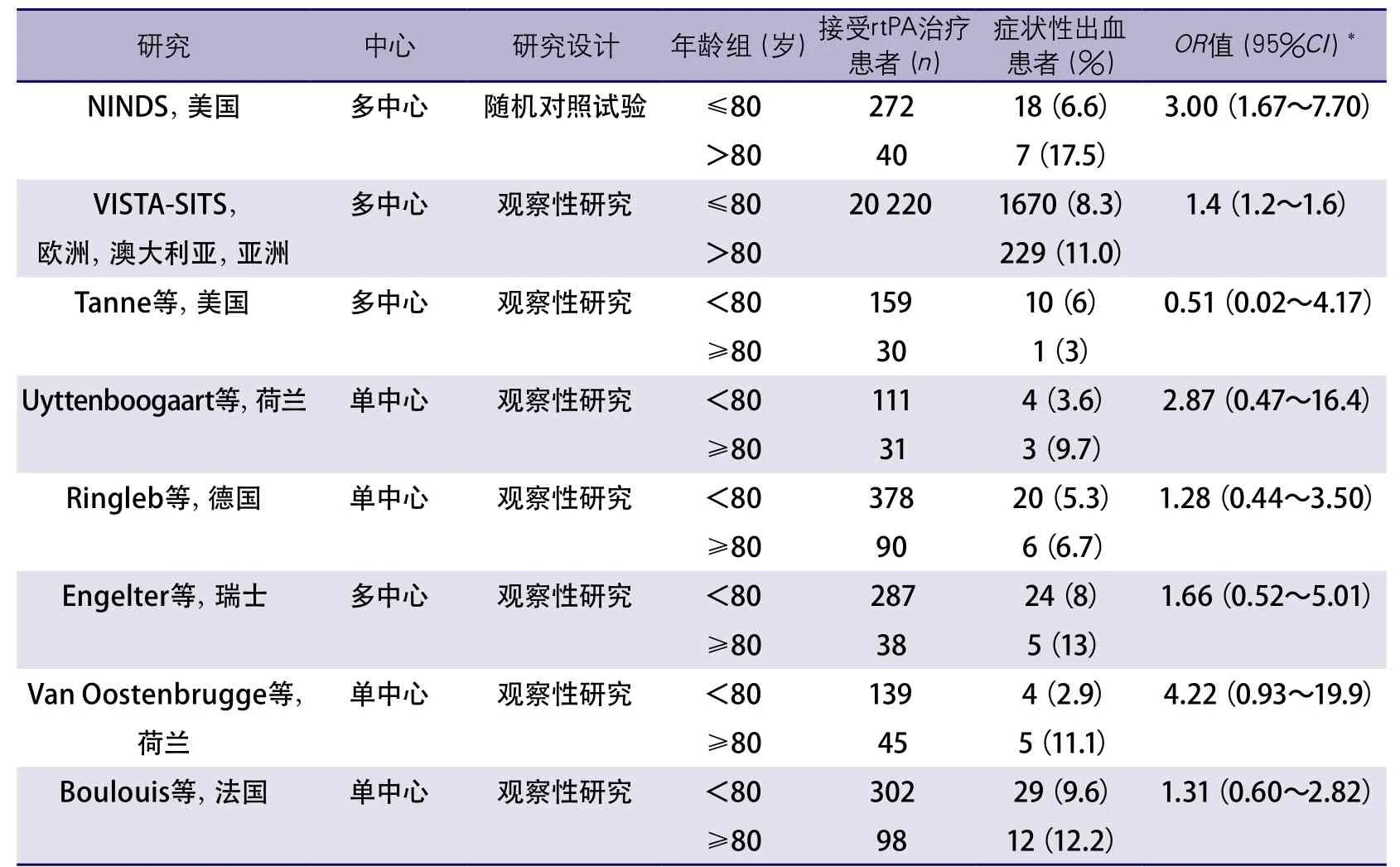
表10 根据NINDS症状性颅内出血定义不同年龄组患者接受rtPA溶栓治疗后发生sICH的风险
2.4 儿童的溶栓治疗
儿童卒中定义为发生于1月龄~18岁的卒中。卒中也可能会发生于<1月龄的患者(新生儿及婴儿)。在美国,年龄<18岁儿童的缺血性卒中发病率为0.63~6.4/100 000人每年。
儿童及新生儿卒中的诊断及治疗有一些特别之处(表11)。
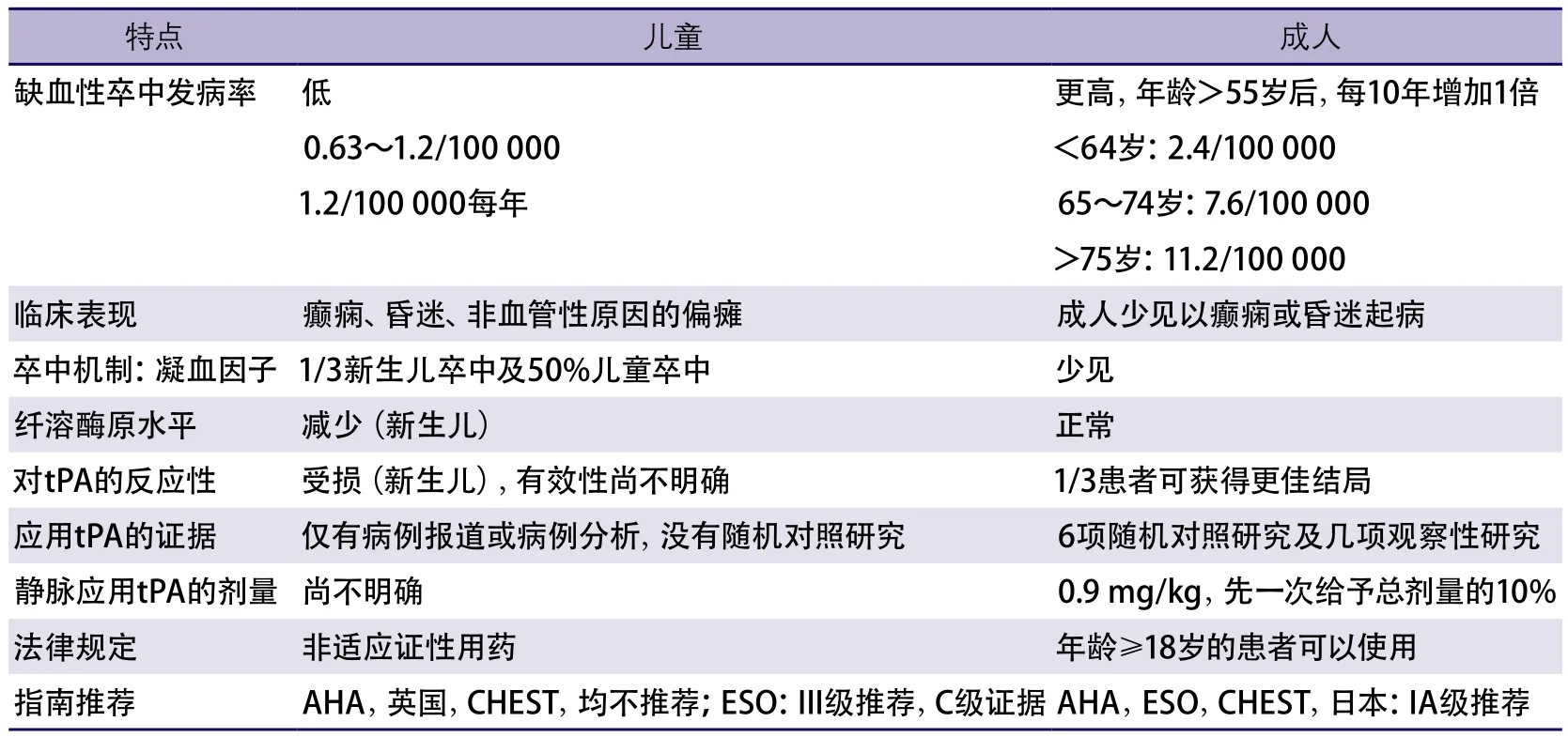
表11 成人卒中及儿童卒中诊断与治疗的比较
儿童卒中的最初诊断因其临床症状的多样性而颇具挑战性(如:昏迷、癫痫及偏瘫),这些症状多见于非血管性卒中。所有评价静脉阿替普酶治疗获益的大型随机对照试验均除外了年龄≤18岁的卒中患者。儿童卒中的机制与成年人不同。例如,2/3的新生儿卒中及大于50%婴儿及儿童卒中归因于凝血因子异常。此外,先天性心脏畸形、血管畸形及感染性疾病均为儿童卒中较常见,但是成人卒中少见的病因。成人及儿童(特别是新生儿)的生理学机制存在差异,这影响了溶栓后患者的临床反应及并发
症的发生风险。例如,与年龄较大的儿童及成人相比,新生儿的纤溶酶原水平较低。因此,新生儿对阿替普酶的反应性受损。增加阿替普酶剂量,不仅不会增加血栓溶解,还会增加新生儿纤溶酶原浓度。儿童溶栓的证据仅限于单中心研究、病例分析或其他医学指征(如:用于透析管阻塞后再通,颅静脉血栓静脉窦内溶栓)。按照规定,FDA现仅批准阿替普酶用于年龄≥18岁的患者。
目前,尚无已发表的关于新生儿及儿童应用阿替普酶的随机对照试验。大部分儿童患者应用阿替普酶的证据来源于观察性研究。一项来源于国家住院系统数据库的大型回顾性研究表明,在2904例纳入研究的儿童卒中患者中,仅有46例(1.6%)接受了静脉内或动脉内阿替普酶治疗。国际儿童脑卒中研究(International Pediatric Stroke Study,IPSS)报道了相似的结果[在687例儿童卒中患者中仅有15例(2.2%)接受了阿替普酶的治疗]。卒中发病至接受静脉内阿替普酶治疗的中位时间为3.3 h(范围为2.0~52.0 h),接受动脉内阿替普酶治疗的中位时间为4.5 h(范围为3.8~24.0 h)。共2例患者死亡(1例大面积梗死伴脑疝患者,1例脑干梗死患者)。出院时,1例患者体健,12例患者仍有神经功能损伤。15例患者中,4例患者接受阿替普酶治疗后出现ICH,但上述出血事件均未被判定为急性症状性出血。
在大辛辛那提/肯塔基州北部130万居民以人群为基础的研究中,在3个独立研究阶段(1993年至1994年,1999年及2005年),共纳入29例儿童缺血性卒中患者。其中包括共7例新生儿卒中(≤28日龄),4例婴儿卒中(>28 d至<1岁),11例儿童卒中(年龄在1~14岁),7例儿童卒中(15~17岁)。研究者以2007年AHA/ASA成人急性缺血性卒中管理指南作为参考,确定儿童患者应用阿替普酶可能的治疗标准。按照成人标准,29例儿童卒中中仅1例可接受阿替普酶治疗(3%)。研究者还指出,若排除有相对禁忌证,如癫痫发作的患者,美国每年有约178例儿童患者满足阿替普酶治疗的入选标准。
AHA/ASA儿童卒中指南同样不推荐儿童缺血性卒中患者在临床研究之外的情况下,静脉应用阿替普酶治疗。上述儿童缺血性卒中患者不包括年龄较大的,满足成人阿替普酶治疗标准青少年。对于此类患者目前尚无共识。最新的AHA/ASA急性缺血性卒中管理指南提出将年龄>18岁作为静脉阿替普酶治疗的纳入标准之一。这项纳入标准基于FDA的批准及指南。但需注意的是,专科医生在急性卒中治疗时可调整标准。
一篇系统综述报道了17例儿童接受静脉内溶栓(n=6),动脉内溶栓(n=10)或机械溶栓(n=1)的病例,其均未发生症状性颅内出血,但2例出现了非症状性颅内出血。16例儿童患者(94%)存活,12例儿童患者(71%)获得良好结局(mRS评分0或1)。目前NINDS正开展一项儿童患者剂量递增静脉内应用阿替普酶溶栓的临床研究。这项研究以多中心观察性研究(IPSS)的结果为基础。儿童卒中溶栓研究(Thrombolysis in Pediatric Stroke,TIPS)是一项国际、多中心研究。该研究持续5年,旨在确定2~17岁儿童在急性缺血性卒中发病4.5 h内接受静脉阿替普酶溶栓治疗时的最大安全剂量,即从3种剂量(0.75 mg/kg,0.9 mg/kg,1.0 mg/kg)中,确定最大安全剂量。该研究的主要结局事件为sICH。sICH定义为:发生PH2事件,或阿替普酶治疗后36 h内发生颅内出血,且颅内出血被判定为神经功能恶化(儿童NIHSS评分最少变化≥2分)的最重要的原因。但不幸的是,该研究过早终止,因为缺少自然出现的满足研究要求的患者。
2.5 年龄相关问题:推荐建议
1.对于满足静脉阿替普酶溶栓要求的年龄≥18岁的患者,年龄>80岁及年龄<80岁时均推荐发病3 h内静脉阿替普酶溶栓治疗。高龄是卒中预后不良的危险因素,但其风险不能抵消溶栓治疗的获益。尽管年龄更高的患者较对照组可能获得更差的结局,更高的死亡率及更高发生症状性出血的风险,且上述风险大于年龄<80岁患者较对其对照组的风险,但在所有年龄组别中,静脉应用阿替普酶溶栓均可使患者发病后3个月时功能独立的可能性增高(Ⅰ级推荐;A级证据)。
2.儿童(新生儿、儿童及年龄<18岁的青少年)应用静脉阿替普酶治疗的有效性及风险尚不明确(Ⅱb级推荐,B级证据)。
