超声在自身免疫性胰腺炎与胰腺癌鉴别诊断中的价值
2016-01-11孟德莉,邢玲玲,刘祖平
超声在自身免疫性胰腺炎与胰腺癌鉴别诊断中的价值
孟德莉邢玲玲刘祖平
自身免疫性胰腺炎(autoimmune pancreatitis, AIP)是一种特殊的慢性胰腺炎,约占5%~6%,临床并不多见[1]。AIP的发病机制目前尚不十分清楚,其主要临床表现为胰头局限性肿块及梗阻性黄疸,影像学表现为弥漫性病变,与胰腺癌的占位性病变较为相似,成为因误诊为胰腺癌而行外科手术的最常见良性病变[2]。组织病理活检是鉴别两者的最准确方法,但多数情况下难以获得有效的胰腺组织。近年来,随着超声显像仪性能不断改进,胰腺病变的诊断准确率明显提高[3-4]。本研究回顾性分析25例AIP与44例胰腺癌的超声成像特点,探讨超声在AIP与胰腺癌鉴别诊断中的临床价值。
一、资料与方法
1.一般资料:收集2008年1月至2014年6月间绍兴市第六人民医院收治的25例AIP患者,诊断均符合2008年AIP的亚洲标准[5],即影像学检查胰腺弥漫性或局限性肿大,血清Ig G升高,或胰腺淋巴细胞、浆细胞浸润伴纤维化。25例AIP患者中男性19例,女性6例;年龄48~76岁,平均(57±4)岁。选择同期经手术或病理确诊的44例胰腺癌(pancreatic cancer, PC)患者,其中男性24例,女性20例;年龄44~75岁,平均(53±5)岁。PC中胰腺导管癌29例,黏液腺癌11例,腺泡细胞癌4例。所有患者均有完整的常规超声、超声造影等影像学资料。
2.超声检查:采用Toshiba Aplio 500超声仪(PHILIPS IU22),探头频率为7~13 MHz。首先使用二维超声进行腹部扫查,观察并记录胰腺病灶数量、形态、边界、大小、有无钙化点及囊性病变等,再使用彩超记录病灶内部以及周围组织的血流分布情况。然后启动造影模式。指导患者保持自然平缓呼吸,维持探头位置不动,切换至实时灰阶造影成像模式,将超声造影剂SonoVue加入5 ml生理盐水充分混匀后制成混悬液经肘静脉快速注射,速度2~5 ml/s。记录动态图并存盘,观察病灶增强及消退的模式。
由2位富有经验的高年资医师独立分析常规超声和超声造影图像并作出诊断,若对结果存在异议,则经讨论后作出最后诊断。

DOI:10.3760/cma.j.issn.1674-1935.2015.01.016
作者单位:312000浙江绍兴,绍兴市第六人民医院超声科(孟德莉、邢玲玲);绍兴市第六人民医院病理科(刘祖平)
通信作者:邢玲玲,Email: 1902215293@qq.com
3.统计学处理:应用SPSS 17.0统计软件包对数据进行统计分析。计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
二、结果
1.常规超声图像特征:25例AIP中17例为局灶性病变,呈粗糙低回声,其中位于胰头13例,胰尾4例;胰腺增大,胰胆管呈串珠样扩张。8例表现为胰腺弥漫性肿大,回声明显减弱,彩超可见点状血流信号。24例可见胰腺外器官及组织改变,包括胆囊壁或胆管壁增厚22例,胆总管后壁性狭窄23例,脾大13例。44例PC均为局灶性病变,形态不规则,边界不清,呈低回声;胰头增大,结节状或肿大,胰腺体尾部萎缩11例,血管侵犯23例。
AIP组的总胆管扩张、胰胆管扩张、血管受累明显少于PC组,而胆囊壁或胆管壁增厚、胆总管后壁性狭窄、脾大明显多于PC组,差异均有统计学意义(表1)。
2.超声造影图像特征:AIP以高增强为主,多呈点状、线状、环状增强,增强边界平滑;PC病灶以不均匀、低增强为主,且增强边界不清。
3.两种检查方法的诊断价值:常规超声检查诊断AIP的敏感性、特异性、准确性分别为76.0%(19/25)、52.3%(23/44)%、60.9%(42/69);超声造影检查为72.0%(18/25)、61.4%(27/44)、65.2%(45/69);常规超声和超声造影联合诊断为92.0%(23/25)、84.1%(37/44)、87.0%(60/69)。联合诊断的特异性及准确性均显著高于单项检查,差异均有统计学意义(P值均<0.05)。
讨论AIP患者早期无特异性症状,常被临床忽视,随着病情的渐进性进展,多数患者可出现无痛性黄疸、腹痛及体重下降等症状。AIP可分为弥漫性和局限性两种类型,其中局限性AIP的病变部位以胰头居多,影像学表现为局灶性低密度肿块,与PC极为相似,导致其误诊率居高不下[6]。由于PC以手术治疗为主,而AIP以激素治疗为主,AIP误诊为PC就会接受手术治疗。文献报道称约10%的AIP等良性炎症性胰腺疾病因误诊而接受手术[7]。因此,术前准确鉴别诊断AIP对患者治疗方案的选择具有重要的意义。
与MRI、CT、ERCP等检查相比,超声检查具有无创性、价格低廉、适合短期内复查等优势,尤其适用于胰腺病变的初筛。AIP超声声像图首先表现为胰腺形态的改变,多呈弥漫性或局限性肿大,粗糙低回声。这图像表现可能与淋巴细胞、浆细胞弥漫性浸润胰腺组织,以及纤维组织过度增生有关[8]。本组68%患者超声显示为局灶性病变,其中7例病变部位在胰头的患者高度疑似胰头实质性占位性病变,后经穿刺活检病理检查排除PC,说明超声引导下的穿刺活检有助于AIP 的早期诊断,尤其是对于预行手术治疗的患者。
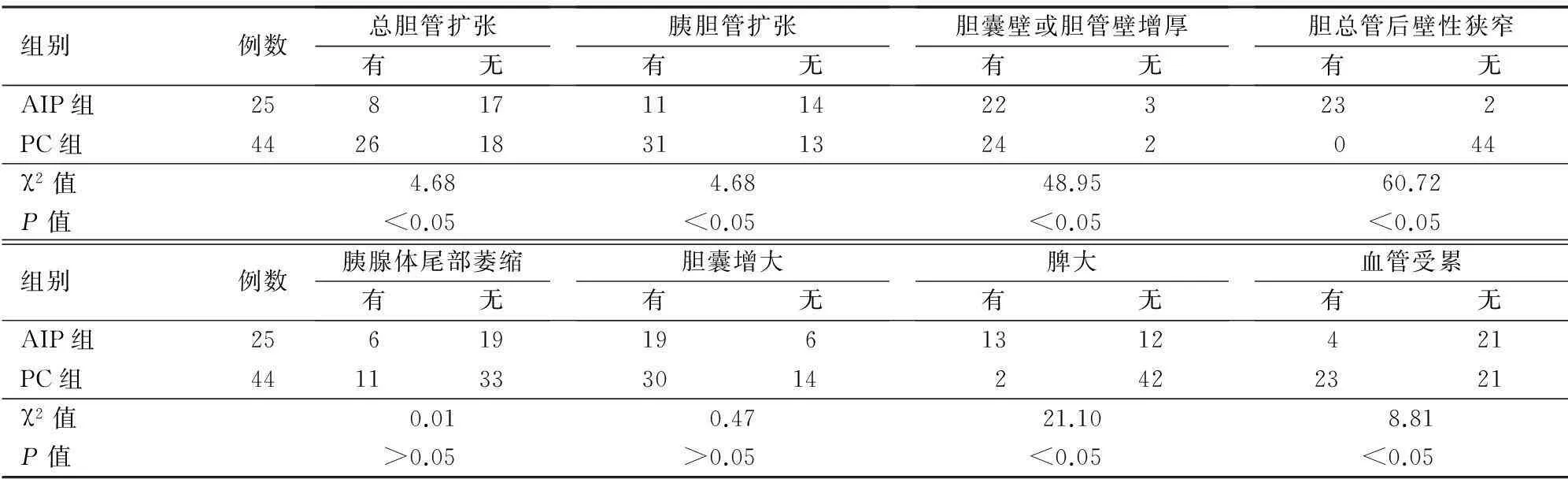
表1 AIP和PC患者的常规超声征象比较
AIP是一种全身性的免疫炎症疾病,68%~88%的AIP患者可累及胆管[9]。当炎症累及胆总管胰腺段时,可因管壁增厚而出现相应的超声声像图改变。本组24例患者可见胰腺外器官及组织改变,其中以胆囊壁或胆管壁增厚、胆总管后壁性狭窄、脾大常见。胰头癌虽伴有胆囊增大及胆管扩张,但一般不会导致胆总管后壁性狭窄及胆道壁增厚,该声像差异可与AIP进行鉴别诊断。AIP患者伴有脾大可能是由于肿胀胰腺压迫静脉或闭塞性静脉炎所致,故当胰腺肿大伴脾大时应考虑AIP的可能。
超声造影是基于病灶的血供进行观察。胰腺的血供极为丰富,超声造影可清晰显示胰腺以及肿瘤的微血管。本组病例中,AIP病灶以高增强为主,且早于周围胰腺腺体增强,而PC则表现为低增强。谢晓燕等[10]研究指出,以低增强诊断PC,其敏感性为86.7%,特异性为53.8%。此外,部分学者认为,由于炎症和纤维化进展程度不同,AIP增强早期的表现存在多样性。当炎症反应明显时主要表现为高增强,而随着病程迁延、加重,胰腺内纤维化加重及微血管密度降低,则逐渐转变为低增强[11-12]。
本研究结果显示,联合常规超声及超声造影诊断AIP的特异性、准确性为84.1%、87.0%,高于单独常规超声或单独超声造影的特异性及准确性,说明两者联合检查可明显减少误诊率。常规超声是胰腺病变重要的初筛手段,对不典型的局灶性胰腺炎及胰腺癌的鉴别诊断价值不高,而超声造影有助于鉴别胰腺病变良恶性。
参考文献
[1]Shimosegawa T,Chari ST,Frulloni L,et al.International consensus diagnostic criteria for autoimmune pancreatitis: guidelines of the International Association of Pancreatology[J].Pancreas,2011,40(3):352-358.
[2]Lo RS,Singh RK,Austin AS,et al.Autoimmune pancreatitis presenting as a pancreatic mass mimicking malignancy[J].Singapore Med J,2011,52(4):e79-e81.
[3]Hocke M,Ignee A,Dietrich CF.Contrast-enhanced endoscopic ultrasound in the diagnosis of autoimmune pancreatitis[J].Endoscopy,2011,43(2):163-165.
[4]祝毛玲,徐灿,金震东,等.超声图像特征参数分析在胰腺癌鉴别诊断中的应用[J].中华消化内镜杂志,2012,23(1):15-18.
[5]Otsuki M,Chung JB,Okazaki K,et al.Asian diagnostic criteria for autoimmune pancreatitis:consensus of the Japan Korea Symposium on Autoimmune Pancreatitis[J].J Gastroenterol,2008,43(6):403-408.
[6]Ikeura T,Miyoshi H,Uchida K,et al.Relationship between autoimmune pancreatitis and pancreatic cancer: a single-center experience[J].Pancreatology,2014,14(5):373-379.
[7]田笑,周欢,杨颖,等.胰胆管扩张的CT表现对胰头癌与胰头部肿块型慢性胰腺炎的诊断意义[J].河北医药,2011,33(2): 197-198.
[8]卢颖,黄光亮,谢晓燕,等.自身免疫性胰腺炎超声表现及与胰腺癌的鉴别[J].中华超声影像学杂志,2014,23(4): 308-310.
[9]Zhang X,Zhang X,Li W,et al.Clinical analysis of 36 cases of autoimmune in China[J].PLoS One,2012,7(9):e44808.
[10]谢晓燕,许尔蛟,徐辉雄,等.超声造影表现在胰腺实性局灶性病变鉴别诊断中的意义[J].中国医学科学院学报,2008,30(1):35-39.
[11]Numata K,Ozawa Y,Kobayashi N,et al.Contrast-enhanced sonography of autoimmune pancreatitis:comparison with pathologic findings[J].J Ultrasound Med,2004,23(2):199-206.
[12]张新刚,温锋,董幼丹,等.自身免疫性胰腺炎与胰腺癌在影像学方面的鉴别诊断研究[J].中国医师进修杂志,2013,36(15): 4-8.
收稿日期:(2014-11-20)
(本文编辑:屠振兴)
