英夫利昔和免疫抑制剂联合治疗克罗恩病的疗效及安全性的Meta 分析
2015-12-31林梦娟余保平
林梦娟,余保平
武汉大学人民医院消化内科,湖北 武汉430060
克罗恩病(Crohn's disease,CD)是消化道的慢性非特异性炎症,其主要特征是病程进展过程中可出现复发与缓解交替现象,并可出现肠梗阻、肠瘘及脓肿等并发症。2009 年美国胃肠病学相关指南推荐使用5-氨基水杨酸及糖皮质激素类药物为一线治疗方案,当一线治疗方案失败时可选用免疫抑制剂治疗,以上传统治疗方案均失败时可考虑使用英夫利昔(Infliximab,IFX)[1]。现已证实,免疫抑制剂,如硫唑嘌呤(azathioprine,AZA)、6-巯基嘌呤(6-mercaptopurine,6-MP)、甲氨蝶呤(methotrexate,MTX)及英夫利昔在诱导和维持CD 的缓解中均有明显疗效,两者均属于有效的二线治疗方案。然而,当英夫利昔和免疫抑制剂联合应用时,其疗效及安全性与单一用药相比是否更优,还有待进一步的研究证实[1]。目前尚缺乏比较两种方案疗效及安全性的Meta 分析。本研究的目的是在基于有相似试验设计的前瞻性临床随机对照试验(RCT)的基础上进行Meta 分析,以评估英夫利昔和免疫抑制剂联合治疗方案在诱导和维持CD 缓解中的有效性和安全性。
1 资料与方法
1.1 检索策略 检索PubMed、Medline、EMBASE、ISI、SCI/SSCI/A&HCI 及Collaboration Controlled Trial Register 等英文数据库,以及中国知网(CNKI)、万方数据库(WanFang Data)、维普数据库(VIP)和中国生物医学文献数据库(CBM)等中文数据库,查找相关的临床随机对照试验(RCT)。检索时间均为建库至2014 年8 月。文献语种限定为英文和中文。英文数据库的检索策略为:Infliximab and azathioprine or 6-mercaptopurine or methotrexate, immunosuppresives or immunomodulator and Crohn's disease。中文数据库的检索策略为:“英夫利西”与“硫唑嘌呤”或“6-巯基嘌呤”或“甲氨蝶呤”或“免疫抑制剂”或“免疫调节剂”与“克罗恩病”。检索纳入文献的参考文献以全面收集该方面的临床随机对照试验。通过浏览题目及摘要,确定符合标准的文献,并进一步查找及浏览全文确定是否纳入该文献。
1.2 纳入及排除标准 纳入标准:(1)研究对象为成年CD 患者,且设有随机对照组,组间基线相似,组间研究对象具有可比性;(2)研究对象分组应包括英夫利昔和免疫抑制剂联合治疗组和单药治疗组;(3)结局测量指标:必须包含一定时间节点的临床缓解率,可包含内镜下黏膜愈合情况、生化指标改善情况及不良反应发生情况;(4)可以获取文献全文。排除标准:(1)研究对象年龄<18 岁者、妊娠者、对英夫利昔高敏者、患有较严重的系统性疾病及曾接受生物治疗的患者;(2)非随机对照试验;(3)非同期对照和无对照试验;(4)同一文章的重复发表;(5)试验设计不正确;(6)数据处理有误、可靠性低、质量较差的文章。
1.4 文献的质量评价 按照Cochrane 系统评价员手册5.0.2 版对纳入的文献进行方法学质量评价[2]。质量评价的标准包括:(1)随机分配方法;(2)分配方案的隐藏;(3)研究对象、治疗方案实施者、研究结果测量者采用盲法;(4)结果数据的完整性,随访有无失访、退出或丢失,收集的资料是否完整,结果是否同时采用意向性分析方法;(5)选择性报告研究结果;(6)其他偏倚来源。总之,以上描述可以归结为以下3 个原则:(1)随机,体现在对产生随机序列的方法的描述;(2)双盲,体现在对双盲方法的描述;(3)对退出和失访的描述,体现在对有退出和失访进行比较积极的描述,如阐述退出和失访的患者数目及其原因。按照上述评价标准,被纳入文献被分为3 个质量等级:A级:低度偏倚,完全满足上述质量标准;B 级:中度偏倚,部分满足上述质量标准;C 级:高度偏倚,完全不满足上述质量标准。
1.5 统计学处理 采用Cochrane 协作网提供的Revman 5.2 软件进行统计分析。对收集的数据进行ITT分析,即除将具有有效试验结果的受试者包含在试验终点的结果分析中之外,还应包括失访、退出、丢失和收集资料不完整的受试者。用χ2检验和I2检验验证所纳入临床试验的异质性,如果各试验同质(P >0.10或I2<50%)则可采用固定效应模型进行数据处理;如果各试验具有异质性(P <0.10 或I2>50%)则采用随机效应模型进行数据处理。将各研究的数据合并,计算不同时间节点总临床缓解率及黏膜愈合率,并得到合并的OR 值及其95%CI,P <0.05 为差异有统计学意义。并采用漏斗图进行发表偏倚的分析[3]。
2 结果
2.1 文献检索结果 初检出182 篇文献,阅读题目和摘要后,剔除重复发表、综述、病例报道后,共纳入20篇。通过进一步阅读全文排除不符合纳入标准的文献,最后纳入8 个随机对照试验,共涉及9 篇[4-12]文献,其中中文文献2 篇[4-5],英文文献7 篇[6-12]。共纳入研究对象1 286 例,其中接受英夫利昔治疗的患者517 例,接受免疫抑制剂(硫唑嘌呤、6-巯基嘌呤、氨甲喋呤)治疗的患者344 例,接受联合治疗的患者425例。所有纳入研究对研究对象的选择均制定了明确的纳入和排除标准,组间基线资料包括年龄、性别等,差异无统计学意义(P >0.05)。纳入研究的一般情况及有效性指标如表1 所示。

表1 纳入研究的一般情况及有效性指标Tab 1 General informations and valid indications of the studies
2.2 纳入研究的质量评价 本文3 个研究[6-8]均使用且具体阐明了随机分配方案和盲法,并对失访进行了积极的分析,数据处理方法合理,试验设计较好,文献质量较高,偏倚较小,完全满足上述质量标准,属于A级文献;王智云等[4]、段泽星等[5]、Schröder 等[9]、Accent Ⅰ[10-11]和Accent Ⅱ[10-12]的研究提及随机分配的方案,但未具体阐明,且未使用盲法,对失访的描述较为消极,实验设计不完善,存在中度偏倚,部分满足上述质量标准,属B 级文献。
2.3 疗效比较
2.3.1 10 ~14 周诱导缓解率比较:有5 篇研究[4,6-9]共12 个队列报道了10 ~14 周的诱导缓解率,其中联合治疗组与英夫利昔及免疫抑制剂比较时,各试验差异不显著,不具有异质性(I2=0,P >0.10,见图1 ~2),采用固定效应模型进行ITT 分析。联合治疗组与单药治疗组进行比较时,各试验差异显著,具有异质性(Chi2=7.54,P =0.11,I2=47%),采用随机效应模型进行ITT 分析。10 ~14 周时联合治疗组和单药治疗组的诱导缓解率分别为53.4%(288/539)、36.9%(198/536),差异有统计学意义(OR =2.09,95%CI:1.34 ~3.27,P=0.001,见图3)。
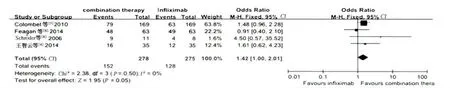
图1 10 ~14 周时联合治疗组与英夫利昔组诱导缓解率的疗效比较Fig 1 Comparison of clinical remission rates of combination therapy group and Infliximab group at weeks 10 ~14

图2 10 ~14 周时联合治疗组与免疫抑制剂组诱导缓解率的疗效比较Fig 2 Comparison of clinical remission rates of combination therapy group and immunosuppressants group at weeks 10 ~14

图3 10 ~14 周时联合治疗组与单药治疗组诱导缓解率的疗效比较Fig 3 Comparison of clinical remission rates of combination therapy group and monotherapy group at weeks 10 ~14
2.3.2 20 ~30 周维持缓解率比较:有5 个研究[4-5,7-9]共13 个队列报道了20 ~30 周的临床缓解率,各组间差异不显著,不具有异质性(I2=0,P >0.10,见图4~6),采用固定效应模型进行ITT 分析。20 ~30 周时联合治疗组和单药治疗组的临床缓解率分别为57.5%(283/492)、36.8%(180/489),两者比较,差异有统计学意义(OR = 2. 36,95% CI:1. 82 ~3. 05,P <0.00001,见图6)。
——丰富内涵,品质发展。挖掘乡村传统文化和乡俗风情,加强乡村文物保护利用和文化遗产保护传承,吸收现代文明优秀成果,在保护传承基础上创造性转化、创新性发展,提升农村农民精神面貌,丰富乡村旅游的人文内涵,推动乡村旅游精品化、品牌化发展。
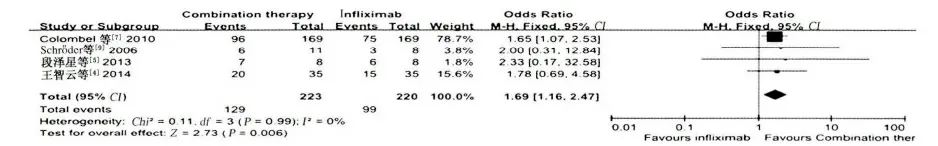
图4 20 ~30 周时联合治疗组与英夫利昔组维持缓解率的疗效比较Fig 4 Comparison of clinical remission rates of combination therapy group and Infliximab group at weeks 20 ~30
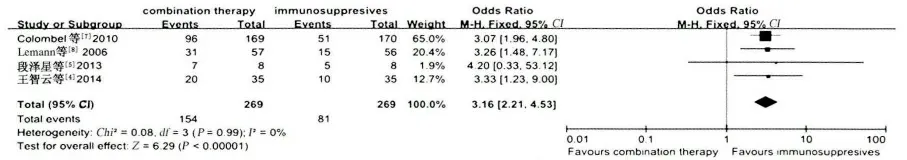
图5 20 ~30 周时联合治疗组与免疫抑制剂组维持缓解率的疗效比较Fig 5 Comparison of clinical remission rates of combination therapy group and immunosuppressants group at weeks 20 ~30

图6 20 ~30 周时联合治疗组与单药治疗组维持缓解率的疗效比较Fig 6 Comparison of clinical remission rates of combination therapy group and monotherapy group at weeks 20 ~30
2.3. 3 48 ~52 周维持缓解率比较:有6 个研究[6-9,10-11,10-12]共15 个队列报道了48 ~52 周的临床缓解率,各试验差异不显著,不具有异质性(I2=0,P >0.10),采用固定效应模型进行ITT 分析。联合治疗组与英夫利昔治疗组比较,其临床缓解率分别为45.2%(147/325)、37. 1% (176/474),差异无统计学意义(OR=1.29,95%CI:0.95 ~1.73,P=0.10,见图7)。联合治疗组与免疫抑制剂组比较时,其临床缓解率分别为41.9%(129/308)、22.3%(67/301),差异有统计学意义(OR = 2. 53,95% CI:1. 78 ~3. 61,P <0.00001,见图8)。48 ~52 周时联合治疗组和单药治疗组的临床缓解率分别为43.6%(276/633)、31.4%(243/775),差异有统计学意义(OR =1.66,95%CI:1.32 ~2.07,P <0.00001,见图9)。

图7 48 ~52 周时联合治疗组与英夫利昔组维持缓解率的疗效比较Fig 7 Comparison of clinical remission rates of combination therapy group and Infliximab group at weeks 48 ~52
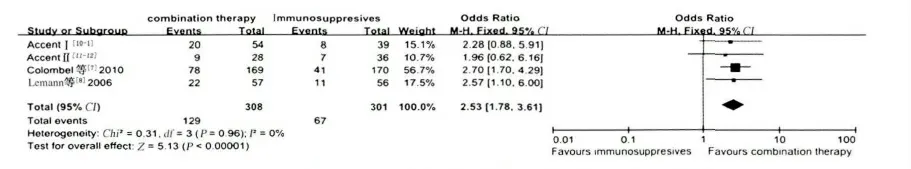
图8 48 ~52 周时联合治疗组与免疫抑制剂组维持缓解率的疗效比较Fig 8 Comparison of clinical remission rates of combination therapy group and immunosuppressants group at weeks 48 ~52

图9 48 ~52 周时联合治疗组与单药治疗组维持缓解率的疗效比较Fig 9 Comparison of clinical remission rates of combination therapy group and monotherapy group at weeks 48 ~52
2.3.4 20 ~30 周时黏膜愈合情况比较:有4 个研究[4-5,7-8]共11 个队列报道了20 ~30 周时黏膜愈合情况,各组间差异不显著,不具有异质性(I2=0,P >0.10),采用固定效应模型进行ITT 分析(见图10 ~12)。20 ~30 周时联合治疗组和单药治疗组的黏膜愈合率分别为48.0%(135/281)、27.3%(73/267),两者比较,差异有统计学意义(OR=2.62,95%CI:1.81 ~3.81,P <0.00001,见图12)。
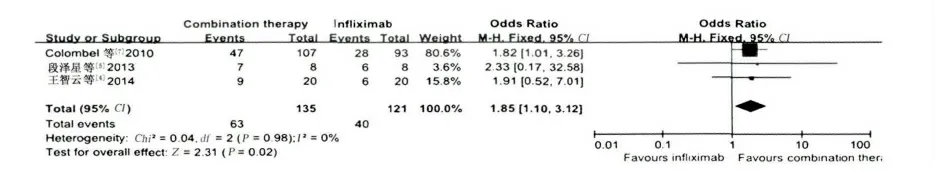
图10 20 ~30 周时联合治疗组与英夫利昔组促进黏膜愈合疗效的比较Fig 10 Comparison of mucosal healing rates of combination therapy group and Infliximab group at weeks 20 ~30
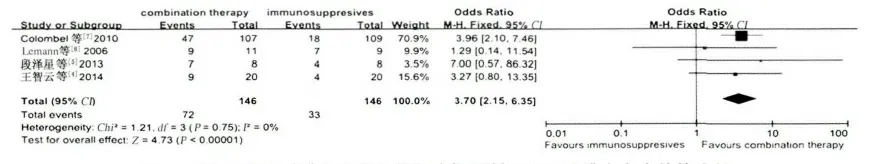
图11 20 ~30 周时联合治疗组与免疫抑制剂组促进黏膜愈合疗效的比较Fig 11 Comparison of mucosal healing rates of combination therapy group and immunosuppressants group at weeks 20 ~30
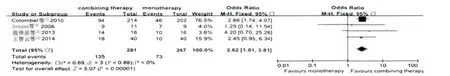
图12 20 ~30 周时联合治疗组与单药治疗组促进黏膜愈合疗效的比较Fig 12 Comparison of mucosal healing rates of combination therapy group and monotherapy group at weeks 20 ~30
2.3.5 生化指标改善情况:王智云等[4]研究显示,26周末时联合治疗组的白细胞计数、血沉、C 反应蛋白明显低于其他两组,而血清白蛋白、血清总蛋白明显高于其他两组。段泽星等[5]研究显示,26 周末时联合治疗组血红蛋白较治疗前显著升高(P <0.05),血沉和C反应蛋白较治疗前均显著降低(P <0.05)。而Feagan等[6]研究却显示联合治疗组与英夫利昔组相比并不能降低C 反应蛋白水平。
2.4 安全性比较 为了比较其安全性,同样的8 个试验[4-12]被纳入此项研究。然而,AccentⅠ[10-11]和Accent Ⅱ[10-12]中免疫抑制剂的单一药物治疗方案的有关安全性的数据未给出,除此之外,共有12 个比较两者安全性的研究。有关的安全性指标包括:不良反应总例数、严重不良反应的例数、感染、严重感染的例数、输液反应、过敏反应、手术及恶性肿瘤的例数。Lemann 等[8]研究是按发生的例数计算的,而不是按患者数计算的。尽管不能收集完整的纳入研究的安全性指标,但是从可获取的数据中可以观察到,联合治疗方案并不增加不良反应的发生率。王智云等[4]、段泽星等[5]、Feagan 等[6]、Colombel 等[7]、Lemann 等[8]、Schröder 等[9]研究均认为联合治疗并不增加不良反应发生率,是一个较为安全的治疗方案(见表2)。

表2 纳入研究的安全性指标Tab 2 Safety indicators of the studies
2.5 发表偏倚分析 对图9 中的相关研究作漏斗图(见图13),图形较对称,且主要集中在中部,提示无明显发表偏倚。
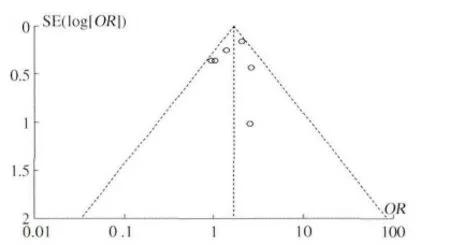
图13 漏斗图Fig 13 Funnel figure
3 讨论
该Meta 分析显示,英夫利昔和免疫抑制剂联合治疗具有更好的临床疗效,更能促进黏膜愈合及改善生化指标,且不良反应的发生率无明显增加。其可能的机制为:(1)免疫抑制剂可以抑制英夫利昔的免疫原性,从而减少英夫利昔抗体的产生,因此可以延长英夫利昔的有效作用时间[13];(2)两种药物可能在抑制细胞凋亡方面具有协同作用[14];(3)硫唑嘌呤的活性代谢物6-硫代鸟嘌呤核苷酸水平的增加(每8 ×108的红细胞中高于400 pmol)与英夫利昔的疗效有很强的相关性[15]。
此Meta 分析可能存在的偏倚:(1)纳入研究的数量有限。经全面检索后,本篇文章共纳入8 项研究,纳入研究的数量较少。(2)纳入的研究存在B 级质量的文献。王智云等[4]、段泽星等[5]、Schröder 等[9]、Accent I[10-11]和Accent Ⅱ[10-12]由于试验设计不够完善,存在中度偏倚,属于B 级文献,将影响该研究结论的可靠性。段泽星等[5]和Schröder 等[9]两研究的样本量较少,样本量选择的随意性较大,没有经过具体的计算推测最少样本量。(3)不同研究采用的时间节点不同,数据收集不完整。然而只有具有同一时间节点的数据才具有可比性。但纳入的研究中具有同一时间节点的研究的数量较少,因此各单一比较组间纳入的病例数较少,影响了结果的可靠性。(4)混杂因素在各组间不均衡。在评估联合治疗的安全性及有效性时需要考虑免疫抑制剂的种类,但是由于纳入研究的数量有限,我们不能逐一分析每一种免疫抑制剂的疗效及安全性。(5)纳入研究的方案设计不同。王智云等[4]、段泽星等[5]、Feagan 等[6]、Accent I[10-11]及Accent Ⅱ[10-12]的研究在整个过程中均规律地使用英夫利昔,而Lemann 等[8]和Schröder 等[9]的研究在整个试验的过程中分别使用了3 次和2 次英夫利昔。然而在维持疾病缓解方面两种设计没有明显的差异。Lemann 等[8]认为英夫利昔治疗只是一个过渡到免疫抑制剂治疗的桥梁。但是过渡方案潜在的缺点在于停止英夫利昔治疗能促进英夫利昔抗体的形成,当需要再次使用英夫利昔时,其疗效可能因此大打折扣。(6)纳入的研究存在失访,导致收集的资料不完整,此篇文章只进行了ITT 分析,未进行PP 分析,将导致各组有效率偏低。
尽管该篇研究支持联合治疗方案,但是,我们更建议今后的临床试验应充分克服目前存在的局限性,严格遵守CONSORT 标准[16],进行大样本量的更长随访时间的随机盲法研究,采用客观、国际认可的且有利于交流的终点疗效评价指标,为二次评价提供高质量的研究证据,以更好地评价其疗效和论证其推广价值。
[1] Lichtenstein GR,Hanauer SB,Sandborn WJ,et al. Management of Crohn's disease in adults[J]. Am J Gastroenterol,2009,104(2):465-483.
[2] Heggins JPT,Green S. Cochrane handbook for systematic reviews of interventions,version 5. 0. 2[updated September 2009][OL]. The Cochrane Collaboration,2009,Available from www. cochranehandbook.org.
[3] Egger M,Smith GD. Bias in location and selection of studies[J].BMJ,1998,316(7124):61-66.
[4] Wang ZY,Zheng L,Zhang MH. Effect observation of infliximab combined with azathioprine on treatment of patients with Crohn's disease[J]. Journal of Clinical Medicine in Practice,2014,18(1):75-78.王智云,郑柳,张明红.英夫利昔单抗与硫唑嘌呤联用治疗克罗恩病临床疗效观察[J]. 实用临床医药杂志,2014,18(1):75-78.
[5] Duan ZX,Luo JQ,Li WQ. Efficacy of infliximab combined with azathioprine for moderate to severe Crohn's disease[J]. Chin J Gastroenenterol,2013,18(4):229-232.段泽星,罗俊卿,李伟强. 英夫利西单抗联合硫唑嘌呤治疗中重度克罗恩病的疗效研究[J]. 胃肠病学,2013,18(4):229-232.
[6] Feagan BG,McDonald JW,Panaccione R,et al. Methotrexate in combination with infliximab is no more effective than infliximab alone in patients with Crohn's disease[J]. Gastroenterology,2014,146(3):681-688.
[7] Colombel JF,Sandborn WJ,Reinisch W,et al. Infliximab,azathioprine,or combination therapy for Crohn's disease [J]. N Engl J Med,2010,362(15):1383-1395.
[8] Lemann M,Mary JY,Duclos B,et al. Infliximab plus azathioprine for steroid-dependent Crohn's disease patients:a randomized placebocontrolled trial[J]. Gastroenterology,2006,130(4):1054-1061.
[9] Schröder O,Blumenstein I,Stein J. Combining infliximab with methotrexate for induction and maintenance of remission in refractory Crohn's disease:a controlled pilot study[J]. Eur J Gastroen Hepat,2006,18(1):11-16.
[10] Lichtenstein GR,Diamond RH,Wagner CL,et al. Clinical trial:benefits and risks of immunomodulators and maintenance infliximab for IBD-subgroup analyses across four randomized trials[J]. Aliment Pharmacol Ther,2009,30(3):210-226.
[11] Hanauer SB,Feagan BG,Lichtenstein GR,et al. Maintenance infliximab for Crohn's disease:the ACCENT I randomized trial[J]. Lancet,2002,359(9317):1541-1549.
[12] Sands BE,Anderson FH,Bernstein CN,et al. Infliximab maintenance therapy for fistulizing Crohn's disease[J]. N Engl J Med,2004,350(9):876-885.
[13] Baert F,Noman M,Vermeire S,et al. Influence of immunogenicity on the long-term efficacy of Infliximab in Crohn's disease[J]. N Engl J Med,2003,348(7):601-608.
[14] Scallon BJ,Moore MA,Trinh H,et al. Chimeric anti-TNF-a monoclonal antibody cA2 binds recombinant transmembrane TNF-alpha and activates immune effector functions [J]. Cytokine,1995,7(3):251-259.
[15] Roblin X,Serre-Debeauvais F,Phelip JM,et al. Drug interaction between infliximab and azathioprine in patients with Crohn's disease[J].Aliment Pharmacol Ther,2003,18(9):917-925.
[16] Schulz KF,Altman DG,Mother D. Consort 2010 statement:updated guidelines for reporting parallel group randomized trials[J]. J Pharmacol Pharmacother,2010,1(2):100-107.
