深在性囊性胃炎1 例
2015-12-31王小玮徐永红田字彬
闫 领,王小玮,徐永红,田字彬,毛 涛
青岛大学附属医院消化内科,山东 青岛266005
病例 患者,女,50 岁,上腹阵发性隐痛伴烧心6 个月,大便2 ~3 次/d,为黄色不成形便,无腹胀、恶心、呕吐,无反酸、嗳气,无发热、寒颤,发病以来进食一般,体质量减轻约4 kg。既往“高血压病”15 年余,自服“安内真、马来酸依那普利”,血压控制在130 ~140/80 ~90 mmHg,“小三阳”病史数年,曾口服抗病毒药物(具体不详)治疗。查体无明显阳性体征。于2013 年11 月26 日在青岛大学附属医院行胃镜检查及活检,提示(胃窦)慢性浅表-萎缩性胃炎伴轻度肠上皮化生,胃窦中部后壁见1 处大小约1.8 cm×2.2 cm 的半球形隆起,H.pylori(+);于2013 年12 月3 日行超声胃镜检查提示胃窦后壁见一大小1.8 cm×2.0 cm 隆起(见图1),病灶处可见低回声团块,呈梭形,向腔内外突出,内部回声均匀,边界清,大小约0.5 cm×1.0 cm,平滑肌瘤可能性大(见图2)。期间未行规范诊疗,症状持续。2014 年4 月23 日患者为明确胃黏膜下肿物性质于我院行内镜黏膜下剥离术(endoscopic submucosal dissection,ESD),术前完善上腹部CT 扫描提示胃窦壁增厚(见图3),术中胃窦中部后壁见大小约1.5 cm×1.8 cm 广基隆起,表面光滑,病变深达固有肌层,予以完整切除送检。
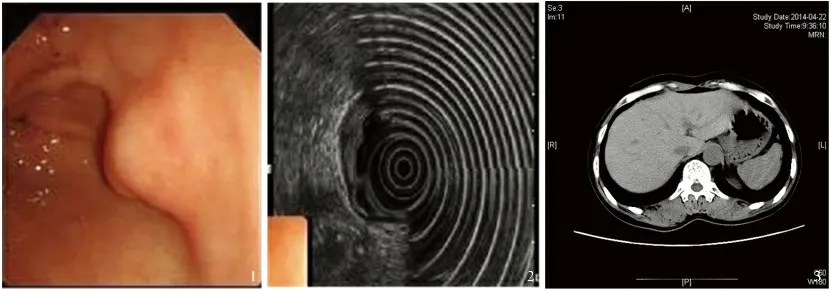
图1 胃镜检查:胃窦黏膜隆起样病变;图2 超声显像:低回声团块,起源于黏膜肌层;图3 术前上腹部CT:胃窦壁局部略厚Fig 1 Gastroscopy:gastric antrum mucosal lesion;Fig 2 Ultrasound imaging:low echo mass,originated from the mucous membrane;Fig 3 Upper abdomen CT:local thickness of gastric wall
病理检查:送检组织肌层内见数个囊性扩张的腺体伴淋巴细胞浸润,诊断为深在性囊性胃炎(gastritis cystica profunda,GCP)(见图4),H.pylori(-);免疫组化示:CK7(+),Villin(+),CDX-2(+),CK20(-),ER(-),PR(-),Ki67 阳性率约5%(见图5 ~9)。术后1 周复查上腹部CT 扫描提示符合胃术后表现,胃窦局部壁增厚。术后随访患者恢复良好。
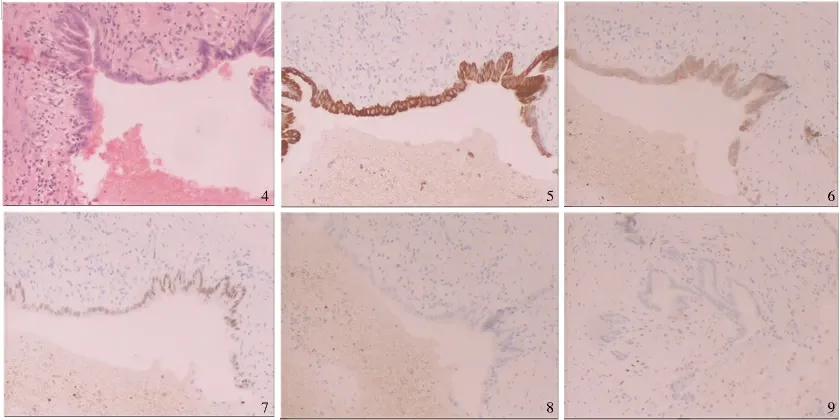
图4 苏木精-伊红染色(200 ×);图5 CK7 分子(+);图6 绒毛蛋白(+);图7 尾侧型同源转录因子-2(+);图8 雌激素受体(-);图9孕激素受体(-)Fig 4 HE(200 ×);Fig 5 CK7(+);Fig 6 Villin(+);Fig 7 Caudal type homeo box transcription factor-2,CDX-2(+);Fig 8 Estrogen receptor,ER(-);Fig 9 Progestrone receptor,PR(-)
讨论 GCP 是胃正常腺体穿过黏膜层向黏膜下层生长并扩张成囊的一种病变。1981 年,Franzin 等[1]对81 例因各种胃黏膜病变而行胃镜下热切或胃切除的标本进行研究时发现胃腺囊状扩张者72 例,约50%深达黏膜下层,胃腺改变类似结肠的深在性囊性结肠炎,因此将该病命名为GCP。
GCP 是一种罕见的胃黏膜下病变,目前国内外报道不足50例[2],其病因和发病机理尚不明确。该病多见于男性,中位年龄60 岁。GCP 患者多有腹痛、腹胀、食欲不振、出血、贫血等表现,部分患者腹部CT 可见胃壁不规则增厚或伴有胃腔内外隆起性肿物而就诊,约19%的患者无明显症状。该病最常见于胃体(62%)和胃底(24%),胃镜检查可见胃黏膜炎症,活组织检查可无异常,可能与活检过浅有关。超声内镜检查可见特异性的胃壁增厚伴局部深达黏膜下层甚至固有肌层的不规则低回声区,黏膜表面正常。典型的病理表现为黏膜肌层连续性破坏,胃小凹延长,腺体囊性扩张并增生[3]。该患者术前胃镜及超声胃镜检查可见一均匀低回声、规则半球形隆起,起源于黏膜肌层,与平滑肌瘤相似,但是术后病变切除组织提示GCP,与胃镜活检较浅、活检取材较少、病理诊断存在误差、对GCP 认识不足等有关,因此胃镜检查出现漏检。
通常认为GCP 是一种良性病变,但也有关于其与胃癌相关的报道[4-6],其发病机理主要是慢性炎症、缺血、异物刺激胃黏膜腺体或引起胃黏膜异位导致的腺体增生[7],另外,Roepke等[8]报道了钾离子通道蛋白2(K+channel 2,KCNE 2)特异性缺失可引起GCP 及胃癌。既往文献报道65%的GCP 患者出现于胃手术后,且多在吻合口的胃侧。随着内镜诊疗手段的发展、内镜下黏膜切除术(endoscopic mucosal resection,EMR)及ESD 的应用,发现部分GCP 患者并没有胃手术史,偶有病理检查提示不典型增生,因此也有学者认为该病与胃癌发病有某种关系或是一种癌前病变[4]。
目前GCP 尚无统一诊断标准和防治措施。常规胃镜通常不能明确诊断,需与淋巴瘤、间质细胞瘤、胃癌和Ménétrier's 病等鉴别诊断[5]。取材部位及深度对该病诊断影响较大,因此内镜下活检漏检率较高,超声胃镜检查并行穿刺活检有助于诊断。本病无特效药物治疗,发现后大多行手术切除治疗,随着内镜诊疗技术的不断发展,ESD 或EMR 已逐渐成为主要的诊断和治疗方法。
[1] Franzin G,Novelli P. Gastritis cystica profunda[J]. J Histopathol,1981,5(5):535-547.
[2] Li RJ,Chen G,Li M. One case report of gastritis cystica profunda[J].Chin J Dig Endosc,2013,30(4):221.李仁君,陈刚,李敏. 深在性囊性胃炎一例[J]. 中华消化内镜杂志,2013,30(4):221.
[3] Tsuji T,Iwahashi M,Nakamori M,et al. Multiple early gastric cancer with gastritis cystica profunda showing various histological types[J].Hepatogastroenterology,2008,55(84):1150-1152.
[4]Mitomi H,Iwabuchi K,Amemiya A,et al. Immunohistochemical analysis of a case of gastritis cystica profunda associated with carcinoma development[J]. Scand J Gastroenterol,1998,33(11):1226-1229.
[5] Park KH,Chung YH,Shin C,et al. Immunohistochemical study on the distribution of the voltage-gated potassium channels in the gerbil hippocampus[J]. Neurosci Lett,2001,298(1):29-32.
[6] Yamashita M,Hirokawa M,Nakasono M,et al. Gastric inverted hyperplastic polyp. Report of four cases and relation to gastritis cystica profunda[J]. APMIS,2002,110(10):717-723.
[7] Machicado J,Shroff J,Quesada A,et al. Gastritis cystica profunda:Endoscopic ultrasound findings and review of the literature[J]. Endosc Ultrasound,2014,3(2):131-134.
[8] Roepke TK,Purtell K,King EC,et al. Targeted deletion of Kcne2 causes gastritis cystica profunda and gastic neoplasia[J]. PLoS One,2010,5(7):e11451.
