食品乳状液冻融稳定性的研究进展*
2015-12-25简俊丽毛丽娟刘夫国高彦祥袁芳
简俊丽,毛丽娟,刘夫国,高彦祥,袁芳
(中国农业大学食品科学与营养工程学院功能配料与食品添加剂研发中心植物源功能食品北京市重点实验室,北京,100083)
乳状液(emulsion)是一种非均多相分散体系。常见的乳状液由油水两相组成,其中一相以液滴的形式分散在另一相中,被分散的一相称为分散相或内相,分散的一相称为连续相或外相。乳状液通常有2种类型,即水包油(O/W)型乳状液和油包水(W/O)型乳状液[1]。本文主要针对食品乳状液在冷冻-解冻过程中失稳机理,特别是油水两相在冷冻过程中的结晶化特点进行分析,并总结了影响乳液冻融稳定性的因素及改善方法。
1 乳状液的稳定性
乳状液具有良好的乳化性能,其中水包油型乳状液在食品工业中应用广泛,如加工蛋黄酱、调味料、饮料、冰激凌等。乳状液中加入乳化剂在油水界面形成界面膜,通过静电或空间位阻效应阻止油滴相互靠近,进而维持乳液的稳定性。乳状液破乳直接影响产品的外观、质地、风味,降低消费者的接受度。受乳液组成、加工技术(加热、冷冻和机械搅拌等)、重力和其他因素(pH、离子强度等)的影响,乳状液常表现出絮凝、聚结、乳析或沉淀、相转换和奥氏熟化等失稳现象(见图 1)[2]。
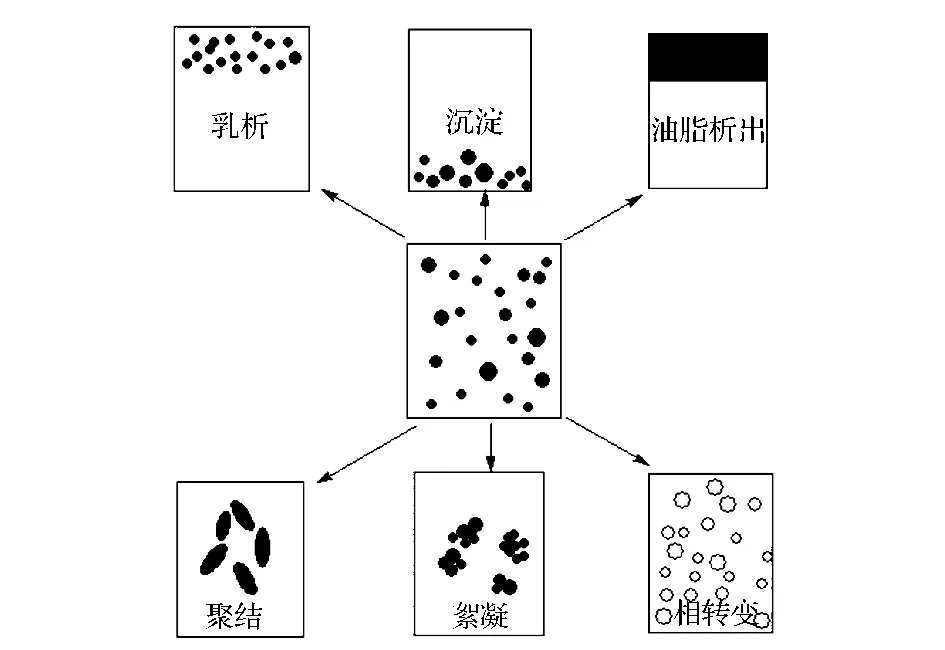
图1 乳液失稳示意图Fig.1 Emulsion instability diagram
絮凝和聚结是指在加入的乳化剂不足或其他不利条件下,2个或多个液滴相互靠近发生絮凝、聚并或部分聚并的现象。在浓度较低的体系,絮凝使液滴粒径变大,加速乳析或沉淀的产生。乳析/沉淀是指组成乳状液的颗粒受颗粒大小、颗粒与水相相对密度大小及水相黏度等的影响可能会发生乳析、沉淀等现象,如油滴密度小于水相的密度,受重力作用会向上运动,而乳液中的一些其他成分如添加在乳液中的调味成分向下运动,产生不稳定现象。油脂析出:乳液液滴产生聚并的速率和程度与表面活性剂分子包裹油滴的状态有关,若表面活性剂分子在油滴周围形成致密且较厚的界面层,会在油滴间形成较强的斥力,防止油滴相互靠近。但当乳化剂加入不足或形成的界面层较薄,液滴间产生絮凝或聚结,并最终导致油脂析出。相转变是其连续相和分散相发生逆转的过程。该过程受多种因素的影响,如油水体积比、温度、离子强度、乳化条件和表面活性剂组成等。如温度引起的相转变,对于某一特定的表面活性剂-油-水体系而言,存在着一个较窄的温度范围,在该温度以上,表面活性剂溶于油相,而在该温度以下,表面活性剂溶于水相;随温度逐渐升高,体系由O/W型乳液转变为W/O型乳液,发生相转变。
2 乳状液冻融过程中的失稳机理
冷冻是保持食品营养和感官特性、抑制化学和微生物引起的腐败以及延长食品货架期的有效方式。但许多水包油型乳液经冷冻-解冻过程后破乳,性质受到破坏,限制了其在一些食品中的应用。乳状液冷冻过程即油相和水相从液态到固态的转变过程。该过程中油水两相结晶化(晶核形成、冰晶大小和冰晶增长速率等)是影响乳状液冻融稳定性的关键因素,而油水两相的结晶化受很多因素如乳化剂类型、溶质、冷冻条件等因素的影响。
如果油相在水相之前结晶,可能会发生部分聚并,导致乳液失稳,如图2所示。
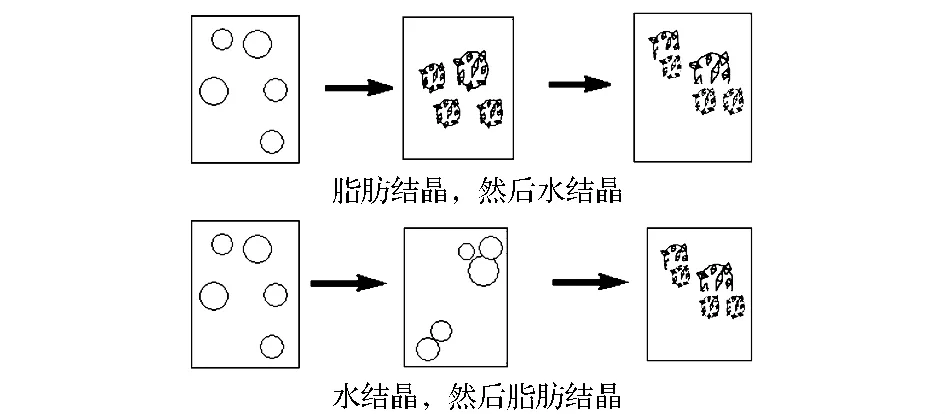
图2 乳状液冻融过程失稳机理[3]Fig.2 Instability mechanism of emulsion during freezing-thawing
当有部分油相结晶时,油滴相互碰撞,结晶油滴渗透到未结晶流动区域,流动区域液态油滴会流动到其他地方,加强了油滴间的相互作用,可能形成含有部分结晶油滴的无规则聚集体,温度继续降低到水结晶,冰晶膨胀占据结晶油滴的位置,结晶的水越来越多,未冷冻部分油滴浓度越来越大且相互靠近,这个冷冻浓缩过程可能造成絮凝、聚并甚至是油脂析出。当体系解冻后,结晶油滴溶解,并与未结晶油滴融合到一起,会导致液滴絮凝和油脂析出。较薄的界面层、高脂肪浓度及其他机械力的施加会加速部分聚并的速率,而脂肪晶体的数量、大小、位置、脂肪浓度、界面层性质及其他施加条件影响部分聚并的程度[3]。
其他理化过程也会导致冷冻乳液的失稳。例如,水相中部分冰晶形成时,未冷冻部分没有足够的自由水水合吸附在油滴上的蛋白分子,引起界面蛋白和表面活性剂脱水,产生构象和表面活性的改变,这会增加液滴间的反应,使乳液失稳。另外,未冻结的水相中的溶质浓度和离子强度增大、pH的变化等因素会增强带电油滴间的静电作用,产生絮凝,降低乳液稳定性[4]。
3 影响乳状液冻融稳定性的因素和改善方法
3.1 水相组成
3.1.1 糖
乳液中加入多糖可以减少其在冷冻过程中形成的冰晶的量,增加乳液中未冷冻的水的量和水相的粘度,使油滴运动变得困难,且能在油滴周围形成界面层,降低油滴聚结现象的发生[2-3,5-6],因而可以有效提高乳状液的冻融稳定性。Mun等[7]研究了多糖(果胶或卡拉胶)和麦芽糖糊精对乳液冻融稳定性的影响。结果表明加入果胶或卡拉胶的乳液比未加的乳液冻融稳定性好,且当乳液中有麦芽糖糊精存在时,乳液冻融稳定性得到提高。Zhao等再次验证了麦芽糖糊精对乳状液冻融稳定性的提高作用[8]。双糖的加入也能起到类似作用,如 Degner[9]加入150 mmol/L的蔗糖于乳液调料,发现蔗糖能抑制冰晶生长,防止液滴聚集和相分离。
3.1.2 盐和多元醇
盐和多元醇能改变冻融乳液中冰晶的形成状态,提高乳液冻融稳定性。如研究几种不同的盐(LiCl、NaCl、KCl,RbCl和 CsCl)在乳液冻融循环中的作用,发现500 mmol/L的LiCl和 NaCl能够有效抑制鸡蛋磷脂(12 mg/mL)稳定的大豆油(200 mg/mL)乳液的聚结现象的产生。5种盐提高乳液冻融稳定性的效果依次是:Li+=Na+>Rb+~Cs+~K+[10]。乳液中加入多元醇能降低水的冰点,减少冰晶的生成量,从而提高乳液冻融稳定性。Donsì等[11]研究表明,卵磷脂乳液体系冻融后不稳定,加入100 mg/g聚乙二醇后体系的冻融稳定性显著提高,乳液经10次冻融循环液滴粒径未发生显著变化。可能是由于聚乙二醇可能与磷脂分子形成氢键而吸附在液滴表面,减少液滴间的相互作用。
3.1.3 抗冻蛋白
抗冻蛋白(antifreeze protein,AFP)是一类抑制冰晶生长的蛋白质,能降低水溶液的冰点,改变晶核形态,防止小的冰晶凝结变大,使形成的晶粒体积小且均匀[12]。抗冻蛋白来源于一些极区鱼类、昆虫、耐寒的植物、真菌和细菌。目前发现的抗冻蛋白种类主要有抗冻糖蛋白(AFGPs)、I型抗冻蛋白(AFPI)、Ⅱ型抗冻蛋白(AFPⅡ)、Ⅲ型抗冻蛋白(AFPⅢ)和Ⅳ型抗冻蛋白(AFPⅣ)[13]。Regand 等[14]研究发现,冬小麦草提取物中的AFP添加到冰激凌中能有效抑制冰晶增长。在冰激凌中添加AFP的量为0.025~0.037 mg/g时,冰晶重结晶的速率降低40% ~46%,并且加入AFP的冰激凌更加细腻,口感较好。
3.1.4 乳化剂
乳化剂可能通过不同的机制提高乳液的稳定性:(1)改变油相和水相中晶核生成和冰晶的增长速率;(2)使脂肪滴之间产生斥力,不会相互靠近发生聚集;(3)在油滴周围生成界面膜,维持界面膜的完整性[3]。
常用的乳化剂有乳蛋白和小分子表面活性剂。酪蛋白和乳清蛋白是牛奶中两种主要蛋白,具有良好的乳化性。Thanasukarn等[15]研究表明,加入乳清分离蛋白和酪蛋白的乳液稳定性很好,蛋白吸附在油滴周围形成较厚的界面膜,通过空间阻力和静电排斥防止油滴相互靠近,维持乳液稳定性。且添加乳清分离蛋白的乳液比加入酪蛋白的乳液稳定性稍好,不同的蛋白乳化剂由于结构的不同,对乳液冻融稳定性的影响存在差异,如乳清分离蛋白是典型的球蛋白,而酪蛋白为无序蛋白。Palazolo[16]等研究不同蛋白浓度(5,10和20 mg/g)的天然和热变性的大豆分离蛋白(NSI和DSI)作为单一乳化剂,使用葵花子油制备的乳液的冻融稳定性,并与酪蛋白酸钠乳液比较。结果发现,5 mg/g的 NSI和 DSI很不稳定,油脂析出,乳液稳定性随蛋白浓度(5~20 mg/g)升高而增加,而加入酪蛋白酸钠的乳液絮凝程度和粒径都较小,稳定性较好。
3.2 油相组成
脂肪结晶特点影响乳液冻融稳定性。脂肪晶体形成的大小和形状与冷冻条件和油脂种类等有关。油脂可能导致乳液不稳定的方式如下:(1)脂肪结晶可能导致油滴周围界面层的破坏,使得油滴相互靠近,乳液解冻后发生部分聚结;(2)油滴结晶可能发生形状的改变,使总的表面积变化,可能使乳液中没有足够的乳化剂稳定油滴而发生聚结[3-4]。
不同的油脂种类,因其含有的脂肪酸种类和比例存在差异,对乳液冻融稳定的影响也不一样。如不同植物油(葵花籽油、菜籽油和中链甘油三酯)组成的油相对蛋黄酱乳液冻融稳定性的影响不同。菜籽油和中链甘油三酯制备的乳液冻融稳定性低,经一次冻融循环发生严重的油相分离,因为这2种油中含有较高的单不饱和脂肪酸,且在-25℃结晶甘油三酯含量高。葵花籽油制备的乳液稳定性最好,两次冻融循环后粒径没有显著增加[17]。Cramp[18]等采用同系列正构烷烃(C10~C18)制备 (40 wt%)水包油乳液,冻融后只有当油相不冻结而水相冻结时才稳定,使用正十六烷制备乳液经冻融后发现约27%正十六烷液滴失稳。
3.3 冷冻速率
温度低于水相的冰点时,会生成晶核,随之冰晶增长,冷冻速率影响晶核形成和增长的速率。不同的冷冻速率对乳液稳定性的影响存在差异。一般而言,速冻要比慢冻的效果好,速冻生成冰晶小而均匀,慢冻则形成较大冰晶,易造成乳液絮凝和相分离,造成乳液冻融稳定性下降,对食品品质产生不利影响。Degner[5]发现慢冻(-0.015 ℃ /min)可能造成脂肪滴絮凝和聚结,比速冻(-0.11℃/min)产生的液滴平均粒径大。
除了上述控制油相和水相组成、调控冷冻速率外,还可以通过设计乳液组成结构及其他物理、化学方法提高乳液稳定性。
3.4 设计乳液组成结构
3.4.1 层层自组装形成多层乳液
层层自组装(Layer-by-Layer)技术制备多层乳液,是提高乳液稳定性的有效方式。首先在均质过程使离子型乳化剂吸附在油滴表面形成单层乳液。然后往体系中加入带相反电荷的聚合电解质,使其吸附在液滴表面,此时油滴被双层界面乳化剂-电解质包裹,即形成双层乳液。该过程可以重复进行,制备3层甚至多层乳液[19]。如图3所示过程。

图3 层层自组装技术制备水包油乳液[20]Fig.3 Oil-in-water emulsion prepared by layer-by-layer self-assembly technique
一些电解质(如表面活性剂、生物大分子、大分子复合物和胶体粒子)可以通过层层自组装技术,对油滴实现多层包裹[19]。实验证明双层或3层的多组份乳液有较好的稳定性,可耐受不利环境(加热、冻融、高离子强度、脂质氧化等)[20-21]。
如采用层层自组装法制备含不同界面组成的50 mg/g的乳液:单层乳液(β-乳球蛋白)、双层乳液(β-乳球蛋白-ι-卡拉胶)和 3 层乳液(β-乳球蛋白-ι-卡拉胶-明胶),3种类型的乳液进行3次冻融循环(-20℃,22 h;40℃,2 h)。结果表明,单层和双层乳液一次冻融后不稳定,发生液滴聚集和乳析现象;3层乳液由于在油滴表面有较厚的界面膜,冻融后稳定性更好。该研究使用的层层自组装技术可以有效提高食品乳液的冻融稳定性[22]。Thanasukarn[23]等的研究结果也表明,SDS-壳聚糖-果胶3层乳液要比 SDS、SDS-壳聚糖的单层和双层乳液冻融稳定性更好。多层乳液形成较厚的界面膜包裹在油滴周围,增加了油滴间的斥力,抑制聚结的产生,提高乳液稳定性[22-24]。
3.4.2 酶交联形成多层乳液
静电作用进行层层组装形成多层乳液,当环境条件如pH或离子强度发生改变时会导致蛋白-多糖之间的静电作用减弱,破坏界面膜,降低乳液稳定性。通过酶交联(漆酶、谷氨酰胺转移酶等)形成共价结合的界面膜能克服环境改变对其的破坏作用。酶交联技术是提高多层乳液功能特性和稳定性的重要方法,特别对于含有蛋白和糖类的多层体系,通过交联作用能形成具有弹性和抗性的界面膜,对提高乳液热稳定性、冻融稳定性及抵抗其他不利环境条件pH、离子强度有重要意义[25-27]。
Zeeb[25]等采用漆酶研究酶交联甜菜果胶-鱼明胶形成双层乳液的冻融稳定性。发现与未进行酶处理的单层乳液相比,酶交联的双层乳液经2次冻融循环(-8℃、22 h;25℃、2h)后稳定性较高。
3.5 糖基化反应
通过糖基化,蛋白分子共价结合多糖可以增加乳液界面膜的厚度,在一定程度防止界面膜被破坏,抑制乳液冻融过程出现聚结和油脂析出,提高乳液的冻融稳定性[28-29]。
窦超然等[28]以麦芽糊精和大豆分离蛋白为原料,通过糖基化反应制备冻融稳定性很好的糖基化大豆分离蛋白。结果表明,经过糖基化处理的大豆分离蛋白乳液的抗乳化分层能力,要明显高于未经处理的大豆分离蛋白乳液。Xu等[29]采用乳清分离蛋白和葡聚糖通过干热法制备糖基化反应产物Ⅰ(80℃,2h)和产物Ⅱ(60℃,5d),并研究2种产物制备的乳液的冻融稳定性。结果发现与乳清分离蛋白、乳清分离蛋白和葡聚糖混合物制备的乳液相比,糖基化反应产物制备的乳液冻融稳定性显著提高,且产物Ⅱ由于接枝程度高,比产物Ⅰ的冻融稳定性好。作者推测由于葡聚糖叠加在油滴周围的界面层,增加了油滴间的静电斥力,提高了乳液稳定性。
4 结论与展望
乳状液在冷冻、贮藏及解冻过程中,稳定性受多种因素的影响,可能出现不稳定现象,从而造成食品感官、营养价值下降或缩短食品货架期等,可以通过控制产品组成(水相和油相)、冷冻条件(冷冻速率、温度)及解冻条件提高其冻融稳定性,使乳状液在食品中得到良好应用。提高乳状液冻融稳定性对改善某些食品的品质具有重要作用,如冰激凌、乳液调料、蛋黄酱等,可以使产品具有更细腻口感和保留更多的营养成分。目前关于加工条件对乳状液冷冻过程的研究较少,因此今后研究中应深入探究加工条件对乳状液稳定性的影响,例如高压冷冻技术,该方法能产生较小结冰颗粒,对食品破坏小,是一种提高乳状液冻融稳定性的有效方式[30-31]。此外,通过合理的结构设计来提高乳液的冻融稳定性也将成为研究热点。
[1] McClements D J.Critical review of techniques and methodologies for characterization of emulsion stability[J].Crit Rev Food Sci,2007,47(7):611-649.
[2] Ghosh S,Cramp GL,Coupland JN.Effect of aqueous composition on the freeze-thaw stability of emulsions[J].Colloids and Surfaces A:Physicochem Eng Aspects,2006,272(1/2):82-88.
[3] Degner B M,Chung C,Schlegel V,et al.Factors influencing the freeze-thaw stability of emulsion-based foods[J].Compr Rev Food Sci F,2014,13(2):98-111.
[4] Ghosh S,Coupland JN.Factors affecting the freeze-thaw stability of emulsions[J].Food Hydrocolloid,2008,22(1):105-111.
[5] Degner B M,Olson K M,Rose D,et al.Influence of freezing rate variation on the microstructure and physicochemical properties of food emulsions[J].J Food Eng,2013,119(2):244-253.
[6] Fernaa'ndez PP,Martino MN,Zaritzky NE,et al.Effects of locust bean,xanthan and guar gums on the ice crystals of a sucrose solution frozen at high pressure[J].Food Hydrocolloid,2006,21(4):507-515.
[7] Mun S,Cho Y,Decker E A,et al.Utilization of polysaccharide coatings to improve freeze-thaw and freeze-dry stability of protein-coated lipid droplets[J].J Food Eng,2008,86(4):508-518.
[8] ZHAO J,XIANG J,WEI T,et al.Influence of environmental stresses on the physicochemical stability of orange oil bilayer emulsions coated by lactoferrin-soybean soluble polysaccharides and lactoferrin-beet pectin[J].Food Research International,2014,66:216-227.
[9] Thanasukarn P,Pongsawatmanit R,McClements D J.Impact of fat and water crystallization on the stability of hydrogenated palm oil-in-water emulsions stabilized by whey protein isolate[J].Colloidsand SurfacesA:Physicochem.Eng.Aspects,2004,246(1-3):49-59.
[10] Komatsu H,Okada S,Handa T.Suppressive effects of salts on droplet coalescence in a commercially available fat emulsion during freezing for storage[J].Journal of Pharmaceutical Science,1997,86(4):497-502.
[11] Donsì F,WANG Y W,HUANG Q R.Freeze-thaw stability of lecithin and modified starch-based nanoemulsions[J].Food Hydrocolloid,2011,25(5):1 327-1 336.
[12] Tam R Y,Rowley C N,Petrov I,et al.Solution conformation of C-linked antifreeze glycoprotein analogues and modulation of ice recrystallization[J].J Am Chem Soc,2009,131(43):15 745-15 753.
[13] 李树峰,曹允考,郝丽,等.抗冻蛋白的研究进展及其应用[J].东北农业大学学报,2003,34(1):90-94.
[14] Regand A,Goff H D.Ice recrystallization inhibition in ice cream as affected by ice structuring proteins from winter wheat grass[J].Journal of Dairy Science,2006,89(1):49-57.
[15] Thanasukarn P,Pongsawatmanit R,McClements D J.Influence of emulsifier type on freeze-thaw stability of hydrogenated palm oil-in-water emulsions[J].Food Hydrocolloid,2004,18:1 033-1 043.
[16] Palazolo G G,Sobral P A,Wagner J R.Freeze-thaw stability of oil-in-water emulsions prepared with native and thermally-denatured soybean isolates[J].Food Hydrocolloid,2011,25(3):398-409.
[17] Magnusson E,Rosén C,Nilsson L.Freeze-thaw stability of mayonnaise type oil-in-water emulsions[J].Food Hydrocolloid,2011,25(4):707-715.
[18] Cramp G L,Docking A M,Ghosh S,et al.On the stability of oil-in-water emulsions to freezing[J].Food Hydrocolloid,2004,18(6):899-905.
[19] Guzey D,McClements DJ.Formation,stability and properties of multilayer emulsions for application in the food industry[J].Adv Colloid Interfac,2006,128:227-248.
[20] Gu Y S,Decker A E,McClements D J.Production and characterization of oil-in-water emulsions containing droplets stabilized by multilayer membranes consisting of betalactoglobulin,iota-carrageenan and gelatin[J].Langmuir,2005,21(13):5 752-5 760.
[21] Gu Y S,Regnier L,McClements D J.Influence of environmental stresses on stability of oil-in-water emulsions containing droplets stabilized by beta-lactoglobulin-iota-carrageenan membranes[J].J Colloid Interf Sci,2005,286(2):551-558.
[22] Gu Y S,Decker E A,McClements D J.Application of multi-component biopolymer layers to improve the freezethawst ability of oil-in-water emulsions:β-Lactoglobulin-lcarrageenan-gelatin[J].J Food Eng,2007,80(4):1 246-1 254.
[23] Thanasukarn P,Pongsawatmanit R,McClements D J.Utilization of layer-by-layer interfacial deposition technique to improve freeze-thaw stability of oil-in-water emulsions[J].Food Res Int,2006,39(6):721-729.
[24] Aoki T,Decker E A,McClements D J.Influence of environmental stresses on stability of O/W emulsions containing droplets stabilized by multilayered membranes produced by a layer-by-layer electrostatic deposition technique[J].Food Hydrocolloid,2005,19(2):209-220.
[25] Zeeb B,Fischer L,Weiss J.Cross-linking of interfacial layers affects the salt and temperature stability of multilayered emulsions consisting of fish gelatin and sugar beet pectin[J].J Agr Food Chem,2011,59(19):10 546-10 555.
[26] Zeeb B,Gibis M,Fischer L,et al.Crosslinking of interfacial layers in multilayered oil-in-water emulsions using laccase:Characterization and pH-stability[J].Food Hydrocolloid,2012,27(1):126-136.
[27] Zeeb B,Salminen H,Fischer L,et al.Impact of heat and laccase on the ph and freeze-thaw stability of oil-in-water emulsions stabilized by adsorbed biopolymer nanoparticles[J].Food Biophys,2014,9(2):125-137.
[28] 窦超然,于国萍,宋岩,等.冻融稳定型糖基化大豆分离蛋白的制备[J].食品工业,2013,34(4):3-5.
[29] XU D,YUAN F,WANG X,et al.The effect of whey protein isolate-dextran conjugates on the freeze-thaw stability of oil-in-water emulsions[J].J Disper Sci Technol,2011,32(1):77-83.
[30] ZHU S,Ramaswamy H S,Simpson B K.Effect of highpressure versus conventional thawing on color,drip loss and texture of Atlantic salmon frozen by different methods[J].LWT-Food Sci Technol,2004,37(3):291-299.
[31] Tironi V,Lamballerie M,Le-Bail A.Quality changes during the frozen storage of sea bass(Dicentrarchus labrax)muscle after pressure shift freezing and pressure assisted thawing[J].Innov Food Sci Emerg,2010,11(4):565-573.
